Деление твердых тел на металлы полупроводники и диэлектрики
Обновлено: 18.05.2024
Зонная теория твердых тел позволила с единой точки зрения истолковать существование металлов, диэлектриков и полупроводников, объясняя различие в их электрических свойствах, во-первых, неодинаковым заполнением электронами разрешенных зон и, во-вторых, шириной запрещенных зон.
Степень заполнения электронами энергетических уровней в зоне определяется заполнением соответствующих атомных уровней. Если при этом какой-то энергетический уровень полностью заполнен, то образующаяся энергетическая зона также запол нена целиком. В общем случае можно говорить о валентной зоне, которая полностью заполнена электронами и образована из энергетических уровней внутренних электронов свободных атомов, и о зове проводимости (свободной зоне), которая либо частично заполнена электронами, либо свободна и образована из энергетических уровней внешних «коллективизированных» электронов изолированных атомов.
В зависимости от степени заполнения зон электронами и ширины запрещенной зоны возможны четыре случая, изображенные на рис. 314.
На рис. 314, а самая верхняя зона, содержащая электроны, заполнена лишь частично, т. е. в ней имеются вакантные уровни. В данном случае электрон, получив сколь угодно малую энергетическую «добавку» (например, за счет теплового движения или электрического поля), сможет перейти на более высокий энергетический уровень той же зоны, т. е. стать свободным и участвовать в проводимости. Внутривенный переход вполне возможен, так как, например, при 1 К энергия теплового движения kT » 10 -4 эВ, т. е. гораздо больше разности энергий между соседними уровнями зоны (примерно 10 -22 эВ). Таким образом, если в твердом теле имеется зона, лишь частично заполненная электронами, то это тело всегда будет проводником электрического тока. Именно это свойственно металлам.
Твердое тело является проводником электрического тока и в том случае, когда валентная зона перекрывается свободной зоной, что в конечном счете приводит к не полностью заполненной зоне (рис. 314, б). Это имеет место для щелочно-земельных элементов, образующих II группу таблицы Менделеева (Be, Mg, Ca, Zn, . ). В данном случае образуется так называемая «гибридная» зона, которая заполняется валентными электронами лишь частично. Следовательно, в данном случае металлические свойства щелочно-земельных элементов обусловлены перекрытием валентной и свободной зон.
Помимо рассмотренного выше перекрытия зон возможно также перераспределение электронов между зонами, возникающими из уровней различных атомов, которое может привести к тому, что вместо двух частично заполненных зон в кристалле окажутся одна полностью заполненная (валентная) зона и одна свободная зона (зона проводимости). Твердые тела, у которых энергетический спектр электронных состояний состоит только из валентной зоны и зоны проводимости, являются диэлектриками или полупроводниками в зависимости от ширины запрещенной зоны DE.
Если ширина запрещенной зоны кристалла порядка нескольких электрон-вольт, то тепловое движение не может перебросить электроны из валентной зоны в зону проводимости и кристалл является диэлектриком, оставаясь им при всех реальных температурах (рис. 314, в). Если запрещенная зона достаточно узка (DЕ порядка 1 эВ), то переброс электронов из валентной зоны в зону проводимости может быть осуществлен сравнительно легко либо путем теплового возбуждения, либо за счет внешнего источ ника, способного передать электронам энергию DЕ,и кристалл является полупроводником (рис. 314, г).
Различие между металлами и диэлектриками с точки зрения зонной теории состоит в том, что при 0 К в зоне проводимости металлов имеются электроны, а в зоне проводимости диэлектриков они отсутствуют. Различие же между диэлектриками и полупроводниками определяется шириной запрещенных зон: для диэлектриков она довольно широка (например, для NaCl DЕ = 6 эВ), для полупроводников - достаточно узка (например, для германия DE = 0,72 эВ). При температурах, близких к 0 К, полупроводники ведут себя как диэлектрики, так как переброса электронов в зону проводимости не происходит. С повышением температуры у полупроводников растет число электронов, которые вследствие теплового возбуждения переходят в зону проводимости, т. е. электрическая проводимость проводников в этом случае увеличивается.
Классификация твердых тел по электропроводности
По своим электрическим свойствам твердые тела разделяются на проводники (металлы), полупроводники, и диэлектрики (изоляторы).
К проводникам относится класс веществ, которые имеют в своем составе электрические заряды, расположенные на микроносителях (электроны, ионы), и которые могут перемещаться даже под действием слабых электрических полей. С точки зрения зонной теории к проводникам (металлам) относятся вещества, имеющие или не полностью заполненную энергетическую зону, или частично перекрывающиеся полностью заполненную и свободную зоны, что в конечном счете приводит к не полностью заполненной зоне (рис. 6.1, а). В таком случае при наложении внешнего электрического поля электроны могут переходить на более высокие энергетические уровни в зоне, вследствие чего они приобретают скорость направленного движения, участвуя в электрическом токе.
К диэлектрикам (изоляторам) относятся вещества, которые не проводят электрический ток. С точки зрения зонной теории это вещества, у которых заполнены все состояния энергетических зон вплоть до валентной зоны, а первая свободная зона находится на расстоянии не менее 2…3 эВ (рис.6.1, с).
К полупроводникам относятся вещества, которые по свойствам проводимости занимают промежуточное положение между проводниками и диэлектриками. Кроме того, их электропроводность увеличивается с увеличением температуры, освещенности, под воздействием электрических полей и механических напряжений; особенно резко их электропроводность зависит от примесей.
С точки зрения зонной теории полупроводниками являются вещества, имеющие полностью заполненные зоны, в том числе и валентную зону, а ближайшая незаполненная зона – зона проводимости - отстоит на расстоянии не более 2…3 эВ (рис.1.7, б). В этом случае при 0 К все энергетические уровни заняты, а переходы между уровнями запрещены принципом Паули, такие взаимные переходы, если они осуществляются, не сопровождаются изменением макросостояния кристалла и не могут участвовать в обмене энергией с внешним электрическим полем. Для того чтобы полупроводник мог принимать энергию внешнего электрического поля и проводить тем самым электрический ток, необходимо часть электронов перевести через запрещенную зону в зону проводимости. Тем самым в валентной зоне появятся свободные места на разрешенных энергетических уровнях («дырки») и электроны - в зоне проводимости, которые там имеют возможность принимать энергию внешнего электрического поля. Место «дырок» также может заниматься электронами более глубоких энергетических уровней и, таким образом, под действием внешнего электрического поля может осуществляться направленное движение электронов и в зоне проводимости и в зоне валентной – идет электрический ток. Для переброса электронов в зону проводимости и потребуется энергия тех воздействий, о которых было сказано выше.
Деление веществ на полупроводники и изоляторы условно. Хорошим изолятором является алмаз с шириной запрещенной зоны 5,6 эВ, а хороший полупроводник германий имеет ширину запрещенной зоны менее 1 эВ.
6.3 Электрические свойства полупроводников
Важнейшим свойством полупроводников (см. п. 1.4) является зависимость их электрических свойств от таких внешних факторов, как температура, освещенность, давление, электрические и магнитные поля. Формальным, но не решающим признаком принадлежности вещества к полупроводникам является величина электропроводности, которая для них может принимать значения в пределах s = 10 6 …10 ‑8 Ом ‑1 ×м ‑1 ; для металлов - s » 10 8 …10 5 Ом ‑1 ×м ‑1 ; для изоляторов - s < 10 ‑12 Ом ‑1 ×м ‑1 .
Характерной является температурная зависимость электрических свойств полупроводников. В отличие от металлов с увеличением температуры сопротивление полупроводников падает. Опыт дает зависимость сопротивления полупроводников от температуры в виде
где Еа – энергия активации, величина, характерная для полупроводников различного типа.
В некоторой области температур сопротивление полупроводников может возрастать с ростом температуры. Такие полупроводники называются вырожденными.
Резкая зависимость сопротивления полупроводников от температуры и освещенности дает возможность использовать их для преобразования соответствующих сигналов в электрические. Приборы при этом называются терморезисторы, фоторезисторы и прочее.
Собственные и примесные полупроводники. Полупроводники, проводимость которых обусловлена переходами электронов из заполненной валентной зоны в зону проводимости, называются собственными. Полупроводники, проводимость которых обусловлена ионизацией примеси, называются примесными. Примесные полупроводники, в свою очередь, делятся на электронные и дырочные полупроводники. В электронных полупроводниках основными носителями тока являются электроны, возникающие при ионизации атомов примеси. Такие примеси называются донорными, или донорами. В дырочном полупроводнике основными носителями тока являются дырки (см. п. 1.3). Дырки возникают в валентной зоне при переходе электронов этой зоны на примесные уровни. Такие примеси называются акцепторными, или акцепторами (принимающими).
6.4 Механизм проводимости полупроводников
Механизм проводимости собственных полупроводников рассмотрим на примере элемента четвертой группы, типичного полупроводника Ge. Атомы четырехвалентного германия образуют кубическую решетку, в которой каждый атом связан парноэлектронной связью с четырьмя ближайшими атомами. Двумерная модель кристалла с такой связью при Т=0 К приведена на рис. 6.2, а. Валентные электроны принадлежат своим атомам и, кроме того, благодаря перекрытию электронных облаков они могут переходить от атома к атому при встречном движении других электронов – атомы обмениваются электронами и электроны могут перемещаться по всему кристаллу. Однако такое движение является чисто хаотическим и не может участвовать в направленном движении под действием внешнего электрического поля – ток в полупроводнике отсутствует. Для создания электрического тока валентные электроны необходимо оторвать от атомов, сделать их свободными.
С точки зрения зонной теории ток в полупроводнике при низких температурах отсутствует, так как все энергетические уровни валентной зоны заняты, и некуда принять энергию такого взаимодействия. Зонная структура полупроводникового кристалла при Т = 0 К представлена на рис. 1.8, б. Для перевода электронов в зону проводимости энергии электрического поля недостаточно. Чтобы электрон перешел в зону проводимости и стал свободным, требуется энергия, соизмеримая с внутриатомной и с шириной запрещенной зоны. Такой энергией может быть энергия теплового движения с учетом распределения электронов по энергиям, энергия фотонов или других энергичных частиц. Такие электроны составляют обычный электронный механизм проводимости. Однако в собственном полупроводнике имеется и другой механизм создания электрического тока. Действительно, в валентной зоне после ухода электрона появилось свободное состояние ‑ дырка, которое позволяет электронам более глубоких уровней перемещаться по полю, принимая, например, энергию внешнего электрического поля. Перемещение дырки – это перемещение одного положительного некомпенсированного заряда атомов. Поэтому движение дырки, обусловленное движением совокупности электронов в противоположном направлении, осуществляет перенос положительного заряда. Движение свободного состояния в глубь валентной зоны может рассматриваться как движение некоторой частицы, имеющей положительный заряд и некоторую эффективную массу. В собственном полупроводнике, следовательно, осуществляется электронный (отрицательный) и дырочный (положительный) механизмы проводимости. Число электронов в зоне проводимости всегда равно числу дырок в валентной зоне в собственном полупроводнике.
Механизм проводимости электронных полупроводников рассмотрим на примере элемента четвертой группы, типичного полупроводника Ge с донорной примесью пятивалентного элемента. Атомы четырехвалентного германия образуют кубическую решетку, в которой каждый атом связан парноэлектронной связью с четырьмя ближайшими атомами. Если пятивалентный атом примеси, например фосфора, мышьякаили сурьмы, замещает в решетке нормальный атом, то после образования четырех ковалентных связей с ближайшими соседями останется один валентный электрон, который будет локализован вблизи атома примеси (рис. 6.3, а). При этом в энергетическом спектре кристалла у дна зоны проводимости появляется дополнительный энергетический уровень Ед примесного атома, на котором находится "лишний" электрон (рис. 6.3, б)
Избыточный электрон движется в кулоновском поле примесного атома. Если атом примеси получает энергию Е (например, за счет тепловых колебаний решетки), превышающую Eс - Eд - энергию ионизации примеси (Eс – энергия электрона у дна зоны проводимости), то избыточный электрон покидает атом примеси и становится носителем тока. На энергетической диаграмме это соответствует переходу электрона с донорного уровня в зону проводимости (см. рис. 1.10, б). Избыточный электрон имеет теперь возможность обмениваться энергией с внешним электрическим полем, перемещаясь на более высокие свободные уровни в зоне проводимости, ‑ стать электроном проводимости. В целом же кристалл остается электрически нейтральным, поскольку электрон остается в кристалле.
Механизм проводимости примесных дырочных полупроводников рассмотрим на примере трехвалентной примеси бора. Введение в Ge или Si примеси атомов трехвалентного элемента В приводит к появлению дырок ‑ незаполненных химических связей (рис. 6.4, а). При этом вблизи потолка валентной зоны появляются свободные энергетические уровни примесного атома (рис. 6.4, б).
Если одиниз электронов в валентной зоне получает энергию, достаточную для перехода на акцепторный уровень Eа, то происходит ионизация примеси - атом примеси становится отрицательным ионом, а дырка становится подвижной. В электрическом поле дырка ведет себя подобно положительному заряду, двигаясь в направлении вектора напряженности электрического поля. Примеси, захватывающие электроныиз валентной зоны, называются акцепторами. Помимо примесных атомов появление разрешенных уровней в запрещенной зоне связано также с нарушением идеальной периодичности решетки: вакансии, атомы в междуузлиях, дислокации и тому подобное.
Концентрация электронов и дырок определяет удельную электропроводность полупроводника, поскольку энергия ионизации примесей соизмерима с энергией тепловых колебаний решетки (kT = 0,026 эВ при комнатной температуре), то в первую очередь активизируется примесный механизм проводимости. И, если, например, концентрация электронов в зоне проводимости преобладает над концентрацией дырок, то проводимость полупроводника будет электронной, а полупроводник - электронным или n - типа. Если преобладает концентрация дырок над концентрацией электронов, то проводимость будет дырочной, а полупроводник – дырочным или р- типа.
С повышением температуры концентрация примесных носителей тока быстро достигает насыщения – примесь истощается, а собственная проводимость (смешанного типа) растет и при высоких температурах становится определяющей электропроводность полупроводника. Зависимость логарифма концентрации носителей тока, а значит и электропроводности полупроводника от обратной температуры приведена на рис. 6.5. При низких температурах (1/Т велико) существенную роль играет примесная проводимость (участок 1); участок 2 соответствует температурам истощения примесей; участок 3 ‑ проводимость практически собственная.
Тип проводимости полупроводника можно установить экспериментально, используя результаты исследования эффекта Холла в полупроводниках.
Металлы, диэлектрики и полупроводники по зонной теории
Зонная теория позволила с единой точки зрения истолковать существование металлов, диэлектриков и полупроводников, объясняя различие в их электрических свойствах, во-первых, неодинаковым заселением электронами разрешенных зон, и во-вторых, шириной запрещенных зон.
Рассматривая заполнение электронами разрешенных зон необходимо использовать два правила: 1) Электроны стремятся занять самые низкие энергетические уровни. 2) Принцип Паули: на одном энергетическом уровне не может быть более двух электронов. Эти электроны должны иметь разные спины.
Степень заполнения электронами энергетических уровней в зоне определяется заполнением соответствующего атомного уровня. Если уровень атома полностью заполнен, то и зона полностью заполнена. Из незанятых уровней образуются свободные зоны, из частично заполненных – частично заполненные зоны. В общем случае можно говорить о валентной зоне, которая полностью заполнена и образовалась из энергетических уровней внутренних электронов свободных атомов и о зоне проводимости (свободной зоне), которая либо частично заполнена, либо свободна и образована из энергетических уровней внешних коллективизированных электронов изолированных атомов (рис.2).
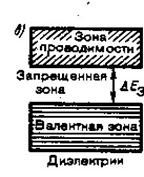 | Самая верхняя зона целиком занятая электронами (при Т=0 К) называется валентной. Зона, заполненная электронами частично (при Т = 0 К), называется зоной проводимости. Определим изменение энергии электрона, находящегося на некотором уровне в разрешенной зоне, под действием внешнего поля с напряженностью . Энергия приобретаемая электроном на длине свободного пробега , где - средняя длина свободного пробега электрона в кристалле равная примерно 10 -8 м в электрическом поле с напряженностью В/м, которая соответствует обычным источникам тока, эВ. |
| Рис.2. |
Это означает, что возможны только внутризонные переходы, так как междузонные переходы имеют много большую энергию. Необходимым условием электрической проводимости является наличие в разрешенной зоне свободных энергетических уровней на которые электрическое поле сторонних сил могло бы перевести электроны. В зависимости от степени заполнения зон электронами и ширины запрещенной зоны возможны три случая, изображенных на рис.3.
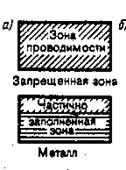 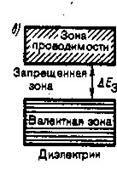  |
| (а) (б) (в) |
| Рис.3 |
3а). Зона проводимости заполнена лишь частично., то есть в ней имеются вакантные уровни. В этом случае электроны, получив сколь угодно малую энергетическую добавку (от поля или теплового движения) переходят на более высокий энергетический уровень той же зоны, то есть они участвуют в проводимости. Такой переход возможен, так как 1 К = 10 -4 эВ, что много больше расстояния между уровнями равному 10 -22 эВ. Таким образом, если в твердом теле имеется зона, лишь частично заполненная электронами, то это тело всегда будет проводником электрического тока. Именно это свойственно металлам.
3б). Возможно также такое перераспределение электронов между зонами, возникающими из уровней различных атомов, которое привело к тому, что вместо двух частично заполненных зон кристалла окажется одна целиком заполненная (валентная) зона и одна свободная зона (зона проводимости). Твердые тела, у которых энергетический спектр электронных состояний состоит только из валентной зоны и зоны проводимости, являются диэлектриками или полупроводниками в зависимости от ширины запрещенной зоны. Если ширина запрещенной зоны кристалла порядка нескольких электрон –вольт, то тепловое движение не может перебросить электроны из валентной зоны в зону проводимости и кристалл является диэлектриком, оставаясь им при всех реальных температурах.
3в). Если запрещенная зона достаточно узка ( эВ), то переход электронов из валентной зоны в зону проводимости может быть осуществлен сравнительно легко путем теплового возбуждения, либо за счет внешнего источника, способного передать электронам энергию , и кристалл является полупроводником.
Различие между металлами и диэлектриками с точки зрения зонной теории состоит в том, что при 0 К в зоне проводимости металлов имеются электроны, а в зоне проводимости диэлектриков они отсутствуют. Различие же между диэлектриками и полупроводниками определяется шириной запрещенных зон: для диэлектриков она довольно широка (например для NaCl =6 эВ), а для полупроводников достаточно узка (для германия =0,72 эВ). При температурах близких к 0 К полупроводники ведут себя как диэлектрики, то есть переброс электронов в зону проводимости не происходит.
Сущность зонной теории проводимости заключается в следующем:
1). При объединении атомов в кристалл твердого тела возникают энергетические зоны.
2). Ширина запрещенных зон и характер заполнения электронами разрешенных зон обуславливают электрические свойства твердого тела – оно может быть или металлом, или полупроводником, или диэлектриком.
По зонной теории
Степень заполнения электронами энергетических уровней в зоне определяется заполнением соответствующего атомного уровня.
В общем случае можно говорить о валентной зоне,которая полностью заполнена электронами и образована из энергетических уровней внутренних электронов свободных атомов, и о зонепроводимости (свободной зоне),которая либо частично заполнена электронами, либо свободна и образована из энергетических уровней внешних «коллективизированных» электронов изолированных атомов.
В зависимости от степени заполнения зон электронами и ширины запрещенной зоны возможны четыре случая, изображенные на рис.17. На рис. 17, а самая верхняя зона, содержащая электроны, заполнена лишь частично, т. е. в ней имеются вакантные уровни. В данном случае электрон, получив сколь угодно малую энергетическую «добавку» (например, за счет теплового движения или электрического поля), сможет перейти на более высокий энергетический уровень той же зоны, т. е. стать свободным и участвовать в проводимости. Внутризонный переход вполне возможен, так как, например, при 1 К энергия теплового движения kТ ≈10 –4 эВ, т.е. гораздо больше разности энергий между соседними уровнями зоны (примерно 10 -22 эВ). Таким образом, если в твердом теле имеется зона, лишь частично заполненная электронами, то это тело всегда будет проводником электрического тока. Именно это свойственно металлам.
Твердое тело является проводником электрического тока и в том случае, когда валентная зона перекрывается свободной зоной, что в конечном счете приводит к не полностью заполненной зоне (рис. 17, б), Это имеет место для щелочно-земельных элементов, образующих IIгруппу таблицы Менделеева (Ве, Мg, Са, Zn, . ). В данном случае образуется так называемая «гибридная» зона, которая заполняется валентными электронами лишь частично. Следовательно, в данном случае металлические свойства щелочно-земельных элементов обусловлены перекрытием валентной и свободной зон.
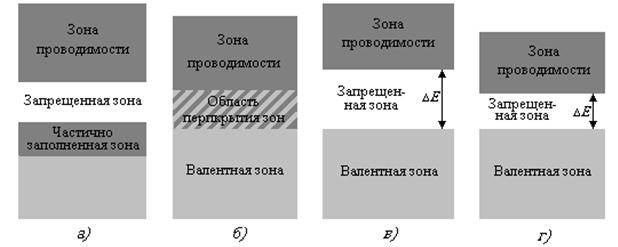
Помимо рассмотренного выше перекрытия зон возможно также перераспределение электронов между зонами, возникающими из уровней различных атомов, которое может привести к тому, что вместо двух частично заполненных зон в кристалле окажутся одна целиком заполненная (валентная) зона и одна свободная зона (зона проводимости). Твердые тела, у которых энергетический спектр электронных состояний состоит только из валентной зоны и зоны проводимости, являются диэлектриками или полупроводниками в зависимости от ширины запрещенной зоны, ΔЕ.
Если ширина запрещенной зоны кристалла порядка нескольких электрон-вольт, то тепловое движение не может перебросить электроны из валетной зоны в зону проводимости и кристалл является диэлектриком, оставаясь им при всех реальных температурах (рис. 17, в). Если запрещенная зона достаточно узка (ΔЕ порядка 1 эВ) то переброс электронов из валентной зоны в зону проводимости может быть осуществлен сравнительно легко либо путем теплового возбуждения, либо за счет внешнего источника, способного передать электронам энергию ΔЕ, и кристалл является полупроводником (рис. 17, г).
Различие между металлами и диэлектриками с точки зрения зонной теории состоит в том, что при 0 К в зоне проводимости металлов имеются электроны, а в зоне проводимости диэлектриков они отсутствуют. Различие же между диэлектриками и полупроводниками определяется шириной запрещенных зон: для диэлектриков она довольно широка (например, для NaCl ΔЕ = 6 эВ), для полупроводников – достаточно узка (например, для германия ΔЕ '= 0,72 эВ). При температурах, близких к 0 К, полупроводники ведут себя как диэлектрики, так как переброса электронов в зону проводимости не происходит. С повышением температуры у полупроводников растет число электронов, которые вследствие теплового возбуждении переходят в зону проводимости, т. е. электрическая проводимость проводников в этом случае увеличивается.
Металлы, полупроводники и диэлектрики
В зависимости от ширины запрещенной зоны (Eg) все твердые тела подразделяются на металлы (Eg < 0,08 эВ), диэлектрики (Eg > 3 эВ), полупроводники (0,08 эВ < Eg < 3 эВ).
Металл – кристалл, в котором либо имеется зона проводимости, в которой не все энергетические уровни заняты электронами, либо зона проводимости и валентная зона перекрываются. Ширина запрещенной зоны равна нулю, или ее величина меньше тепловой энергии кристалла, которая составляет величину порядка 3kT, что при T=300К примерно равно 0,08 эВ. В металлах число свободных электронов сравнимо с числом атомов в том же объеме (~10 22 атом/см 3 ), при этом концентрация электронов не зависит от температуры. Электропроводность при T»300K велика. Металлами являются кристаллические вещества с металлическим типом химической связи.
Диэлектрик и полупроводник имеют ширину запрещенной зоны больше, чем энергия тепловых колебаний решетки. Если ширина запрещенной зоны не слишком велика, то существует вероятность перехода электронов из валентной зоны в зону проводимости за счет тепловых колебаний решетки, либо за счет поглощения кванта света. Условной границей подразделения кристаллов на полупроводники и диэлектрики является ширина запрещенной зоны, при которой возможен переход электрона из валентной зоны в зону проводимости при поглощении кванта видимого света. Энергия кванта, соответствующего коротковолновой границе видимой области света (l ~ 400 нм), составляет величину hn ~ 3 эВ.
В полупроводниковых кристаллических веществах химическая связь относится к ковалентному или смешанному ионно-ковалентному типу.
Диэлектрик – кристалл, имеющий ширину запрещенной зоны много больше, чем энергия тепловых колебаний (Е>>kT), концентрация свободных электронов равна нулю. Электропроводность незначительна, слабо зависит от температуры. Как правило, это молекулярные кристаллы и вещества с ионным или ион-ковалентным типом химической связи.
Пример 1. Металлический кристалл Li. Валентные электроны 2s 1 . 2s-атомные орбитали образуют зону, которая заполнена только наполовину.
Пример 2. Металлический кристалл Mg. Валентные электроны 3s 2 . Валентная зона магния заполнена электронами полностью, свободные уровни, которые могли бы обеспечить перемещение электронов в валентной зоне, отсутствуют. Ближайшая по энергии зона, зона проводимости, образованная свободными 3p атомными орбиталями, перекрывается с валентной зоной.
Пример 3. Кристалл Si. Валентные электроны 3s 2 3p 2 . Кремний – ковалентный кристалл, связи осуществляются электронами, располагающимися на sp 3 -гибридных орбиталях, которые образуют как валентную зону, так и зону проводимости. Каждый атом кремния имеет 4 sp 3 -гибридные орбитали, то есть в кристалле, состоящем из N атомов, имеется 8N энергетических состояний электронов. Нижняя по энергии половина из них при Т=0 К полностью заселена, образуя валентную зону, а верхняя свободна, образуя зону проводимости. В отличие от магния, в кристалле кремния валентная зона и зона проводимости не перекрываются. Ширина запрещенной зоны составляет величину Eg=1,12 эВ. Кристалл кремния – полупроводник.
Пример 4. Кристалл NaCl. Химическая связь в этом кристалле относится к ионному типу. Валентную зону образуют заполненные орбитали Cl - – 3s 2 3p 6 , а зону проводимости свободные орбитали Na + – 3s 0 . В кристалле хлорида натрия, так же как и в случае с кристаллом кремния, валентная зона и зона проводимости не перекрываются. Но ширина запрещенной зоны много больше, чем у кремния, Eg = 7,7 эВ, хлорид натрия – диэлектрик.
Кристаллические материалы
Наиболее близким к идеальному понятию кристалл является монокристаллический материал. Монокристалл (монос – один) – твердое вещество с непрерывной кристаллической решеткой во всем объеме физического тела. Линейные размеры монокристаллов могут составлять доли микрометра и доходить до ~1 м. Монокристаллы, в силу своего внутреннего строения, обладают анизотропными свойствами. Анизотропия (анизос – неравный, тропос – направление) – зависимость физических и физико-химических свойств тела от направления в кристалле. Если в рассматриваемом физическом теле имеется несколько различным образом ориентированных, связанных между собой сильными химическими связями монокристаллов, то данное тело представляет собою блочный монокристалл. Границы отдельных блоков (монокристаллов) – дефекты кристаллической структуры.
Гораздо более распространены в природе твердые тела, состоящие из большого числа произвольно ориентированных относительно друг друга мелких монокристаллов, сцепленных как сильными, так и слабыми химическими связями. Такие тела называются поликристаллами (полис – многочисленный). Поликристаллические тела, вследствие усреднения анизотропных свойств отдельных произвольно ориентированных монокристаллов, обладают изотропией физических и физико-химических свойств.
Дефекты кристаллической решетки.
Другим типом дефектов являются нарушения регулярности решетки, связанные с примесями, которые появились в кристалле случайно (химические примеси) или были введены в него преднамеренно (легирующие добавки). С дефектами связаны многие физические и химические свойства кристаллов (электропроводность, прочность, оптические свойства, коррозионная стойкость и др.).
Различают точечные дефекты, одномерные (дислокации) и двумерные (поверхности, границы кристаллических зерен), объемные (пузыри). Дефекты возникают как в процессе кристаллизации, так и в результате внешних воздействий на кристалл. Создание дефектов связано с разрывом имеющихся химических связей между атомами кристалла или образованием дополнительных связей.
Точечные дефекты.
Простейшими из точечных дефектов в полупроводниках являются электроны проводимости и дырки. Электронно-дырочная пара образуются в результате асимметричного разрыва химической связи между атомами кристалла при поглощении тепловой энергии. При этом один из атомов приобретает избыточный отрицательный заряд за счет дополнительного валентного электрона (электрон проводимости), а другой – избыточный положительный заряд (дырка). Оба дефекта могут перемещаться по кристаллу независимо друг от друга. Электрон проводимости перемещается путем эстафетной передачи избыточного электрона от атома к атому, а дырка – путем эстафетного захвата электрона от атома к атому.
В процессе образования электронно-дырочных пар большую роль играют примесные атомы, находящиеся в узлах кристаллической решетки. Атомы примеси, имеющие число валентных электронов большее, чем число связей с ближайшими соседями (электронно-избыточные примеси), являются источником электронов проводимости. Образующиеся при этом дырки локализованы на примесном атоме и не могут мигрировать по кристаллу. Атомы примеси, имеющие число валентных электронов меньше, чем число связей с ближайшими соседями (электронно-дефицитные примеси), являются источником дырок, а электрон будет локализован на атоме примеси.
Энергия, необходимая для образования электронно-дырочных пар, может быть сообщена кристаллу не только нагреванием, но и при поглощении электромагнитного излучения. Причем энергия кванта электромагнитного излучения должна быть больше, чем ширина запрещенной зоны (энергии ионизации химической связи).
Необходимо отметить, что в кристаллах диэлектриков электронно-дырочные пары не образуются при подводе тепловой энергии из-за большой величины ширины запрещенной зоны. Они могут быть образованы при поглощении электромагнитного излучения достаточной энергии или ионизирующего излучения.
В кристаллах могут быть дефекты, образованные без разрыва химической связи, напримерэкситоны(от лат. excito – возбуждаю) – квазичастицы, представляющие собою возбужденные состояния атомов кристаллической решетки. Возбуждения могут передаваться от атома к атому, мигрируя по кристаллу.
Точечные дефекты, связанные с нарушением регулярности расположения частиц в кристалле, могут быть собственными – разупорядочение решетки, и примесными – присутствие в кристалле посторонних атомов (рис. 4.14).
Рис. 4‑14 Точечные дефекты в решетке ионного кристалла: A + G – катионы в узлах решетки; B - G − анионы в узлах решетки; вакансии: Vc – катионные; Va – анионные; межузельные ионы: A + I – катион; B - I − анион; примесные ионы в узле решетки: катион (P + G) или анион (P - G); примесный атом или ион в межузельном положении (PI)
Собственные дефекты: вакансия – отсутствие в узле решетки частицы, образующей кристалл; межузельные атомы или ионы.
В ионных кристаллах отсутствие в узле решетки катиона или аниона (катионные и анионные вакансии) нарушает баланс электрических зарядов в кристалле. Поэтому в кристалле должно быть либо равное количество катионных и анионных вакансий (дефекты Шоттки), либо на каждую ионную вакансию необходимо равное количество межузельных частиц того же знака (дефекты Френкеля).
Собственные дефекты образуются в кристалле в результате теплового движения частиц при температурах выше 0 К. Для создания собственного дефекта частица должна перейти из узла решетки в междоузлие, для этого частице необходимо преодолеть потенциальный барьер, который называется энергией образования дефекта (Ед). Вероятность преодоления потенциального барьера и образования дефекта определяется количеством частиц, имеющих энергию большую, чем энергия Ед. Из молекулярно-кинетической теории известно, что доля таких частиц зависит от температуры и пропорциональна множителю . Таким образом, каждой температуре соответствует равновесная концентрация собственных дефектов (n), которая экспоненциально увеличивается с ростом температуры:
где А – предэкспоненциальный множитель, k – константа Больцмана; T – температура, К.
Точечные примесные дефекты связаны с присутствием в твердом веществе химических примесей. Примесный атом или ион может находиться в узле решетки или в межузельном положении. Где будет находиться примесная частица, как правило, зависит от соотношения ее размеров и размеров частиц, образующих решетку.
Точечные дефекты вызывают нарушение регулярного расположения частиц кристалла в их ближайшем окружении (искажение кристаллической решетки), тем самым увеличивая энергию кристаллической решетки (рис. 4.15).
Рис. 4‑15. Искажение кристаллической решетки точечными дефектами. Электронные возбуждения: электроны (e - ) A+ē®A - , дырки (p + ) A-ē®A + , экситоны (ex 0 ) A * . Собственные точечные дефекты: вакансии (V), межузельные атомы (I) Примесный точечный дефект: решеточный примесный атом (PG), межузельный примесный атом (PI)
Дефекты могут захватывать электрон или отдавать его (захватывать дырки), могут взаимодействовать друг с другом, образовывая более сложные структуры (ассоциаты). Например, в щелочно-галоидных кристаллах (А + В - ) анионная вакансия может захватить электрон Vaē (электрон располагается на орбиталях катионов, окружающих анионную вакансию), и образуется так называемый F-центр. Если межузельный анион отдает электрон (захватывает дырку), то образуется H-центр (В 0 ), который может с ближайшим решеточным анионом образовать молекулярный ион В2 - (Vк-центр).
Линейные дефекты кристаллической решетки – дислокации.
Дислокации – дефекты кристаллической решетки, представляющие собой линии, вдоль которых нарушено правильное чередование атомных плоскостей. Дислокации появляются в кристалле в результате пластической деформации или в процессе роста кристалла. Простейшими типами дислокаций являются краевые и винтовые дислокации (рис. 4.16).
Рис. 4‑16 Краевая (а) и винтовая (б) дислокации.
Кристаллическая решетка в непосредственной близости от дислокации находится в искаженном состоянии, поскольку в ней размещается дополнительное число атомов. Нормальный порядок расположения атомов восстанавливается в обоих направлениях от дислокации на расстоянии нескольких постоянных решетки.
Плотность дислокаций (концентрация дислокаций) в кристалле бывает очень велика, достигая 10 6 дислокаций на 1 см 2 .
Аморфные твердые тела
В аморфных твердых телах, в отличие от кристаллов, в которых существует пространственная периодичность в равновесных положениях атомов, атомы колеблются около хаотически расположенных точек. Основные отличия свойств аморфных веществ от кристаллических связаны именно с нерегулярностью расположения частиц. Хотя в аморфных веществах отсутствует дальний порядок, на расстояниях, сравнимых с длиной химических связей, пространственное расположение ближайших соседних частиц сохраняется, то есть имеется ближний порядок.
Такая разупорядоченность структуры является следствием недостаточной подвижности частиц при кристаллизации. Частицы при достаточно быстром охлаждении теряют подвижность и не успевают образовать кристаллическую решетку, то есть занять места в пространстве, отвечающие минимуму энергии. Таким образом, аморфное состояние вещества является нестабильным, обладающим избыточной энергией, и при определенных условиях может самопроизвольно переходить в кристаллическое состояние. В отличие от кристаллов, для которых существует фиксированная температура плавления, переход аморфного вещества из твердого состояния в жидкое происходит в некотором температурном интервале. Аморфные тела обладают изотропностью физико-химических свойств.
Аморфное вещество, которое образуется при охлаждении жидкости и переходе ее в твердое состояние без кристаллизации, называется стеклом.
В стеклообразное состояние переходят вещества с преимущественно ковалентным типом связи, например, некоторые оксиды (SiO2, P2O5, B2O3). Стеклами являются также и большинство органических полимеров.
Для описания строения стеклообразного состояния вещества существуют две основные модели.
Теория кристаллитов рассматривает стекло как совокупность мельчайших монокристаллических областей – кристаллитов.
Теория непрерывной неправильной сетки предполагает, что в стекле, как и в монокристалле, существует пространственная сетка из химически связанных атомов. Но, в отличие от монокристалла, отсутствует строгое периодическое повторение фрагментов сетки.
Пример. Диоксид кремния (SiO2) может существовать как в кристаллическом состоянии – кварц, так и в стеклообразном - кварцевое стекло (плавленый кварц). И в том и в другом состоянии структурной единицей является тетраэдр SiO2, в центре которого находится ион кремния, а в вершинах – ионы кислорода. Тетраэдры связаны между собой через ионы кислорода, которые одновременно принадлежат двум тетраэдрам. В кристаллическом состоянии структура периодически повторяется, а в стеклообразном состоянии она искажена и не повторяется в объеме (рис. 4.17).
Рис. 4‑17 Проекция структуры кристаллического и стеклообразного SiO2: ● - атом кремния, ○ - атом кислорода
К аморфным веществам относятся также и мелкодисперсные порошки, состоящие из частиц, размер которых составляет величину порядка 10÷100 длин химической связи (наночастицы), например сажа – мелкодисперсный углерод. Вещество в таком состоянии, в отличие от поликристаллов, не имеет фиксированной температуры плавления.
Читайте также:
