Диаграммы состояния металлических систем
Обновлено: 03.05.2024
Бутыгин В.Б., Степаненко Н.А. Диаграммы фазового равновесия двойных систем
- формат pdf
- размер 3.08 МБ
- добавлен 30 июня 2012 г.
Учебное пособие. Алт гос. техн. ун-т им. И.И. Ползунова. – Барнаул: Изд-во АлтГТУ, 2010.- 84с. Изложены вопросы строения сплавов. Рассмотрены основные типы диаграмм состояния двойных сплавов и их строение. Разобрана диаграмма Fe-Ц и типы железоуглеродистых сплавов. Даны контрольные вопросы для проверки приобретенных знаний, а также индивидуальные задания по диаграмме Fe-Ц и по диаграммам состояния двойных систем.
Вол А.Е., Каган И.К. Строение и свойства двойных металлических систем. Т.4
- формат pdf
- размер 23,23 МБ
- добавлен 10 декабря 2014 г.
М.: Государственное издательство физико-математической литературы, 1979. — 576 с. В справочном руководстве даются сведения о диаграммах состояния, кристаллической структуре, физических и химических свойствах двойных сплавов и химических соединений. В первых трех томах были приведены данные о двойных металлических системах элементов, названия которых начинаются на буквы А — И (от азота до иттрия включительно). Настоящий четвертый том охватывает дв.
Кубашевски О. Диаграммы состояния двойных систем на основе железа (2/2)
- формат pdf
- размер 88,80 МБ
- добавлен 22 декабря 2016 г.
М.: Металлургия, 1985. — 184 с. Справочник содержит критически переработанные данные о диаграммах состояния двойных систем на основе железа и кристаллической структуре промежуточных фаз, представленные публикациями до конца 1981 г. Диаграммы состояния построены в основном по экспериментальным данным и в некоторых случаях, там, где это возможно, по результатам термодинамических расчетов. Книга рассчитана на самые широкие круги исследователей, прои.
Лякишев Н.П. Диаграммы состояний двойных металлических систем. Том 3. Книга 2
- формат djvu
- размер 5.35 МБ
- добавлен 12 декабря 2009 г.
Справочник в 3 томах: том 3, книга 2, 448 с. Приведены критически рассмотренные и обобщенные сведения о диаграммах состояния двойных металлических систем, знание которых необходимо для выбора и разработки промышленных металлических материаллов, технологии их производства и практического использования. Содержатся сведения об образующихся в соединениях и их кристаллических структурах, типах и температурах фазовых превращений, взаимных растворимостя.
Лякишев Н.П. Диаграммы состояния двойных металлических систем. В 3-х томах.Том 1-3
- формат djvu
- размер 34.38 МБ
- добавлен 11 января 2011 г.
Лякишев Н.П. Диаграммы состояния двойных металлических систем. Том 1
- формат djvu
- размер 14.33 МБ
- добавлен 12 декабря 2009 г.
Справочник в 3 томах: том 1, 992 с. Приведены критически рассмотренные и обобщенные сведения о диаграммах состояния двойных металлических систем, знание которых необходимо для выбора и разработки промышленных металлических материаллов, технологии их производства и практического использования. Содержатся сведения об образующихся в соединениях и их кристаллических структурах, типах и температурах фазовых превращений, взаимных растворимостях компоне.
Лякишев Н.П. Диаграммы состояния двойных металлических систем. Том 2
- формат djvu
- размер 15.1 МБ
- добавлен 12 декабря 2009 г.
Справочник в 3 томах: том 2, 1024 с. Приведены критически рассмотренные и обобщенные сведения о диаграммах состояния двойных металлических систем, знание которых необходимо для выбора и разработки промышленных металлических материаллов, технологии их производства и практического использования. Содержатся сведения об образующихся в соединениях и их кристаллических структурах, типах и температурах фазовых превращений, взаимных растворимостях компон.
Лякишев Н.П. Диаграммы состояния двойных металлических систем. Том 3, книга 1
- формат djvu
- размер 10.24 МБ
- добавлен 12 декабря 2009 г.
Справочник в 3 томах: том 3, книга 1, 872 с. Приведены критически рассмотренные и обобщенные сведения о диаграммах состояния двойных металлических систем, знание которых необходимо для выбора и разработки промышленных металлических материаллов, технологии их производства и практического использования. Содержатся сведения об образующихся в соединениях и их кристаллических структурах, типах и температурах фазовых превращений, взаимных растворимостя.
Торопцева Е.Л. Диаграммы состояния двойных систем
- формат djvu
- размер 739.26 КБ
- добавлен 06 ноября 2010 г.
Учебное пособие / Е. Л. Торопцева. -Липецк: ЛГТУ, 2008. -80 с. Приведены основы теории для практического навыка освоения курса «Диаграммы состояний», а также задачи для контроля знаний студентов. Предназначены для студентов 2 курса специальностей 150105.65 "Металловедение и термическая обработка металлов", 150702.65 "Физика металлов".
Хансен М., Андерко К. Структура двойных сплавов. Том 2
- формат pdf
- размер 43,05 МБ
- добавлен 05 ноября 2014 г.
М.: Металлургиздат, 1962. — 609 с. (1488 с. (сквозная нумерация с томом 1)). Книга является вторым, полностью переработанным изданием справочника Der Aufbau der Zweistofflegierungen, Springer — Verlag, Berlin, 1936. Co времени первого издания этой книги было опубликовано необычайно большое число работ по диаграммам состояния бинарных систем и по кристаллической структуре промежуточных фаз, причем эти работы были рассеяны по самым разнообразным ме.
Эллиот Р.П. Структуры двойных сплавов. Том 2
- формат pdf
- размер 27.82 МБ
- добавлен 20 августа 2013 г.
М.: Металлургия, 1970. — 472 с. Книга является дополнением к справочнику М. Хансена и К. Андерко «Структуры двойных сплавов» (Металлургиздат, 1962). В ней обобщены новые данные по 1719 двойным диаграммам состояния и кристаллическим структурам фаз, опубликованные в 1957—1961 гг., а также старые работы, не отраженные в справочнике. Большинство новых диаграмм состояния — это системы тугоплавких, редких, редкоземельных и радиоактивных металлов. Перв.
5. Диаграммы состояния сплавов
Сплавы можно получать при соединении большинства металлов друг с другом, а также с неметаллами. Диаграммы состояния сплавов дают наглядное представление о протекающих в сплавах превращениях в зависимости от их химического состава и температуры.
При построении диаграмм состояния сплавов на оси абсцисс указывают химический состав или концентрацию сплава в процентах. Для этого горизонтальную линию определенной длины делят на сто одинаковых частей и каждое деление принимают за 1 % одного из компонентов сплава.
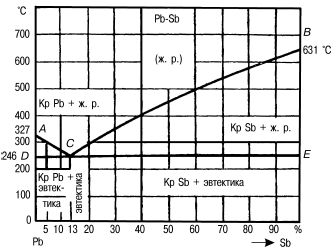
Рис. 5. Диаграмма состояния сплавов системы свинец—сурьма (Pb—Sb)
Точка А соответствует чистому свинцу, а точка В – чистой сурьме. По оси ординат в определенном масштабе указывают температуру. Для того чтобы построить диаграмму состояния сплавов, сначала строят ряд кривых охлаждения сплавов одних и тех же элементов с различной концентрацией.
На основе этих кривых строят диаграмму. Сплавы, компоненты которых при затвердевании образуют только механические смеси, относятся к первой группе. Диаграмма этих сплавов условно называется диаграммой состояния первого рода. Диаграмма сплавов, образующих при затвердевании только твердые растворы, называется диаграммой состояния второго рода. Наиболее типичными для диаграмм первого рода являются сплавы свинца с сурьмой.
Построение диаграммы (первого рода) состояния сплавов Pb—Sb:
1) кривые охлаждения доэвтектических сплавов;
2) диаграмма состояния сплавов Pb—Sb;
3) кривые охлаждения заэвтектических сплавов. Диаграмма построена для пяти видов сплава свинца с сурьмой:
1) 5 % сурьмы и 95 % свинца;
2) 10 % сурьмы и 90 % свинца;
3) 20 % сурьмы и 80 % свинца;
4) 40 % сурьмы и 60 % свинца;
5) 80 % сурьмы и 20 % свинца.
Все они имеют две критические температуры: верхнюю и нижнюю. Изучение процессов кристаллизации этих сплавов показывает, что верхняя критическая температура соответствует началу, а нижняя – концу затвердевания сплава. Таким образом, процесс кристаллизации сплавов Pb—Sb резко отличается от кристаллизации чистых металлов. Сплавы кристаллизуются в интервале температур, а чистые металлы – при постоянной температуре.
Механическая смесь кристаллов, выделяющихся из жидкого сплава одновременно, называется эвтектикой (в переводе с греческого – «хорошо сложенный»). Сплавы указанной концентрации называют эвтектическими. Линия АСВ на диаграмме называется линией ликвидуса (в переводе с греческого – «жидкий»). Выше этой линии любой сплав свинца с сурьмой находится в жидком состоянии. Линия ДСВЕ получила название линии солидуса (в переводе с греческого – «твердый»), или эвтектической линии. Точка С показывает состав эвтектики. Сплавы, расположенные левее этой точки, называют доэвтектическими, правее ее – заэвтектическими. В структуре доэвтектических сплавов, кроме эвтектики, всегда есть некоторое количество свинца, а в заэвтектических, кроме эвтектики, – сурьмы.
Данный текст является ознакомительным фрагментом.
Продолжение на ЛитРес
Аккумуляторы для мобильных устройств – оценка состояния
Аккумуляторы для мобильных устройств – оценка состояния Владимир ВасильевКак правило, большинство людей редко задумывается о состоянии аккумуля-тора своего мобильника, полагая, что он верой и правдой будет нам служить долгое время. Проходит время: месяц, два, три … . На
Оценка состояния аккумулятора потребителем
Оценка состояния аккумулятора потребителем Оценка реальной электрической емкости. Сделать это можно двумя способами. Первый способ – качественный и очень приблизительный. Заключается он в примерной оценке среднего времени продолжительности работы вашего мобильника.
Профессиональная оценка состояния аккумулятора
Профессиональная оценка состояния аккумулятора Тут уж не посидишь перед зарядным устройством с часами в руках. Особенно когда необходимо произвести входной контроль, например, сотни аккумуляторов. Для принятия решений в этом случае требуются количественные и точные
5.2.3. Экранные состояния объектов
5.2.3. Экранные состояния объектов Элементы человекоориентированного интерфейса должны быть доступными для начинающего пользователя и эффективными для опытного пользователя, причем переход от одного к другому не должен требовать переучивания. Хороший интерфейс должен
13.2.3. Общий обзор состояния производства наночастиц
13.2.3. Общий обзор состояния производства наночастиц Коммерческое использование любого метода должно быть обосновано экономически. В лабораторных условиях ученым удалось разработать множество интересных и красивых способов синтеза нанопорошков, но очень многие из них
18.2. Обзор состояния и перспектив промышленности
18.2. Обзор состояния и перспектив промышленности В настоящее время можно уверенно утверждать, что примерно к 2015 году осуществляемые и планируемые научно-технические разработки в области нанотехнологий приведут к весьма серьезным качественным и количественным
17.Основные термодинамические параметры состояния газа
17.Основные термодинамические параметры состояния газа ДавлениеР – мера силы, которая действует на единицу поверхности:Р = lim ?Fn / ?S = dFn/ dS,где DS ? 0; ?Fn – сила, направленная перпендикулярно участку поверхности.Удельный объемV – величина, обратная плотности rвещества:v = 1 / r= dV/
18. Состояния тел. Термодинамическая система. Адиабатический процесс
18. Состояния тел. Термодинамическая система. Адиабатический процесс Существуют три агрегатных состояния: твердое, жидкое и газообразное.Если параметры системы не изменяется со временем, то можно говорить о термодинамическом равновесии системы.Совокупность тел и полей,
25. Уравнение состояния идеального газа
25. Уравнение состояния идеального газа Уравнение состояния идеального газа описывает связь между его температурой и давлением. Поскольку давление идеального газа в замкнутой системе P = 1/3 О mn<v2>, P= nkT, то уравнение идеального газа будет выглядеть следующим образом:P =
26. Универсальное уравнение состояния идеального газа
26. Универсальное уравнение состояния идеального газа Отношение массы mгаза (вещества) к количеству газа (вещества) vэтой системы называют молярной массой газа (вещества):М = m/ v.Размерность молярной массы следующая: [M] = 1 кг / 1 моль.Следствие из закона Авогадро позволяет
41. Уравнение состояния Ван-дер-Ваальса
41. Уравнение состояния Ван-дер-Ваальса В общем случае для реальных газов при вычислении параметров состояния нельзя использовать уравнение состояния pv = RT,которое верно для идеальных газов.Общее уравнение состояния для реальных газов. в котором коэффициенты Bi –
43. Частные производные параметров состояния. Термические коэффициенты
43. Частные производные параметров состояния. Термические коэффициенты Свойства реальных веществ описываются термическими коэффициентами.Определение 1. Коэффициентом объемного расширенияaназывается изменение объема вещества при повышении его температуры на один
3.3. Диаграммы состояния ювелирных сплавов
3.3. Диаграммы состояния ювелирных сплавов В ювелирной технике применяются сплавы на основе благородных металлов: серебра, золота и платины. Это основные металлы. Для имитации золотых и серебряных сплавов используют некоторые сплавы на основе меди и алюминия. Они
26. Выбор сплавов для определенного назначения на основе анализа диаграмм состояния
26. Выбор сплавов для определенного назначения на основе анализа диаграмм состояния Чистые металлы используют в электрорадиотехнике (проводниковые, электровакуумные). Основнымиконструкционными материалами являются металлические сплавы. Сплавом называют вещество,
27. Строение и свойства железа; метастабильная и стабильная фазовые диаграммы железо-углерод. Формирование структуры углеродистых сталей. Определение содержания углерода в стали по структуре
27. Строение и свойства железа; метастабильная и стабильная фазовые диаграммы железо-углерод. Формирование структуры углеродистых сталей. Определение содержания углерода в стали по структуре Сплавы железа с углеродом являются самыми распространенными металлическими
Диаграммы состояния двойных металлических систем

ОГЛАВЛЕНИЕ
Предисловие.
Ac—Ag. Актиний—серебро.
Ac—Аи. Актиний—золото . .
Ас—В. Актиний—бор . . . .
Ac—Be. Актиний—бериллий
Ас—Сг. Актиний—хром . . .
Ас—Н. Актиний—водород .
Ас—Мо. Актиний—молибден
Ас—О. Актиний—кислород
Ac—Pt. Актиний—платина .
Ag—-Аl. Серебро—алюминий
Ag—Аг. Серебро—аргон . . .
Ag—As. Серебро—мышьяк .
Ag—At. Серебро—астатин .
Ag—Аи. Серебро—золото . ,
Ag—В. Серебро—бор.
Ag—Ва. Серебро—барий . . .
Ag—Be. Серебро—бериллий
Ag—Bi. Серебро—висмут . .
Ag—С. Серебро—углерод . .
Ag—Са. Серебро—кальций .
Ag—Cd. Серебро—кадмий . .
Ag—Се. Серебро—церий . . .
Ag—Со. Серебро—кобальт . .
Ag—Сг. Серебро—хром . . .
Ag—Cs. Серебро—цезий . . .
Ag—Си. Серебро—медь .
Ag—Dy. Серебро—диспрозий
Ag—Ег. Серебро-тэрбий . . .
Ag—Ей. Серебро—европий ,
Ag—Fe. Серебро—железо . .
Ag—Ga. Серебро-таллий . .
Ag—Gd- Серебро-гадолиний
Ag—Ge. Серебро—германий
Ag—Н. Серебро-Водород
Ag—Hf. Серебро—гафний . .
Ag—Hg. Серебро—ртуть . . ,
Ag—Но. Серебро—гольмий .
Ag—In. Серебро—индий
Ag—Ir. Серебро—иридий .
Al—Am. Алюминий—америций
Al—As. Алюминий—мышьяк
Al—Au. Алюминий—золото . .
Al—В. Алюминий—бор.
Al—Ва. Алюминий—барий . . .
Al—Be. Алюминий—бериллий
Al—Bi. Алюминий—висмут . .
А1—С. Алюминий—углерод . .
А1—Са. Алюминий—кальций .
Al—Cd. Алюминий—кадмий . .
М—Се. Алюминий—церий . .
А1—Со. Алюминий—кобальт . .
А1—Сг. Алюминий—хром . . .
Al—Cs. Алюминий—цезий . . .
А1—Си. Алюминий—медь . . . .
Al—Dy. Алюминий—диспрозий
А1—Ег. Алюминий—эрбий . . .
А1—Ей. Алюминий—европий .
Al—Fe. Алюминий—железо . .
Al—Ga. Алюминий—галлий . .
Al—Gd. Алюминий—гадолиний
Al—Ge. Алюминий—германий
Al—Н. Алюминий—водород
Al—Hf. Алюминий—гафний . .
Al—Hg. Алюминий—ртуть . . .
А1—Но. Алюминий—гольмий .
Al—I. Алюминий—иод
Al—In. Алюминий—индий . . .
Al—Ir. Алюминий—иридий . .
А1—К. Алюминий—калий . . .
Al—La. Алюминий—лантан . .
Al—Li. Алюминий—литий . . .
Al—Lu. Алюминий—лютеций .
Al—Mg. Алюминий—магний . .
А1—Мп. Алюминий—марганец
А1—Мо. Алюминий—молибден
А1—N. Алюминий—азот . . . .
Al—Na. Алюминий—натрий . .
Al—Nb. Алюминий—ниобий . .
Al—Nd. Алюминий—неодим . .
Al—Ni. Алюминий—никель . .
Al—Np. Алюминий—нептуний
А1—О. Алюминий—кислород .
Al—Os. Алюминий—осмий . . .
А1—Р. Алюминий—фосфор . .
Al—-РЬ. Алюминий—свинец . .
Al—Pd. Алюминий—-палладий
А1—Рг. Алюминий—празеодим
Al—Pt. Алюминий—платина .
Al—Pu. Алюминий—плутоний
Al—Rb. Алюминий—рубидий .
Al^Re. Алюминий—рений . . .
Al—Rh. Алюминий—родий . . .
Al—Ru. Алюминий—рутений .
Al—S. Алюминий—сера . . . .
Al—Sb. Алюминий—сурьма . .
Al—Sc. Алюминий—скандий .
Al—Se. Алюминий—селен . . .
Al—Si. Алюминий—кремний .
Al—Sm. Алюминий—самарий .
Al-^Sn. Алюминий—олово . . .
Al—Sr. Алюминий—стронций
Al—Та. Алюминий—тантал . .
Al—ТЬ. Алюминий—тербий . .
А1—Те. Алюминий—теллур . .
A3—Тп. Алюминий—торий . . .
Al—Ti. Алюминий—титан . . .
Al—Т1. Алюминий-таллий . .
А1—Тш. Алюминий—тулий . . .
Al—U. Алюминий—уран . . . .
Al—V. Алюминий—ванадий .
Al—W. Алюминий—вольфрам
Al—Y. Алюминий—иттрий . .
A3—Yb. Алюминий—иттербий .
Al—Zn. Алюминий—цинк . . .
Al—Zr. Алюминий—цирконий
Am—Be. Америций—бериллий .
Am—С. Америций—углерод . .
Am—Сг. Америций—хром
Am—Fe. Америций—железо . .
Am—Н. Америций—водород . .
Am—N. Америций—азот . . . .
Am—О. Америций—кислород .
Am—Pt. Америций—платина . .
Am—Pu. Америций—плутоний .
Am—S. Америций—сера . . . .
As—Аи. Мышьяк—золото
Cf—Mo. Калифорний—молибде
CI—Mo. Хлор—молибден .
CI—Re. Хлор—рений .
CI—Те. Хлор—теллур.
Cm—Сг. Кюрий—хром .
Cm—О. Кюрий—кислород . . .
Со—Сг. Кобальт—хром.
Со—Си. Кобальт—медь .
Со—Dy. Кобальт—диспрозий .
Со—Ег. Кобальт—эрбий .
Со—Fe. Кобальт—железо .
Со—Ga. Кобальт—галлий .
Со—Gd. Кобальт—гадолиний .
Со—Ge. Кобальт—германий . .
Со—Н. Кобальт—водород . . .
Со—Hf. Кобальт—гафний . . .
Со—Но. Кобальт—гольмий . . .
Со—In. Кобальт—индий .
Со—Ir. Кобальт—иридий . . .
Со—К. Кобальт—калий .
Со—La. Кобальт—лаптан .
Со—Li. Кобальт—литий .
Со—Lu. Кобальт—лютеций . .
Со—Mg. Кобальт—магний . . .
Со—Мп. Кобальт—марганец . .
Со—Мо. Кобальт—молибден . .
Со—N. Кобальт—азот.
Со—Na. Кобальт—натрий .
Со—No. Кобальт—ниобий . . .
Со—Nd. Кобальт—неодим . . .
Со—N1. Кобальт—никель .
Со—О. Кобальт—кислород . .
Со—Os. Кобальт—осмий .
Со—РЬ. Кобальт—свинец .
Со—Pd. Кобальт—палладий . .
Со—Рг. Кобальт—празеодим .
Со—Pt. Кобальт—платина . . .
Со—Pu. Кобальт—плутоний . .
Со—Re. Кобальт—рений .
Со—Rh. Кобальт—родий .
Со—Ru. Кобальт—рутений . . .
Со—S. Кобальт—сера .
Co—Sb. Кобальт—сурьма . .
Со—Sc. Кобальт—скандий .
Со—Se. Кобальт—селен . . .
Со—Si. Кобальт—кремний
Со—Sm. Кобальт—самарий .
Со—Sn. Кобальт—олово-. . .
Со—Та. Кобальт—тантал . .
Со—ТЬ. Кобальт—тербий . .
Со—Тс. Кобальт—технеций
Со—Те. Кобальт—теллур . .
Со—Th. Кобальт—торий . .
Со—Ti. Кобальт—титан . . .
Со—TI. Кобальт—таллий . .
Со—Тт. Кобальт—тулий . .
Со—L. Кобальт—уран . . .
Со—V. Кобальт—ванадий .
Со—W. Кобальт—вольфрам
Со—Y. Кобальт—иттрий . .
Со—Yb. Кобальт—иттербий
Со—Zn. Кобальт—цинк . . .
Со—Zr. Кобальт—цирконий
Сr—Cs. Хром—цезий . . . .
Сr—Си. Хром—медь .
Сr—Dy. Хром—диспрозий .
Сr—Ег. Хром—эрбий . . . .
Сr—Ей. Хром—европий . . .
Сr—Fe. Хром—железо . . .
Сr—Ga. Хром—галлий . . . .
Сr—Gd. Хром—гадолиний .
Сr—Ge. Хром—германий . .
Сr—H. Хром—водород . . .
Сr—Gf. Хром—гафний . . .
Сr—Hg. Хром—ртуть.
Сr—Но. Хром—гольмий . . .
Сr—In. Хром—индий . . . .
Сr—Ir. Хром—иридий . . .
Сr—К. Хром—калий . . . .
Сr—La. Хром—лантан . . . .
Сr—Li. Хром—литий . . . .
Сr—Lu. Хром—лютеций . .
Сr—Mg. Хром—магний . . .
Сr—Мn. Хром—марганец . .
Сr—Мо. Хром—молибден . .
Cr—N. Хром—азот . . .
Сг—Na. Хром—натрий .
Cr—Nb. Хром—ниобий .
Cr—Nd. Хром—неодим .
Cr—Ni. Хром—никель .
Cr—Np. Хром—нептуний
Сг—О. Хром—кислород
Сг—Os. Хром—осмий . .
Сг—Р. Хром—фосфор .
Сг—РЬ. Хром—свинец . .
Сг—Pd. Хром—палладий
Сг—Рг. Хром—празеодим
Cr—Pt. Хром—платина .
Cr—Pu. Хром—плутоний
Cr—Rb. Хром—рубидий
Cr—Re. Хром—рений . .
Cr—Rh. Хром—родий . .
Сг—Ru. Хром—рутений .
Cr—S. Хром—сера . . . .
Сг—Sb. Хром—сурьма . . .
Cr—Sc. Хром—скандий . .
Cr—Se. Хром—селен . . . .
Cr—Si. Хром—кремний
Cr—Sm. Хром—самарий
Сг—Sn. Хром—олово . . .
Сг—Та. Хром—тантал . . .
Cr—ТЬ. Хром—тербий . . .
Сг—Тс. Хром—технеций .
Сг—Те. Хром—теллур . . .
Cr—Th. Хром—торий . . .
Сг—Ti. Хром—титан . . .
Сг—Тт. Хром—тулий . . .
Сг—U. Хром—уран . . . .
Cr—V. Хром—ванадий . .
Cr—W Хром—вольфрам .
Cr—Y. Хром—иттрий . .
Cr—Yb. Хром—иттербий .
Cr—Zn. Хром—цинк . . . .
Сг—Zr. Хром—цирконий
Cs—Cu. Цезий—медь . . .
Cs—Fe Цезий—железо . .
Cs—Ga. Цезий—галлий . .
Cs—Ge. Цезий—германий
Cs—Н. Цезий—водород .
Cs—Hf. Цезий—гафний
Cs—Hg. Цезий—ртуть . . .
Cs—In. Цезий—индий . .
Cs—К Цезий—калий . .
Cs—Li. Цезий—литий . .
Cs—Mg. Цезий—магний . .
As—В. Мышьяк—бор .
As—Ва. Мышьяк—барий
As—Be. Мышьяк—бериллий . .
As—Bi. Мышьяк—висмут . . . .
As—Bk. Мышьяк—берклий . . .
As—С. Мышьяк—углерод . . .
As—Са. Мышьяк—кальций . . .
As—Cd. Мышьяк—кадмий . . .
As—Се. Мышьяк—церий . . . .
Cs—Mo. Цезий—молибден
Cs—N. Цезий—азот . .
Cs—Na. Цезий—натрий
Cs-Nb. Цезий-ниобий
Cs—О. Цезий—кислород
Cs—Pb. Цезий—снинец
Cs—Рг. Цезий—празеодим
Dy—Mo. Диспрозий—молибден
Dy—Nb. Диспрозий—ниобий
Dy—Nd. Диспрозий—неодим
Dy—Ni. Диспрозий—никель .
Dy—Pb. Диспрозий—свинец .
Dy—Pd. Диспрозий—палладий
Dy—Pr. Диспрозий—празеод^
Dy—Pm. Диспрозий—прометий
Dy—Re. Диспрозий—рений .
Dy—S. Диспрозий—сера . .
Dy—Sb. Диспрозий—сурьма .
Dy—Sc. Диспрозий—скандий
Dy—Si. Диспрозий—кремний
Dy—Sm. Диспрозий—самарий
Dy—Та. Диспрозий—тантал .
Dy—Tb. Диспрозий—тербий .
Dy—Те. Диспрозий—теллур .
Dy—Th. Диспрозий—торий
Dy—Тт. Диспрозий—тулий
Dy—W, Диспрозий—вольфрам
Dy—Y. Диспрозий—иттрий .
Dy—Zr. Диспрозий—цирконий
Er—Fe. Эрбий—железо . .
Ег—Ga. Эрбий—галлий . .
Ег—Gd. Эрбий—гадолиний
Er—Ge. Эрбий—германий
Ег—Н. Эрбий—водород
Ег—Ш. Эрбий—гафний
Er—Hg. Эрбий—ртуть .
Ег—Но. Эрбий—гольмий
Er—In. Эрбий—индий
Ег—La. Эрбий—лантан
Er—Lu. Эрбий—лютеций
Ег—Mg. Эрбий—магний . .
Ег—Мп. Эрбий—марганец
Ег—Мо. Эрбий—молибден
Er—Nb. Эрбий—ниобий . .
Er—Nd- Эрбий—неодим . .
Ег—Ni. Эрбий—никель . .
Ег—О. Эрбий—кислород
Er—Pd. Эрбий—палладий
Ег—Pm. Эрбий—прометий
Ег—Ро. Эрбий—полоний .
Ег—Рг. Эрбий—празеодим
Ег—Pt Эрбий—платина .
Er—Pu. Эрбий—плутоний
Ег—Re. Эрбий—рений . .
Er—Rh. Эрбий—родий . .
Ег—S. Эрбий—сера .
Er—Sb. Эрбий—сурьма . .
Ей—Y. Европий—иттрий .
Ей—Yb. Европий—иттербий
Ей—Zn. Европий—цинк . . .
Eu—Zr. Европий—цирконий
F—Ru. Фтор—рутений . . .
Fe—Ga. Железо—галлий , .
Fe—Gd. Железо—гадолиний
Fe—Ge. Железо—германий
Fe—H. Железо—водород .
Fe—Hf. Железо—гафний .
Fe—Hg. Железо—ртуть . . .
Fe—Но. Железо—гольмий .
Fe—In. Железо—индий . .
Fe—1г. Железо—иридий . .
Fe—К. Железо—калий . . .
Fe—Кг. Железо—криптон .
Fe—La. Железо—лантан . .
Fe—Li. Железо—литий . . .
Fe—Lu. Железо—лютеций .
Fe—Mg. Железо—магний . ,
Fe—Мп. Железо—марганец
Fe—Мо. Железо—молибден
Fe—N. Железо—азот .
Fe—Na. Железо—натрий . .
Fe—Nb. Железо—ниобий . .
Fe—Nd. Железо—неодим .
Fe—Ni. Железо—никель . .
Fe—О. Железо—кислород
Fe—Os. Железо—осмий . .
Fe—Р. Железо—фосфор
Fe—Pb. Железо—свинец . -
Fe—Pd. Железо—палладий
Fe—Рот. Железо—прометий
Fe—Рг. Железо—празеодим
Fe—Pt. Железо—платина .
Fe—Pu. Железо—плутоний
Fe—Re. Железо—рений . . .
Fe—Rh, Железо—родий . . .
Fe—Rn. Железо—радон
Fe—Ru. Железо—рутений ,
Fe—S. Железо—сера . . . .
Fe—Sb. Железо—сурьма . .
Fe—Sc. Железо—скандий .
Fe—Sc. Железо—селен . . ,
Fe—Si. Железо—кремний .
Fe—Sm. Железо—самарий .
Fe—Sn. Железо—олово . . .
Fe—Sr. Железо—стронций
Fe—Т. Железо—тритий . .
Fe—Та. Железо—тантал
Cs—Rb. Цезий—рубидий
Cs—S. Цезий—сера .
Cs—Sb. Цезий—сурьма
Cs—Se. Цезий—селен .
Cs—Si. Цезий—кремний
Cs—Sn. Цезий—олово . .
Cs—Sr. Цезий—стронций
Cs—Те. Цезий—теллур
Cs—Ti. Цезий—титан .
Cs—TI. Цезий—таллий
Cs—V. Цезий—ванадий
Cs—Y. Цезий—иттрий
Cs—Zn. Цезий—цинк .
Cs—Zr. Цезий—цирконий
Си—Dy. Медь—диспрозий
Си—Кг. Медь—эрбий
Си—Ей. Медь—европий
Си—Fe Медь—железо .
Си—Ga. Медь—галлий .
Си—Gd. Медь—гадолиний
Си—Ge. Медь—германий
Си—Н. Медь—водород
Си—Hf. Медь—гафний
Си—Hg. Медь—ртуть . .
Си—Но. Медь—гольмий
Си—In. Медь—индий .
Си—Ir. Медь—иридий
Си—К. Медь—калий .
Си—La. Медь—лантан .
Си—Li. Медь—литий .
Си—Lu. Медь—лютеций
Си—Mg. Медь—магний .
Си—Мп, Медь—марганец
Си—Мо. Медь—молибден
Си—N. Медь—азот . . .
Си—Na. Медь—натрий .
Си—Nb. Медь—ниобий
Си—Nd. Медь—неодим .
Си—Ni. Медь—никель .
Си—О. Медь—кислород
Си—Os. Медь—осмий .
Си—Р- Медь-фосфор
Си—РЬ. Медь—свинец
Cu—Pd. Медь—палладий . . .
Си—Рт. Медь— прометий . . .
Си—Ро. Медь—полоний .
Си—Рг. Медь—празеодим . .
Си—Pt. Медь—платина .
Си—Pu. Медь—плутоний . . .
Си—Rb. Медь—рубидий .
Си—Re. Медь—рений .
Си—Rh. Медь—родий .
Си—Ru. Медь—рутений .
Си—S. Медь—сера.
Си—Sb. Медь—сурьма.
Си—Sc. Медь—скандий .
Си—Se. Медь—селен.
Си—Si. Медь—кремний .
Си—Sm. Медь—самарий .
Си—Sn. Медь—олово.
Си—Sr. Медь—стронций . . .
Си—Та. Медь—тантал.
Си—ТЬ. Медь—тербий.
Си—Тс. Медь—технеций . . .
Си—Те. Медь—теллур.
Си—Th. Медь—торий .
Си—Ti. Медь—титан.
Си—Т1. Медь—таллий.
Си—Тт. Медь—тулий .
Си—U. Медь—уран .
Си—V. Медь—ванадий .
Си—W. Медь—вольфрам . . .
Си—Y. Медь—иттрий.
Си—Yb. Медь—иттербий . . .
Си— Zn. Медь—цинк.
Си—Zr. Медь—цирконий . . .
D— Fe. Дейтерий—железо
D— Nb. Дейтерий—ниобий .
D—Та. Дейтерий—тантал . .
D—V. Дейтерий—ванадий .
D—Zr. Дейтерий—цирконий
Dy—Ег. Диспрозий—эрбий
Dy—be. Диспрозий—железо .
Dy—Ga. Диспрозий—галлий .
Dy— Н Диспрозий—водород
Dy—Hg. Диспрозий—ртуть . .
Dy—Но. Диспрозий—гольмий
Dy—In. Диспрозий—индий .
Dy—Ir. Диспрозий—иридий
Dy—La. Диспрозий—лантан .
Dy—Lu. Диспрозий—лютеций
Dy—Mg. Диспрозий—магний
Dy—Мп. Диспрозий—марганец
Диаграмма состояния системы железо – хром (Fe-Cr)
Наиболее ранние исследования сплавов системы относятся к началу текущего столетия. К этому времени были достаточно точно установлены кривые плавкости, область существования твердых растворов хрома в γ - Fe , а также концентрационные и температурные пределы образования σ -фазы.
Диаграмма состояния в обобщенном виде по данным приведена на рис. На кривых ликвидус и солидус при 22 % (ат.) С r и 1507 °С наблюдается минимум. Хром стабилизирует о. ц. к. модификации железа и образует с этими модификациями непрерывные ряды твердых растворов. Область твердых растворов хрома в г. ц. к. модификации железа сравнительно узкая и простирается до 13,3 % (ат.) С r . Хром снижает температуру полиморфного α↔γ - превращения железа от 910 до 830 °С при содержании ~7,5 % (ат.). При дальнейшем увеличении содержания хрома эта температура резко возрастает. При содержании в сплавах —50% (ат.) С r и температуре ~815°С происходит фазовая перекристаллизация α -твердого раствора с образованием так называемой α -фазы. Реакция α ↔ σ протекает крайне медленно, и необходимы продолжительные выдержки для ее завершения. Фаза σ обладает сложной тетрагональной структурой с 30 атомами в элементарной ячейке и обычно образуется в системах - на основе переходных металлов. Фазы σ, как правило, обладают достаточно широкими областями гомогенности. В системе железо — Хром эта область при 600 °С простирается от 43 до 49 % (ат.) С r . Периоды решетки σ -фазы а =0,880 нм, с=0,5444 нм и мало изменяются в пределах области гомогенности.
В сплавах системы образуются три сверхструктурные фазы β, θ, σ с областями гомогенности 41,9—44,2 % (ат.) С r ; 45,7—47,2 % (ат.) С r и 49,2—51,5 % (ат.) С r . В настоящее время методами высокотемпературного термического анализа и измерением электросопротивления показано, что Хром является мономорфным металлом.
При содержании 0,001 % (по массе) С и 0,002 % (по массе) N также при изменении концентрации углерода и азота в указанных пределах несколько смещается в сторону увеличения содержания хрома (на 0,7—0,8 %) положение γ/(α+γ)- и (α + γ)/α -границ двухфазной области, разделяющей γ- и α -твердые растворы.
На основе измерения электросопротивления, твердости и намагниченности построена низкотемпературная часть диаграммы состояния системы железо — Хром . Ниже 550 °С твердый раствор α и σ -фаза становятся неустойчивыми и расслаиваются на два твердых раствора (богатых и бедных хромом) с о. ц. к. решеткой. В отсутствие σ -фазы расслоение α -твердого раствора начинается при более высокой температуре. На рис. приведена низкотемпературная часть диаграммы состояния системы железо — хром, штриховой линией показано начало расслоения α -твердого раствора при отсутствии σ -фазы.
Наличие области расслоения в системе согласуется с термодинамическими данными, а именно: положительным отклонением от закона идеальных растворов и положительной теплотой смещения. Это означает, что твердые растворы а- и σ -фаза при понижении температуры становятся менее устойчивыми и должны распадаться на твердые растворы с меньшим и большим содержанием хрома . Температурный интервал стабильности σ -фазы соответствует 440—820 °С.

УДК 669.017.11
Диаграммы состояния двойных металлических систем: Справочник: В 3 т.: Т.2 / Под общ. ред. Н.П. Лякишева. — М.: Машиностроение, 1997. — 1024 с, ил.
ISBN 5-217-01569-1
УДК 669.017.11
Диаграммы состояния двойных металлических систем: Справочник: В 3 т.: Т.
3. Кн. 2 / Под общ. ред. Н.П. Лякишева. -М.: Машиностроение, 2000. - 448 с: ил.
ISBN 5-217-02932-3
Агеев Н.В. (ред) Диаграммы состояния металлических систем, опубликованные в 1964 году. Выпуск 10
- формат djvu
- размер 7.84 МБ
- добавлен 16 января 2012 г.
Приложение к журналу "Металлургия" и выпуску "Металловедение и термическая обработка" за 1966 год. Москва (Люберцы), Производственно-издательский комбинат ВИНИТИ, 1966, 240 страниц в соответствии с нумерацией в книге, в файле - 314 страниц не считая обложек.
Банных О.А., Будберг П.Б., Алисова С.П. и др. Диаграммы состояния двойных и многокомпонентных систем на основе железа
- формат djvu
- размер 7.7 МБ
- добавлен 08 августа 2010 г.
Справ. изд. М.: Металлургия. 1986. 440 с. Приведены обширные и наиболее достоверные данные о диаграммах состояния систем на основе железа. Впервые обобщены сведения о трех- и многокомпонентных диаграммах, которые позволят обосновать и быстро определить оптимальный состав сплава, режим его плавки, литья, обработки давлением и термической обработки, что имеет очень большое значение для правильного выбора конструкционных сплавов, содержащих нескольк.
Диаграммы состояния металлических систем, опубликованные в 1969 году. Выпуск 15
- формат djvu
- размер 6.53 МБ
- добавлен 08 января 2012 г.
Приложение к журналу "Металлургия" и выпуску "Металловедение и термическая обработка" за 1971 год. Москва (Люберцы), Производственно-издательский комбинат ВИНИТИ, 1971, 263 с. Под ред. Н.В.Агеева
Диаграммы состояния металлических систем, опубликованные в 1972 году. Выпуск 18
- формат djvu
- размер 7.87 МБ
- добавлен 08 января 2012 г.
Приложение к журналу "Металлургия" и выпуску "Металловедение и термическая обработка" за 1974 год. Москва (Люберцы), Производственно-издательский комбинат ВИНИТИ, 1975, 268 с. Под ред. Н.В.Агеева
Иванов В.Е., Папиров И.И., Тихинский Г.Ф., Амоненко В.М. Чистые и сверхчистые металлы
- формат pdf
- размер 19.05 МБ
- добавлен 11 апреля 2011 г.
М.: Металлургия. 1965. 263 с. В монографии рассмотрена теория разделения металлов при испарении, даны расчеты разделения двойных металлических систем. Рассмотрены достоинства и недостатки разделения металлов в глубоком вакууме. Описана аппаратура, используемая для дистилляции.
Лякишев Н.П. и др. Алюминотермия
- формат djvu
- размер 9.8 МБ
- добавлен 20 октября 2011 г.
М.: Металлургия, 1978. - 424 с. УДК 669.168.5 Ил_182_Табл_128_Список лит-222 назв. Лякишев Н.П., Плинер Ю.Л., Игнатенко Г.Ф., Лаппо С. И. Книга посвящена вопросам теории алюминотермического процесса, находящего широкое применение при производстве чистых металлов, ферросплавов и лигатур. В ней рассматриваются физико-химические основы взаимодействия окислов металлов с алюминием; излагаются термодинамические условия протекания восстановительных ре.
- формат pdf
- размер 20.77 МБ
- добавлен 29 октября 2010 г.
М.: Металлургия, 1978. - 424 с. Лякишев Н.П., Плинер Ю.Л., Игнатенко Г.Ф., Лаппо С. И. УДК 669.168.5 Ил .182. Табл .128. Список лит.: 222 назв. Книга посвящена вопросам теории алюминотермического процесса, находящего широкое применение при производстве чистых металлов, ферросплавов и лигатур. В ней рассматриваются физико-химические основы взаимодействия окислов металлов с алюминием; излагаются термодинамические условия протекания восстановител.
Лякишев Н.П. Энциклопедический словарь по металлургии. В двух томах
- формат pdf
- размер 88.46 МБ
- добавлен 24 февраля 2010 г.
М.: Интермет Инжиниринг, 2000. – 821 с. Гл. ред. Н.П. Лякишев В Словаре помещены более 6000 статей-терминов, содержащих систематизированные сведения по металлургии как области науки и производства, а также смежным ей научным дисциплинам и отраслям промышленности. Для инженерно-технических работников всех специальностей, может быть полезен широкому кругу читателей, интересующихся вопросами техники.
Райнз Ф. Диаграммы фазового равновесия в металлургии
- формат pdf
- размер 14.42 МБ
- добавлен 22 сентября 2011 г.
Перевод с англ. – М.: Металлургиздат, 1960. – 376 с. В книге излагаются основы учения о диаграммах равновесия сплавов из одного, двух, трех и четырех компонентов. Описание диаграмм состояния иллюстрируется многочисленными примерами из практической металлографии и термической обработки черных и цветных металлов и сплавов. Каждая глава книги содержит практические упражнения, помогающие читателю приобрести навыки самостоятельного пользования диаграм.
Савицкий Е.М., Терехова В.Ф., Буров И.В. Сплавы редкоземельных металлов
- формат pdf
- размер 29.79 МБ
- добавлен 24 апреля 2011 г.
М.: Издательство Академии наук СССР, 1962. - 268с. В монографии представлен большой экспериментальный материал авторов и последние литературные данные по физико-химическим свойствам редкоземельных металлов, иттрия и скандия. Приведены диаграммы состояния двойных и тройных металлических систем редкоземельных металлов с элементами периодической системы с рассмотрением общих принципов легирующего поведения редкоземельных металлов. Дано подробное опи.
Читайте также:
