Электронное строение и классификация металлов
Обновлено: 05.05.2024
Если провести в Периодической таблице Д.И. Менделеева символическую линию из верхнего левого угла в нижний правый угол, то все элементы, находящиеся ниже этой линии, будут металлами.
Металлы можно охарактеризовать при помощи нескольких свойств, которые будут общими для всех элементов. К таким характеристикам следует отнести высокую электрическую проводимость и теплопроводность, пластичность, благодаря которой металлы можно подвергать ковке, прокатке, штамповке или вытягиванию в проволоку, металлический блеск и непрозрачность.
В зависимости от температуры кипения все металлы подразделяют на тугоплавкие (Tкип> 1000 o С) и легкоплавкие (Tкип< 1000 o С). Примером тугоплавких металлов может быть – Au, Cu, Ni, W, легкоплавких – Hg, K, Al, Zn.
Электронное строение металлов и их особенности
Атомы металлов, также как, и неметаллов состоят из положительно заряженного ядра внутри которого находятся протоны и нейтроны, а по орбитам вокруг него движутся электроны. Однако, по сравнению с неметаллами, атомные радиусы металлов намного больше. Это связано с тем, что валентные электроны атомов металлов (электроны внешнего энергетического уровня) расположены на значительном удалении от ядра и, как следствие, связаны с ним слабее. По этой причине металлы характеризуются низкими потенциалами ионизации и легко отдают электроны (являются восстановителями в ОВР) при образовании химической связи.
Все металлы за исключением ртути представляют собой твердые вещества с атомной кристаллической решеткой. Рассмотрим строение металлов в кристаллическом состоянии. В атомах металлов имеются «свободные» электроны (электронный газ), которые могут перемещаться по кристаллу даже под действием слабых электрических полей, что обусловливает высокую электропроводимость металлов.
Среди металлов присутствуют s-, p-, d- и f-элементы. Так, s- элементы – это металлы I и II групп Периодической системы (ns 1 , ns 2 ), р- элементы – металлы, расположенные в группах III – VI (ns 2 np 1-4 ). Металлы d-элементы имеют большее число валентных электронов по сравнению с металлами s- и p-элементами. Общая электронная конфигурация валентных электронов металлов d-элементов – (n-1)d 1-10 ns 2 . Начиная с 6 периода появляются металлы f-элементы, которые объединены в семейства по 14 элементов (за счет сходных химических свойств) и носят особые названия лантаноидов и актиноидов. Общая электронная конфигурация валентных электронов металлов f-элементов – (n-2)f 1-14 (n-1)d 0-1 ns 2 .
Примеры решения задач
| Задание | При взаимодействии 6,0 г металла с водой выделилось 3,36 л водорода (н.у.). Определите этот металл, если он в своих соединениях двухвалентен. |
| Решение | Запишем уравнение реакции растворения металла в воде. Поскольку металл двухвалентен, его реакция с водой будет описываться уравнением следующего вида: |
Согласно уравнению реакции:
N (Ме) =n (Н2) = 3,36/22,4 = 0,15 моль.
Найдем относительную атомную массу металла:
Ar(Ме) = m / n= 6,0/0,15 = 40 г/моль
Следовательно, этот металл — кальций.
| Задание | При действии на смесь меди и железа массой 20 г избытком соляной кислоты выделилось 5,6 л газа (н.у.). Определить массовые доли металлов в смеси. |
| Решение | Известно, что медь не растворяется в соляной кислоте, поскольку стоит в ряду активности металлов после водорода, т.е. выделение водорода происходит только в результате взаимодействия хлороводородной кислоты с железом. |
Запишем уравнение реакции:
Найдем количество вещества водорода:
Согласно уравнению реакции n(H2) : n(Fe) = 1:1, т.е.n(H2) = n(Fe) = 0,25 моль. Тогда масса железа будет равна (молярная масса – 56 г/моль):
Занятие 1. Электронное строение и классификация металлов
Металлы, или вещества, находящиеся в металлическом состоянии, обладают электронным строением, характеризующимся наличием незаполненных подуровней в валентной зоне. Валентные электроны не связаны с определенными атомами, а принадлежат всему металлическому телу, образуя электронный газ, окружающий каркас из положительно заряженных ионов.
Металлическая связь между атомами ненаправленная. Каждый атом стремится окружить себя как можно большим числом соседних атомов, следствием чегоявляется высокая компактность металлов.
Электроны, образующие электронный газ, называют электронами проводимости, поскольку они легко перемещаются во внешнем электрическом поле, создаваяэлектрический ток.
Незаполненность валентных энергетических зон металлов определяет их высокую электропроводность,теплопроводность, металлический блеск и др. Все металлыимеют положительный температурный коэффициент электрического сопротивления, т. е. при Т→0 К R → 0 (у полупроводников и неметаллов при Т→0 К R→∞).
По ряду характерных признаков металлы делят на две группы: черные и цветные. К черным относят железо и его сплавы (стали, чугуны). Остальные металлы и сплавы на их основе – цветные.
Нередко к металлам железной группы относят Ni, Co и Мn.
Металлы с температурой плавления выше 1800 0 С называют тугоплавкими. К ним принадлежи Тi, Zг. Сг, V, Nb, Mo, Wи др.
Металлы с низкой температурой плавления (Hg, Sn, Bi, Cd, Pb, Zn, Sb и др.) относят к легкоплавким.
К легким относят металлы с низкой плотностью. К ним принадлежат нашедшие широкое техническое применение Mg, Be, Al, Ti.
Металлы (Ag, Au, Os, Ir, Pt, Rh, Pd и др.) составляют группу благородных. Они химически инертны.К благородным металлам часто относят медь, обладающую химической стойкостью в сухой атмосфере.
К редкоземельным металлам (РЗМ) относят металлы группы лантана – лантаноиды(Се, Рг, Nd и др.) и сходные с ними Y и Sc.
Металлы актиноидной (урановой) группы составляют используемые в атомной технике актиноиды (Th, Pa, U и др.).
Li, Na, К и др. (их используют в качестве теплоносителей в быстрых ядерных реакторах с высоко энергетической активной зоной) составляют группу щелочноземельных металлов.
Ряд металлов (Fe, Ni, Co, Gd), в связи с особенностями их электронного строения, обладает ферромагнетизмом –способностью сильно намагничиваться во внешнем магнитном поле. Основные свойства ферромагнетиков определяются доменной структурой их кристаллов. Домен –это область кристалла размером 10 -4 . 10 -6 м, которая при отсутствии внешнего магнитного поля спонтанно (самопроизвольно) намагничена до насыщения. Магнитные моменты отдельных доменов направлены различно, поэтому полный магнитный момент ферромагнетика равен нулю.
Занятие 2. Кристаллическое строение металлови дефекты кристаллических структур
Большинство металлов имеют кристаллическую решетку. Положительно заряженные ионы, образующие каркас металлического тела, совершают непрерывные тепловые колебания около точек, закономерно расположенных в определенных местах пространства. Эти точки являются узлами воображаемой пространственной кристаллической решетки.
Наименьший объем кристалла, при трансляции которого по координатным осями воспроизводится вся кристаллическая решетка, называется элементарной кристаллической ячейкой.Ячейка характеризуется параметрами а, Ь и с – периодами кристаллической решетки (расстояниями между атомами, расположенными на ребрах ячейки, направленных по осям х, у и z соответственно) и углами между координатными осями – a (между осями х и z), β (между у и z), γ (между x и у).
Различают простые и сложные кристаллические решетки. В элементарной ячейке простой решетки атомы (ионы) расположены только в вершинах образующего ячейку многогранника. В сложных – они могут находиться также внутри многогранника или на его гранях.
Металлы имеют сложные кристаллические решетки. В большинстве случаев – это кубическая объемно-центрированная (ОЦК), кубическая гранецентрированная (ГЦК) и гексагональная плотноупакованная (ГПУ).
В элементарной ячейке ОЦК атомы находятся в вершинах куба и внутри него, в точке пересечения пространственных диагоналей. В ячейке ГЦК атомы расположены в вершинах куба и в центре каждой грани. В ячейке ГПУ атомы находятся в вершинах правильной шестигранной призмы, в центре каждого ее основания и, кроме того, три атома заключены внутри призмы.
Размеры элементарной ячейки определяются размерами образующих ее атомов. При этом полагают, что атомы, представляемые в виде жестких шаров, касаются друг друга в направлениях ячейки с наиболее плотным их расположением.
Во многих случаях в разных температурных интервалах один и тот же металл обладает различными кристаллическими решетками. Такое явление носит название полиморфизм или аллотропия.
Важными характеристиками кристаллической решетки являются коэффициент компактности, координационное число, базис.
Коэффициент компактности – это отношение объема принадлежащих кристаллической ячейке атомов к объему всей ячейки. Следует иметь в виду, что в кристаллической решетке часть атомов, составляющих ячейку, относится не только к данной ячейке, но и к ячейкам, находящимся по соседству. Например, атом, расположенный в вершине кубической ячейки (простая кубическая, ОЦК, ГЦК) принадлежит еще семи соседним ячейкам, т.е. данной ячейке принадлежит лишь 1/8 атома.
Коэффициент компактности простой кубической решетки равен 52 %, ОЦК – 68 %, ГЦК – 74 % (столь же компактна решетка ГПУ). Остальное пространство занято порами. В ячейке ГЦК в центре расположена крупная октаэдрическая пора с радиусом, равным 0,41 радиуса атома. В ячейке ОЦК больших пор нет. Поры, расположенные на ребрах ячейки, имеют радиус, равный 0,16 радиуса атома.
Координационное число – это число атомов, находящихся в кристаллической решетке на равном наименьшем расстоянии от данного атома. Каждый атом простой кубической решетки имеет 6 ближайших соседей, расположенных на расстоянии длины ребра куба (на расстоянии периода решетки). Координационное число такой решетки обозначают К6. В ОЦК решетке у каждого атома 8 ближайших соседей и координационное число равно 8 (К8). В ГЦК и ГПУ решетках каждый атом имеет 12 ближайших соседей. Соответственно координационные числа К12 и Г12.
Чем выше координационное число, тем плотнее пространственная кристаллическая решетка материала.
Базис кристаллической решетки – это таблица координат атомов, принадлежащих элементарной ячейке, рассматриваемой в пространственных координатных осях. Базис простой кубической решетки (0,0,0), ОЦК – (0,0,0; 1/2,1/2,1/2), ГЦК – (0,0,0; 1/2,0,1/2; 0,1/2,1/2; 1/2,1/2,0).
Пространственное положение кристаллографических плоскостей (плоскостей, проходящих через определенные группы атомов кристаллической решетки), а также кристаллографических направлений характеризуется кристаллографическими индексами.
Индексы плоскости – это три целых числа, заключенных в круглые скобки и представляющих собой приведенные к целым числам значения обратных величин отрезков, отсекаемых плоскостью на осях х, у, z.За единицы длины принимают параметры решетки а, b, с. Например, плоскость, включающая пространственные диагонали куба, имеет индексы (101). Если плоскость отсекает отрицательные отрезки, то знак минус ставится над соответствующим индексом. Кристаллографические индексы отражают положение не только данной плоскости, но целого семейства плоскостей, ей параллельных.
Индексы направлений – это три числа, заключенных в квадратные скобки и представляющих собой приведенные к целым значениям координаты любой точки направления после его параллельного переноса в начало координат. За единицы принимают параметры кристаллической решетки. Например, направление совпадающее с пространственной диагональю куба, имеет индексы [111]. Если направление имеет отрицательные координаты, то над соответствующим индексом ставится знак минус.
В различных направлениях кристаллической решетки плотность расположения атомов различна, что влечет за собой различие в свойствах кристалла в зависимости от направления, в котором это свойство измерено – анизотропию. В поликристаллических телах в пределах отдельных зерен наблюдается явление анизотропии. Однако, поскольку ориентация кристаллической решетки в различных зернах различна, в целом по куску материала свойства усредняются. Поэтому реальные металлы являются изотропными,т.е. телами с примерно одинаковыми свойствами по всем направлениям. Поскольку их изотропность является не истиной, а усредненной, то их принято называть квазиизотропами. Если каким-либо способом, например давлением, сориентировать кристаллические решетки в зернах одинаково (создать текстуру деформации), то такое поликристаллическое тело станет анизотропным.
Реальные кристаллы всегда содержат дефекты – искажения правильного расположения атомов в пространстве. Различают точечные, линейные, поверхностные и объемные дефекты.
Точечные дефекты по размерам сравнимы с межатомными расстояниями. К ним относятся вакансии (отсутствие атома в узле кристаллической решетки), межузельные или дислоцированные атомы (атом находится в межузельном пространстве кристаллической решетки) и примесные атомы. Среди последних различают атомы замещения (чужеродный атом занимает место в узле кристаллической решетки) и атомы внедрения (чужеродный атом находится в межузельном пространстве решетки).
Линейные дефекты по размерам в двух направлениях сравнимы с межатомными расстояниями, а в третьем простираются на многие тысячи периодов кристаллической решетки. Важнейшими видами линейных несовершенств являются краевые (линейные) и винтовые дислокации.
Образование краевых дислокаций вызвано присутствием в кристаллической решетке неполных кристаллографических плоскостей. Такие полуплоскости, не имеющие продолжения в нижней или верхней частях кристаллической решетки, называются экстраплоскостями. Краевая дислокация представляет собой область упругих искажений, проходящих вдоль края экстраплоскости. Различают положительные и отрицательные дислокации. Положительная дислокация (ее отмечают знаком ┴.) возникает, если экстраплоскость находится в верхней части кристалла, если в нижней – отрицательная (ее отмечают знаком ┬).
Винтовая дислокация – это область упругих искажений кристаллической решетки, проходящая вдоль линии, вокруг которой атомные плоскости изогнуты по винтовой поверхности. В зависимости от направления изгиба различают правые и левые винтовые дислокации.
Дислокации (краевые и винтовые) не могут обрываться внутри кристалла. Они выходят на границы кристалла, прерываются другими дислокациями или образуют дислокационные петли.
Поверхностные дефекты малы только в одном направлении. Они представляют собой упругие искажения кристаллической решетки по границам зерен или их фрагментов (блоков мозаичной структуры). Различают большеугловые (высокоугловые) и малоугловые (низкоугловые) границы.
Большеугловые границы представляют собой области в несколько периодов кристаллической решетки, на протяжении которых решетка одной кристаллографической ориентации переходит в решетку другой ориентации. Такое строение имеют межзеренные границы.
Малоугловые границы представляют собой цепочки дислокаций (дислокационные стенки), отделяющие одну часть кристаллической решетки от другой (один блок мозаичной структуры от другого). Плотность расположения дислокаций зависит от угла между кристаллографическими плоскостями в соседних блоках. Чем угол больше (в пределах до нескольких угловых градусов), тем чаще расположены дислокации.
Объемные дефекты представляют собой искажения решетки, вызванные наличием пор, трещин, раковин и других макронарушений непрерывности кристаллической решетки.
Кристаллическая структура металлов. Общая характеристика и классификация металлов
В технике под металлами понимают материалы, обладающие целым комплексом специфических физических, химических, технологических, эксплуатационных и механических свойств.
Физические свойства отражают поведение материалов в различных тепловых, электромагнитных и гравитационных полях. К наиболее характерным физическим свойствам металлов следует отнести металлический блеск, высокую электро- и теплопроводность, способность испускать электроны при нагреве, а также сравнительно высокую плотность большинства металлов.
Химические свойства отражают способность материалов взаимодействовать с другими веществами. С точки зрения химических свойств металлы это химические элементы, расположенные в левой части таблицы Менделеева. Атомы этих элементов содержат на внешней электронной оболочке небольшое число электронов, слабо связанных с ядром. Вступая в химические взаимодействия с неметаллами, атомы металлов легко отдают им свои внешние валентные электроны и становятся положительно заряженными ионами.
Технологические свойства отражают способность материалов подвергаться тому или иному виду обработки. К наиболее характерным технологическим свойствам металлов следует отнести их относительно хорошую деформируемость (в частности, штампуемость и ковкость), а также хорошую свариваемость и возможность получать изделия методом литья.
Эксплуатационные свойства характеризуют поведение материалов в реальных условиях эксплуатации. Среди эксплуатационных свойств металлов можно выделить их неплохую износостойкость.
Механические свойства отражают способность материалов сопротивляться деформации и разрушению под воздействием различного рода нагрузок. К наиболее характерным механическим свойствам металлов относят их достаточно высокую пластичность и вязкость, а также твёрдость и прочность.
Физические и химические свойства металлов наиболее подробно изучаются в рамках дисциплин «Физика» и «Химия». Материаловедение большее внимание уделяет механическим и технологическим свойствам материалов.
Все металлы делят на две большие группы: на чёрные металлы и цветные металлы.
Чёрные металлы отличаются специфическим темно-серым цветом, высокой температурой плавления и относительно высокой твёрдостью. Цветные металлы имеют характерную белую, желтую или красную окраску, и отличаются от чёрных металлов большей пластичностью, меньшей твёрдостью и невысокой температурой плавления.
Чёрные металлы, в свою очередь, подразделяют на 5 групп:
1. Металлы группы железа – Fe, Cо, Ni и Mn.
Fe составляет основу самых распространённых в промышленности сплавов – сталей и чугунов. Остальные металлы этой группы применяются либо в качестве добавок к железоуглеродистым сплавам, либо в качестве основы для соответствующих сплавов (кобальтовых, никелевых и т.п.).
2. Тугоплавкие металлы – Ti, V, Cr, Mo, W и др.
Металлы этой группы имеют температуру плавления выше, чем у железа, т.е. более 1539°С. Их обычно используют в качестве добавок к легированным сталям, либо в качестве основы для специальных сплавов (например, титановых или хромовых). Вольфрам в чистом виде используют для изготовления нитей накала электроламп.
3. Урановые металлы или актиноиды – Ac, Th и т.д. Применяются, как правило, для изготовления сплавов, используемых в атомной энергетике.
4. Редкоземельные металлы или лантаноиды – La, Ce и т.д. Эти металлы обычно встречаются в смешанном виде и имеют близкие свойства. Их используют для изготовления специальных сплавов, обладающих особыми физическими и иными свойствами.
5. Щелочные металлы – Li, Na, K и т.д. Отличаются высокой химической активностью и поэтому в свободном виде не используются.
Цветные металлы подразделяют на 3 группы:
1. Легкие металлы – Al, Mg, Be. Обладают сравнительно низкой плотностью. Al из-за своей высокой электропроводности широко применяется для изготовления электропроводов. Кроме того, Al используют для получения алюминиевых сплавов, широко применяемых в машиностроении.
2. Благородные металлы – Ag, Au, Pt и т.д. в том числе Cu. Данные металлы отличаются высокой пластичностью, электропроводностью и коррозионной стойкостью. Благодаря этим свойствам они широко применяются в микроэлектронике и ювелирном деле. Медь используют также для получения бронз и латуней. Слитки благородных металлов, размещённые в банках, играют роль фактических денег.
3. Легкоплавкие металлы – Sn, Pb, Zn, Hg и т.д. Имеют сравнительно низкую температуру плавления. Температура плавления ртути (Hg) ниже комнатной и поэтому данный металл в обычных условиях является жидким. Sn и Pb используют для изготовления припоев, те сплавов, служащих для соединения деталей методом пайки.
Наиболее распространенным металлом на земном шаре является алюминий (8,8%). На втором месте находится железо (4,65%), которое к тому же является одним из наиболее дешёвых металлов.
2.2 Металлическая межатомная связь и модель «электронного газа»
Вышеназванные характерные свойства металлов, в большинстве своём, могут быть объяснены спецификой межатомного взаимодействия и особенностями структуры металлов. Атомы металлов, находящихся в твёрдом стоянии, связаны между собой особым типом химической связи, которую называют металлической связью. Такая связь устанавливается посредством обобществления всех валентных электронов атомами материала. Валентные электроны, потерявшие связь со своими атомами, оказываются принадлежащими всему металлу в целом и, будучи относительно свободными, образуют в объёме металла так называемый «электронный газ» или точнее «электронную жидкость». Сами же атомы при этом становятся положительно заряженными ионами. Таким образом, на атомарном уровне металлы выглядят как совокупность расположенных в узлах кристаллической решётки положительно заряженных ионов, которые омываются газом относительно свободных электронов или иначе «электронной жидкостью» (рис. 7).
Рис. 7. Модель «электронного газа (жидкости)»
Наличием в объёме металла электронного газа или жидкости объясняются многие свойства металлов. Так, если к металлу приложить разность потенциалов, то под воздействием электрического поля относительно свободные электроны наряду с хаотическим движением приобретут направленное движение в сторону от минуса к плюсу. Другими словами в металле возникнет электрический ток. Поскольку в металлах свободных носителей заряда, т.е. электронов, достаточно много, их электропроводность оказывается очень высокой. Эти же электроны проводимости весьма эффективно могут переносить тепловую энергию от разогретого участка металла к более холодным областям, и этим объясняется высокая теплопроводность металлов. Кроме того, электронная жидкость хорошо отражает фотоны, т.е. частицы света, и тем самым обеспечивает металлам характерный блеск.
При пластическом деформировании металлов наблюдается сдвиг атомных слоёв относительно друг друга и металлическая связь способствует этому процессу. В данном случае электронная жидкость играет роль своеобразного клея, соединяющего атомные слои, и одновременно роль своеобразной смазки, облегчающей процесс скольжения этих слоёв. В результате металлы оказываются достаточно пластичными материалами.
Металлическая связь, в отличие от ковалентной связи, не является строго направленной в пространстве и допускает произвольное число взаимодействующих частиц. В результате атомы металлов, стремясь к более выгодной и устойчивой конфигурации, обладающей меньшей свободной энергией, располагаются в пространстве наиболее компактным образом. Этим, в частности, объясняется относительно высокая плотность большинства металлов. Плотным атомным упаковкам металлов соответствуют следующие типы кристаллических структур:
1. Объёмоцентрированная кубическая структура или ОЦК-структура. Такую структуру описывает ОЦК-решётка, элементарная ячейка которой выглядит следующим образом:
Рис. 8. Элементарная ячейка ОЦК-структуры.
В узлах этой кристаллической решётки располагаются атомы, а точнее ионы, соответствующего металла. Координационное число в данном случае равно 8 (на ближайшем равном расстоянии от любого атома находится 8 аналогичных атомов). Коэффициент компактности равен 0,68. Это означает, что 68% объёма металла занято атомами, а остальную его часть составляют пустоты. Это достаточно плотное расположение атомов. Базис образуют два атома соответствующего металла (один атом, расположенный в центре ОЦК-ячейки, полностью ей принадлежит, и ещё один атом (8 по ⅛) дают узлы, расположенные в вершинах ячейки). ОЦК-структура наблюдается у таких металлов как Cr, Mo, W, V и др.
2. Гранецентрированная кубическая структура или ГЦК-структура. Эту структуру описывает ГЦК-решётка, элементарная ячейка которой выглядит следующим образом:
Рис. 9. Элементарная ячейка ГЦК-структуры.
В узлах решётки также располагаются атомы соответствующих металлов. Координационное число здесь равно 12, а коэффициент компактности имеет значение 0,74. Базис образуют четыре атома металла (каждый атом, расположенный в центре грани принадлежит ячейке только наполовину, а поскольку таких атомов 6, то получается ровно 3; плюс один атом дают вершины ячейки). ГЦК-структура характерна для Al, Cu, Ni, Ag, Au и Pt.
3. Гексагональная плотноупакованная структура или ГПУ-структура. Эту структуру описывает соответствующая ГПУ-решётка. Хотя ГПУ-решётку можно построить и с помощью меньшей по объёму ячейки, в данном случае в качестве элементарной ячейки лучше подойдёт шестигранная призма, которая нагляднее отражает гексагональную симметрию структуры (рис. 10).
Рис. 10. Элементарная ячейка ГПУ-структуры.
Координационное число для такой структуры равно 12 (если за начало отсчёта принять атом, расположенный в центре грани, то на равном ближайшем расстоянии от него находится 6 атомов, плюс по 3 атома сверху и снизу). Коэффициент компактности, как и у ГЦК-структуры, имеет значение 0,74. Это наивысшая степень упаковки атомов. Базис образуют 6 атомов соответствующего металла (3 атома внутри призмы полностью ей принадлежат; атомы в центре верхней и нижней грани принадлежат ячейке только наполовину, а каждый из 12 атомов в вершинах призмы принадлежит рассматриваемой ячейке лишь на 1/6 часть, поскольку находится на пересечении 6 аналогичных ячеек). ГПУ-структура наблюдается у таких металлов как Mg, Zn, Be и др.
Иногда у металлов наблюдается тетрагональная или простая гексагональная структура, но гораздо реже, чем три вышеназванные структуры.
Общие сведения о строении металлов
Металлы и их сплавы в твердом состоянии имеют кристаллическое строение. Их атомы (ионы, молекулы) располагаются в пространстве в строго определенном порядке и образуют пространственную кристаллическую решетку.
Пространственные кристаллические решетки образуются при переходе металла из жидкого состояния в твердое. Этот процесс называется кристаллизацией.
Кристаллизация состоит из двух стадий. В жидком состоянии металла его атомы находятся в непрерывном движении. При понижении температуры движение атомов замедляется, они сближаются и группируются в кристаллы. Образуются так называемые центры кристаллизации (первая стадия). Затем идет роет кристаллов вокруг этих центров (вторая стадия). Вначале кристаллы растут свободно. При дальнейшем росте кристаллы отталкиваются, рост одних кристаллов мешает росту соседних, в результате чего образуются неправильной формы группы кристаллов, которые называют зернами.
Размер зерен существенно влияет на эксплуатационные и технологические, свойства металлов.
Классификация металлов и сплавов
В технике все металлы и сплавы принято делить на черные и цветные. К черным металлам относятся железо и сплавы на его основе. Этими сплавами являются чугуны и стали. К цветным — все остальные металлы и сплавы. Ко второй группе относят цветные металлы и их сплавы. Они получили такое название потому, что имеют различную окраску. Например, медь светло-красная, никель, олово, серебро - белые, свинец - голубовато-белый, золото - желтое. Это деление на черные и цветные металлы условно.
Наряду с черными и цветными металлами выделяют еще группу благородных металлов: серебро, золото, платину, рутений и некоторые другие. Они названы так потому, что практически не окисляются на воздухе даже при повышенной температуре и не разрушаются при действии на них растворов кислот и щелочей.
1. Чугун - сплав железа с углеродом (более 2%) и другими добавками.
2. Сталь - сплав железа с углеродом (менее 2%) и другими добавками.
3. Латунь - сплав меди с цинком (10 - 50%)
4. Бронза - сплав меди с оловом (до 20%)
5. Константан - сплав меди (60%), никеля (38%), марганца (1-2%)
6. Мельхиор - сплав меди (80%) и никеля (20%)
7. Нихром - сплав никеля (60%), железа (14-18%), хрома (18%)
8. Баббиты - сплав свинца (65%), олова (15-17%) сурьмы (15-17%), меди (2%)
9. Дюралюминий - сплав алюминия (90%), меди (3-5%), магния (4%)
10. Силумин - сплав алюминия (86 - 88%) и кремния (12-14%)
11. Магналий - сплав алюминия (80 - 97%) с магнием (3-20%)
Классификация сталей
Химический состав.
Сталями принято называть сплавы железа с углеродом, содержащие до 2,14% углерода. В зависимости от химического состава различают стали углеродистые и легированные. В свою очередь углеродистые стали могут быть:
малоуглеродистыми, т. е. содержащими углерода менее 0,25%;
среднеуглеродистыми, содержание углерода составляет 0,25-0,60%
высокоуглеродистыми, в которых концентрация углерода превышает 0,60%
Легированные стали подразделяют на:
низколегированные содержание легирующих элементов до 2,5%
среднелегированные, в их состав входят от 2,5 до 10% легирующих элементов;
высоколегированные, которые содержат свыше 10% легирующих элементов.
Назначение
Конструкционные, предназначенные для изготовления строительных и машиностроительных изделий.
Инструментальные, из которых изготовляют режущий, мерительный, штамповый и прочие инструменты. Эти стали содержат более 0,65% углерода.
С особыми физическими свойствами, например: электротехническая сталь; с особыми химическими свойствами, например: нержавеющие, жаростойкие или жаропрочные стали.
Качество
В зависимости от содержания вредных примесей: серы и фосфора-стали подразделяют на:
Стали обыкновенного качества, содержание до 0.06% серы и до 0,07% фосфора.
Качественные - до 0,035% серы и фосфора каждого отдельно.
Высококачественные - до 0.025% серы и фосфора.
Особовысококачественные, до 0,025% фосфора и до 0,015% серы.
Сталь обыкновенного качества подразделяется еще и по поставкам на 3 группы:
С таль группы А поставляется потребителям по механическим свойствам (такая сталь может иметь повышенное содержание серы или фосфора);
сталь группы Б - по химическому составу;
сталь группы В - с гарантированными механическими свойствами и химическим составом
Степень раскисления
По степени удаления кислорода из стали, т. е. По степени её раскисления, существуют:
спокойные стали "сп"; кипящие стали - слабо раскисленные "кп"; полуспокойные стали, "пс".
Нелегированные конструкционные стали обыкновенного качества
Обозначают по ГОСТ 380-94 буквами "Ст" и условным номером марки (от 0 до 6) в Например:
Ст1кп2 - углеродистая сталь обыкновенного качества, кипящая, № марки 1, второй категории, поставляется потребителям по механическим свойствам (группа А);
Нелегированные конструкционные качественные стали.
В соответствии с ГОСТ 1050-88 эти стали маркируются двухзначными числами, показывающими среднее содержание углерода в сотых долях процента: 05 ; 08 ; 10 ; 25 ; 40 и т.д.


Папиллярные узоры пальцев рук - маркер спортивных способностей: дерматоглифические признаки формируются на 3-5 месяце беременности, не изменяются в течение жизни.
Поперечные профили набережных и береговой полосы: На городских территориях берегоукрепление проектируют с учетом технических и экономических требований, но особое значение придают эстетическим.

© cyberpedia.su 2017-2020 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!
Кристаллическое строение металлов

Металлы – особая группа элементов в периодической таблице Менделеева. В отличие от неметаллов элементы этой группы являются исключительно восстановителями с положительной степенью окисления, а также обладают пластичностью, твёрдостью, упругостью, что обусловлено кристаллическим строением металлов.
Общее строение
Металлы – твёрдые вещества, имеющие кристаллическое строение. Исключение составляет ртуть – жидкий металл. Кристаллические решётки представляют собой упорядоченные определённым образом атомы металла. Каждый атом состоит из положительно заряженного ядра и нескольких отрицательно заряженных электронов. В атомах металлов недостаточно электронов, поэтому они являются ионами.
Единица кристаллической решётки – элементарная кристаллическая ячейка, в условных узлах и на гранях которой находятся положительно заряженные ионы. Их удерживают вместе металлические связи, возникающие за счёт беспорядочного движения отделившихся от атомов электронов (благодаря чему атомы превратились в ионы).
Отрицательно заряженные электроны держат на равном расстоянии положительно заряженные электроны, предавая кристаллической решётке правильную геометрическую форму.
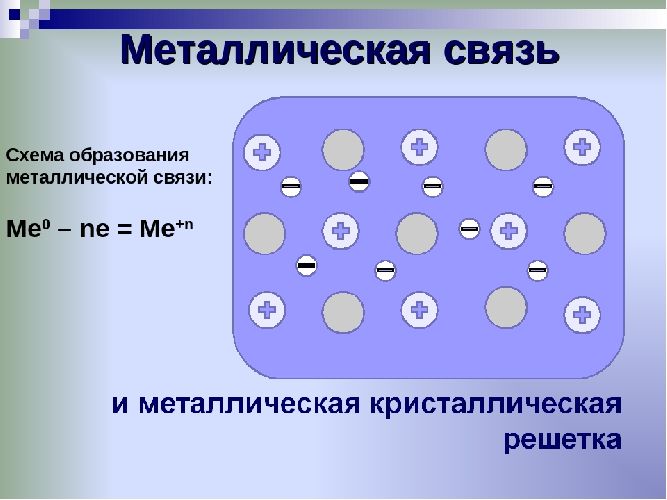
Рис. 1. Схема металлической связи.
Свободное движение электронов обусловливает электро- и теплопроводность металлов.
Виды решёток
Элементарные кристаллические ячейки могут иметь различную конфигурацию. В связи с этим выделяют три типа кристаллических решёток:
- объемно-центрированная (ОЦК) кубическая – состоит из 9 ионов;
- гранецентрированная (ГЦК) кубическая – включает 14 ионов;
- гексагональная плотноупакованная (ГПУ) – состоит из 17 ионов.
ОЦК представляет собой куб, в узлах которого находится по атому. В центре куба, на пересечении диагоналей располагается девятый ион. Этот тип характерен для железа, молибдена, хрома, вольфрама, ванадия.
Элементарной кристаллической ячейкой типа ГЦК является куб с ионами в узлах и в середине каждой грани – на пересечении диагоналей. Такое строение имеют медь, серебро, алюминий, свинец, никель.
Третий тип имеет вид гексагональной призмы, в узлах которой находится по шесть ионов с каждой стороны. Посередине между шестью узлами располагается по одному иону. В середине призмы между шестиугольными гранями находится равносторонний треугольник, который составляют три иона.
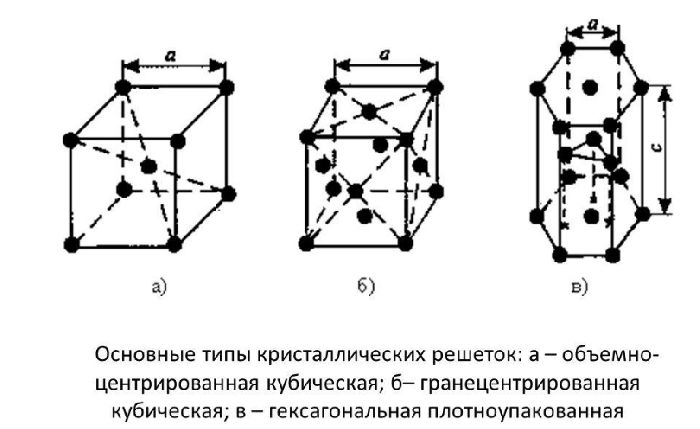
Рис. 2. Типы решёток.
Металл может содержать большое количество дефектов атомного строения. Дефекты влияют на свойства металла.
Характеристика решётки
Кристаллические решётки характеризуются компактностью или степенью наполненности. Компактность определяют показатели:
- параметр решётки – расстояние между атомами;
- число атомов;
- координационное число – количество соседних ячеек;
- плотность упаковки – отношение объёма, занимаемого атомами, к полному объёму решётки.
При подсчёте количества атомов следует помнить, что атомы в узлах и на гранях входят в состав соседних ячеек.
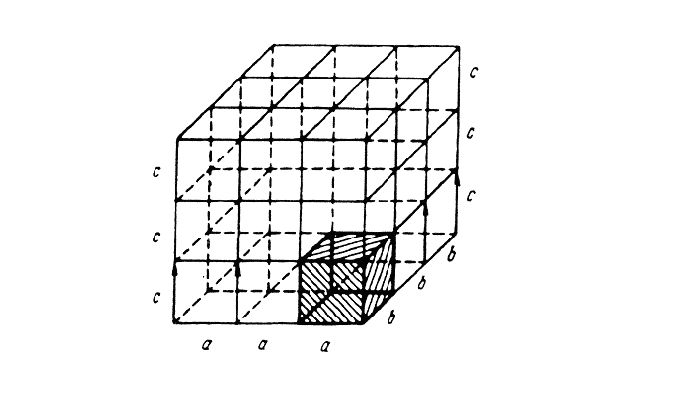
Рис. 3. Кристаллические ячейки составляют решётку.
Что мы узнали?
Узнали кратко об атомно-кристаллическом строении металлов. Металлы – твёрдые кристаллические вещества. Единицей решётки является элементарная кристаллическая ячейка. Благодаря металлическим связям ионы в узлах ячеек удерживаются на одинаковом расстоянии. Различают три типа кристаллических решёток – ОЦК, ГЦК и ГПУ, отличающихся количеством атомов и геометрической формой.
Читайте также:
