Энергия электронов в металле
Обновлено: 08.07.2024
Для вывода формулы туннельного тока в системе металл-диэлектрик-металл (формула John G. Simmons, см. пункт 1.2.1), необходимо ввести ряд упрощающих положений и напомнить некоторые основы электронной теории металлов.
- Во-первых, будем считать, что всё твёрдое тело (металл) представляется как трехмерная потенциальная яма с гладким дном (так называемая модель Зоммерфельда) и электроны между собой не взаимодействуют. Энергия электрона, покоящегося на дне такой ямы, меньше, чем уровень вакуума – энергия покоящегося электрона, находящегося на бесконечности от поверхности тела. Глубина потенциальной ямы U определяется усреднённым полем положительных ионов решётки и всех электронов.
- Во-вторых, так как все электроны считаются невзаимодействующими, то решение уравнения Шредингера для системы электронов сведется к решению уравнения Шредингера для одного электрона, движущегося в этом усреднённом поле, что позволяет использовать формулы (3) пункта 1.1.1 или (4) in пункта 1.1.2.
- В третьих, в потенциальном ящике с гладким дном зависимость разрешённых значений энергии от разрешённых значений волнового вектора оказывается точками на параболической зависимости энергии от компонент волнового вектора для свободного электрона в пустом пространстве. Если масса электронов m изотропна во всём пространстве, то справедливо , где , , – импульсы электрона вдоль соответствующих осей.
Из статистической физики [1] известно, что в системе, находящейся в термодинамическом равновесии с температурой T , все квантовые состояния с одним и тем же значением энергии E заполнены электронами одинаково. Среднее число электронов находящихся в одном квантовом состоянии с энергией E при температуре T определяется распределением Ферми-Дирака:
где = (11600) –1 eV/К – постоянная Больцмана, – параметр, имеющий размерность энергии и называемый химическим потенциалом.
Химический потенциал определяется из условия нормировки
где ne – число электронов зоны проводимости на единицу объема (концентрация), – число электронных состояний на единицу объема в интервале энергий от E до E + dE. n(E) называется энергетической плотностью числа состояний.
В металле при температуре, стремящейся к абсолютному нулю, электроны заполняют все квантовые состояния с энергиями вплоть до уровня называемого уровнем Ферми. Все квантовые состояния с энергией выше уровня Ферми свободны от электронов. Для металла химический потенциал слабо зависит от температуры, поэтому его можно заменить значением при T = 0:
где m – масса электрона. Если ne измеряется в системе единиц СГС, тогда .
Если система находится в тепловом равновесии и состоит из нескольких подсистем, то уровни Ферми, для каждой подсистемы должны совпадать (рис. 1). Если же между двумя подсистемами (телами) приложено напряжение V , то уровень Ферми тела, связанного с плюсом источника напряжения, понижается, а другого тела – повышается. При этом уровни Ферми первого и второго тела отличаются на величину eV (рис. 2).
Рис. 1. Модель потенциального барьера МДМ для случая, когда система находится в термодинамическом равновесии;
j1 и j2 – работы выхода левого и правого металла соответственно.
Рис. 2. Модель потенциального барьера МДМ для случая, когда положительный потенциал приложен к правому металлу. Разность потенциалов V.
Выводы.
При решении задачи о туннелировании электронов в системе металл-диэлектрик-металл (пункт 1.2.1) будем считать, что:
Поверхностная и внутренняя энергия металла
Металлические изделия формируют основную базу инфраструктурного обеспечения инженерных коммуникаций, выступают сырьем для машиностроительной промышленности и строительства. В каждой из указанных областей использование таких элементов сопрягается с высокой ответственностью. На монтажные и коммуникационные конструкции воздействуют и химические, и механические нагрузки, что обуславливает необходимость первичного анализа свойств материала. Для понимания эксплуатационных параметров используется такое понятие, как энергия металла, которая определяет поведение отдельного элемента или конструкции в тех или иных условиях эксплуатации.

Свободная энергия
Множество процессов в структуре металлических изделий определяется характеристиками свободной энергии. Наличие в материале ионов с таким потенциалом приводит к их перемещению в другие среды. Например, в ходе взаимодействия с растворами, содержащими аналогичные ионы, металлические элементы уходят в контактную смесь. Но это происходит в случаях, когда свободная энергия металлов превосходит аналогичные показатели в растворе. В результате может сформироваться положительная обкладка двойного электрического поля за счет свободных электронов, оставшихся вблизи металлической поверхности. Укрепление данного поля также выступает барьером для прохождения новых ионов – таким образом, создается граница раздела фаз, препятствующая переходам элементов. Процесс такого перемещения продолжается до того момента, пока в новообразованном поле не будет достигнута предельная разность потенциалов. Пиковая граница определяется балансом разностей потенциалов в растворе и металле.
Поверхностная энергия
При попадании новых молекул на металлическую поверхность происходит освоение свободных зон. В процессе перемещения молекулы занимают на поверхности микротрещины и участки раздела мелких зерен – это сегменты кристаллической решетки. По такой схеме происходит изменение свободной поверхностной энергии, которая понижается. В твердых телах также можно наблюдать процессы облегчения пластического течения на поверхностных участках. Соответственно, поверхностная энергия металлов обуславливается силами притяжения молекул. Здесь же стоит отметить величину поверхностного натяжения, которая зависит от нескольких факторов. В частности, ее определяет геометрия молекул, их силы и количество атомов в структуре. Также имеет значение и расположение молекул в поверхностном слое.
Поверхностное напряжение

Обычно процессы натяжения происходят в гетерогенных средах, которые отличаются поверхностью раздела несмешивающихся фаз. Но следует заметить, что наряду с натяжением проявляются и другие свойства поверхностей, обусловленные параметрами их взаимодействия с другими системами. Совокупность данных свойств определяет большинство технологических показателей металла. В свою очередь, энергия металла, с точки зрения поверхностного натяжения, может определять параметры коалесценции капель в сплавах. Технологи, таким образом, выявляют характеристики огнеупоров и флюсов, а также их взаимодействие с металлической средой. Помимо этого, поверхностные свойства оказывают влияние на скорость термотехнологических процессов, среди которых выделение газов и вспенивание металлов.
Зонирование энергии и свойства металла
Уже отмечалось, что конфигурация распределения молекул по структуре металлической поверхности может определять отдельные характеристики материала. В частности, специфический отблеск многих металлов, а также их непрозрачность обуславливаются распределением энергетических уровней. Скопление энергий в свободных и занятых уровнях способствует наделению любого кванта двумя энергетическими уровнями. Один из них будет находиться зоне валентности, а другой — в участках проводимости. При этом нельзя сказать, что распределение по энергиям электронов в металле является стационарным и не предполагает изменений. Элементы валентной зоны, к примеру, могут поглощать световые кванты, мигрируя в зону проводимости. В результате свет поглощается, а не отражается. По этой причине металлы имеют непрозрачную структуру. Что касается блеска, то его обуславливает процесс испускания света при возвращении активизированных излучением электронов на низкие уровни энергии.
Внутренняя энергия

Данный потенциал формируется энергией ионов, а также тепловым движением электронов проводимости. Косвенно эта величина характеризуется собственными зарядами металлических структур. В частности, для стали, которая пребывает в контакте с электролитами, автоматически устанавливается собственный потенциал. С изменениями внутренней энергии связаны многие неблагоприятные процессы. Например, по этому показателю можно определить коррозионные и деформационные явления. В таких случаях внутренняя энергия металла обуславливает наличие микро- и макронарушений в структуре. Более того, частичное рассеивание данной энергии под действием той же коррозии обеспечивает и потерю определенной доли потенциала. На практике эксплуатации металлических изделий негативные факторы изменения внутренней энергии могут проявляться в виде структурных разрушений и снижении пластичности.
Энергия электрона в металле
При описаниях совокупности частиц, которые взаимодействуют между собой в твердом теле, применяются квантово-механические представления об энергии электронов. Обычно используются дискретные значения, которые определяют характер распределения данных элементов по уровням энергии. В соответствии с требованиями квантовой теории, измерение энергии электронов производится в электрон-вольтах. Считается, что в металлах потенциал электронов на два порядка превышает энергию, которая рассчитывается по кинетической теории газов в условиях комнатной температуры. При этом энергия выхода электронов из металлов и, в частности, скорость движения элементов не зависит от температуры.
Энергия иона в металле
Расчет энергии ионов позволяет определять характеристики металла в процессах плавления, возгонки, деформации и т. д. В частности, технологи выявляют показатели прочности на разрыв и упругость. Для этого вводится и понятие кристаллической решетки, в узлах которой находятся ионы. Энергетический потенциал иона обычно рассчитывается с учетом его возможности разрушительного воздействия на кристаллическое вещество с образованием составных частиц. На состояние ионов может повлиять и кинетическая энергия электронов, выбиваемых из металлов в процессе столкновения. Поскольку в условиях повышения разности потенциалов в среде электродов до тысячи вольт скорость перемещения частиц значительно увеличивается, накапливаемого потенциала хватает для расщепления встречных молекул на ионы.
Энергия связи
Металлы характеризуются смешанными типами связи. Ковалентная и ионная связки не имеют резкого разграничения и зачастую перекликаются между собой. Так, процесс упрочнения металла под действием легирования и пластического деформирования объясняется как раз перетеканием металлической связки в ковалентное взаимодействие. Независимо от вида данных связей, все они определяются как химические процессы. При этом у каждой связи есть энергия. Например, ионное, электростатической и ковалентное взаимодействие может обеспечивать потенциал в 400 кДж. От конкретной величины будет зависеть и энергия металла при взаимодействии с разными средами и под механическими нагрузками. Металлические связки могут характеризоваться разными показателями прочности, но в любом проявлении они будут не сопоставимы с аналогичными свойствами в ковалентных и ионных средах.
Свойства металлических связей
Одним из первостепенных качеств, которые характеризуют энергию связей, является насыщаемость. Данное свойство определяет состояние молекул и, в частности, их структуру и состав. В металле частицы существуют в дискретном виде. Прежде для понимания эксплуатационных свойств комплексных соединений применялась теория валентных связей, однако в последние годы она утратила свое значение. При всех своих преимуществах данная концепция не объясняет ряд имеющих большое значение свойств. Среди них можно отметить спектры поглощения в соединениях, магнитные качества и другие характеристики. Зато при расчетах энергии поверхности в металлах можно выявить такое свойство, как воспламеняемость. Оно определяет способность металлических поверхностей возгораться без детонирующих активаторов.
Состояние металлов

Большинство металлов характеризуется валентной конфигурацией с электронным строением. В зависимости от свойств данной структуры, определяется и внутреннее состояние материала. На основе этих показателей и с учетом связей можно сделать выводы о значениях температуры плавления конкретного металла. К примеру, мягкие металлы, среди которых золото и медь, отличаются пониженной температурой плавления. Это объясняется уменьшением количества не спаренных электронов у атомов. С другой стороны, мягкие металлы имеют высокие показатели теплопроводности, что, в свою очередь, объясняется высокой подвижностью электронов. Кстати, металл, накапливающий энергию в условиях оптимальной проводимости ионов, обеспечивает высокую электропроводность за счет электронов. Это одна из важнейших эксплуатационных характеристик, которые определяются металлическим состоянием.
Заключение

Химические свойства металлов во многом определяют их технико-физические качества. Это позволяет специалистам ориентироваться на энергетические показатели материала, с точки зрения возможности его использования в тех или иных условиях. Кроме того, энергия металла не всегда может рассматриваться в качестве самостоятельной. То есть собственный потенциал может изменяться в зависимости от характера взаимодействия с другими средами. Наиболее выразительны связи металлических поверхностей с другими элементами на примере процессов миграции, когда происходит заполнение свободных энергетических уровней.
Энергия Ферми
Распределение электронов по различным квантовым состояниям подчиняется принципу Паули, согласно которому в одном состоянии не может быть двух одинаковых (с одинаковым набором четырех квантовых чисел) электронов, они должны отличаться какой-то характеристикой, например направлением спина. Следовательно, по квантовой теории, электроны в металле не могут располагаться на самом низшем энергетическом уровне даже при 0 К. Принцип Паули вынуждает электроны взбираться вверх «по энергетической лестнице».
Электроны проводимости в металле можно рассматривать как идеальный газ, подчиняющийся распределению Ферми-Дирака. Если μ0 – химический потенциал электронного газа при T = 0 К, то, среднее число Е равно
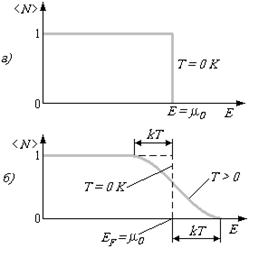
Для фермионов (электроны являются фермионами) среднее число частиц в квантовом состоянии и вероятность заселенности квантового состояния совпадают, так как квантовое состояние либо может быть не заселено, либо в нем будет находиться одна частица. Это означает, что для фермионов f(Е), где f(Е) – функция распределения электронов по состояниям. Из (1) следует, что при Т = 0 К функция распределений E < μ0, и E > μ0,. График этой функции приведен на рис. 15, а. В области энергий от 0 до μ0 функция E = μ0 она скачкообразно изменяется до нуля. Это означает, что при Т = 0 К все нижние квантовые состояния, вплоть до состояния с энергией E = μ0, заполнены электронами, а все состояния с энергией, большей μ0, свободны. Следовательно, μ0 есть не что иное, как максимальная кинетическая энергия, которую могут иметь электроны проводимости в металле при 0 К. Эта максимальная кинетическая энергия называется энергией Фермии обозначается ЕF.( ЕF = μ0). Поэтому распределение Ферми — Дирака обычно записывается в виде
Наивысший энергетический уровень, занятый электронами, называется уровнем Ферми.Уровню Ферми соответствует энергия Ферми ЕF:, которую имеют электроны на этом уровне. Уровень Ферми, очевидно, будет тем выше, чем больше плотность электронного газа. Работу выхода электрона из металла нужно отсчитывать не от дна «потенциальной ямы», как это делалось в классической теории, а от уровня Ферми, т. с. от верхнего из занятых электронами энергетических уровней.
Для металлов при не слишком высоких температурах выполняется неравенство kT EF. Это означает, что электронный газ в металлах практически всегда находится в состоянии сильного вырождения. Температура T0 вырождения находится из условия kT0 = EF . Она определяет границу, выше которой квантовые эффекты перестают быть существенными. Соответствующие расчеты показывают, что для электронов в металле Т0 ≈ 10 4 К, т.е. для всех температур, при которых металл может существовать в твердом состоянии, электронный газ в металле вырожден.
При температурах, отличных от 0 К, функция распределения Ферми-Дирака (2) плавно изменяется от 1 до 0 в узкой области (порядка kT ) в окрестности ЕF (рис. 15, б). (Здесь же для сравнения пунктиром приведена функция распределения при Т = 0 К.) Это объясняется тем, что при T > 0 небольшое число электронов с энергией, близкой к ЕF, возбуждается за счет теплового движения и их энергия становится больше ЕF. Вблизи границы Ферми при Е < ЕF заполнение электронами меньше единицы, а при Е >ЕF. — больше нуля. В тепловом движении участвует лишь небольшое число электронов, например при комнатной температуре Т ≈ 300 К и температуре вырождения T0 = 3 10 4 К, — это 10 -5 от общего числа электронов.
Если (Е — ЕF) >> kТ («хвост» функции распределения), то единицей в знаменателе (2) можно пренебречь по сравнению с экспонентой и тогда распределение Ферми — Дирака переходит в распределение Максвелла — Больцмана.
Работа выхода электронов из металла. Контактные явления
Электроны проводимости в кристалле находятся в потенциальной яме. Выход из нее требует совершения работы по преодолению силы, действующей на электрон со стороны кристалла. Найдем эту силу. Обладая энергией теплового движения, электроны могут выскакивать из кристалла на расстояние в несколько периодов. Вышедший из кристалла и находящийся у его поверхности на расстоянии х электрон индуцирует в металле заряд е+ (рис.97). Этот наведенный заряд действует на вышедший электрон так, как если бы он был сосредоточен под поверхностью металла на глубине х в точке, симметричной той, в которой находится электрон (см. Эл-во §5). Индуцированный заряд е+ называется электрическим изображением заряда е-. Оба точечные заряда притягиваются друг к другу с силой Кулона . (14.1)
Но это и есть сила притяжения металлом вышедшего из него электрона. Под действием этой силы электрон втягивается обратно в металл. Чтобы удалить электрон из металла, надо совершить работу по преодолению этой силы, перемещая электроны на бесконечность из точки, расположенной на расстоянии х0 от поверхности металла. В качестве х0 можно взять межатомное расстояние.
На рис.98 показана зависимость потенциальной энергии электрона от расстояния х до атомной плоскости – стенки металла. Энергетическое расстояние еj от уровня Ферми до нулевого уровня называют термодинамической работой выхода электрона, величину j – потенциалом выхода. Уровень Ес обозначает дно зоны проводимости, где Е = 0. У металлов работа выхода еj заключена в пределах 1,8 ¸ 5,3 эВ. Меньше всего она у щелочных металлов, больше – у золота, серебра, платины (табл. 14.1).
| Таблица 14.1 | |||
| Металл | еj, эВ | Металл | еj, эВ |
| Литий Li | 2,38 | Платина Pt | 5,32 |
| Натрий Na | 2,35 | Ванадий V | 4,58 |
| Калий К | 2,22 | Вольфрам W | 4,54 |
| Рубидий Rb | 2,16 | Золото Au | 4,30 |
| Цезий Cs | 1,18 | Серебро Ag | 4,30 |
Большое влияние на работу выхода оказывают мономолекулярные адсорбированные слои. Например, слой атомов цезия Cs на вольфраме W (рис.99). Цезий щелочной металл. Его внешний, валентный электрон связан с ядром значительно слабее, чем валентные электроны в вольфраме. Поэтому атомы цезия отдают вольфраму свои валентные электроны и превращаются в положительные ионы. Между этими ионами и их электрическими изображениями в вольфраме возникает сила притяжения, удерживающая ионы цезия на поверхности вольфрама. Поле этого двойного электрического слоя помогает выходу электронов из вольфрама. По этому в присутствии слоя цезия работа выхода электрона из вольфрама уменьшается с 4,54 эВ до 1,38 эВ. Подобно цезию действуют одноатомные слои бария Ba, церия Cе, тория Th и др.
2. Термоэлектронная эмиссия.
С повышением температуры металла поверхность Ферми разрыхляется, энергия электронов увеличивается, и они поднимаются на более высокие уровни (рис.100). Соответственно уменьшается работа выхода электронов. Поэтому концентрация вылетевших из кристалла электронов в пристеночном слое растет. Процесс испускания электронов нагретым металлом называется термоэлектронной эмиссией.
Формально термоэлектронная эмиссия есть всегда, когда Т > 0 К. Но заметной она становится при температурах Т > 800 К.
Облако термоэлектронов находится в динамическом равновесии. Число вылетевших из металла электронов в каждый промежуток времени примерно равно числу электронов, втянутых в металл. Поэтому суммарный ток эмиссии равен нулю.
На основе термоэлектронной эмиссии построен ламповый вакуумный диод (рис.101). Здесь К – катод, обычно нагреваемая вольфрамовая спираль, А – анод, холодная металлическая пластина обычно цилиндрической формы. По оси этого цилиндра натягивается спираль катода. Оба электрода помещаются в стеклянный сосуд с высоким вакуумом.
Если между катодом и анодом создавать электрическое поле с напряжением U, как показано на рис.101, то термоэлектроны под действием этого поля будут перемещаться от катода к аноду. Возникает электрический ток в вакууме. Вольтамперная характеристика вакуумного диода показана на рис.102. С повышением анодного напряжения U ток I через анод растет почти пропорционально U. Но при достижении некоторого значенья Iнас перестает увеличиваться. Это предельное значение Iнас называют ток насыщением. Он возникает тогда, когда все электроны, вылетевшие из нагретого катода, захватываются полем и переносятся к аноду.
С повышением температуры катода ток насыщения увеличивается. Разделив ток насыщения на поверхность S катода, получаем плотность тока насыщения jнас = iнасçS. В 1901г. Оуэн Ричардсон, исходя из классических представлений, теоретически нашел зависимость плотности тока насыщения от температуры поверхности катода. Уточненная Дешманом в 1923г. с учетом квантовых представлений, зависимость jнас(Т) имеет вид: . Формула Ричардсона-Дэшмана (14.2)
Здесь еj – работа выхода, А – константа, имеющая разное значение у разных металлов и колеблющаяся около теоретического значения А= 1,2·10 6 Аç(м 2 К 2 ).
3. Контактная разность потенциалов.
Рассмотрим процессы, происходящие при контакте двух разных металлов. Допустим, до электрического контакта металл 1 (на рис.103 слева) имеет работу выхода еj1, а работа выхода металла 2 больше, j2 > j1.
Приведем металлы в состояние электрического контакта, то есть сблизим их до такого расстояния, при котором возможен эффективный обмен электронами. Поскольку работа выхода электронов из металла 2 больше, то уровень Ферми в металле 2 ниже, чем в металле 1. В результате электроны проводимости с уровня Ферми металла 1 начинают переходить на уровень Ферми металла 2.
В результате такого перехода электронов металл 2 заряжается отрицательно, энергия электронов и, соответственно, уровень Ферми в нем повышаются. Металл 1 заряжается положительно, энергия электронов и уровень Ферми в нем понижаются. Между металлами возникает контактная разность потенциалов j12.
Суммарное перетекание зарядов прекратится, когда уровни Ферми сравняются, а разность потенциалов между проводниками будет равна разности потенциалов выхода, j12 = j2 - j1, и встречные потоки электронов сравняются n21=-n12 (рис.103 справа). Контактная разность потенциалов между проводниками создает для электронов, переходящих в проводник с большей работой выхода, потенциальный барьер высотой еj12.
Оценим количество электронов, перетекающих из одного металла в другой при возникновении контактной разности потенциалов j12. Будем считать, что между контактирующими металлами остается зазор шириной d, а заряды концентрируются на контактирующих поверхностях. Тогда заряд Q на каждой из поверхностей, необходимый для создания напряжения j12, найдется из формулы плоского конденсатора, . (14.3)
Как видно из таблицы 14.1, контактная разность потенциалов В. Расстояние d между металлами не может быть меньше параметра решетки а » 0,3 нм. Полагая j12 =1 В и d = 0,3 нм, получаем максимальную плотность заряда на контактирующих поверхностях.
Разделив на заряд электрона получаем, что на 1 м 2 поверхности приходится 2·10 17 электронов. Если диаметр атомов взять равным постоянной решетки а = 0,3 нм, то на 1 м 2 поверхности в одноатомном слое металла размещается атомов. Если атомы металла содержат по одному валентному электрону, то для создания контактной разности потенциалов 1 В потребовалось всего лишь (2×10 17 ç10 19 )´100% = 2% электронов проводимости одноатомного поверхностного слоя.
4. Закон Вольта.
Контактную разность потенциалов открыл в девяностых годах XVIII века итальянец Александр Вольта. В серии экспериментов 1792–1794 годов он установил, что в цепочке из ряда последовательно соединенных металлов контактная разность потенциалов зависит лишь от крайних металлов. Этот опытный факт называется законом Вольта. Действительно, пусть имеется цепочка из металлов 1,2,3,4 (рис.104). Работа выхода металлов еj1, еj2, еj3, еj4. На границе каждой пары возникает контактная разность:
Просуммировав левые и правые части, получаем: . (14.5)
Сумма всех контактных ЭДС (левой части равенства) равна контактной ЭДС крайних металлов в цепочке (правая часть равенства). Если концы цепи замкнуть, то независимо от количества звенев сумма контактных разностей потенциалов равна нулю. Тока в цепи нет.
5. Термо-ЭДС.
Сумма контактных разностей потенциалов в замкнутой цепи равна нулю лишь при условии, что температуры всех контактов одинаковы. В 1821 г. Томас Зеебек, сжимая концы висмутовой и медной пластинок теплыми пальцами обнаружил, что если цепь замкнута, то в ней протекает ток. Это явление возникновения ЭДС в цепи из разных металлов при перепаде температур между спаями называют эффектом Зеебека или термоэлектричеством. В рамках классической электронной теории можно дать простое толкование явлению Зеебека и получить зависимость термо-ЭДС от перепада температур.
Пусть имеется замкнутая цепь из двух металлов 1 и 2 со спаями A и B (рис.105). Полагаем, что электроны проводимости на верхних уровнях зоны проводимости распределяются в силовом поле решетки по закону Больцмана.
Здесь n01 и n02 – концентрация электронов проводимости на уровнях Ферми. В силу полной заполняемости этих уровней будем полагать n01 = n02; U1 и U2 – потенциальная энергия электронов в металлах 1 и 2. Она может изменяться от нуля на уровне Ферми до еj (работа выхода) на нулевом уровне. Разделим первое уравнение на второе.
Разделив разность U1 –U2 на заряд электрона е, получаем концентрационную разность потенциалов между металлами 1 и 2. . (14.9)
Если температуры спаев ТА и ТB одинаковы, то концентрационная ЭДС в замкнутой цепи, так же, как контактная разность потенциалов, равна нулю. Тока в цепи нет. Если же температуры спаев разные, ТА ¹ ТB, то в цепи возникает термо-ЭДС (рис.106). Концентрационные перепады потенциалов в контактах А и B разные.
Учитывая грубость классических приближений, обычно выделяют лишь температурную зависимость, которая хорошо подтверждается опытом при малых перепадах температур, . (14.12)
Термо-ЭДС, возникающая в цепи из разных металлов, широко применяется для измерения температур в диапазоне от 0 К до » 1000°С. Соответствующее устройство из двух разных металлов называется термопарой. Один спай термопары поддерживается при постоянной температуре, например при 0 о С в сосуде с тающим льдом, другой помещают в ту среду, температуру которой хотят измерить. О величине температуры можно судить как по величине термотока, измеряемого гальванометром, так и более точно по величине термо-ЭДС, измеряемой методом компенсации. С помощью термопар можно измерять температуру с точностью до сотых долей градуса.
6. Эффект Пельтье,1834 г.
Он обратен эффекту Зеебека и состоит в том, что при пропускании тока по цепи из разных металлов один контакт у металла нагревается, другой охлаждается.
Пусть в цепи из двух разных металлов действует источник тока – батарея Б. В результате в цепи идет постоянный ток I (рис.107). Проходя спай B, электроны, идущие по цепи на рисунке против часовой стрелки, дополнительно ускоряются полем контактного потенциала. Их скорость дрейфа увеличивается, поэтому при столкновении с узлами электроны передают им большую, по сравнению со средней, энергию. Спай В нагревается больше, чем рядом расположенные участки проводников.
В спае А электроны тормозятся контактным полем, их скорость дрейфа уменьшается, поэтому спай А нагревается меньше, чем рядом расположенные участки проводов. Кроме того, для установления равновесия этих электронов с электронным газом им необходимо приобрести еще энергию. Эту энергию они черпают из решетки. В результате спай А охлаждается больше, чем нагревается. В итоге теплота в спае А поглощается.
Выделяющаяся или поглощающаяся теплота Пельтье QП в контакте пропорциональна заряду It, прошедшему через контакт. . (14.13)
Здесь П – коэффициент Пельтье связан с дифференциальной термо-ЭДС соотношением: П = аDT.(14.14)
Где DТ – разность температур между контактами.
Эффект Пельтье позволяет создавать малогабаритные холодильные устройства. Их особенность в том, что изменяя направление тока в цепи, можно один и тот же контакт заставить как поглощать тепло (холодильник), так и выделять его (нагреватель).
7. Эффект Томсона.
В 1853 – 54 г.г. Рудольф Клаузиус и Уильям Томсон независимо друг от друга применили к явлениям термоэлектричества принципы термодинамики. В процессе построения термодинамической теории термоэлектричества Томсон установил, что неравномерно нагретый проводник должен вести себя как система находящихся в контакте физически разнородных участков. На этом основании Томсон пришёл к заключению и подтвердил его экспериментально, что в однородном неравномерно нагретом проводнике должно выделяться или поглощаться тепло Пельтье (тепло Томсона). Само явление назвали эффектом Томсона.
Принципиальная схема экспериментальной установки изображена на рис.108
Концы двух одинаковых проводящих стержней помещены в два термостата с разными температурами Т1 и Т2. Допустим, Т1 > Т2. Тогда градиент температуры в верхнем стержне направлен по току I, а в нижнем – против тока. В результате в одном стержне выделяется тепло Томсона (его температура выше), а в другом – поглощается.
Знак эффекта у разных проводников разный. В висмуте и цинке, например, тепло выделяется, если поток тепла и электрический ток совпадают по направлению (на рисунке нижний проводник). А в Fe, Pt, Sb при тех же условиях тепло поглощается. С изменением направления тока знак эффекта во всех проводниках меняется.
Тепло Томсона Q, выделяющееся в проводнике, пропорционально перепаду температур ΔТ, току I, протекающему по проводнику, и времени t Q = σΔTIt.
Здесь σ – коэффициент Томсона. Он зависит от материала провода и от его температуры. Коэффициент σ невелик. У металлов он порядка 10 –5 ВçК. За положительное направление тока принимают направление градиента температур, то есть направление от холодного конца проводника к горячему. Если тепло при этих условиях выделяется (проводник нагревается), эффект Томсона считается положительным.
Количественно эффект Томсона исследовал в 1867 г. Франсуа Леру. В установке, собранной по схеме рис. 108, к поверхности стержней он присоединял спаи термопар. Пока тока через стержни не было, термоЭДС в цепи термопар была равна нулю. При включении тока через стержни появлялась термоЭДС, величина и знак которой позволяли определить коэффициент Томсона σ.
8. Закон Джоуля – Ленца в замкнутой цепи всегда выполняется. Суммарный эффект Пельтье и Томсона в замкнутой цепи равен нулю, поскольку наряду с участками цепи, где тепло Пельтье и Томсона выделяется, всегда есть участки, где такое же тепло поглощается.
Читайте также:
