Избыток металлического натрия формула
Обновлено: 04.07.2024
В результате реакции предельного двухатомного спирта массой 30,4 г с избытком металлического натрия получено 8,96 л (н. у.) газа. Указанный спирт не взаимодействует со свежеполученным осадком гидроксида меди(ІІ).
На основании этих данных:
1) произведите вычисления, необходимые для установления молекулярной формулы спирта и запишите молекулярную формулу спирта;
2) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле;
3) приведите уравнение реакции его взаимодействия с металлическим натрием.
Данную задачу проверяют не автоматически, а вручную. Ознакомьтесь с критериями оценки, правильным решением и сами себе поставьте оценку от 0 до 3 баллов. Даже если вы ошиблись в цифровом ответе, можно получить несколько баллов за правильный ход решения. Форма для оценки находится внизу страницы.
| Содержание верного ответа и указания по оцениванию (допускаются иные формулировки ответа, не искажающие его смысла) | Баллы |
|---|---|
| Ответ правильный и полный, содержит следующие элементы: 1) правильно произведены вычисления, необходимые для установления молекулярной формулы вещества, и записана молекулярная формула вещества; 2) записана структурная формула органического вещества, которая отражает порядок связи и взаимное расположение заместителей и функциональных групп в молекуле в соответствии с условием задания; 3) с использованием структурной формулы органического вещества записано уравнение реакции, на которую даётся указание в условии задания | 3 |
| Правильно записаны два элемента ответа | 2 |
| Правильно записан один элемент ответа | 1 |
| Все элементы ответа записаны неверно | 0 |
| Максимальный балл | 3 |
1) Напишем примерное уравнение реакции:
C X n H X 2 n ( O H ) X 2 + 2 N a → C X n H X 2 n ( O N a ) X 2 + H X 2 ↑ \ce(OH)2 + 2Na -> C_nH_(ONa)2 + H2 ^> C X n H X 2 n ( O H ) X 2 + 2 N a
C X n H X 2 n ( O N a ) X 2 + H X 2 ↑
Выбрана формула двухатомного спирта в уравнении реакции.
Найдём количество вещества водорода:
Исходя из уравнения реакции видим, что количество вещества водорода равно количеству вещества спирта:
Молярную массу исходного вещества можно найти исходя из массы, данной в условии, и количества вещества, найденного нами:
С помощью молярной массы можем определить молекулярную формулу:
2) В задании уже указано, что это спирт, причём многоатомный. Также есть подсказка, что он не взаимодействует со свежеприготовленным оскадком гидроксида меди, а, значит, что гидроксильные группы расположены не рядом, а у разных атомов углерода. Тогда структурная формула выглядит следующим образом:
3) Уравнение реакции вещества с натрием:
H O − C H X 2 − C H X 2 − C H X 2 − O H + 2 N a → N a O − C H X 2 − C H X 2 − C H X 2 − O N a + H X 2 ↑ \ce NaO-CH2-CH2-CH2-ONa + H2 ^> H O − C H X 2 − C H X 2 − C H X 2 − O H + 2 N a
N a O − C H X 2 − C H X 2 − C H X 2 − O N a + H X 2 ↑
Избыток металлического натрия формула
Формула металлического натрия
В обычных условиях натрий представляет собой серебристо-белый (в тонком слое — с фиолетовым оттенком), легкий, очень мягкий, низкоплавкий металл (относится к группе щелочных металлов) (рис. 1).
Пар натрия имеет темно-красный цвет и состоит из атомов Na (преобладают) и молекул Na2.
Весьма реакционноспособный; на воздухе покрывается оксидной пленкой (тускнеет), воспламеняется приумеренном нагревании. Устойчив в атмосфере аргона и азота. Сильный восстановитель; энергично реагирует с водой, кислотами, неметаллами.
Хорошо сохраняется под слоем бензина или керосина, легко суспендируется в кипящих инертных растворителях (толуол, ксилол, гептан, октан и др.). В инертной атмосфере расплавленный натрий быстро распределяется по поверхности некоторых твердых веществ (NaCl, Na2СО3, уголь, железо, Аl2О3, ZrO2), образуя серо-черные моноатомные покрытия. Окрашивает пламя газовой горелки в желтый цвет.

Рис. 1. Металлический натрий. Внешний вид.
Химическая формула металлического натрия
Химическое обозначение натрия – Na от латинского слова «natrium». Этот химический элемент расположен в третьем периоде в IА группе Периодической таблицы Д.И. Менделеева. Относится к элементамs-семейства. Металл. Относительная атомная масса натрия равна 22,9898 а.е.м.
Электронная формула металлического натрия
В ядре атома натрия содержится 11 протонов и 12 нейтронов (массовое число равно 23). В атоме натрия есть три энергетических уровня, на которых находятся 11 электронов (рис. 2).
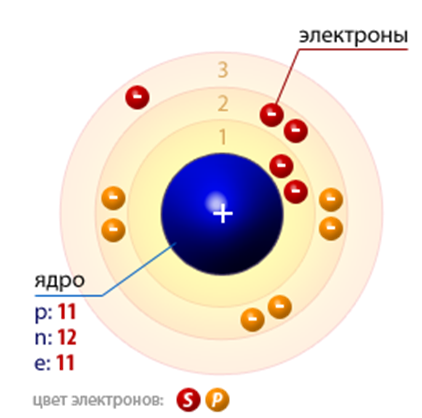
Рис. 2. Строение атома натрия.
Электронная формула атома натрия в основном состоянии имеет следующий вид:
Примеры решения задач
| Задание | Определите молекулярную формулу кальциевой селитры, в которой массовые отношения кальция, азота и кислорода равны 10:7:24. Относительная молекулярная масса кальциевой селитры 164. |
| Решение | Для того, чтобы узнать, в каких отношениях находятся химические элементы в составе молекулы необходимо найти их количество вещества. Известно, что для нахождения количества вещества следует использовать формулу: |
Найдем молярные массы кальция, азота и кислорода (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел). Известно, что M = Mr, значит M(Ca)= 40 г/моль, Ar(N)=14 г/моль, а М(O) = 32 г/моль.
Тогда, количество вещества этих элементов равно:
n (Ca) = m (Ca) / M (Ca);
n (Ca) = 10 / 40 = 0,25 моль.
n (N) = 7 / 14 = 0, 5 моль.
n (O) = 24 / 16 = 1,5 моль.
Найдем мольное отношение:
n(Ca) :n(N):n(O) = 0,25 : 0,5 : 1,5= 1 : 2 : 6,
т.е. простейшая формула соединения кальция, азота и кислорода имеет вид CaN2O6 и молярную массу 164 г/моль [M(CaN2O6) = Ar(Ca) + 2×Ar(N) + 6×Ar(O) = 40 + 2×14 + 6×16 = 40 + 28 + 96 = 164 г/моль]
Чтобы найти истинную формулу органического соединения найдем отношение полученных молярных масс:
Значит формула соединения кальция, азота и кислорода имеет вид CaN2O6или Ca(NO3)2. Это нитрат кальция.
| Задание | Установите массовую формулу вещества, содержащего 55,2% калия, 14,6% фосфора и 30,2% кислорода. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле: |
ω (Х) = n × Ar (X) / M (HX) × 100%.
Обозначим количество моль элементов, входящих в состав соединения за «х» (калий), «у» (фосфор) и «z» (кислород). Тогда, мольное отношение будет выглядеть следующим образом (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел):
x:y:z = ω(K)/Ar(K) : ω(P)/Ar(P) : ω(O)/Ar(O);
x:y:z= 55,2/39 : 14,6/31 : 30,2/16;
x:y:z= 1,4 : 0,5: 1,9 = 3 : 1: 4.
Значит формула соединения калия, фосфора и кислорода будет иметь вид K3PO4. Это фосфат калия.
Тест по теме Решение задач по химии
N.B. Разделение на темы вопросов по химии носит приблизительный характер, так как сам формат большинства вопросов ЕГЭ по химии исключает возможность однозначного отнесения вопроса к одной определённой теме.
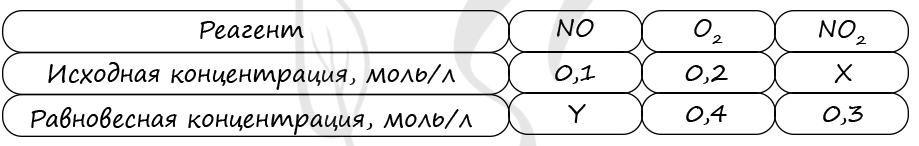
6752. В реактор постоянного объёма поместили некоторое количество оксида азота (IV) и кислорода. В результате протекания обратимой реакции в реакционной системе

установилось химическое равновесие.
Используя данные, приведённые в таблице, определите исходную концентрацию оксида азота(IV) и равновесную концентрацию оксида азота(II).

Верный ответ: 63
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6752.
6773. Сколько граммов щавелевой кислоты следует растворить в 200 г 5%-ного раствора её, чтобы массовая доля кислоты стала равной 8%? (Запишите число с точностью до десятых.)
Верный ответ: 6,5
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6773.
6780. Насыщенный при 20°С раствор нитрата серебра массой 140 г охладили до 0°С (растворимость нитрата серебра при 20°С 228 г/100 г воды, а при 0°С - 125 г/100 г воды), выпавшую в осадок безводную соль отделили, а от оставшегося раствора отобрали порцию массой 19,22 г. Вычислите, какой объем смеси сероводорода и азота (при н.у.), содержащий 40% сероводорода по массе, необходимо пропустить через эту порцию раствора, чтобы полностью осадить содержащиеся в ней ионы серебра (указывайте единицы измерения искомых физических величин).
2) Определим массу раствора и массу растворенного нитрата серебра после охлаждения

После охлаждения масса раствора равна (140 - 43,9) = 96,1 г. Масса растворенного нитрата серебра равна (97,3 - 43,9) = 53,4 г
3) Вычислим массу и объем сероводорода, который прореагирует с порцией раствора 96,1 : 19,22 = 5 ⟹ в порции раствора содержится 53,4 : 5 = 10,68 г
n(AgNO3) = 10,68 : 170 = 0,0628 моль
n(H2S) = 0,5n(AgNO3) = 0,0314 моль
m(H2S) = 0,0314 · 34 = 1,067 г, V(H2S) = 0,0314 · 22,4 = 0,7 л
4) Вычислим объем смеси
m(N2) = 0,6 · m(H2S) : 0,4 = 0,6 · 1,067 : 0,4 = 1,6 г
n(N2) = 1,6 : 28 = 0,057 моль, V(N2) = 0,057 · 22,4 = 1,27 л
V(смеси) = 0,7 + 1,27 = 1,97 л
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6780.
6781. В результате реакции предельного двухатомного спирта массой 30,4 г с избытком металлического натрия получено 8,96 л (н. у.) газа. Указанный спирт не взаимодействует со свежеполученным осадком гидроксида меди(II).
На основании этих данных:
1) произведите вычисления, необходимые для установления молекулярной формулы спирта и запишите молекулярную формулу спирта;
2) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле;
3) приведите уравнение реакции его взаимодействия с металлическим натрием.
Определена молекулярная формула вещества:
M(CnH2n(OH)2) = 12n + 2n + 34 = 76 г/моль
14n + 34 = 76
14n = 42
n = 3
Молекулярная формула: C3H6(OH)2
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6781.
6787. В реактор постоянного объёма поместили некоторое количество оксида азота(II) и кислорода. В результате протекания обратимой реакции в реакционной системе
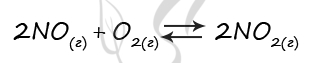
установилось химическое равновесие.
Используя данные, приведённые в таблице, определите исходную концентрацию кислорода и равновесную концентрацию оксида азота(II).

Верный ответ: 52
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке ;)
При обращении указывайте id этого вопроса - 6787.
Читайте также:
