Как происходит кристаллизация металлов
Обновлено: 17.05.2024
Эмпирически доказано, что при небольшом давлении с уменьшением температуры все вещества (исключение - гелий) превращаются в твердые тела, то есть кристаллизуются.
Если давление достаточно высоко, то большое количество веществ превращается из жидкостей в твердые вещества. Вещества, называемые аномальными, сохраняют свою жидкую фазу вплоть до $T=0K$ при большом давлении. К таким веществам относят те вещества, плотность которых уменьшается при переходе от жидкости к твердому состоянию. Температура плавления таких веществ уменьшается при росте давления. К аномальным веществам относят, например:
Кристаллизацией называют переход из состояния жидкости в твердое состояние при определенных температуре и давлении.
В процессе кристаллизации выделяется теплота, которую именуют теплотой кристаллизации.
Кристаллизация – это фазовый переход первого рода. Она происходит при давлении ниже тройной точки.
Соотношение давления и температуры в фазовом переходе первого рода задает уравнение Клапейрона - Клаузиуса:
где $L$ - скрытая теплота кристаллизации; $V_2$ - удельный объем вещества в твердом состоянии; $V_1$ - удельный объем этого же вещества в виде жидкости.
У большого количества веществ удельный объем в процессе перехода из жидкого состояния в твердое, становится меньше, соответственно плотность растет. Получается, что для этих веществ давление в состоянии фазового перехода $p$ при увеличении температуры увеличивается, поскольку $\frac >0$.
Металлы могут находиться в трех состояниях:
- в виде газа;
- жидкости;
- твердом состоянии,
это зависит от температуры и давления.
Химически чистые металлы обладают температурой плавления, при которой они переходят из твёрдого состояния в жидкость, и температурой кипения, при которой они становятся газами.
Готовые работы на аналогичную тему
Температуры плавления металлов могут колебаться:
- от $-38,9^0 C$ у ртути;
- до $+3410^0C$ у вольфрама.
Возникновения кристаллической решетки идет в процессе перехода металла из состояния жидкости в состояние твердого тела. Если условия в этом процессе являются идеальными, то результатом этого перехода атомы расположатся в геометрически верной структуре, между ними будут определенные расстояния, то есть атомы составят кристаллическую решетку. Так, в процессе медленного охлаждения получают монокристаллы, масса которых достигает 200 грамм и больше. Эти кристаллы используют, например, в полупроводниковой технике.
Кривые охлаждения расплавов
Остывание расплавленного металла при уменьшении температуры происходит плавно (рис.1), кривая $A$. Однако, если достигается температура кристаллизации $T_k$, возникает горизонтальный отрезок, который связывают с наличием выделения скрытой теплоты кристаллизации, компенсирующей отвод теплоты. При дальнейшем уменьшении температуры металл становится твердым, и его температура продолжает уменьшаться.
Рисунок 1. Кривые охлаждения расплавов. Автор24 — интернет-биржа студенческих работ
В реальной действительности кривая кристаллизации несколько иная (рис.1 $B$). Это происходит потому, что металл в состоянии жидкости, способен существовать при температуре более низкой ($T_p$), чем температура кристаллизации. Температуру $T_p$ называют температурой переохлаждения ($T_p$ В процессе кристаллизации металлов можно выделить две стадии:
- Возникновение центов кристаллизации.
- Рост кристаллов.
Существует несколько схем, которые объясняют процесс кристаллизации жидких металлов. В расплаве возникают центы кристаллизации. При уменьшении температуры ниже, чем $T_p$ (или $T_k$) за короткий отрезок времени в веществе возникают новые центры кристаллизации, они растут. При свободном процессе кристаллизации появляется первичная ось, потом возникают вторичные оси и оси высших порядков. Кристаллы обретают древовидную (дендритную) форму.
В настоящих условиях кристаллизация протекает поначалу с большой скоростью, но при взаимном столкновении увеличивающихся кристаллов скорость процесса уменьшается. До тех пор, пока кристалл находится в жидкости, он обладает правильной формой. Когда кристаллы сталкиваются между собой, они срастаются, правильная форма их нарушается. Так появляются кристаллы с неправильной формой, называемые зернами (кристаллитами).
Факторы, влияющие на кристаллизацию
На прохождение процесса кристаллизации оказывают основное влияние:
- Наличие температуры переохлаждения.
- Скорость и направление отвода теплоты.
- Наличие примесей в металле, которые являются центрами кристаллизации.
Отметим, что в направлении отвода тепла в процессе кристаллизации, кристалл растет существенно быстрее, чем в других направлениях. Это ведет к возникновению неправильной формы кристаллов.
Рассмотрим кристаллизацию стали. Слитки стали создают в металлических изложницах. В этих емкостях металл не способен кристаллизоваться одновременно во всем объеме, поскольку теплота отводится от вещества не равномерно. Процесс затвердевания начинается у стенок и дна емкости, так как эти части имеют более низкую температуру, чем вещество внутри. Твердая сталь имеет более высокую плотность, чем ее расплав, в этой связи в слитке в верхней части, в результате уменьшения объема возникает усадочная раковина.
По химическому составу вещество будет неоднородным. Оси растущего кристалла имеют больше легкоплавких элементов, затвердевающих медленнее.
Кристаллизация металлов
Схема роста кристаллов показана на рис. 2. Кристалл растет в направлении, противоположном отводу тепла. Сначала образуется главная ось кристалла 1, затем на главной оси образуются оси первого порядка 2, на них – оси второго порядка 3, на них – оси следующего порядка и т. д., пока в этом объеме есть жидкий металл.
Атомы жидкости пристраиваются к атомам кристаллов, создавая их форму и обеспечивая их рост. Сначала кристаллы растут свободно, сохраняя правильную геометрическую форму до момента их соприкосновения. В месте соприкосновения кристаллов рост их отдельных осей и граней прекращается. В результате к окончанию процесса кристаллизации кристаллы не имеют правильной геометрической формы, но сохраняют свое древовидное строение. Кристаллы древовидной формы называются дендритами (см. рис. 2).
Дендритное строение – признак литого состояния металла (слиток, отливка). При значительной пластической деформации литого металла форма и размеры кристаллов изменяются – дендриты дробятся, из них образуются новые кристаллы неопределенной формы, называемые зернами (рис. 3). Зернистое строение – признак деформированного металла (прокат, поковки, штампованные полуфабрикаты).
Рис. 2. Дендритная кристаллизация: а – схема дендритного строения
по Чернову; б – схема кристаллизации слитка; дендриты: Чернова (в),
на поверхности сурьмы (г) и алюминия (д)
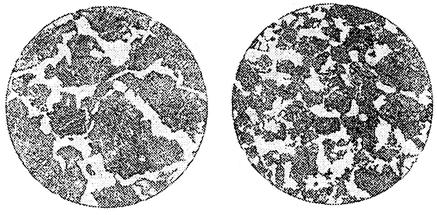
Рис. 3. Микроструктура доэвтектоидной стали:
а – крупнозернистая; б – мелкозернистая
Размер кристаллов металла во многом определяет его прочностные свойства: чем мельче кристаллы, тем выше сопротивление металла ударным и циклическим нагрузкам. Итак, в процессе кристаллизации два фактора определяют строение металла: число центров кристаллизации и скорость роста кристаллов из этих центров.
Проследим за изменением температуры металла при охлаждении жидкости через равные промежутки времени (рис. 4). Сначала температура жидкого металла понижается равномерно в зависимости от скорости охлаждения V1, V2, V3. Затем понижение температуры прекращается и на кривой охлаждения появляется горизонтальный участок (площадка). В это время отвод тепла компенсируется выделением скрытой теплоты кристаллизации и металл переходит в твердое состояние (образуются и растут кристаллы). После окончания кристаллизации температура вновь равномерно понижается, металл охлаждается в твердом состоянии.
При теоретической температуре кристаллизации (температуре плавления) жидкий металл и твердые кристаллы могут существовать одновременно и бесконечно долго. Следовательно, кристаллизация может происходить только при определенном переохлаждении металла ниже теоретической (равновесной) температуры. Разность между теоретическим и фактическим значениями температуры кристаллизации металла называется степенью переохлаждения:
где Тпл – теоретическая (равновесная) температура кристаллизации (плавления) металла;
Тк – фактическая температура кристаллизации данного металла.
Степень переохлаждения металла зависит от скорости охлаждения V1, V2, V3 (см. рис. 4).
Скорости охлаждения V1 соответствует малая степень переохлаждения DТ1. Охлаждение расплава со скоростью V2 вызывает увеличение степени переохлаждения DТ2, а большая скорость охлаждения V3 приведет к увеличению степени переохлаждения DТ3, и кристаллизация будет происходить при более низкой температуре. В итоге это скажется на факторах процесса кристаллизации:
Vохл ®DТ®ЧЦК – СРК, (2)
где ЧЦК – число центров кристаллизации;
СРК – скорость роста кристаллов из этих центров.
Однако не всегда имеется возможность регулировать скорость охлаждения жидкого металла. Методом получения мелких кристаллов при затвердевании металла является создание искусственных центров кристаллизации. Для этого в расплавленный металл вводят специальные вещества, называемые модификаторами. Процесс искусственного регулирования количества и размеров кристаллов называется модифицированием.
КРИСТАЛЛИЗАЦИЯ
чивому состоянию с меньшей энергией Гиббса (свободной энергией) G, т.е. когда энергия Гиббса кристалла меньше, чем энергия Гиббса жидкой фазы (рис.10). Если превращение происходит с небольшим изменением объема, то G=U-TS, где U – внутренняя энергия системы, T – абсолютная температура, S – энтропия.
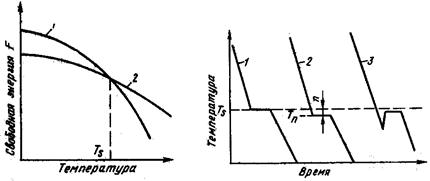
Рис.10 Изменение свободной энергии жидкого (1) и кристаллического (2) состояния в зависимости от температуры
Рис.11. Кривые охлаждения при кристаллизации: теоретический (1) и реальный (2) процессы кристаллизации, (3) – процесс кристаллизации со скачкообразным повышением температуры кристаллизации
Выше температуры Тs меньшей свободной энергией обладает вещество в жидком состоянии, ниже этой температуры – вещество в твердом состоянии. Тs – есть равновесная (теоретическая) температура кристаллизации, при которой металл в обоих состояниях находится в равновесии. Для начала кристаллизации необходимо, чтобы процесс был термодинамически выгоден системе и сопровождался уменьшением свободной энергии системы. Это возможно при некотором переохлаждении жидкости. Температура, при которой практически начинается кристаллизация, называется фактической температурой кристаллизации. Разность между теоретической и фактической температурой кристаллизации есть величина или степень переохлаждения.
Процесс перехода металла из жидкого состояния в кристаллическое можно изобразить кривыми в координатах температура – время (рис.11). Охлаждение металла в жидком состоянии сопровождается плавным понижением температуры и может быть названо простым
охлаждением, так как при этом нет качественного изменения состояния. При достижении температуры кристаллизации на кривой температура – время появляется горизонтальная площадка, связанная с выделением скрытой теплоты кристаллизации. По окончании кристаллизации, т.е. полного перехода в твердое состояние, температура снова начинает снижаться, а твердое кристаллическое вещество охлаждается. Теоретически процесс кристаллизации изображен кривой 1. Кривая 2 показывает реальный процесс кристаллизации с переохлаждением. Кривая 3 иллюстрирует процесс кристаллизации для некоторых металлов, когда из-за большого переохлаждения скрытая теплота выделяется в первый момент настолько бурно, что температура кристаллизации скачкообразно повышается.
Процесс кристаллизации состоит из двух элементарных процессов: возникновение зародышей, или центров кристаллизации и рост кристаллов из этих центров. Схематически процесс зарождения и роста кристаллов показан на рис.12. По мере развития процесса кристаллизации в нем участвует все большее число кристаллов. Поэтому процесс вначале ускоряется, а затем, когда взаимное столкновение растущих кристаллов начинает препятствовать их росту, замедляется. Кроме того, при столкновении и срастании кристаллов их правильная форма нарушается. Поэтому реальные зерна имеют неправильную форму.
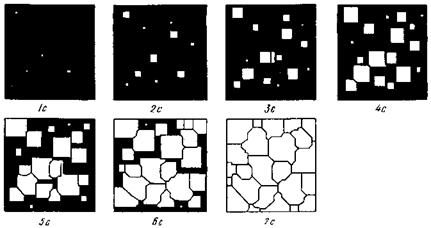
Рис.12. Модель процесса кристаллизации. Под рисунком указано время течения процесса в секундах
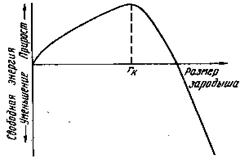
Процесс кристаллизации, как уже было сказано выше, может протекать только при условии уменьшения свободной энергии.
Рис.13. Изменение свободной энергии в зависимости от размера зародыша, rк – критический размер зародыша
Поэтому размер возникшего зародыша должен быть больше некоторого rk (рис.13), называемого критическим (устойчивым) размером.
Кроме самопроизвольного (гомогенного) образования зародышей кристаллизации может происходить и гетерогенное образование, когда в расплавленном материале присутствуют частички примесей, имеющих одинаковую кристаллическую решетку с исходным материалом. Эти примесные частицы и будут центрами кристаллизации.
Кристаллы, образующиеся в процессе затвердевания металла, могут иметь различную форму в зависимости от скорости охлаждения, характера и количества примесей. Чаще всего в процессе кристаллизации образуются разветвленные (древовидные) кристаллы, получившие название дендритов (рис.14).
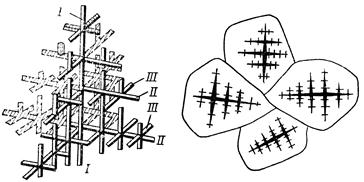
Рис.14. Схема роста кристалла и образования зерна: а – дендрит с осями I, II, III порядка; б – зерна из дендритов
При образовании кристаллов их развитие идет в основном в направлении, перпендикулярном к плоскостям с максимальной плотностью упаковки атомов. Это приводит к тому, что первоначально образуются длинные ветви, так называемые оси первого (I) порядка. Одновременно с удлинением осей первого порядка на их ребрах зарождаются и растут перпендикулярные к ним такие же ветви второго (II) порядка и т.д. Дендритное строение характерно для литого материала.
Структура литого слитка состоит из трех основных зон (рис.15). Первая зона – наружная мелкозернистая корка 1, состоящая из дезориентированных мелких кристаллов – дендритов. При первом соприкосновении со стенками формы в тонком прилегающем слое жидкого металла возникает сильное переохлаждение, сопровождающееся зарождением большого числа центров кристаллизации, что приводит к образованию мелкозернистой структуры. Вторая зона – зона столбчатых кристаллов 2. Степень переохлаждения меняется. В результате из небольшого числа центров кристаллизации начинают расти нормально ориентированные к поверхности корки столбчатые кристаллы. Третья зона – зона равноосных кристаллов 3. Температура застывающего металла почти полностью уравнивается во всем объеме слитка, что и вызывает образование равноосной структуры.
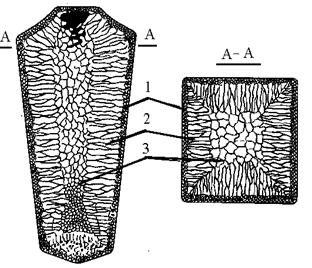
Рис.15. Схема строения стального слитка:
1 – мелкозернистая корка, 2 – столбчатые кристаллы, 3-равноосные кристаллы
Жидкий металл имеет больший объем, чем закристаллизовавшийся, поэтому залитый в форму металл в процессе кристаллизации сокращается в объеме, что приводит к образованию пустот, называемых усадочными
раковинами. Усадочная раковина обычно окружена наиболее загрязненной частью металла, в котором после затвердевания образуются микро- и макропоры и пузыри.
Резюме
Кристаллизацией называется переход металла из жидкого состояния в твердое (кристаллическое). Кристаллизация протекает в условиях, когда система переходит к термодинамически более устойчивому состоянию.
Процесс перехода металла из жидкого состояния в кристаллическое можно изобразить кривыми в координатах время – температура.
Процесс кристаллизации состоит из двух элементарных процессов: возникновение зародышей, или центров кристаллизации и рост кристаллов из этих центров.
Процесс образования зародышей кристаллизации может происходить самопроизвольно (гомогенное образование), а может идти и по гетерогенному пути образования.
Чаще всего в процессе кристаллизации образуются разветвленные (древовидные) кристаллы, получившие название дендритов.
Кристаллизовавшийся слиток имеет три основных зоны.
Первая зона – наружная мелкозернистая корка, состоящая из дезориентированных мелких кристаллов – дендритов. Вторая зона – зона столбчатых кристаллов. Третья зона – зона равноосных кристаллов.
В процессе кристаллизации происходит образование пустот, называемых усадочными раковинами. Усадочная раковина обычно окружена наиболее загрязненной частью металла, в котором после затвердевания образуются микро- и макропоры и пузыри.
Вопросы для повторения
1. Что такое кристаллизация? В каких условиях происходит этот процесс? Объяснить термодинамику процесса.
2. Какие элементарные процессы составляют процесс кристаллизации?
3. Что представляют собой образовавшиеся кристаллы? Какие основные зоны затвердевшего слитка Вы знаете?

Любое вещество может находиться в одном из четырех агрегатных состояний: твердом, жидком, газообразном и плазменном. Агрегатное состояние определяется энергией взаимодействия атомов. Стабильным (равновесным) при определенных внешних условиях является состояние вещества, при котором оно обладает минимумом свободной энергии. Свободная энергия — часть внутренней энергии вещества. Внутренняя энергия вещества — это сумма потенциальной энергии (энергии взаимодействия) и кинетической энергии частиц (тепловые колебания). Часть внутренней энергии, высвобождающаяся при переходе вещества из одного состояния в другое,называется свободной энергией. Чем больше высвободится свободной энергии, тем меньшей энергией будет обладать вещество, тем более стабильно его состояние. Свободную энергию можно представить как аналог потенциальной энергии (рис. 1).
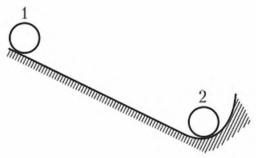
Рисунок 1 - Стремление системы к уменьшению свободной энергии
В положении 1 шарик имеет максимальную потенциальную энергию. Это положение не является устойчивым, шарик скатывается в положение 2, при котором его потенциальная энергия будет равна 0. Вещество может находиться в метастабильном состоянии (закаленная сталь). Такое состояние не обладает минимумом свободной энергии, но является достаточно устойчивым (стабильным). Вещество в метастабильном состоянии может находиться бесконечно долго при условии постоянства внешних факторов.
Первичная кристаллизация металлов и сплавов. Кристаллизация — это переход металла из жидкого состояния в твердое с образованием кристаллического строения. Это первичная кристаллизация (в отличие от вторичной, когда кристаллы металлических фаз выделяются из твердого вещества).
Рассмотрение кристаллизации для металлов и сплавов на их основе связано с тем, что эти материалы получают методом литья, тогда как многие неметаллические материалы производят другими способами. Ряд неметаллических материалов существует в природном виде (углерод), многие химические соединения получают путем химических реакций: карбиды — карбидизацией, нитриды — азотированием и т.п. Процесс кристаллизации (затвердевания) обусловлен стремлением системы к переходу в более устойчивое термодинамическое состояние. При изменении внешних условий, например температуры, свободная энергия системы меняется различно для жидкого и твердого (кристаллического) состояния (рис. 2). Выше температуры Ts более стабильным
является жидкое состояние, так как металл в этом состоянии имеет меньший запас свободной энергии. Ниже температуры Ts меньшим запасом свободной энергии обладает металл в твердом состоянии. При температуре величины свободных энергий твердого и жидкого состояний равны. Это означает, что металл может находиться в обоих состояниях бесконечно долго, так как переход из одного состояния в другое не будет сопровождаться уменьшением свободной энергии. Температура Ts получила название теоретической температуры кристаллизации.
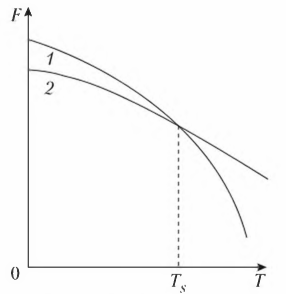
Рисунок 2 - Изменение свободной энергии (Ts) в зависимости от температуры (Т) жидкого (1) и твердого (2) состояния вещества
Для начала кристаллизации необходимо, чтобы свободная энергия металла в твердом состоянии стала меньше свободной энергии жидкого состояния. Это становится возможным при охлаждении жидкости ниже Ts. Температура, при которой фактически начинается процесс кристаллизации, называется фактической температурой кристаллизации (Тк). Охлаждение жидкого металла ниже теоретической температуры кристаллизации называется переохлаждение, а разность между теоретической и фактической температурой кристаллизации — степенью переохлаждения (ΔТ):
Степень переохлаждения зависит от скорости охлаждения жидкого металла. С увеличением скорости охлаждения понижается фактическая температура кристаллизации и, следовательно, возрастает степень переохлаждения. Процесс кристаллизации можно описать с помощью кривых охлаждения, построенных в координатах «температура — время» (рис. 3). Охлаждение в жидком состоянии сопровождается плавным понижением температуры (участок 1 кривой охлаждения), при достижении температуры кристаллизации на кривой охлаждения появляется горизонтальная площадка (участок 2 кривой охлаждения), т.е. охлаждение (понижение температуры) останавливается. Это вызвано тем, что отвод тепла компенсируется выделяющейся в процессе кристаллизации скрытой
теплотой кристаллизации. После полного перехода металла из жидкого состояния в твердое температура вновь начинает плавно снижаться (участок 3 кривой охлаждения). Увеличение скорости охлаждения от V1 до V3 приводит к увеличению степени
переохлаждения (см. рис. 3).
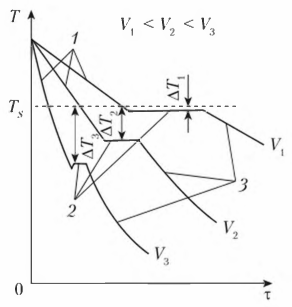
Рисунок 3 - Кривые охлаждения металла
Кристаллизация начинается с образования в жидком металле центров кристаллизации и продолжается за счет роста их числа и размеров (рис. 4). Процесс кристаллизации можно охарактеризовать двумя параметрами: числом центров кристаллизации (ЧЦК),

Рисунок 4- Схема процесса кристаллизации
образующихся в единицу времени в единице объема (1 см 3 /с), и скоростью роста кристаллов (СК ) [мм /с]. Эти параметры зависят от степени переохлаждения, а следовательно, от скорости охлаждения при кристаллизации металла. В соответствии с законом Таммана для каждой степени переохлаждения указанные параметры могут иметь только одно значение (рис. 5).
При теоретической температуре кристаллизации ( Ts) значения ЧЦК и СК равны 0 и кристаллизация происходить не может. При повышении степени переохлаждения значения ЧЦК и СК возрастают, процесс кристаллизации идет быстро. Это объясняется тем, что при высоких температурах, близких к Тs подвижность атомов велика. При определенных степенях переохлаждения значения ЧЦК и СК достигают максимума, после чего снижаются вследствие уменьшения подвижности атомов при низких температурах.
Размер образовавшихся в процессе кристаллизации зерен зависит от соотношения величин ЧЦК и СК, т.е. определяется степенью переохлаждения (скоростью охлаждения
металла в процессе кристаллизации). При малых степенях переохлаждения (низкой скорости охлаждения металла) образуется малое число центров кристаллизации, которые
растут с большой скоростью,---- АТ' (см. рис. 5). В этом случае структура металла после окончания кристаллизации будет крупнозернистой. При больших степенях переохлаждения, напротив, ЧЦК велико, а СК мала (ДГ" - АТ”'), поэтому структура металла получается мелкозернистой.
Если степень переохлаждения настолько велика, что значения ЧЦК и СК близки к пулю, кристаллизации не происходит. При этом образуется твердое тело, имеющее не кристаллическое строение с «правильным» расположением атомов, а аморфное — с хаотическим расположением атомов — «твердая жидкость». Аморфное состояние
характерно для неметаллических материалов (стекла, полимеры). Для получения аморфного состояния у металлических материалов требуется очень большая скорость охлаждения 10 6 . 10 7 °С/с.
Читайте также:
