Как сделать металлическую окалину
Обновлено: 19.05.2024
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH - | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | - | - | Н | Н | Н | |
| F - | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | - | Н | Р | Р |
| Cl - | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br - | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I - | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | - | - | - | Н | - | - | Н | - | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS - | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | - | Н | ? | Н | Н | ? | М | М | - | Н | ? | ? |
| HSO3 - | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | - | Н | Р | Р |
| HSO4 - | Р | Р | Р | Р | Р | Р | Р | Р | - | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 - | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | - | Р |
| NO2 - | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | - | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO - | Р | Р | Р | Р | Р | Р | Р | Р | Р | - | Р | Р | - | Р | Р | Р | Р | Р | Р | Р | - | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые (
Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую:
Скопируйте эту ссылку, чтобы разместить результат запроса " " на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Внимание, если вы не нашли в базе сайта нужную реакцию, вы можете добавить ее самостоятельно. На данный момент доступна упрощенная авторизация через VK. Здесь вы можете выбрать параметры отображения органических соединений. Эти параметры действуют только для верхнего изображения вещества и не применяются в реакциях.
Корректная работа сайта обеспечена на всех браузерах, кроме Internet Explorer. Если вы пользуетесь Internet Explorer, смените браузер. На сайте есть сноски двух типов: Подсказки - помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация - такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Железная окалинаНа поверхности изделий, получаемых путем горячей прокатки, присутствует железная окалина. Ее возникновение обусловлено особенностями данного производственного процесса. Окалина значительно сокращает коррозионную стойкость материала и усложняет последующую обработку, поэтому необходимо полное ее удаление.
Процесс образованияРассматриваемое покрытие представлено продуктом окисления металла. Его формирование связано с высокими температурами и происходит при обработке металла температурой либо давлением. Прокат в любом случае покрыт окисным слоем. Он образуется на открытом воздухе в сухих условиях в виде пленок. Изначально они невидимы даже под микроскопом. Под термическим воздействием толщина окисного слоя возрастает до видимых размеров. Железной окалиной называют толстое покрытие, формирующееся при термическом воздействии в условиях открытого воздуха.
Они представлены гематитом, магнетитом, вюститом. Первые два оксида железа характеризуются большой плотностью и соединены промежуточной структурой. Вюстит наоборот представлен пористым соединением. От названных выше оксидов он отличается большей диффузинной проницаемостью. Вюстит имеет с ними непрочную связь.
Структура железной оксидной пленки определяется окружающими условиями и температурой. Так, в кислородосодержащей среде при нагреве более 570 °C и быстром охлаждении формируется трехслойное покрытие. Внешний слой представлен гематитом, следующий – магнетитом и внутренний – вюститом. Как было отмечено, первые два имеют кристаллическую структуру и прочно взаимосвязаны. Внутренний слой пористой структуры непрочно контактирует с ними. Это обуславливает малое электросопротивление железной оксидной пленки и легкое ее отслаивание.
Так, при меньшем нагреве слой вюстита получается тонким. В случае формирования железной окалины при высокой концентрации пара либо окислов углерода при малом количестве кислорода и температурах более 1000 °C гематит восстанавливается, вследствие чего отсутствует в составе. Таким образом, соотношение слоев напрямую определяется температурой. Так, при 700 °C толщина вюстита составляет 100 мкм, в то время как для магнетита и гематита – 10 и 1 мкм соответственно. Другими словами, состав железной окалины в значительной степени зависит от температуры. Так, при 700-900 °C она представлена почти на 90% вюститом, примерно на 10% магнетитом и менее чем на 1% гематитом. При большем нагреве и избытке кислорода происходит замещение вюстита гематитом. В любом случае формирование слоев железной окалины происходит последовательно в соответствии с их расположением. При охлаждении вюстит утрачивает устойчивость и распадается до железа и гематита. Ввиду этого пленка обретает гематит-магнетитовый состав. При восстановлении гематит и магнетит переходят в железо и воду. Следовательно, в результате получается прокатная окалина, состоящая из железа.
Выше приведены основные закономерности и факторы возникновения железной окалины. В промышленных условиях процесс ее образования весьма сложен и может происходить неоднократно. Методы удаленияУдаление окалины осуществляют тремя способами. Механический метод включает следующие варианты: пропускание материала через ряд роликов, обработку дробью и прочими абразивными материалами. Первая технология основана на деформации металла скручиванием, изгибом, растяжением. Такой способ позволяет убрать большую часть окалины. Его считают черновой обработкой, и после очищают материал дополнительно. Во втором случае осуществляют механическое воздействие на железную окалину металлической дробью, песком и прочими абразивными материалами. Наконец, существуют механизированные технологии, связанные с применением микрорезцовых инструментов, проволочных щеток, наждачных лент и т. д. Химические методы подразумевают обработку деталей в кислотах, солях, щелочах, называемую травлением. При этом большое значение имеет растворимость составляющих железную окалину соединений в кислотах. Так, вюстит легко подвержен ему, в отличие от магнетита. Гематит считают нерастворимым. Травление дифференцируют на химическое и электрохимическое. Далее рассмотрены некоторые варианты. Травление серной кислотой связано с образованием водорода и проникновением его в металл, что ведет к водородной хрупкости, снижающей механические параметры и затрудняющей последующую обработку материала. Поэтому с целью сокращения наводораживания приходится долго выдерживать металл по завершении травления либо нагревать при сушке. К тому же во избежание разрушения металла кислотой после растворения железной окалины используют ингибиторы. Нужно отметить, что в нагретом растворе сталь разрушается быстрее. Травление соляной кислотой идет по тем же закономерностям. Однако, в отличие от серной, для этого не требуется нагрев. Напротив, при температуре более 40°C выделяются хлороводородные соединения. В процессе травления формируются хлористые соли железа. В целом обработка соляной кислотой, в сравнении с серной, обеспечивает лучшую очистку при меньшем наводораживании стали.
Электрохимический способ существенно повышает скорость очистки металла от окалины и сокращает водородную хрупкость, а также расход раствора. Его дифференцируют на анодный, катодный и смешанный варианты. Выбор способа очистки определяется многими факторами, среди которых состав изделия, целевые параметры, последующая обработка и т. д. Оксид железа (II,III)1. Горение железа (ЗАПОМНИ! Железо реагирует с кислородом именно до железной окалины, не до оксида железа(III): 3Fe + 2O2 = Fe3O4 2. Реакция железа с водяным паром при нагревании: 3Fe + 4H2O = Fe3O4 + 4H2 СоставНаружный слой оксида железа — гематит. Он обладает большой твёрдостью (1030 ед. по шкале Виккерса), абразивностью и очень плохо растворяется в кислотах. Под ним в условиях частичной нехватки кислорода формируется более мягкий и почти нерастворимый в кислотах магнетит. Ближе всего к металлу находится рыхлый и мягкий вьюстит, который легко поддается устранению механическим путём или кислотным травлением. Толщина каждого из трёх слоёв зависит от температуры обработки стали. Так, при превышении порога в 570 °C образуется чётко выраженная трёхслойная структура окалины. Дальнейшее повышение температуры ведёт к увеличению толщины вьюстита. Если же сталь обрабатывается при температурах ниже 570 °C, то в составе окалины преобладают магнетит и гематит. По цвету железной окалины можно определить температуру обработки стали. Так, при температуре в 700–750 °C в составе окалины больше гематита, из-за чего она приобретает рыжевато-красный оттенок. Образовавшийся при высокотемпературном (900–1000 °C) прокате слой оксидов из-за более высокого процента вьюстита становится чёрным. раскалить железо — с французского на русский
Что такое отжиг металлаОтжиг металла применяется для получения равновесной и однородной структуры при подготовке изделия к последующей термической или механической обработке, а также для улучшения его физических характеристик после операций резания, сварки, штамповки, прокатки или закалки. Цель отжига — устранить внутренние неоднородности стали, улучшить ее зернистость и равномерность кристаллической решетки, а также снять остаточное напряжение, вызываемое деформацией изделия при различных видах обработки. Особенности этой технологии позволяют:
Одной из характерных особенностей такой термообработки является то, что остывание нагретого металла происходит естественным образом, без применения охлаждающих сред. А температура нагрева при отжиге зависит от состава стали и требуемого результата. Как закалить металл в домашних условиях? | Дом и семьяИ действительно, убедившись на собственном опыте, могу подтвердить: часто лезвие топора современного производства то недокалено (заминается), то, наоборот, перекалено (выкрашивается). Досадно! Причем проверить качество закалки при покупке практически невозможно. Да, с определенной степенью точности можно узнать, как закален ваш ручной инструмент, проведя по режущей кромке напильником. Если напильник очень сильно «липнет» к металлу, почти сто процентов вероятности — недокал, кромка будет слишком мягкой (и не будет держать заточку).Если напильник будет «отскакивать» от поверхности, «гладить» ее, ваша рука не будет при нажатии встречать никакого сопротивления, — это, скорее всего, перекал. Кромка лезвия будет выкрашиваться, более того, инструмент при усилии на изгиб может сломаться. Согласитесь, пользоваться в работе было бы крайне неудобно как изделием из пластилина, так и из стекла — один мнётся, второе ломается. Проблема в том, что продавец не позволит вам «строгать» напильником еще не купленный инструмент. И не примет обратно «построганный». Как же быть, если вы купили инструмент некачественной закалки? Выбрасывать? Продолжать пользоваться, сетуя на брак? Ни первое, ни второе! Вы можете закалить металл в дачных условиях.
Итак, будем считать, что вы готовы. Кладите инструмент в костер, на угли! Чем они белее, тем выше их температура. И контролируйте процесс. Цвет поверхности инструмента в месте закаливания должен быть ярко-малиновым, но ни в коем случае не белым! Если вы перегреете металл, он может просто «сгореть». Следите за тем, чтобы цвет распределялся равномерно, на закаливаемой кромке не должно быть темных участков. Если цвет будет недостаточно ярким — «синюшным», то вы «отпустите» сталь, она будет мягкой. Ни разу не замечали, что какие-нибудь «железяки» после костра становятся очень мягкими (слишком пластичными)? Кстати, так можно «размягчить» сталистую проволоку: сильно нагреть и дать ей медленно остыть. И не старайтесь добела накалить весь инструмент: вам же нужно закалить только режущую кромку! Что ж, представим себе, что закаливаемый инструмент «созрел». Ну, так хватаем его и окунаем в емкость с маслом, чуть «побулькивая» им! Секунды три-четыре, затем резко вынули, секунды две подождали и снова резко отпустили в масло и «побулькали» уже чуть дольше — секунд пять-шесть (до «синюшного» цвета). И тут же — в емкость с водой до полного остывания. Желательно «помешать» воду закаливаемым инструментом для более резкого охлаждения.
Вот такой процесс. Если вы все сделаете правильно — качественная закалка металла вам гарантирована. Разумеется, таким способом нельзя превратить «сырец» из вторчермета в первосортную сталь. Но хотя бы закалка будет нормальной. Этому способу меня научил старый кузнец дядя Коля, и до сих пор я на качество своей закалки не жаловался. Слышал, кто-то использует вместо масла обыкновенный кипяток. Не знаю, попробуйте! Только учтите, что много раз повторять процедуру закалки одного и того же «объекта» вредно: металл «устает», теряет свойства, и потом — только переплавка… Физические свойстваОксид железа (II,III) при комнатной температуре образует чёрные кристаллы кубической сингонии, пространственная группа F d3m, параметры ячейки a = 0,844 нм , Z = 8 (структура шпинели). При 627 °С α -форма переходит в β -форму. При температуре ниже 120—125 К существует моноклинная форма. Ферромагнетик с точкой Кюри 858 К (585 °С). Обладает электрической проводимостью. Полупроводник. Электропроводность низкая. Истинная удельная электропроводность монокристаллического магнетита максимальна при комнатной температуре ( 250 Ом−1·см−1 ), она быстро снижается при понижении температуры, достигая значения около 50 Ом−1·см−1 при температуре перехода Вервея (фазового перехода от кубической к низкотемпературной моноклинной структуре, существующей ниже TV = 120—125 К ). Электропроводность моноклинного низкотемпературного магнетита на 2 порядка ниже, чем кубического ( ~1 Ом−1·см−1 при TV ); она, как и у любого типичного полупроводника, очень быстро уменьшается с понижением температуры, достигая нескольких единиц ×10−6 Ом−1·см−1 при 50 К . При этом моноклинный магнетит, в отличие от кубического, проявляет существенную анизотропию электропроводности — проводимость вдоль главных осей может отличаться более чем в 10 раз . При 5,3 К электропроводность достигает минимума ~10−15 Ом−1·см−1 и растёт при дальнейшем понижении температуры. При температуре выше комнатной электропроводность медленно уменьшается до ≈180 Ом−1·см−1 при 780—800 К , а затем очень медленно растёт вплоть до температуры разложения. Кажущаяся величина электропроводности поликристаллического магнетита в зависимости от наличия трещин и их ориентировки может отличаться в сотни раз. Образует кристаллогидрат состава Fe3O4·2H2O. Химико-термическая обработкаХимико-термическая обработка (ХТО) стали — совокупность операций термической обработки с насыщением поверхности изделия различными элементами (углерод, азот, алюминий, кремний, хром и др.) при высоких температурах. Поверхностное насыщение стали металлами (хром, алюминий, кремний и др.), образующими с железом твердые растворы замещения, более энергоемко и длительнее, чем насыщение азотом и углеродом, образующими с железом твердые растворы внедрения. При этом диффузия элементов легче протекает в решетке альфа-железо, чем в более плотноупакованной решетке гамма-железо. Химико-термическая обработка повышает твердость, износостойкость, кавитационную, коррозионную стойкость. Химико-термическая обработка, создавая на поверхности изделий благоприятные остаточные напряжения сжатия, увеличивает надежность, долговечность. Примечания
Нитроцементация (цианирование) сталиНитроцементация (цианирование) стали — химико-термическая обработка с одновременным поверхностным насыщением изделий азотом и углеродом при повышенных температурах с последующими закалкой и отпуском для повышения износо- и коррозионной устойчивости, а также усталостной прочности. Нитроцементация может проводиться в газовой среде при температуре 840..860°С — нитроцианирование, в жидкой среде — при температуре 820…950°С — жидкостное цианирование в расплавленных солях, содержащих группу NaCN. Нитроцементация эффективна для инструментальных (в частности, быстрорежущих) сталей; она используется для деталей сложной конфигурации, склонных к короблению. Однако, поскольку этот процесс связан с использованием токсичных цианистых солей, он не нашел широкого распространения. ПрименениеО проектеПроект «Декамерон» создан для людей, которые видят потенциал в себе, как в литераторе или просто любителе, в человеке, умеющем или желающем выразить свои мысли. Вы можете рассказывать интересные истории, быть услышанным и оцененным почтенными слушателями или таким же, как Вы. Можете рассказать историю, затрагивающую практически любой аспект человеческой души и человеческих взаимоотношений. Перелистывая дни «Декамерона», Вы можете найти интересную историю тематического дня, а так же рассказать свою. «Декамерон» — это период из десяти дней, каждый из которых имеет свою тематику, каждый из которых приходит в свое время, но Вы можете, авторизовавшись (т.е. указав свой псевдоним и пароль) или зарегистрировавшись, рассказать свою историю в любой из подходящих по тематике дней. Цензура на сайте практически отсутствует, исключая моменты откровенного хулиганства, а также несовпадения истории соответствующей тематике, в этом случае Ваша история просто переносится в соответствующий день «Декамерона». По возможности, следуйте тематике дня: I. О том, что теплит нашу душу. II. О людях, подвергавшимся многоразличным испытаниям. и с которыми, в конце концов и сверх всякого ожидания, все хорошо закончилось III. О том, как люди благодаря своему хитроумию добивались того, о чем страстно мечтали или же вновь обретали утраченное. IV. О своей несчастной любви. V. О том, как влюбленным, после мытарств и злоключений, в конце концов улыбалось счастье. VI. О том, как люди, уязвленные чьей-либо шуткой, платили тем же, или быстрыми и находчивыми ответами предотвращали утрату, опасность и бесчестье. VII. О тех шутках, какие во имя любви или же ради своего спасения , вытворяли со своими догадливыми и не очень догадливыми мужьями жены. VIII. О том, какие шутки ежедневно проделывают друг над другом люди: женщина над мужчиной, или же мужчина над женщиной. А может мужчина над мужчиной или женщина над женщиной, почему бы и нет? IX. О чем угодно и о ком угодно. X. О тех людях, которые совершили нечто щедрое или великодушное в делах любви, либо в иных. Используемое оборудование сегодняВ термических цехах для закалки, отпуска и отжига изделий из стали, как правило, используют одно и то же оборудование. Нагрев осуществляют в камерных печах с открытыми или закрытыми источниками тепла, а также индукционными и газопламенными установками. Отдельные виды этого оборудования могут работать с защитными средами из вакуума или химически нейтральных газов. Для выполнения изотермических операций применяют печи или ванны с расплавленными металлами и солями. Транспортировка изделий производится специальными тележками с рельсовыми направляющими, при этом остужение изделий на воздухе обычно осуществляется прямо на этих транспортных средствах. Для погрузки и разгрузки деталей используются мостовые и консольные краны и кран-балки. Технология производства металлопроката | Опыт. Исследования. Результаты.
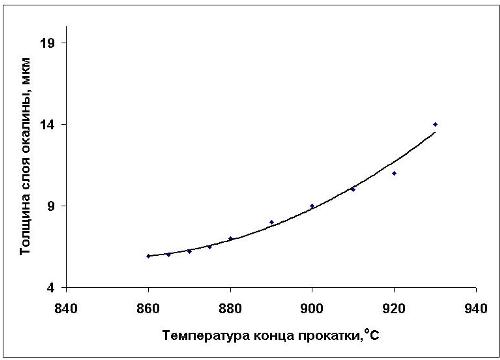
Влияние температуры и условий охлаждения на формирование железной окалины
Одним из факторов, влияющих на толщину слоя железной окалины, является температура конца прокатки. Оптимальной считается температура около 850 о С. С повышением температуры увеличивается и толщина железной окалины , что особенно заметно при температурах более 900 о С (рисунок 1). Уменьшение образования окалины можно получить за счет увеличения скорости прокатки. Так, например, при температуре конца прокатки 880 о С наибольшее уменьшение слоя окалины железа достигается при скорости 5-8,5 м/с. При дальнейшем увеличении скорости толщина слоя окалины меняется незначительно. Стоит отметить также, что образование окалины в воде идет более интенсивно, чем на воздухе, поэтому продолжительность охлаждения полос перед сматыванием желательно снижать до минимума.
Рисунок 1- Зависимость толщины слоя окалины от температуры конца прокатки. Однако, при прокатке на станах с охлаждением на рольгангах и холодильниках имеет место образование толстого слоя окалины железа (до 40 мкм), так как охлаждение проводится на воздухе при большом доступе кислорода. В этом случае температура конца прокатки играет большую роль, чем скорость. Температура сматывания металла в рулон в диапазоне 600-700 о С не оказывает влияния на увеличение слоя железной окалины. Однако, чем выше температура сматывания, тем больше вероятность получения толстой пленки окалины на кромках переднего и заднего концов полосы, которые соприкасаются с атмосферой. Следует также отметить, что увеличение температуры сматывания полосы в рулон приводит к образованию слоя гематита на концах полосы, что нежелательно вследствие его низкой растворимости в кислотах. Минимальная толщина слоя окалины на поверхности широких горячекатаных полос, которые получены на полунепрерывном стане с водяным охлаждением, имеет место на расстоянии ~ 30 мм от края полосы, и толщина слоя железной окалины увеличивается к краям и в середине на ~6,5 г/м 2 при общей массе окалины ~ 50 г/м 2 . На узких полосах, полученных на непрерывном стане после водяного охлаждения перед сматыванием полосы в рулон, различия в толщине слоя окалины железа по краям и середине еще больше. Имеет место и неравномерность изменения толщины пленки окалины от середины к краям в поперечном направлении. На узких полосах, которые охлаждались на воздухе перед сматыванием, количество окалины равномерно увеличивается от края к середине. По длине широкой полосы нет заметной разницы в толщине слоя окалины между началом, серединой и концом рулона. На узких полосах имеется небольшое изменение в середине полосы при водяном охлаждении, а при охлаждении на воздухе толщина окалины снижается к концу рулона. Неравномерность толщины слоя окалины объясняется разными условиями окалинообразования на различных участках полосы. Если система водяного охлаждения работает эффективно, то различия в толщине слоя окалины по середине полосы уменьшаются. Небольшое увеличения слоя окалины по кромкам связанно с более свободным доступом воздуха. Механизм образования железной окалины на поверхности стали
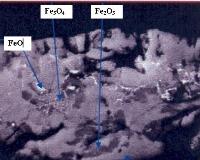
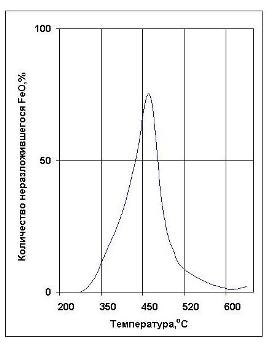
Железная окалина представляет собой продукт окисления металла. Образование железной окалины связанно с процессами термической обработки или обработки металла давлением при высоких температурах.. На поверхности стального проката всегда присутствует окисный слой. Состав и структура окисных соединений будет зависеть от марки стали, состава окружающей среды, температуры, режима термообработки, наличия и количества окислителей, например кислорода и ряда других факторов. В сухой воздушной среде при низких температурах возникают очень тонкие окисные пленки, которые невозможно увидеть даже при увеличении поверхности металла под микроскопом. При увеличении температуры толщина окисного слоя увеличивается, и получаются хорошо различимые окисные слои. При производстве проката поверхность металла часто подвергается высокотемпературному воздействию в присутствии кислорода воздуха, что приводит к образованию толстого многослойного окисного слоя, называемого окалиной. При окислении образуются разные оксиды железа, такие как FeO (вюстит), Fe 3 O 4 (магнетит), Fe 2 O 3 (гематит). Гематит и магнетит являются весьма плотными структурами и прочно соединены друг с другом через промежуточную структуру - Fe 2 O 3 . Слой вюстита является относительно пористым, его соединения как с металлом, так и с магнетитом непрочны. Диффузионная проницаемость магнетита и гематита по сравнению с вюститом незначительна. Все это предопределяется их лучшее защитное действие против окисления. Структура оксидной пленки зависит от температуры и от состава оксидирующей атмосферы. В кислородсодержащей атмосфере при температуре выше 570 о С оксидная пленка состоит из трех слоев. Наружный слой – Fe 2 O 3 прочно связан со средним, имеющим состав и кристаллическую структуру магнетита. Внутренний слой – вюстит, характеризуется повышенной рыхлостью и пористостью. Контакт внутреннего и среднего слоев непрочный. Поэтому, оксидная пленка легко отслаивается и имеет малое электросопротивление. При температуре ниже 570 о С закисная фаза становится неустойчивой и распадается по реакции: Поэтому, в данном случае оксидная пленка, практически состоит из магнетита и гематита. Восстановление полученной оксидной пленки происходит по реакциям: Восстановленный слой состоит из практически чистого железа. Зависимость скорости превращения окислов от температуры представлена на рисунке 1.
Рисунок 1- Зависимость скорости превращения окислов от температуры Строение окалины на поверхности проката в основном соответствует правилу последовательности превращений. Сначала к металлу примыкает вюстит, затем магнетит, и затем внешний слой — гематит. Вюстит легко растворим в минеральных кислотах, в отличие от магнетита и гематита. Магнетит в меньшей степени растворяется в кислотах. Гематит же считается нерастворимым соединением. Трехслойное образование железной окалины получается только при температуре свыше 570 о С и при высоком содержании кислорода, а также при быстром охлаждении. В других условиях образуется двухслойная или однослойная железная окалина. Если окисление железа проходит при температуре меньше 570 о С, то слой вюстита образуется в виде очень тонкой пленки под слоем окалины, которая состоит из магнетита и гематита. Чем ниже температура, тем тоньше слой вюстита. Если процесс окисления происходит при температуре 700 о С, то толщина слоя вюстита будет 100 мкм, слоя магнетита 10 мкм, а гематита — 1 мкм. Если окалина образуется при низком содержании кислорода и высоком содержании водяного пара или окислов углерода, особенно при температуре свыше 1000 о С, то в составе окалины не обнаруживают гематита, так как он восстанавливается. Окалина железа , образующаяся на поверхности проката представляет собой смесь различных фаз, причем состав окалины и ее структура будут определяться режимом тепловой обработки металла. Обычно образуется трехслойная окалина железа, при этом доля каждого окисного соединения в окалине будет зависеть от температуры окисления. При температуре 700-900 о С окалина железа состоит из 10% магнетита и 90% вюстита, а при увеличении температуры свыше 900 о С и при появлении избытка кислорода вместо вюстита начинает возникать слой гематита. Структура железной окалины, получающейся в промышленных условиях всегда более сложная. Это связанно с влиянием различных легирующих элементов, находящихся в стали, неравномерностью состава стали и особенностями производства металла. Например, условия, определяющие образование прокатной окалины на горячекатаном прокате, зависят также и от режима работы стана горячей прокатки. Перед чистовой группой клетей окалина удаляется водой. Но, при прохождении металла через чистовую группу клетей, и в процессе охлаждения металла, прокатная окалина образуется вновь. И, в зависимости от условий прохождения металла, существует несколько различных типов окалины на горячекатаном металле. Читайте также:
|