Какие металлы относятся к s металлам
Обновлено: 28.09.2024
К p-элементов периодической системы относятся элементы с валентным p-подуровнем. Эти элементы расположены в III, IV, V, VI, VII, VIII группах, главных подгруппах периодической системы Д.И.Менделеева. В периоде орбитальные радиусы атомов с увеличением атомного номера уменьшаются, а энергия ионизации в целом растет. В подгруппах элементов с увеличением номера элемента, размеры атомов в общем увеличиваются, а энергия ионизации уменьшается.
p-Элементы III группы К p-элементов III группе относятся бор B, алюминий Al, галлий Ga, индий In и таллий Tl. По характеру этих элементов бор является типичным неметаллом, остальные - металлы. В пределах подгруппы прослеживаются резкий переход от неметаллу к металлам. Свойствами и поведением бор подобный кремния, что является результатом диагональной сродства элементов в периодической системе, согласно которой смещение в периоде вправо вызывает усиление неметаллического характера, а вниз по группе - металлического, поэтому аналогичные по свойствам элементы оказываются расположенными диагонально рядом, например Li и Mg, Ber и Al, B и Si.
Электронное строение валентных подуровней атомов p-элементов III группы в основном состоянии имеет вид ns 2 np 1 . В соединениях бор и трехвалентные алюминий, галлий и индий, кроме того, могут образовывать соединения со степенью окисления +1, а для таллия последний является довольно характерным.
Алюминий является одним из самых распространенных элементов природы, бор - достаточно распространенный, галлий, индий а таллий распространены мало и очень рассеяны, поэтому относятся к редким.
p-Элементы IV группы К p-элементов IV группы относятся углерод C, кремний Si, германий Ge, олово Sn и свинец Pb. Общая электронная конфигурация валентных подуровней атомов p-элементов в основном состоянии ns 2 np 2 . Вследствие наличия 2-х неспаренных p-электронов в соединениях они могут проявлять степень окисления +2, причем эта тенденция усиливается в направлении к свинцу. Атомы могут переходить в возбужденное состояние с образованием четырех валентных электронов, что обусловливает возникновение соединений со степенью окисления +4. Это состояние является характерным для углерода и кремния, способность к выявлению степени окисления +4 ослабляется в направлении к свинцу.
Характер изменения физических свойств элементов и соответствующих простых веществ свидетельствует о закономерное ослабление неметаллических и усиление металлических свойств в ряду C - Si - Ge - Pb.
Углерод и кремний - типичные неметаллы, образующие атомные кристаллические решетки с ковалентной связью. Их простые вещества характеризуются высокими твердостью, температурами плавления и кипения. Для германия эти параметры остаются относительно большими, что вместе с хрупкостью характеризует его как алмазоподобный кристалл с ковалентным типом связи. В то же время в германию уже обнаружено некоторое взнос металлической связи. На это указывает заметное уменьшение ширины запрещенной зоны и росту электропроводности. Для олова полупроводниковые свойства сохраняются лишь до температуры 13,2°С, при дальнейшем нагревании олово переходит в металлический состояние. Свинец - металл, который не проявляет полупроводниковых свойств. Возрастание металлических свойств сопровождается постепенным уменьшением энергии ионизации элементов, их электроотрицательности и усилением восстановительной способности простых веществ.
p-Элементы V группы К p-элементов V группы относятся азот N, фосфор P, мышьяк As, стибий Sb и висмут Bi, при чем азот и фосфор являются типичными элементами, а остальные элементы образуют подгруппу мышьяка. Электронная конфигурация валентных подуровней элементов в основном состоянии ns 2 np 3 .
На последнем энергетическом уровне атомы элементов этой подгруппы имеют по три одноэлектронные орбита ли, которые могут образовывать три ковалентные связи. В то же время в связывании могут принимать участие двухэлектронная орбиталь, а в случае элементов, размещенных после азота, - также свободные nd-орбитали. Так, азот способен образовывать четвертая ковалентная связь по донорно-акцепторным механизмом с использованием своей неподеленной пары электронов. Примером может служить ион аммония NH4 + и его многочисленные производные. Максимально возможная валентность азота в его соединениях равна 4, и каждая пара электронов четырех ковалентных связей занимает одну из четырех орбиталей.
В отличие от азота остальное атомов p-элементов V группы имеют nd-подуровень, вакантные орбитали которого способны участвовать в образовании дополнительных ковалентных связей, за счет чего их ковалентность может расти до 5.
Факторы увеличения радиусов атомов и уменьшение электроотрицательности в ряду N - P - As - Sb - Bi влияют на свойства простых веществ и соединений элементов: постепенно уменьшается стойкость неметаллических форм простых веществ и увеличивается устойчивость металоподобных (азот — типичный неметал с большой электронегативностью, а висмут — типичный металл, электроотрицательности которого лишь 1,70), ослабляются кислотные и усиливаются основные свойства бинарных соединений элементов, их гидроксидов и тому подобное.
p-Элементы VI группы К p-элементов VI группы относятся кислород O, сера S, селен Se, теллур Te и полоний Po. На валентных подуровням атомов p-Элементы VI группы размещено 6 электронов: электронная конфигурация валентных подуровней атомов в основном состоянии ns 2 np 4 .
За счет использования неспаренных электронов элементы в своих соединениях обнаруживают характерную для них валентность 2. Она может расти в случае образования донорно-акцепторных связей, в которых принимают участие двухэлектронные орбитали. Например, в кислых водных растворах существуют ионы гидроксонию H3O + , в которых атом кислорода соединен с тремя атомами водорода ковалентными связями. В отличие от кислорода атомы остальных p-элементов VI группы имеют свободный nd-подуровень, орбитали которого также способны принимать участие в образовании химических связей, в результате чего валентность серы, селена, теллура и полония может возрастать до 6.
Для атомов p-элементов VI группы характерно присоединение электронов для завершения np-подуровня и образования устойчивой электронной конфигурации следующего благородного газа ns 2 np 6 . Это определяет характерный для них степень окисления -2 в соединениях с менее электронегативными элементами.
С переходом к полонию наблюдается характерное для групп p-элементов уменьшение устойчивости высшей степени окисления. Для полония соединения со степенью окисления +6 очень неустойчивы. Это обусловлено сильным ростом энергетической разницы между ns-и np-подуровнями, что затрудняет участие ns-электронов в образовании химических связей.
В ряду O - S - Se - Te - Po возрастают радиусы атомов, что характерно для групп p-элементов, уменьшение энергии их ионизации и электроотрицательности. Ослабление неметаллических свойств элементов проявляется также в уменьшении стойкости неметаллических форм простых веществ и в росте устойчивости металлических. Это приводит к тому, что в отличие от предыдущих элементов подгруппы полоний уже имеет металлическую кристаллическую решетку и относится к металлам.
p-Элементы VII группы - галогены К p-элементов VII группы относятся фтор F, хлор Cl, бром Br, йод I и астату At. Элементы имеют общее название галогены. Электронная конфигурация валентных подуровней атомов p-элементов VII группы соответствует формуле ns 2 np 5 .
На последнем энергетическом уровне атомы элементов имеют по семь электронов, один из которых является неспаренным. Этим объясняется сходство их свойств. Наличие одноэлектронной орбитали определяет характерную для всех элементов валентность 1. Одновременно галогены (кроме фтора) имеют вакантный nd-подуровень, орбитали которого также могут участвовать в образовании химических связей и увеличивать валентность атомов элементов до 7.
Молекулы галогенов двухатомные, неполярные. Все галогены являются неметаллами. В ряду F - Cl - Br - I - At ослабляются признаки неметаличности: фтор — самый типичный элемент-неметала, а астату обнаруживает некоторые свойства элемента-металла.
В пределах своих периодов галогены характеризуются малыми атомными радиусами, что обуславливает их высокие электроотрицательности и сродство к электрону, поэтому для них в сложных веществах самым стойким является степень окисления -1.
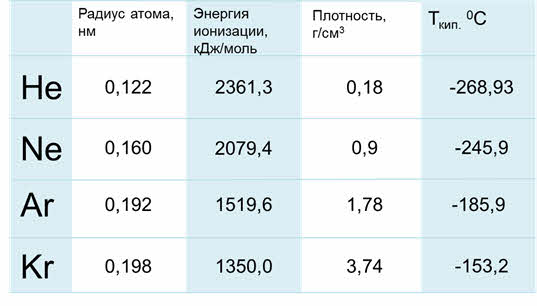
p-Элементы VIII группы К p-элементов VIII группы относятся гелий He, неон Ne, аргон Ar, криптон Kr, ксенон Xe и радон Rh, которые составляют главную подгруппу. Атомы этих элементов имеют завершенные внешние электронные слои, поэтому электронная конфигурация валентных подуровней их атомов в основном состоянии имеет вид 1s 2 (Не) и ns 2 np 6 (остальные элементы). Благодаря очень высокой устойчивости электронных конфигураций они в целом характеризуются большими значениями энергий ионизации и химической инертностью, поэтому их называют благородными (инертными) газами. В свободном состоянии они существуют в виде атомов (одноатомных молекул). Атомы гелия (1s 2 ), неона (2s 2 2p 6 ) и аргона (3s 2 3p 6 ) имеют особо устойчивую электронную структуру, поэтому соединения валентного типа для них неизвестны.
Криптон (4s 2 4p 6 ), ксенон (5s 2 5p 6 ) и радон (6s 2 6p 6 ) отличаются от предыдущих благородных газов большими размерами атомов и, соответственно, меньшими энергиями ионизации. Они способны образовывать соединения, которые зачастую имеют низкую стойкость.
p-Элементы
Химия s-, р-элементов

В этом уроке изучается положение s-, р-элементов в Периодической системе химических элементов Д. И. Менделеева, особенности строения атомов и их свойства.

В данный момент вы не можете посмотреть или раздать видеоурок ученикам
Чтобы получить доступ к этому и другим видеоурокам комплекта, вам нужно добавить его в личный кабинет, приобретя в каталоге.
Получите невероятные возможности



Конспект урока "Химия s-, р-элементов"
Элементы в периодической системе Менделеева делятся на эс, пэ, дэ и эф-элементы. Это разделение осуществляется на основе того, сколько энэргетических уровней имеет электронная оболочка атома и каким уровнем заканчивается заполнение электронной оболочки электронами.
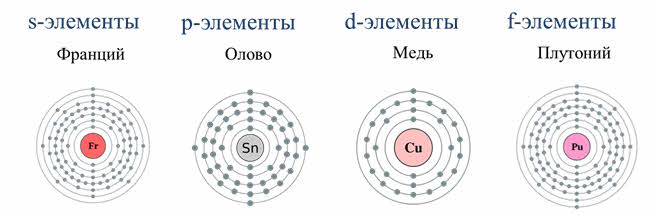
К s-элементам относятся элементы первой А группы – щелочные металлы. Электронная формула щелочных металлов эн-эс-один.
Поэтому для них характерна степень окисления плюс один. Элементы первой А группы обладают сходными свойствами из-за сходного строения электронной оболочки.
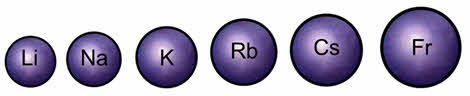
Но при увеличении радиуса в группе от лития к францию связь валентного электрона с ядром ослабевает и уменьшается энэргия ионизации. Атомы щелочных металлов легко отдают свой валентный электрон, поэтому они являются сильными восстановителями.
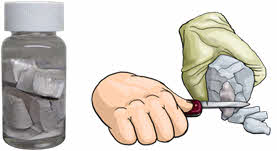
Из-за высокой химической активности щелочные металлы в природе встречаются только в виде соединений. Простые вещества, образованные элементами первой А группы, представляют собой серебристо-белые металлы, которые легко режутся ножом. Все щелочные металлы относятся к лёгким и легкоплавким металлам.
К эс-элементам относятся также элементы второй A группы, из них кальций, стронций, барий называют щелочноземельными металлами. На внешнем энэргетическом уровне у них по два электрона. Из-за своей высокой химической активности они встречаются в природе только в виде соединений. Металлы второй A группы имеют металлический блеск с различными оттенками: от серого до серебристого, температура плавления их выше, чем у щелочных металлов, плотность их меньше пяти грамм на сантиметр кубический, поэтому их относят к легкоплавким металлам.
К p-элементам относятся 30 элементов от третьей А до восьмой А группы периодической системы; пэ-элементы расположены во втором и третьем малых периодах, а также в четвертом, пятом и шестом больших периодах.
Элементы третьей А-группы имеют один электрон на пэ-орбитали. Начиная с четвёртой А и заканчивая восьмой А группой наблюдается заполнение пэ-подуровня до шести электронов. Общая электронная формула пэ-элементов эн-эс-два-эн-пэ-шесть.
В периодах при увеличении заряда ядра атомные радиусы и ионные радиусы пэ-элементов уменьшаются, энэргия ионизации и сродства к электрону возрастают, электроотрицательность увеличивается, неметаллические свойства элементов усиливаются.
Изменение свойств по периодам
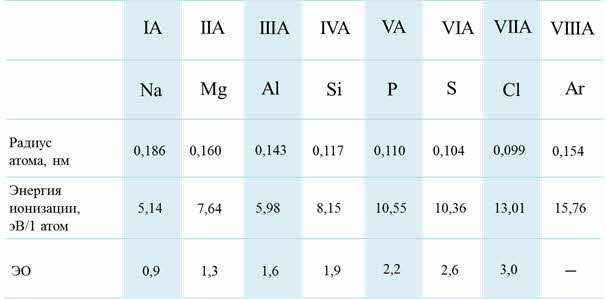
В группах сверху вниз радиусы атомов увеличиваются, энэргия ионизации и сродства к электрону уменьшается, электроотрицательность уменьшается, усиливаются металлические свойства, а неметаллические свойства ослабевают.
Изменение свойств по группам
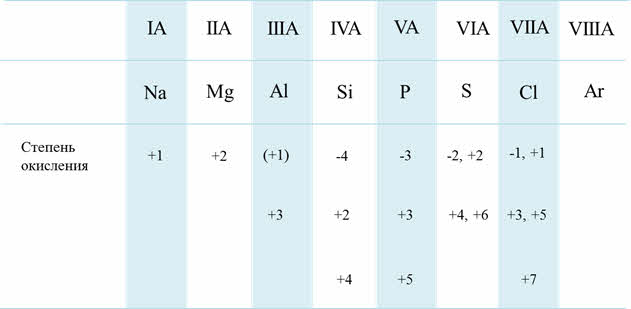
Кроме этого, по периоду с увеличением порядкового номера возрастает высшая степень окисления, а также возможность степеней окисления. Например, у кремния возможны такие степени окисления, как минус четыре, плюс два, плюс четыре; а у хлора – минус один, плюс один, плюс три, плюс пять, плюс семь.
Изменение СО по периоду
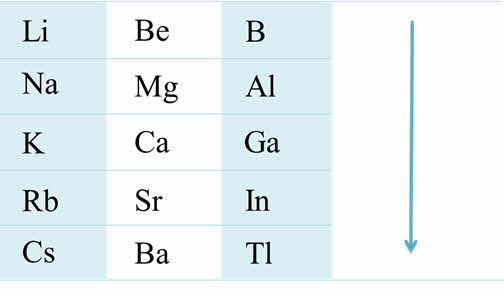
Если рассмотреть от первой до третьей А группы, то можно увидеть, что в группе сверху вниз увеличиваются металлические свойства, а также возрастает активность металлов. Например, во второй A группе металлические свойства и активность бария выражены гораздо сильнее, чем у магния.
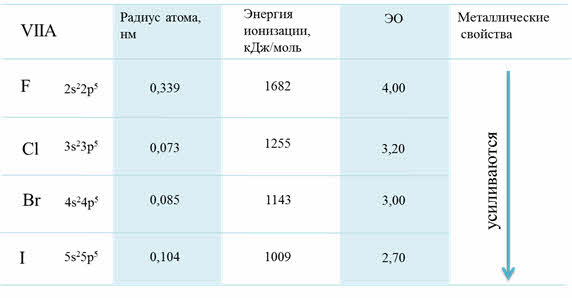
Рассмотрим для примера седьмую A группу – семейство галогенов. В этой группе сверху вниз радиус атома увеличивается, энергия ионизации уменьшается и электроотрицательность также уменьшается.
Возрастание активности металла
Если рассмотреть группы от четвёртой А до седьмой А, то можно проследить, что в этих группах сверху вниз уменьшается активность неметаллов, уменьшается стабильность соединений в высшей степени окисления, возрастает стабильность соединений в более низкой степени окисления. Например, в пятой A группе висмут проявляет металлические свойства и для него, в отличие от фосфора, наиболее характерна степень окисления плюс три.
Изменение свойств в VIIA группе
Благородные газы – элементы восьмой A группы. У них завершён внешний энэргетический уровень, причём у гелия два электрона на внешнем уровне, он относится к эс-элементам, а все остальные благородные газы относятся к пэ-элементам.

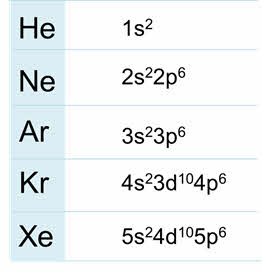
Радиус атомов у благородных газов увеличиваются сверху вниз, энергия ионизации уменьшается, плотность сверху вниз увеличивается, также как температура кипения.
Таким образом, к эс-элементам относятся элементы первой A и второй A группы, к пэ-элементам относятся элементы от третьей до восьмой А группы. Отличительной особенность этих элементов является то, что их валентные электроны расположены на эс- или пэ-подуровне.
По периоду слева направо у них наблюдается уменьшение радиуса атомов, увеличивается энергия ионизации и энергия сродства к электрону, электроотрицательность увеличивается, металлические свойства ослабевают, а усиливаются неметаллические.
В группах сверху вниз наблюдается иная закономерность: радиусы атомов увеличиваются, уменьшается энергия ионизации и энергия сродства к электрону, электроотрицательность уменьшается, металлические свойства усиливаются, а неметаллические ослабевают.
Общая характеристика s-элементов первой и второй групп
s-Элементы – это элементы, у которых происходит заполнение s-подуровня. Данные элементы находятся в главных подгруппах первой и второй групп. S-элементы первой группы включают водород и щелочные металлы, а второй группы – бериллий, магний и щелочноземельные металлы. К s-элементам также относится инертный газ гелий.
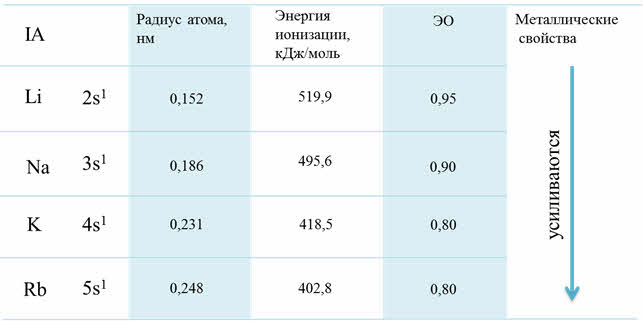
s-металлы первой группы включают: литий (Li), натрий (Na), калий (К), рубидий (Rb), цезий (Сs) и франций (Fr). Данные металлы называются щелочными, так как два главных представителя (натрий и калий) образуют сильные основания – щелочи. На внешнем энергетическом уровне атомов данных элементов находится один электрон, который атомы щелочных металлов легко отдают, превращаясь в однозарядные катионы. С увеличением порядкового номера элементов увеличиваются радиусы атомов, что приводит к усилению восстановительной активности. Щелочные металлы характеризуются незначительной твёрдостью, малой плотностью и низкими температурами плавления.
s -элементы второй группы включают: бериллий (Ве), магний (Мg) и щелочноземельные металлы – кальций (Са), стронций (Sr), барий (Ва) и радий (Rа). Бериллий и магний существенно отличаются от остальных элементов данной группы. Бериллий является амфотерным металлом. Магний образует слабое основание, а щелочноземельные металлы – сильные основания. Данные металлы имеют на внешнем уровне по два электрона и сравнительно легко их отдают, превращаясь в двухзарядные катионы. Они имеют большую, чем щелочные металлы, твёрдость и довольно высокие температуры плавления.
Данные металлы обладают высокой химической активностью. Их активность можно определить по положению в электрохимическом ряду. Следует обратить внимание на то, что литий по положению в электрохимическом ряду самый активный металл (φ 0 = –3,045 В), хотя по положению в периодической таблице он, в сравнении с остальными щелочными металлами, является самым слабым восстановителем.
Это является следствием того, что положение металла в электрохимическом ряду определяется суммой трех величин:
1) энергии разрушения кристаллической решетки;
2) энергии ионизации металла;
3) энергии гидратации образовавшегося иона.
Энергии разрушения кристаллической решетки для данных металлов примерно одинаковы. Энергия ионизации атома лития в подгруппе самая высокая (Е = 5,39 эВ), но энергия гидратации иона лития, благодаря малому радиусу, аномально высокая. По сумме данных трех величин литий в водном растворе электрохимически самый активный металл.
При взаимодействии щелочных металлов с кислородом воздуха: литий образует оксид (Li2О), натрий – пероксид (Na2О2), а калий, рубидий и цезий – надпероксиды (МеО2). Бериллий, магний и щелочноземельные металлы легко окисляются на воздухе с образованием оксидов.
Оксиды щелочных и щелочноземельных металлов взаимодействуют с водой с образованием гидроксидов:
Пероксиды щелочных и щелочноземельных металлов способны взаимодействовать с углекислым газом с выделением кислорода, что позволяет использовать их в системах регенерации воздуха:
Щелочные и щелочноземельные металлы также реагируют с другими неметаллами: галогенами, серой, азотом, водородом. При этом образуются соответствующие галогениды, сульфиды, нитриды и гидриды. Например,
Гидриды полностью разлагаются водой с образованием водорода и гидроксида металла. Например,
Данные металлы вытесняют водород из воды, так как в элекрохимическом ряду стоят левее алюминия. Например,
Бериллий и магний с водой реагируют медленно вследствие малой растворимости образующихся гидроксидов.
Ве(ОН)2 обладает амфотерными свойствами , т.е. взаимодействует с кислотами и щелочами:
Наиболее распространенные соединения данных элементов следующие:
NаCl – хлорид натрия (поваренная соль) консервант пищевых продуктов;
NаОН – гидроксид натрия (каустическая сода). Применяется для получения мыла, очистки нефти и др.
Nа2СО3 – карбонат натрия (кальцинированная сода);
NаНСО3 – гидрокарбонат натрия (питьевая сода);
Калий в виде калийных солей необходим для питания растений.
Магний нужен растениям, так как входит в состав хлорофилла.
СаО – оксид кальция (негашеная известь);
Са(ОН)2 – гидроксид кальция (гашеная известь) широко применяется в строительном деле;
СаSО4·2Н2О – сульфат кальция (гипс);
СаСО3 – карбонат кальция (известняк, мел, мрамор). При его термическом разложении получают негашеную известь и углекислый газ
Следует отметить, что соединения натрия, калия, кальция и магния нужны для жизнедеятельности живых организмов.
Водород и гелий также относятся к s-элементам. Данные элементы по распространенности во Вселенной занимают: водород – первое место, а гелий – второе.
Содержание водорода на Земле составляет ~1 %, но в свободном виде Н2 почти не встречается. Он входит в состав различных соединений. Водород существует в виде трех изотопов: протий 1 1Н, дейтерий 2 1D и тритий 3 1Т. В природе на 6800 атомов водорода приходится 1 атом дейтерия. Вследствие большой разницы в массах физические и химические свойства изотопов водорода и образуемых ими соединений довольно значительно отличаются. Одним из наиболее распространенных в природе химических соединений водорода является вода. На примере данного соединения будет показан общий подход при анализе строения и свойств химических соединений.
Гелий на Земле встречается только в атмосфере и содержание его невелико. В химическом отношении это инертное вещество, поэтому применяется в автогенной сварке для создания инертной среды. Температура плавления гелия – 271,4 о С (при давлении 3,0 МПа), а температура кипения – 269,9 о С, что позволяет использовать его в качестве хладоносителя в физике низких температур.
s-элементы
s-блок в периодической таблице элементов — электронная оболочка, включающая в себя первые два слоя s-электронов.
Эти элементы отличаются тем, что в атомном состоянии высокоэнергичный электрон находится на s-орбитали. Исключая водород и гелий, эти электроны очень легко переходят и формируются в позитивные ионы при химической реакции. Конфигурация гелия химически весьма стабильна, следовательно, именно по этому гелий не имеет стабильных изотопов; иногда, благодаря этому свойству, его объединяют с инертными газами.
Остальные элементы, имеющие этот блок, все без исключения являются сильными восстановителями и поэтому в свободном виде в природе не встречаются. Элемент в металлическом виде может быть получен только с помощью электролиза растворенной в воде соли. Дэви Гемфри, в 1807 и 1808 году, стал первым кто отсоединил соли кислот от s-блок-металлов, за исключением лития, бериллия, рубидия и цезия. Бериллий был впервые отделен от солей независимо двумя учёными: Ф. Вулером и А. А. Бази в 1828 году, в то время как литий был сепарирован Р. Бунзеном только в 1854 году, который, после изучения рубидия, отделил его спустя 9 лет. Цезий не был выделен в чистом виде вплоть до 1881 года, после того как Карл Сеттерберг подверг электролизу цианид цезия.
Опасность и хранение
Все элементы, имеющие s-оболочку, являются опасными веществами. Они пожароопасны, требуют особого пожаротушения, исключая бериллий и магний. Храниться должны в инертной атмосфере аргона или углеводородов. Бурно реагируют с водой, продуктом реакции является водород, например:
,
исключая магний, который реагирует медленно, и бериллия, который реагирует только когда его оксидная плёнка снята с помощью ртути. Литий имеет схожие свойства с магнием, так как находится, относительно периодической таблицы, рядом с магнием.
См. также
- Периодическая система
- Группы химических элементов
Wikimedia Foundation . 2010 .
Полезное
Смотреть что такое "s-элементы" в других словарях:
ЭЛЕМЕНТЫ — (лат. elementa семантич. калька греч. , от ряд, собственно член ряда), термин антич. философии, первоначально «буквы» (алфавита), затем простейшие начала, элементы (ста рослав. транскрипция «стихии»). Уже атомисты (№ 240 Лу.) сравнивали… … Философская энциклопедия
Элементы-индикаторы — элементы, указывающие на наличие м ний и рудных тел. Являются важным поисковым признаком оруденения, когда основные рудообразующие металлы не дают одназначных выводов о ценности геохим. аномалии. Подразделяются на несколько гр.: 1) элементы,… … Геологическая энциклопедия
ЭЛЕМЕНТЫ (КОМПОНЕНТЫ) ПОЛЕЗНЫЕ — составные части полезного ископаемого, представляющие интерес для промышленности. В Э. п. входят элементы главные и второстепенные, включая элементы примеси, элементы спутники и элементы легирующие. Геологический словарь: в 2 х томах. М.: Недра.… … Геологическая энциклопедия
ЭЛЕМЕНТЫ ВТОРОСТЕПЕННЫЕ — присутствующие в руде в низких и чрезвычайно низких содер., но существенно влияющие на промышленную ценность м ния. Обычно не определяют контура рудных залежей. При значительном скоплении Э. в. минимальное бортовое содер. главных полезных… … Геологическая энциклопедия
ЭЛЕМЕНТЫ — ЭЛЕМЕНТЫ (лат. elementa семантическая калька греч. στοιχεία, от στοίχος ряд, собств. член ряда), термин античной философии, первоначально «буквы» (алфавита), затем простейшие начала, элементы (старославянская транскрипция «стихии»). Уже… … Античная философия
Элементы Юнга — Элементы Юнга Юциса Мёрфи (также элементы Юциса Мёрфи) элементы групповой алгебры симметрической группы , определяемые[1] как суммы транспозиций: Элементы попарно коммутируют (более того, элемент коммутирует со всеми… … Википедия
ЭЛЕМЕНТЫ-ПРИМЕСИ — химические элементы, присутствующие в минералах других элементов в виде изоморфных примесей или тонких механических включений; иногда извлекаются в качестве попутных или даже основных (напр., золото из пирита) компонентов. В число элементов… … Большой Энциклопедический словарь
Элементы химические — (a. chemical elements; н. chemische Elemente; ф. elements chimiques; и. elementos quimicos) составные части простых и сложных тел, представляющие собой совокупность атомов c одинаковым зарядом атомных ядер и одинаковым числом электронов в … Геологическая энциклопедия
Элементы-примеси — второстепенные элементы в г. п. и рудах, образующие самостоятельные м лы. Многие из них имеют промышленное значение и путем обогащения могут выделяться в концентраты. См. Элементы второстепенные. Геологический словарь: в 2 х томах. М.: Недра. Под … Геологическая энциклопедия
ЭЛЕМЕНТЫ — № 105 110 сверхтяжёлые искусственно полученные радиоакт. хим. элементы. Элементы с ат. номером 104 110 наз. т р а н с а к т и н о и д н ы м и. Элемент № 105 (нуклид с массовым числом А= 261, T1/2=1,6 с) получен в 1970 в Дубне группой Г. H.… … Физическая энциклопедия
ЭЛЕМЕНТЫ КОРАБЛЯ ТАКТИКО-ТЕХНИЧЕСКИЕ — характеризующие его как боевую единицу следующие: элементы нападения артиллерия, торпеда, мина, глубинные бомбы и т. д.; элементы защиты броня, противоминная защита, противохимическая защита; маневренные элементы скорость хода, поворотливость,… … Морской словарь
Читайте также:
