Коферментные функции витаминов ионов металлов
Обновлено: 04.10.2024
Большинство ферментов для проявления ферментативной активности нуждается в низкомолекулярных органических соединениях небелковой природы (коферментах) и/или в ионах металлов (кофакторах).
Кофакторывыполняют функцию стабилизаторов молекулы субстрата, активного центра фермента и конформации белковой молекулы фермента, а именно третичной и четвертичной структур. В некоторых случаях ионы металла служат "мостиком" между ферментом и субстратом. Они выполняют функцию стабилизаторов активного центра, облегчая присоединение к нему субстрата и протекание химической реакции. В ряде случаев ион металла может способствовать присоединению кофермента. Перечисленные выше функции выполняют такие металлы, как Mg2+, Mn2+, Zn2+, Co2+, Мо2+. В отсутствие металла эти ферменты активностью не обладают. Такие ферменты получили название "металлоэнзимы". Схематично данный процесс взаимодействия фермента, субстрата и металла можно представить следующим образом:
Кофермент, локализуясь в каталитическом участке активного центра, принимает непосредственное участие в химической реакции, выступая в качестве акцептора и донора химических группировок, атомов, электронов. Кофермент может быть связан с белковой частью молекулы ковалентными и нековалентными связями. В первом случае он называется простетической группой (например, FAD, FMN, биотин, липоевая кислота). Вместе с тем известны примеры, когда кофермент присоединяется к ферменту нековалентными связями настолько прочно, что не диссоциирует от белковой молекулы, например тиаминдифосфат. Во втором случае кофермент взаимодействует с ферментом только на время химической реакции и может рассматриваться в качестве второго субстрата. Примеры - NAD+, NADP+. Апофермент обеспечивает специфичность действия и отвечает за выбор типа химического превращения субстрата. Один и тот же кофермент, взаимодействуя с различными апоферментами, может участвовать в разных химических превращениях субстрата. Например, пиридоксальфосфат в зависимости от того, с каким апоферментом взаимодействует, участвует в реакциях трансаминирования или декарбоксилирования аминокислот.
Химическая природа коферментов, их функции в ферментативных реакциях чрезвычайно разнообразны. Традиционно к коферментам относят производные витаминов, хотя помимо них есть значительный класс небелковых соединений, принимающих участие в проявлении каталитической функции ферментов.
К коферментам относят следующие соединения:
гемы, входящие в состав цитохромов, каталазы, пероксидазы, гуанилатциклазы, NO-синтазы и являющиеся простетической группой ферментов;
нуклеотиды - доноры и акцепторы остатка фосфорной кислоты;
убихинон, или кофермент Q, участвующий в переносе электронов и протонов в ЦПЭ;
фосфоаденозилфосфосульфат, участвующий в переносе сульфата;
S-аденозилметионин (SAM) - донор метильной группы;
глутатион, участвующий в окислительно-восстановительных реакциях.
Витамин РРвходит в состав кофермента НАД + и НАДФ + , который принимает участие в ферментативных реакциях по последовательному механизму. Две ферментативные реакции, катализируемые ферментами Е1 и Е2, сопряжены друг с другом посредством кофермента NAD+, служащего в каждом из этих случаев субстратом. Для первого фермента субстратом служит окисленная форма NAD, в качестве второго субстрата выступает донор водорода - пример последовательных реакций, продуктом - восстановленная форма NAD, для фермента Е2 - наоборот.
Витамин В5 – принимает участие в синтезе кофермента А (Ацетил-КоА). Кофермент А (КоА) —коферментацетилирования; один из важнейших коферментов; принимает участие в реакциях переносаацильных групп.МолекулаКоА состоит из остаткаадениловой кислоты, связанной пирофосфатной группой с остаткомпантотеновой кислоты, соединённой пептидной связью с остаткомβ-меркаптоэтаноламина.
С КоА связан ряд биохимических реакций, лежащих в основе окисленияисинтезажирных кислот, биосинтеза жиров, окислительных превращений продуктов распада углеводов. Во всех случаях КоА действует в качестве промежуточного звена, связывающего и переносящего кислотные остатки на другие вещества. При этом кислотные остатки в составе соединения с КоА подвергаются тем или иным превращениям, либо передаются без изменений на определённые метаболиты.
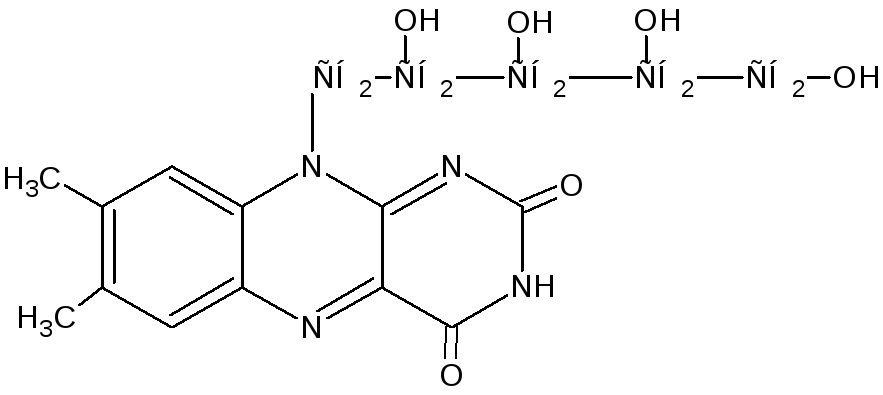
Витамин В2 – принимает участие в формировании кофактора ФАД и ФМН. Флавинадениндинуклеотид —кофактор, принимающий участие во многих окислительно-восстановительных биохимических процессах. FAD существует в двух формах — окисленной и восстановленной, его биохимическая функция, как правило, заключается в переходе между этими формами. FAD может быть восстановлен до FADH2, при этом он принимает два атома водорода. Молекула FADH2 является переносчиком энергии и восстановленныйкоферментможет быть использован каксубстратв реакцииокислительного фосфорилированиявмитохондрии. Молекула FADH2 окисляется в FAD, при этом выделяется энергия, эквивалентная (запасаемая в форме) двум молям ATФ.
22.Кофакторы ферментов: ионы металлов и коферменты. Коферментные функции витаминов (на примере витаминов в6, рр, в2).
Кофакторы выполняют функцию стабилизаторов молекулы субстрата, активного центра фермента и конформации белковой молекулы фермента, а именно третичной и четвертичной структур. В некоторых случаях ионы металла служат "мостиком" между ферментом и субстратом. Они выполняют функцию стабилизаторов активного центра, облегчая присоединение к нему субстрата и протекание химической реакции. В ряде случаев ион металла может способствовать присоединению кофермента. Перечисленные выше функции выполняют такие металлы, как Mg2+, Mn2+, Zn2+, Co2+, Мо2+. В отсутствие металла эти ферменты активностью не обладают. Такие ферменты получили название "металлоэнзимы". Схематично данный процесс взаимодействия фермента, субстрата и металла можно представить следующим образом:
Витамин РР входит в состав кофермента НАД + и НАДФ + , который принимает участие в ферментативных реакциях по последовательному механизму. Две ферментативные реакции, катализируемые ферментами Е1 и Е2, сопряжены друг с другом посредством кофермента NAD+, служащего в каждом из этих случаев субстратом. Для первого фермента субстратом служит окисленная форма NAD, в качестве второго субстрата выступает донор водорода - пример последовательных реакций, продуктом - восстановленная форма NAD, для фермента Е2 - наоборот.
Витамин В5 – принимает участие в синтезе кофермента А (Ацетил-КоА). Кофермент А (КоА) — кофермент ацетилирования; один из важнейших коферментов; принимает участие в реакциях переноса ацильных групп. Молекула КоА состоит из остатка адениловой кислоты, связанной пирофосфатной группой с остаткомпантотеновой кислоты, соединённой пептидной связью с остатком β-меркаптоэтаноламина.
С КоА связан ряд биохимических реакций, лежащих в основе окисления и синтеза жирных кислот, биосинтеза жиров, окислительных превращений продуктов распада углеводов. Во всех случаях КоА действует в качестве промежуточного звена, связывающего и переносящего кислотные остатки на другие вещества. При этом кислотные остатки в составе соединения с КоА подвергаются тем или иным превращениям, либо передаются без изменений на определённые метаболиты.Никотиновая кислота и никотинамид

Витамин В2 – принимает участие в формировании кофактора ФАД и ФМН. Флавинадениндинуклеотид — кофактор, принимающий участие во многих окислительно-восстановительных биохимических процессах. FAD существует в двух формах — окисленной и восстановленной, его биохимическая функция, как правило, заключается в переходе между этими формами. FAD может быть восстановлен до FADH2, при этом он принимает два атома водорода. Молекула FADH2 является переносчиком энергии и восстановленныйкоферментможет быть использован каксубстратв реакцииокислительного фосфорилированиявмитохондрии. Молекула FADH2 окисляется в FAD, при этом выделяется энергия, эквивалентная (запасаемая в форме) двум молям ATФ. Рибофлавин
Коферментная
Тип катализируемой реакции
антиневритный
Фосфат (ТПФ)
Окислительное декарбоксилирование α-кетокислот
Перенос протонов и электронов
(ОВР) (дегидрогеназы)
Пантотеновая
Перенос ацильных групп
(ацилтрансферазы)
B5, PP
Никотиновая кислота,
Антипеллагрический
23.Ингибиторы ферментов. Обратимое и необратимое ингибирование. Конкурентное ингибирование. Лекарственные препараты как ингибиторы ферментов.
К ингибиторам следует относить вещества, вызывающие снижение активности фермента. Следует отметить, что все денатурирующие агенты также вызывают уменьшение скорости любой ферментативной реакции, вследствие неспецифической денатурации белковой молекулы, поэтому денатурирующие агенты к ингибиторам не относят. В основе действия многих лекарственных препаратов и ядов лежит ингибирование активности ферментов, поэтому знание механизмов этого процесса крайне важно для молекулярной фармакологии и токсикологии. Ингибиторы способны взаимодействовать с ферментами с разной степенью прочности. На основании этого различают обратимое и необратимое ингибирование. По механизму действия ингибиторы подразделяют на конкурентные и неконкурентные.
Обратимое ингибирование Обратимые ингибиторы связываются с ферментом слабыми нековалентными связями и при определённых условиях легко отделяются от фермента. Обратимые ингибиторы бывают конкурентными и неконкурентными.
Конкурентное ингибирование К конкурентному ингибированию относят обратимое снижение скорости ферментативной реакции, вызванное ингибитором, связывающимся с активным центром фермента и препятствующим образованию фермент-субстратного комплекса. Такой тип ингибирования наблюдают, когда ингибитор - структурный аналог субстрата, в результате возникает конкуренция молекул субстрата и ингибитора за место в активном центре фермента. В этом случае с ферментом взаимодействует либо субстрат, либо ингибитор, образуя комплексы фермент-субстрат (ES) или фермент-ингибитор (EI). При формировании комплекса фермента и ингибитора (EI) продукт реакции не образуется. Для конкурентного типа ингибирования справедливы следующие уравнения:
Лекарственные препараты как конкурентные ингибиторы Многие лекарственные препараты оказывают своё терапевтическое действие по механизму конкурентного ингибирования. Например, четвертичные аммониевые основания ингибируют ацетилхолинэстеразу, катализирующую реакцию гидролиза ацетилхолина на холин и уксусную кислоту. При добавлении ингибиторов активность ацетилхолинэстеразы уменьшается, концентрация ацетилхолина (субстрата) увеличивается, что сопровождается усилением проведения нервного импульса. Ингибиторы холинэстеразы используют при лечении мышечных дистрофий. Эффективные антихолинэстеразные препараты - прозерин, эндрофоний и др.
Неконкурентное ингибирование Неконкурентным называют такое ингибирование ферментативной реакции, при котором ингибитор взаимодействует с ферментом в участке, отличном от активного центра. Неконкурентные ингибиторы не являются структурными аналогами субстрата. Неконкурентный ингибитор может связываться либо с ферментом, либо с фермент-субстратным комплексом, образуя неактивный комплекс. Присоединение неконкурентного ингибитора вызывает изменение конформации молекулы фермента таким образом, что нарушается взаимодействие субстрата с активным центром фермента, что приводит к снижению скорости ферментативной реакции.
Необратимое ингибирование Необратимое ингибирование наблюдают в случае образования ковалентных стабильных связей между молекулой ингибитора и фермента. Чаще всего модификации подвергается активный центр фермента, В результате фермент не может выполнять каталитическую функцию. К необратимым ингибиторам относят ионы тяжёлых металлов, например ртути (Hg 2+ ), серебра (Ag + ) и мышьяка (As 3+ ), которые в малых концентрациях блокируют сульфгидрильные группы активного центра. Субстрат при этом не может подвергаться химическому превращению. При наличии реактиваторов ферментативная функция восстанавливается. В больших концентрациях ионы тяжёлых металлов вызывают денатурацию белковой молекулы фермента, т.е. приводят к полной инактивации фермента.
Необратимые ингибиторы ферментов как лекарственные препараты. Пример лекарственного препарата, действие которого основано на необратимом ингибировании ферментов, - широко используемый препарат аспирин. Противовоспалительный нестероидный препарат аспирин обеспечивает фармакологическое действие за счёт ингибирования фермента циклооксигеназы, катализирующего реакцию образования простагландинов из арахидоновой кислоты. В результате химической реакции ацетильный остаток аспирина присоединяется к свободной концевой NH2-группе одной из субъединиц циклооксигеназы. Это вызывает снижение образования продуктов реакции простагландинов, которые обладают широким спектром биологических функций, в том числе являются медиаторами воспаления.
24.Регуляция действия ферментов: аллостерические ингибиторы и активаторы. Каталитический и регуляторный центры. Четвертичная структура аллостерических ферментов и кооперативные изменения конформации протомеров фермента.
Аллостерическая регуляция. Во многих строго биосинтетических реакциях основным типом регуляции скорости многоступенчатого ферментативного процесса является ингибирование по принципу обратной связи. Это означает, что конечный продукт биосинтетической цепи подавляет активность фермента, катализирующего первую стадию синтеза, которая является ключевой для данной цепи реакции. Поскольку конечный продукт структурно отличается от субстрата, он связывается с аллостери-ческим (некаталитическим) центром молекулы фермента, вызывая ингиби-рование всей цепи синтетической реакции.
Предположим, что в клетках осуществляется многоступенчатый биосинтетический процесс, каждая стадия которого катализируется собственным ферментом:
Скорость подобной суммарной последовательности реакций в значительной степени определяется концентрацией конечного продукта Р, накопление которого выше допустимого уровня оказывает мощное инги-бирующее действие на первую стадию процесса и соответственно на фермент E1.
Следует, однако, иметь в виду, что модуляторами аллостерических ферментов могут быть как активаторы, так и ингибиторы. Часто оказывается, что сам субстрат оказывает активирующий эффект. Ферменты, для которых и субстрат, и модулятор представлены идентичными структурами, носят название гомотропных в отличие от гетеротропных ферментов, для которых модулятор имеет отличную от субстрата структуру. Взаимопревращение активного и неактивного аллостерических ферментов в упрощенной форме, а также конфор-мационные изменения, наблюдаемые при присоединении субстрата и эффекторов. Присоединение отрицательного эффектора к аллостерическому центру вызывает значительные изменения конфигурации активного центра молекулы фермента, в результате чего фермент теряет сродство к своему субстрату (образование неактивного комплекса).
Аллостерические взаимодействия проявляются в характере кривых зависимости начальной скорости реакции от концентрации субстрата или эффектора, в частности в S-образности этих кривых (отклонение от гиперболической кривой Михаэлиса-Ментен). S-образный характер зависимости v от [ S ] в присутствии модулятора обусловлен эффектом кооперативности. Это означает, что связывание одной молекулы субстрата облегчает связывание второй молекулы в активном центре, способствуя тем самым увеличению скорости реакции. Кроме того, для аллостерических регуляторных ферментов характерна нелинейная зависимость скорости реакции от концентрации субстрата.
Кофакторы ферментов: ионы металлов и коферменты. Коферментные функции витаминов, (на примере трансаминаз и дегидрогеназ, витаминов В6 , РР, В2)
Активность ряда ферментов (простые белки) в норме зависит только от их структуры, тогда как для других, названных холоферментами (сложные белки), требуются кофакторы - вещества небелковой природы, в роли которых могут быть сложные органические соединения (коферменты) и ионы металлов.
Кофактор может образовывать с апоферментом прочные ковалентные связи. В этом случае кофермент называют простетической группой фермента. Примерами могут служить ФАД, ФМН, биотин, ковалентно связанный с остатком лизина в активном центре, Zn 2+ , который содержится в активном центре карбоксипептидазы. В том случае, если кофермент связывается с апоферментом нековалентными связями только на время химической реакции (НАД + и НАДФ + ), он может рассматриваться в качестве второго субстрата данного фермента Один и тот же кофермент может участвовать в разных биохимических реакциях, комплементарно связываясь с разными апоферментами. Собственной каталитической активностью коферменты не обладают.
Апофермент формирует активный центр, отвечает за специфичность действия фермента, фиксирует и ориентирует субстрат в активном центре и создает условия для преобразования субстрата в продукты реакции. Ионы металла выполняют две главные функции.
I). Стабилизируют нативную конформацию фермента, структуру его активного центра и субстрата. 2). Участвуют в ферментативном катализе.
1). Металлоферменты, лишенные ионов металла, либо сохраняют способность к химическому катализу, утрачивая стабильность, либо полностью теряют активность. Например, щелочная фосфатаза - металлофермент, в активном центре которого находится Zn 2+ , лишенная ионов цинка щелочная фосфатаза, теряет ферментативную активность, но восстанавливает ее после добавления металла. В некоторых металлоферментах ион металла (Mg 2+ , Mn 2+ , Zn 2+ , Co 2+ , Мо 2+ ) участвует в образовании связи между молекулой субстрата и активным центром кофермента. в отсутствие иона эти ферменты не обладают активностью. Ряд ферментов в качестве субстрата используют комплекс превращаемого вещества с ионом. Для большинства киназ одним из субстратов служит не молекула АТФ, а комплекс Mg 2+ -ATФ.
2). Ферментативный электрофильный катализ. Ионы металла непосредственно участвуют в катализе и локализованы в активном центре фермента.В активном центре ферментов могут содержатся Zn 2+ , Mn 2+ , Fe 2+ , Си 2+ . Пример элек-трофильного катализа - действие карбоангидразы, содержащей ион цинка в активном центре.
B6 Коферментные функции выполняют два фосфорилированных производных пиридоксина: пиридоксальфосфат и пиридоксаминофосфат. Распад коферментов идет путем дефосфорилирования и окисления с образованием 4-пиридоксиловой кислоты. которая выводится из организма.
Коферментные формы витамина В6 включены в реакции, катализируемые почти всеми классами ферментов. Наиболее значительная группа пиридоксалевых ферментов - аминотрансферазы. Пиридоксальзависимые (пиридоксалевые ферменты) ферменты катализируют взаимопревращения и распад аминокислот (регулируют аминокислотный состав крови при разном аминокислотном составе пиши), участвуют в специфических реакциях метаболизма отдельных аминокислот (серина, треонина, триптофана). Участвуют в обмене липидов, синтезе сфинголипидов. В качестве кофактора ферментов участвуют в начальных стадиях синтеза гема. Влияют на обмен жирных кислот.
PP - предшественник коферментов -никотинамидадениндинуклеотида (НАД + ) и никотинамидадениндинуклеотид-фосфата (НАДФ ), входящих в состав дегидрогеназ и редуктаз.
НАД + и НАДФ + приобретают коферментные функции после присоединения к никотинамиду радикала, включающего остаток рибозы, пирофосфат и нуклеотид - аденин. Витамин РР такими функциями не обладает.
1. НАД + - кофермент дегидрогеназ, участвующих в реакциях окисления глюкозы, жирных кислот, глицерола, аминокислот после их дезаминирования; является коферментом дегидрогеназ цикла Кребса (кроме сукцинатдегидрогеназы). В этих реакциях кофермент выполняет функцию промежуточного акцептора электронов и протонов.
2. НАДН и НАДФН - коферменты реакций (НАДН-оксидазной и НАДФН-оксидазной), способствующих возникновению активных форм кислорода в фагоцитах.
B2 Кофермент ФМН и ФАД
1. ФМН и ФАД - коферменты оксидаз, переносящих электроны с окисляемого субстрата на кислород. Это ферменты распада аминокислот (оксидазы D- и L-аминокислот), нуклеотидов (ксантиноксидаза), биогенных аминов (моно- и диа-минооксидазы).
2. ФАД - кофермент пируват- и альфа-кетоглутаратдегидрогеназных комплексов. Совместно с тиаминпирофосфатом и другими коферментами катализируют окислительное декарбоксилирование кетокислот.
Читайте также:
