Лекция по химии металлы
Обновлено: 21.09.2024
Более 80% известных элементов образуют простые вещества — металлы. К ним относятся s -элементы I и II групп (исключение — водород), все d - и f - элементы, а также р-элементы III группы (кроме бора), IV группы (олово, свинец), V группы cурьма, висмут) и VI группы (полоний).
Особенности строения атомов металлов:
♦ небольшое число электронов на внешнем энергетическом уровне (как правило, один-три электрона). Исключение — атомы р-элементов IV-VI групп;
♦ малые заряды ядер и большие радиусы атомов по сравнению с атомами неметаллов данного периода;
♦ сравнительно слабая связь валентных электронов с ядром;
♦ низкие значения электроотрицательности.
В связи с этим атомы металлов легко отдают валентные электроны и превращаются в положительно заряженные ионы, т. е. м еталлы - восстановители.
Однако способность отдавать электроны проявляется у металлов неодинаково. В периодах с увеличением зарядов ядер атомов уменьшаются их радиусы, увеличивается число электронов на внешнем уровне и усиливается связь валентных электронов с ядром. Поэтому в периодах слева направо восстановительная способностъ атомов металлов уменьшается.
В главных подгруппах с возрастанием атомных номеров элементов увеличиваются радиусы их атомов и уменьшается притяжение (валентных электронов к ядру. Поэтому в главных подгруппах сверху вниз восстановительная активность атомов металлов возрастает. Следовательно, наиболее активными восстановителями являются щелочные и щелочно-земельные металлы.
Только некоторые металлы (золото, платина) находятся в природе в виде простых веществ (в самородном состоянии). Металлы, расположенные в электрохимическом ряду напряжений между оловом и золотом, встречаются как в виде простых веществ, так и в составе соединений. Большинство же металлов находятся в природе в виде соединений — оксидов, сульфидов, карбонатов и т. д. Распространенность металлов в природе уменьшается в ряду:
Содержание в земной коре (массовая доля, %) уменьшается
Получение металлов из их соединений — задача металлургии. Металлургия — наука о промышленном получении металлов из природного сырья. Различают черную (производство железа и его сплавов) и цветную (производство всех остальных металлов сплавов) металлургию. Любой металлургический процесс является процессом восстановления ионов металла различными восстановителями:
Me n + + пе - = Me
В зависимости от условий проведения процесса восстановления различают несколько способов получения металлов.
2. Способы получения металлов
Пирометаллургия — восстановление безводных соединений при высокой температуре
С или СО (карботермия)
Сульфиды предварительно обжигают:
2 = 2 ZnO + 2 S 02
ZnO + С = Zn + 2СО
Fe, Cu, Pb, Sn, Cd, Zn
Mn, Cr, W, Mo, Ti, V
H 2 (водородотермия)
Оксиды активных металлов (МgО, СаО, А1203 и др.) водородом не восстанавливаются
Cu, Ni, W, Fe, Mo, Cd, Pb
Электрометаллургия – восстановление электрическим током
2 1
электролиз 2 Na + Cl 2
Щелочные металлы, Be , Mg , Ca (из расплавленных хлоридов), Al – из расплавленного оксида
К Ni 2+ + 2е - = Ni 2
А 2Н2О - 4е - = O 2 + 4Н + 1
4 + 2Н2О электролиз 2 Ni + О2 + Н2 SO 4
Гидрометаллургия – восстановление из растворов солей
Металл, входящий в состав руды, переводят в раствор, затем восстанавливают более активным металлом:
Задания для самостоятельной работы
1. Атому магния в степени окисления +2 соответствует электронная конфигурация:
а ) 1s 2 2s 2 2 р 6 3s 2 3 р 6 ; в ) 1s 2 2s 2 2 р 4 ;
б) 1 s 2 2 s 2 2р 6 ; г ) 1 s 2 2 s 2 2р 6 3 s 2 ;
2. При частичном восстановлении водородом 30 г оксида кобальта. В получили смесь оксида и металла массой 26,8 г. Определите количество вещества водорода, вступившего в реакцию, и массовую долю кобальта в полученной смеси.
3. При электролизе раствора сульфата меди ( II ) в растворе образовалась кислота (около анода), на нейтрализацию которой затрачен раствор объемом 16 см (р = 1,05 г/см 3 ) с массовой долей гидроксида калия 6%. Вычислите массу меди, которая выделилась на катоде.
4. Для восстановления марганца из оксида марганца(1\/) путем алюмотермии было смешано 10,8 г алюминия и 26,2 г оксида. Определите, какое из исходных веществ осталось и какова его масса.
3. Физические свойства металлов
Все металлы обладают металлической кристаллической решеткой, особенности которой определяют их общие физические и механические свойства.
Общие свойства металлов:
1). Все металлы являются твердыми веществами, за исключением ртути.
2). Металлический блеск и непрозрачность металлов — результат отражения световых лучей.
3). Электро- и теплопроводность обусловлены наличием в металлических решетках свободных электронов.
С повышением температуры электропроводность металлов уменьшается, а с понижением температуры — увеличивается. Около абсолютного нуля для многих металлов характерно явление сверхпроводимости.
4). Металлы обладают ковкостью и пластичностью. По определению М. В. Ломоносова, «металлом называется светлое тело, которое ковать можно». Металлы легко прокатываются в листы, вытягиваются в проволоку, поддаются ковке, штамповке, прессованию.
Специфические физические свойства металлов:
1). по значению плотности металлы делят на легкие (плотность меньше 5 г/см 3 ): Na , Са , Mg , Al , Ti — и тяжелые (плотность больше 5 г/см 3 ): Zn , Cr , Sn , Mn , Ni , С u , Ag , Pb , Hg , Аи, W , Os - самый тяжелый ;
2). по значению температуры плавления — на легкоплавкие ( t пл < 1000 °С): Hg , Na , Sn , Pb , Zn , Mg , Al , Ca , Ag — и тугоплавкие ( t пл > 1000 ° C ): Au , Cu , Mn , Ni , Fe , Ti , Cr , Os , W - самый тугоплавкий;
3). из металлов самые мягкие — щелочные (их можно резать ножом), самый твердый — хром (царапает стекло).
4). по отношению к магнитным полям металлы подразделяют на три группы:
а) ферромагнитные — способны намагничиваться под действием даже слабых магнитных полей ( Fe , Со, Ni );
б) парамагнитные — проявляют слабую способность к намагничиванию даже в сильных магнитных полях ( Al , Cr , Ti );
в) диамагнитные — не притягиваются к магниту ( Sn , С u , Bi ).
4. Химические свойства металлов
Если атомы большинства неметаллов могут как отдавать, так и присоединять электроны, проявляя окислительно-восстановительную двойственность, то атомы металлов способны только отдавать валентные электроны, проявляя восстановительные свойства: Me - пе - = Me п+ (окисление)
Как восстановители металлы взаимодействуют с неметаллами, водой, растворами щелочей, кислот и солей.
1). Взаимодействие металлов с простыми веществами — неметаллами
Металлы при определенных условиях взаимодействуют с неметаллами, например с кислородом образуют оксиды:
Из щелочных металлов только литий сгорает на воздухе с образованием оксида:
Основной продукт окисления натрия — пероксид:
При горении других щелочных металлов образуются супероксиды, например:
Оксиды натрия и калия могут быть получены при нагревании смеси пероксида с избытком металла в отсутствие кислорода:
На реакции пероксида натрия с оксидом углерода (1 V ) основана регенерация воздуха в изолированных помещениях (например, на подводных лодках):
Лекция по химии металлы
Металлы, как и все химические элементы, имеют три формы существования: атомы, простые и сложные вещества. Из 118 элементов периодической системы к металлам относят 96.
Общие физические свойства металлов.
Физические свойства металлов обусловлены металлической кристаллической решёткой и металлической химической связью. Напомним, что для металлов характерны металлический блеск, пластичность, высокая электро- и теплопроводность, рост электрического сопротивления при повышении температуры, а кроме того, такие практически значимые свойства, как ковкость, твёрдость, магнитные свойства.
Металлы — твёрдые при обычных условиях вещества (кроме ртути, которая становится твёрдой и ковкой при низких температурах).
Металлы пластичны и тягучи, кроме хрупких висмута и марганца. Из меди, алюминия, олова, а также золота изготавливают тончайшие листы — фольгу. Золотая фольга может иметь толщину около 100 нм! Такую фольгу используют для золочения предметов интерьера, стен и потолков, изделий из гипса, дерева, металла, стекла и пластика.
Все металлы имеют металлический блеск, большинство из них серебристо-белого или серого цвета. Из-за того, что стронций, золото и медь поглощают в большей степени близкие к фиолетовому цвету короткие волны и отражают длинные волны светового спектра, эти металлы окрашены в светло-жёлтый и медный цвет. Очень тонкие листки серебра и золота имеют совершенно необычный вид — они представляют собой голубовато-зелёную фольгу, а мелкие порошки металлов кажутся тёмно–серыми и даже чёрными. И только порошки магния и алюминия сохраняют серебристо-белый цвет.
В технике металлы принято классифицировать по различным физическим свойствам:
Металлы принято делить на чёрные (железо и его сплавы) и цветные (остальные металлы и сплавы). Соответственно называются и отрасли металлургической промышленности: чёрная и цветная металлургия.
Важнейшими продуктами цветной металлургии являются титан, вольфрам, молибден и другие металлы, которые могут использоваться в качестве специальных легирующих добавок для производства сверхтвёрдых, тугоплавких, устойчивых к коррозии сплавов, широко применяемых в машино– и станкостроении, в оборонно–космической отрасли.
Современные композиционные материалы, выполненные на основе керамики или полимеров, становятся сверхпрочными, если укреплены металлическими нитями из молибдена, вольфрама, титана, специальных сталей и т. д.
Химические свойства металлов.
Во всех реакциях простые вещества — металлы проявляют только восстановительные свойства.

- Металлы взаимодействуют с неметаллами, образуя бинарные соединения. По правилам ИЮПАК названия этих соединений образуются в соответствии со схемой:
Так, с очень активными неметаллами (галогенами, серой) металлы образуют соединения, которые молено рассматривать, как соли бескислородных кислот: 2Na + Сl2 = 2NaCl
Если металл проявляет переменные степени окисления, подобная соль имеет состав, который зависит от окислительных свойств неметалла. Например, железо энергично взаимодействует с хлором, образуя хлорид железа(III): 2Fe + 3Сl2 = 2FeCl3
При взаимодействии железа с серой, окислительная способность которой ниже, чем у галогенов, продуктом реакции является сульфид железа(II): Fe + S = FeS
- При взаимодействии металлов с кислородом образуются оксиды или пероксиды:
Оксиды в этом случае имеют основный или амфотерный характер:
2Mg + O2 = 2MgO
4Аl + 3O2 = 2Аl2O3
Эти реакции сопровождаются выделением большого количества теплоты и очень ярким пламенем, поэтому применяются для изготовления сигнальных ракет, фейерверков, салютов и других пиротехнических средств. Поэтому обращение с ними требует строгого соблюдения правил техники безопасности.
Продуктом горения железа в кислороде является смешанный оксид 3Fe + 2O2 = Fe3O4
- Металлы — простые вещества, образованные элементами IA– и IIА–групп, в полном соответствии с названием этих групп взаимодействуют с водой с образованием щёлочи и водорода. В общем виде эти реакции можно записать так:
2М + 2Н2O = 2МОН + Н2↑, где М — щелочной металл
М + 2Н2O = М(ОН)2 + H2↑, где М — Mg или щёлочноземельный металл.
Для характеристики химических свойств металлов важное значение имеет их положение в электрохимическом ряду напряжений:
К, Са, Na, Mg, Al, Zn, Fe, Sn, Pb, (H2) , Cu, Hg, Ag, Au
Вспомните известные вам из курса основной школы два вывода:
- взаимодействие металлов с растворами кислот происходит, если металл находится в ряду напряжений левее водорода;
- взаимодействие металлов с растворами солей происходит, если металл находится в ряду напряжений левее металла соли.
Лабораторный способом получения водорода:
Zn + 2НСl = ZnCl2 + H2↑
Zn 0 + 2H + = Zn 2+ + H2 0
Аналогично протекает реакция металлов и с органическими кислотами:
2СН3СООН + Zn —> (CH3COO)2Zn + Н2↑
2СН3СООН + Zn –> 2СН3СОO – + Zn 2+ + Н2 0
Реакция между цинком и раствором сульфата меди(II) протекает согласно уравнению:
Zn + CuSO4 = ZnSO4 + Сu
Zn 0 + Сu 2+ = Zn 2+ + Сu 0
Подчеркнём, что в этом случае металл может находиться в ряду напряжений и после водорода, но не после металла соли. Например, реакция замещения серебра медью:
Cu + 2AgNO3 = Сu(NО3)2 + 2Ag
Cu 0 + 2Ag + = Cu 2+ + 2Ag 0
В завершение рассмотрим ещё одно характерное не для всех металлов свойство, которое называется металлотермия. Такие активные металлы, как алюминий, кальций, магний, литий, способны взаимодействовать с оксидами других металлов. Для того чтобы началась такая реакция, смесь активного металла и оксида металла (её называют термитной) необходимо поджечь. После этого процесс сопровождается выделением большого количества теплоты и света (отсюда и название процесса). Металлотермию применяют для получения и более ценных металлов: 2Аl + Сr2О3 = Al2O3 + 2Сг
Химия металлов (таблица)

Конспект урока по химии в 11 классе «Металлы». В учебных целях использованы цитаты из пособия «Химия. 11 класс : учеб, для общеобразоват. организаций : базовый уровень / О. С. Габриелян, И. Г. Остроумов, С. А. Сладков. — М. : Просвещение». Выберите дальнейшее действие:
Лекция по Химии на тему "Металлы"
1. Где расположены металлы в периодической системе химических элементов Д.И.Менделеева?
2. Каковы особенности строения атомов металлов?
3. В чём различие в строении внешнего энергетического уровня у металлов и неметаллов?
4. Сколько наружных электронов имеют атомы металлов главных и побочных подгрупп?
5. В каких формах могут находиться металлы в природе?
6. Как устроена кристаллическая решетка металлов?
7. Каковы физические свойства металлов?
8. Как можно получить металлы из их соединений?
9. Как ведут себя атомы металлов в химических реакциях и почему?
10. Какие свойства – окислителей или восстановителей – проявляют металлы в химических реакциях?
11. Расскажите об электрохимическом ряде напряжений металлов.
12. Перечислите реакции, в которые могут вступать металлы.
13. Каково значение металлов в жизни человека?
1. Особенности электронного строения металлов.
Металлы - это химические элементы, атомы которых отдают электроны внешнего (а иногда предвнешнего) электронного слоя, превращаясь в положительные ионы. Металлы – восстановители Ме 0 – nе = Ме n+ . Это обусловлено небольшим числом электронов внешнего слоя (в основном 1 - 3), большим радиусом атомов, вследствие чего эти электроны слабо удерживаются с ядром.
2. Положение металлов в ПСХЭ.
Легко увидеть, что большинство элементов ПСХЭ – металлы (92 из 114).
Металлы размещены в левом нижнем углу ПСХЭ. Это все элементы, расположенные ниже диагонали В – А t , даже те у которых на внешнем слое 4 электрона ( Je , Sn , Pb ), 5 электронов ( Sb , Di ), 6 электронов ( Po ), так как они отличаются большим радиусом. Среди них есть s и p -элементы – металлы главных подгрупп, а также d и f металлы, образующие побочные подгруппы.
В соответствии с местом, занимаемым в периодической системе, различают переходные (элементы побочных подгрупп) и непереходные металлы (элементы главных подгрупп). Металлы главных подгрупп характеризуются тем, что в их атомах происходит последовательное заполнение электронных s- и р-подуровней. В атомах металлов побочных подгрупп происходит достраивание d- и f-подуровней.
Закономерности в изменении свойств элементов – металлов.
Признаки сравнения
В главной подгруппе
Число электронов на внешнем слое
У элементов – металлов побочных подгрупп свойства чуть-чуть другие.
В побочных подгруппах ( Cu , Ag , Au ) – активност ь элементов – металлов падает. Эта закономерность наблюдается и у элементов второй побочной подгруппы Zn , Cd , Hg . У элементов побочных подгрупп – это элементы 4-7 периодов – с увеличением порядкового элемента радиус атомов изменятся мало, а величина заряда ядра увеличивается значительно, поэтому прочность связи валентных электронов с ядром усиливается, восстановительные свойства ослабевают.
3. Металлическая химическая связь. Кристаллические решетки.
Связь в металлах между («атом-ионами» ) посредством (большого количества не связанных с ядрами подвижных электронов) называется (металлической связью) .
Все металлы являются кристаллическими телами, имеющими определенный тип кристаллической решетки, состоящей из малоподвижных положительно заряженных ионов, между которыми движутся свободные электроны (так называемый электронный газ). Такой тип структуры называется металлической связью.
Тип решетки определяется формой элементарного геометрического тела, многократное повторение которого по трем пространственным осям образует решетку данного кристаллического тела.
Обобщим сведения о типе химической связи, образуемой атомами металлов и строение кристаллической решетки:
- сравнительно небольшое количество электронов одновременно связывают множество ядер, связь делаколизована;
- валентные электроны свободно перемещаются по всему куску металла, который в целом электронейтрален;
- металлическая связь не обладает направляемостью и насыщенностью.
4. Физические свойства металлов
В соответствие именно с таким строением металлы характеризуются общими физическими свойствами.
а) твердость – все металлы кроме ртути, при обычных условиях твердые вещества. Самые мягкие – натрий, калий. Их можно резать ножом; самый твердый хром – царапает стекло.
б) плотность. Металлы делятся на мягкие (5г/см³) и тяжелые (меньше 5г/см³).
в) плавкость. Металлы делятся на легкоплавкие и тугоплавкие.
г) электропроводность, теплопроводность металлов обусловлена их строением. Хаотически движущиеся электроны под действием электрического напряжения приобретают направленное движение, в результате чего возникает электрический ток.
При повышении температуры амплитуда движения атомов и ионов, находящихся в узлах кристаллической решетки резко возрастает, и это мешает движению электронов, и электропроводность металлов падает.
д) металлический блеск – электроны, заполняющие межатомное пространство отражают световые лучи, а не пропускают как стекло. Поэтому все металлы в кристаллическом состоянии имеют металлический блеск. Для большинства металлов в ровной степени рассеиваются все лучи видимой части спектра, поэтому они имеют серебристо-белый цвет. Только золото и медь в большой степени поглощают короткие волны и отражают длинные волны светового спектра, поэтому имеют желтый цвет. Самые блестящие металлы – ртуть, серебро, палладий. В порошке все металлы, кроме Al и Mg , теряют блеск и имеют черный или темно-серый цвет.
е) пластичность. Механическое воздействие на кристалл с металлической решеткой вызывает только смещение слоев атомов и не сопровождается разрывом связи, и поэтому металл характеризуется высокой пластичностью.
Некоторые металлы, например, железо, титан, олово и др. способны по достижении определенных температур изменять кристаллическое строение. Это явление получило название аллотропии или полиморфизма, а сами переходы от одного кристаллического строения к другому называются аллотропическими или полиморфными.
5. Химические свойства металлов
Ряд напряжений характеризует химические свойства металлов: чем меньше электродный потенциал металла, тем больше его восстановительная способность.
А) Взаимодействие с неметаллами ( в названиях полученных веществ окончание
2Mg 0 +O2 0 —>2Mg 2+ O 2- (оксид магния)
Fe 0 +S 0 —>Fe 2+ S 2- ( сульфид железа II)
Б) Взаимодействие с водой. Самые активные металлы реагируют с водой при обычных условиях, и в результате этих реакций образуются растворимые в воде основания и выделяется водород
2Na + 2HOH = 2NaOH + H2
2Li 0 +2H2 + O 2– —> 2Li + O 2- H + + H2 0
Менее активные металлы реагируют с водой при повышенной температуре с выделением водорода и образованием оксида соответствующего металла Zn + H2O = ZnO +H2
В) Взаимодействие с растворами кислот. Происходит при соблюдении ряда условий
· Металл должен находиться левее в ряду напряжений металлов;
· В результате реакции должна образовываться растворимая соль, иначе металл покроется осадком и доступ кислоты к металлу прекратиться;
· Для этих реакций не рекомендуется использовать щелочные металлы, так как они взаимодействуют с водой в растворе кислоты;
· По особому взаимодействуют с металлами концентрированные азотная и серная кислоты;
2H + Cl – +Zn0 → Zn 2+ Cl2 - +H20
Г) Взаимодействие с растворами солей. При этом соблюдаются следующие условия
· Металл должен находиться в ряду напряжений левее металла, образующего соль;
· Для этих реакций не рекомендуется использовать щелочные металлы, так как они взаимодействуют с водой в растворе соли;
Fe 0 +Cu 2+ Cl2 – →Fe 2+ Cl2 – +Cu 0
Д) Взаимодействие со щелочами (только амфотерные)
Магний и щелочноземельные металлы с щелочами не реагируют.
Е) Взаимодействие с оксидами металлов (металлотермия).
Некоторые активные металлы способны вытеснять другие металлы из их оксидов при поджигании смеси.
2Al 0 + Fe 2 O 3 = Al 2 O 3 +2 Fe 0
Ж) Коррозия (будет рассмотрена на другом занятии).
6. Способы получения металлов
Существуют несколько основных способов получения — металлов.
а) Пирометаллургия – это получение металлов из их соединений при высоких температурах с помощью различных восстановителей (C, CO, H2, Al, Mg и др.).
— из их оксидов углем или оксидом углерода (II)
ZnО + С = Zn + СО
Fе2О3 + ЗСО = 2Fе + ЗСО2
— водородом
WO3 + 3H2 =W + 3H2O
СоО + Н2 = Со + Н2О
— алюминотермия
4Аl + ЗМnО2 = 2А12О3 + ЗМn
б) Гидрометаллургия – это получение металлов, которое состоит из двух процессов: сначала природное соединение металла (оксид) растворяют в кислоте, в результате чего получают соль металла. Затем из полученного раствора необходимый металл вытесняют более активным металлом. Например:
Обжигом сульфидов металлов и последующим восстановлением образовавшихся оксидов (например, углем):
2ZnS + ЗО2 = 2ZnО + 2SО2
ZnО + С = СО + Zn
в) Электрометаллургия – это получение металлов при электролизе растворов или расплавов их соединений. Роль восстановителя при этом играет электрический ток.
СuСl2 → Сu 2 + 2Сl -
Катод (восстановление): Сu 2+ - 2е - = Сu 0
Лекция по курсу "Химия" на тему: "Металлы. Гальванический элемент. Уравнение Нернста"
Положение металлов в Периодической системе элементов.
Способы получения металлов
Физические и химические свойства металлов
Электродный потенциал металлов, нормальный водородный потенциал
Гальванический элемент и электродвижущая сила
Ряд напряжений металлов.
Почти 80% элементов в Периодической системе Д.И Менделеева составляют металлы. Это s - элементы I и II группы, все d и f - элементы, а также - элементы главных подгрупп - III группы (все, кроме В), IV - Ge , Sn , Pb , V - Sb , VI - Po
Получение.
Металлы встречаются в природе как в свободном состоянии (самородки – золото и платина), так и в виде химических соединений. Наименее активные металлы, такие как, серебро, медь, ртуть и олово в природе находятся как в свободном, так и в виде соединений с другими химическими элементами. Активные (стоящие в ряду напряжения металлов до олова) – находятся только в соединениях с другими химическими элементами и входят в состав минералов и горных пород.
Физические свойства
Чистые металлы в твёрдом состоянии – это кристаллы, которых частицы вещества расположены в определённом геометрическом порядке, образуя кристаллическую решётку, в узлах которой находятся положительно заряженные ионы и нейтральные атомы, а между ними перемещаются электроны.
Все металлы, за исключением ртути, при обычных условиях, твёрдые вещества. Для металлов характерен металлический блеск.
Химические свойства.
Эти свойства металлов обусловлены характерным строением их внешних электронных оболочек.
Общим химическим свойством металлов является их способность только отдавать электроны, превращаясь в свободные положительно заряженные ионы:
1. Взаимодействие металлов с неметаллами.
а) большинство металлов хорошо реагируют с кислородом, давая оксиды: 2 Mg + O 2 = 2 MgO
б) легко соединяются с галогенами, образуя галогениды (с хлором – хлориды, со фтором –фториды, с бромом – бромиды, с йодом –иодиды):
2 Fe + 3 CI 2 = 2 FeCI 3
в) с азотом металлы образуют нитриды:
г) при определённых условиях металлы взаимодействуют с серой, образуя сульфиды:
д) соединения металлов с углеродом называются карбидами:
е) соединения металлов с фосфором можно получить синтезом (при 600 0 С – 1200 0 С) и называются они фосфидами:
ж) с водородом взаимодействуют непосредственно только щелочные и щелочноземельные металлы, образуя гидриды:
з) с кремнием металлы образуют - силициды:
2 Mg + Si = Mg 2 Si
и) с бором металлы образуют - бориды – применяются в ядерной технике, радиоэлектронике.
Все металлы, стоящие до водорода, вытесняют его из разбавленных растворов кислот, (исключение представляет азотная кислота любой концентрации) свинец не растворяется в серной кислоте, т.к. образуется осадок сульфат свинца.
Ряд стандартных электродных потенциалов справедлив для окислительно-восстановительных процессов, происходящих только в водной среде.
2. Важные химические свойства металлов проявляются в их отношении к воде, растворам кислот, щелочам, солям.
а) Активные металлы (щелочные и щелочноземельные) вытесняют водород из воды с образованием гидроксидов (щёлочи), магний только из горячей воды.
Металлы, стоящие в ряду напряжений, между магнием и кадмием обычно не вытесняют водород из воды. На поверхности этих металлов образуются оксидные плёнки, обладающие защитным действием.
Некоторые тяжёлые металлы взаимодействуют с водой при нагревании с образованием оксида:
б) Металлы, гидроксиды которых амфотерны, взаимодействуют с растворами кислот и щелочей:
в) Более активные металлы вытесняют менее активные ихз растворов их солей: Fe + CuSO 4 ® FeSO 4 + Cu
Устройства, в которых происходит такое превращение, называются химическими источниками электрической энергии. Они делятся на гальванические элементы (ГЭ) и аккумуляторы.
При действии гальванических элементов на электродах возникают электрические потенциалы. Величина этих потенциалов характеризует активность восстановителей и окислителей. Поэтому для её характеристики вместо отдельных потенциалов используется разность потенциалов в гальваническом элементе, образованном электродом, содержащим изучаемый восстановитель или окислитель, и стандартным электродом, потенциал которого условно принимается равным нулю. В качестве такого принимается электрод, образованный платиной, насыщенной водородом при давлении 1 атм. и погружённой в раствор кислоты, содержащей ионы водорода в активной концентрации 1 моль/л. Этот электрод называется нормальным водородным электродом. Водород хорошо растворяется в платине, при этом молекулы водорода распадаются на атомы. Платина не принимает участие в электродных реакциях, она только выполняет роль губки, пропитанной атомарным водородом.
Измеренная разность потенциалов в образованном гальваническом элементе называется электродным, или окислительно – восстановительным, потенциалом изучаемого восстановителя или окислителя.
Величина электродных потенциалов металлов зависит от свойств самих металлов и от активной концентрации их ионов в растворе.
Для определения потенциала того или иного металла, нужно составить ГЭ, одним электродом которого будет нормальный электрод, а другим – испытуемый металл, погружённый в раствор своей соли с концентрацией 1моль/л. Определяемые потенциалы называются стандартными (или нормальными) электродными потенциалами данного металла (табл.).
Если на металлическом электроде идёт процесс окисления, его электродный потенциал имеет отрицательное значение, а процесс восстановления – значение электродного потенциала положительно.
● Ряд металлов, расположенных по нарастанию алгебраической величины их стандартных электродных потенциалов, называется рядом напряжений металлов:
Li, Rb, K, Ba, Sr, Ca, Na, Mg, Al, Mn, Zn, Cr, Fe, Cd,Co, Ni, Sn, Pb,
(H) , Sb, Bi, Cu, Hg, Ag, Pd, Pt, Au
В этот ряд включён и водород, потенциал которого принимается равный нулю. Ряд напряжений металлов характеризует химические свойства металлов:
1. Чем левее расположен металл в ряду напряжений, тем сильнее его восстановительная способность и тем слабее окислительная способность его иона в растворе (т.е. тем легче он отдаёт электроны (окисляется) и тем труднее ионы присоединяют обратно электроны).
2. Каждый металл способен вытеснить из раствора солей те металлы, которые стоят в ряду напряжений правее его, т.е. восстанавливает ионы последующих металлов в электронейтральные атомы, отдавая электроны и сам превращаясь в ионы.
3. Только металлы, стоящие в ряду напряжений левее водорода, способны вытеснять его из растворов кислот.
● Электрод, на котором протекает окисление, называется анодом (-)
● Электрод, на котором протекает восстановление, называется
Действие любого гальванического элемента (ГЭ) основано на протекании в нём окислительно-восстановительной реакции. ГЭ состоит из двух пластин (электродов), изготовленных из различных металлов и погружённых в раствор электролита.
При схематическом изображении ГЭ граница раздела между металлом и раствором обозначается вертикальной чертой, а граница между растворами электролитов – двойной вертикальной чертой. Схема медно - цинкового гальванического элемента записывается в виде:
(–) анод Zn 0 | Zn 2+ ||Cu 2+ | Cu 0 катод (+)
При работе ГЭ, т.е. при замкнутой внешней цепи, цинк окисляется на аноде и в форме ионов переходит в раствор, а на катоде восстанавливается медь:
Zn 0 - 2 ē ® Zn 2+
Cu 2+ + 2 ē ® Cu 0
Протекает окислительно-восстановительная реакция.
Таким образом, в растворе наблюдается направленное движение ионов. Максимальная разность потенциалов электродов, которая может быть получена при работе гальванического элемента, называется электродвижущей силой элемента. Она равна разности равновесных потенциалов катода и анода элемента.
где - потенциал электрода -катода,
- потенциал электрода - анода,
Е - разность двух электродных потенциалов
Для рассматриваемой реакции можно записать:
Гальванический элемент может быть составлен не только из различных, но и из одинаковых электродов, погружённых в растворы одного и того же электролита, различающиеся только концентрацией.
Положение металла в ряду напряжений характеризует восстановительную активность его положительного иона. Чем меньше алгебраическая величина стандартного электродного потенциала, тем более активным восстановителем является атом этого металла и тем слабее проявляются окислительные свойства этих ионов в водных растворах. Зависимость электродного потенциала от концентрации веществ, участвующих в электродных процессах, и от температуры выражается уравнением Нернста:
где: - стандартный электродный потенциал металла, В
R - универсальная газовая постоянная, 8,31 Дж/ (моль•К),
T - абсолютная температура, К
F - постоянная Фарадея, 96500 Кл/моль,
z - число электронов, участвующих в электродном процессе.
Заменяя 2,3• R • T /( z • F ) = 2,3• 8,31•273/(96500• z ) = 0,059/ z , получим:
Какие физические свойства характерны для металлов?
Какие химические свойства характерны для металлов и как они связаны со строением их атомов?
Каковы способы получения металлов из руд?
Указать самый лёгкий и самый тяжёлый, самый мягкий и самый твёрдый металлы
Лекция 15. Общие химические свойства металлов
С химической точки зрения металл – это элемент, который во всех соединениях проявляет положительную степень окисления.Из известных в настоящее время 109 элементов 86 являются металлами. Основной отличительной особенностью металлов является наличие в конденсированном состоянии свободных, не связных с определенным атомом электронов. Эти электроны способны перемещаться по всему объему тела. Наличие свободных электронов определяет всю совокупность свойств металлов. В твердом состоянии большинство металлов имеет кристаллическую высокосимметричную структуру одного из типов: кубическую объемноцентрированную, кубическую гранецентрированную или гексагональную плотноупакованную (рис. 1).
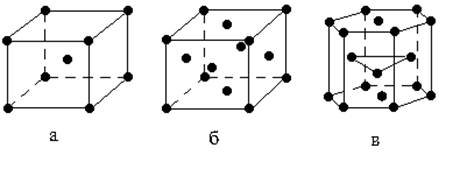
Рис. 1. Типичная структура кристалла металлов: а – кубическая объемноцентрированная; б–кубическая гранецентрированная; в – плотная гексагональная
Существует техническая классификация металлов. Обычно выделяют следующие группы: черные металлы (Fe); тяжелые цветные металлы(Cu, Pb, Zn, Ni, Sn, Co, Sb, Bi, Hg, Cd), легкие металлы с плотностью менее 5 г/см 3 (Al, Mg, Ca и т.д.), драгоценные металлы (Au, Ag и платиновые металлы) и редкие металлы (Be, Sc, In, Ge и некоторые другие).
В химии металлы классифицируются по их месту в периодической системе элементов. Различают металлы главных и побочных подгрупп. Металлы главных подгрупп называют непереходными. Эти металлы характеризуются тем, что в их атомах происходит последовательное заполнение s– и p– электронных оболочек.
Типичными металлами являются s–элементы (щелочные Li, Na, K, Rb, Cs, Fr и щелочноземельные Be, Mg, Ca, Sr, Ba, Ra металлы). Данные металлы расположены в Iа и IIа подгруппах (т. е., в главных подгруппах I и II групп). Этим металлам отвечает конфигурация валентных электронных оболочек ns 1 или ns 2 (n – главное квантовое число). Для данных металлов характерно:
а) металлы имеют на внешнем уровне 1 – 2 электрона, поэтому проявляют постоянные степени окисления +1, +2;
б) оксиды этих элементов носят основной характер (исключение –бериллий, т.к. малый радиус иона придает ему амфотерные свойства);
в) гидриды имеют солеобразный характер и образуют ионные кристаллы;
г) возбуждение электронных подуровней возможно только у металлов IIА группы с последующей sp–гибридизацией орбиталей.
К p–металлам относятся элементы IIIа (Al, Ga, In, Tl), IVа (Ge, Sn, Pb), Vа (Sb, Bi) и VIа (Ро) групп с главными квантовыми числами 3, 4, 5, 6. Данным металлам отвечает конфигурация валентных электронных оболочек ns 2 p z (z может принимать значение от 1 до 4 и равно номеру группы минус 2). Для данных металлов характерно:
а) образование химических связей осуществляется s – и p–электронами в процессе их возбуждения и гибридизации (sp–и spd), однако сверху вниз по группам способность к гибридизации падает;
б) оксиды p– металлов амфотерные или кислотные (основные оксиды только у In и Tl);
в) гидриды p–металлов имеют полимерный характер (AlH3)n или газообразный (SnH4 ,PbH4 и т. д.), что подтверждает сходство с неметаллами, открывающими эти группы.
В атомах металлов побочных подгрупп, называемых переходными металлами, происходит застраивание d– и f– оболочек, в соответствии с чем их делят на d–группу и две f–группы лантаноиды и актиноиды.
К переходным металлам относят 37 элементов d–группы и 28 металлов f–группы. К металлам d–группы относят элементы Ib (Cu, Ag, Au), IIb (Zn, Cd, Hg), IIIb (Sc, Y, La, Ac), IVb (Ti, Zr, Hf, Db), Vb (V, Nb, Ta, Jl), VIb (Cr, Mo, W, Rf), VIIb (Mn, Tc, Re, Bh) и VIII групп (Fe, Co, Ni, Ru, Rh, Pd, Os, Ir, Rt, Hn, Mt, Db, Jl, Rf, Bh, Hn, Mt). Этим элементам отвечает конфигурация 3d z 4s 2 . Исключения составляют некоторые атомы, в том числе атомы хрома с полузаполненной 3d 5 –оболочкой (3d 5 4s 1 ) и меди – с полностью заполненной 3d 10 –оболочкой (3d 10 4s 1 ). Эти элементы обладают некоторыми общими свойствами:
1. все они образуют сплавы между собой и другими металлами;
2. наличие частично заполненных электронных оболочек обусловливает способность d–металлов образовывать парамагнитные соединения;
3. в химических реакциях они проявляют переменную валентность (за немногими исключениями), а их ионы и соединения, как правило, окрашены;
4. в химических соединениях d–элементы электроположительны. "Благородные" металлы, обладая высоким положительным значением стандартного электродного потенциала (Е>0), взаимодействуют с кислотами необычным образом;
5. ионы d–металлов имеют вакантные атомные орбитали валентного уровня (ns, np, (n–1) d), поэтому они проявляют акцепторные свойства, выступая в качестве центрального иона в координационных (комплексных) соединениях.
Химические свойства элементов определяются их положением в Периодической системе элементов Менделеева. Так, металлические свойства сверху вниз в группе возрастают, что обусловлено уменьшением силы взаимодействия между валентными электронами и ядром вследствие увеличения радиуса атома и за счет возрастания экранирования электронами, расположенными на внутренних атомных орбиталях. Это приводит к облегчению ионизации атома. В периоде металлические свойства уменьшаются слева направо, т.к. это связано с увеличением заряда ядра и тем самым с увеличением прочности связи валентных электронов с ядром.
В химическом отношении атомы всех металлов характеризуются сравнительной легкостью отдачи валентных электронов (т.е. малой величиной энергии ионизации) и низким значением сродства к электрону (т.е. малой способностью удерживать избыточные электроны). Как следствие этого низкое значение электроотрицательности, т.е., способность образовывать только положительно заряженные ионы и проявлять в своих соединениях только положительную степень окисления. В связи с этим металлы в свободном состоянии являются восстановителями.
Восстановительная способность разных металлов неодинакова. Для реакций в водных растворах она определяется значением стандартного электродного потенциала металла (т.е. положением металла в ряду напряжений) и концентрацией (активностью) его ионов в растворе.
Взаимодействие металлов с элементарными окислителями (F2, Cl2, O2, N2, S и т.д.). Например, реакция с кислородом, как правило, протекает следующим образом
где n – валентность металла.
Взаимодействие металлов с водой. Металлы, обладающие стандартным потенциалом менее –2,71 В, вытесняют водород из воды на холоде с образованием гидроксидов металлов и водорода. Металлы со стандартным потенциалом от –2,7 до –1,23 В вытесняют водород из воды при нагревании
Остальные металлы с водой не реагируют.
Взаимодействие с щелочами. С щелочами могут реагировать металлы, дающие амфотерные оксиды, и металлы, обладающие высокими степенями окисления, в присутствии сильного окислителя. В первом случае металлы образуют анионы своих кислот. Так, реакция взаимодействия алюминия с щелочью запишется уравнением
в котором, лигандом является ион гидроксида. Во втором случае образуются соли, например K2CrO4 .
Взаимодействие металлов с кислотами. С кислотами металлы реагируют различно в зависимости от численного значения стандартного электродного потенциала (Е) (т.е. от положения металла в ряду напряжения) и окислительных свойств кислоты:
· в растворах галогеноводородов и разбавленной серной кислоты окислителем является только ион Н + , и поэтому с этими кислотами взаимодействуют металлы, стандартный потенциал которых меньше стандартного потенциала водорода:
Me + 2n H + = Me n+ + n H2;
· концентрированная серная кислота растворяет почти все металлы независимо от положения их в ряду стандартных электродных потенциалов (кроме Au и Pt). Водород при этом не выделяется, т.к. функцию окислителя в кислоте выполняет cульфат–ион (SO4 2– ). В зависимости от концентрации и условий проведения опыта cульфат–ион восстанавливается до различных продуктов. Так, цинк в зависимости от концентрации серной кислоты и температуры реагирует следующим образом:
– при очень высокой температуре 4Zn + 5H2SO4(конц.) = 4ZnSO4 + H2S +4H2O;
· в разбавленной и концентрированной азотной кислоте функцию окислителя выполняет нитрат–ион (NO3 – ), поэтому продукты восстановления зависят от степени разбавления азотной кислоты и активности металлов. В зависимости от концентрации кислоты, металла (величины его стандартного электродного потенциала) и условий проведения опыта нитрат–ион восстанавливается до различных продуктов. Так, кальций в зависимости от концентрации азотной кислоты реагирует следующим образом:
Концентрированная азотная кислота не реагирует (пассивирует) с железом, алюминием, хромом, платиной и некоторвми другими металлами.
Взаимодействие металлов друг с другом. При высоких температурах металлы способны реагировать друг с другом с образованием сплавов. Сплавы могут быть твердыми растворами и химическими (интерметаллическими) соединениями (Mg2Pb, SnSb, Na3Sb8, Na2K и др.).
Свойства металлического хрома (…3d 5 4s 1 ). Простое вещество хром представляет собой блестящий на изломе серебристый металл, который хорошо проводит электрический ток, имеет высокую температуру плавления (1890°С) и кипения (2430°С), большую твердость (в присутствии примесей, очень чистый хром мягок) и плотность (7,2 г/см 3 ).
При обычной температуре хром устойчив к действию элементарных окислителей и воде благодаря плотной окисной пленке. При высоких температурах хром взаимодействует с кислородом и другими окислителями.
Cr + Cl2(газ) ® CrCl3 (малиновый цвет)
С металлами при сплавлении хром образует интерметаллиды (FeCr2, CrMn3). При 600°С хром взаимодействует с парами воды:
В электрохимическом отношении металлический хром близок к железу:. Поэтому он может растворяться в неокисляющих (по аниону) минеральных кислотах, таких как галогеноводородные:
Сr + 2HCl ® CrCl2(голубой цвет) + H2.
На воздухе идет быстро следующая стадия:
Окисляющие (по аниону) минеральные кислоты растворяют хром до трехвалентного состояния:
В случае с HNO3(конц) происходит пассивация хрома – на поверхности образуется прочная пленка оксида – и металл не реагирует с кислотой. (Пассивный хром имеет высокий окислительно-восстановительный потенциал = + 1,3 В.)
Основная область применения хрома – металлургия: создание хромистых сталей. Так, в инструментальную сталь вводят 3 – 4% хрома, шарикоподшипниковая сталь содержит 0,5 – 1,5% хрома, в нержавеющей стали (один из вариантов): 18 – 25% хрома, 6 – 10% никеля, < 0,14% углерода, ~0,8% титана, остальное – железо.
Свойства металлического железа (…3d 6 4s 2 ). Железо – белый блестящий металл. Образует несколько кристаллических модификаций, устойчивых в определенном температурном интервале.
Химические свойства металлического железа определяются его положением в ряду напряжений металлов: .
При нагревании в атмосфере сухого воздуха железо окисляется:
В зависимости от условий и от активности неметаллов железо может образовывать металлоподобные (Fe3C, Fe3Si, Fe4N), солеподобные (FeCl2, FeS) соединения и твердые растворы (с C, Si, N, B, P, H).
В воде железо интенсивно корродирует:
При недостатке кислорода образуется смешанный оксид Fe3O4:
Разбавленная соляная, серная и азотная кислоты растворяют железо до двухвалентного иона:
Более концентрированная азотная и горячая концентрированная серная кислоты окисляют железо до трехвалентного состояния (выделяются NO и SO2 соответственно):
Очень концентрированная азотная кислота (плотность 1,4 г/см3) и серная (олеум) пассивируют железо, образуя на поверхности металла оксидные пленки.
Железо используют для получения железоуглеродистых сплавов. Велико биологическое значение железа, т.к. оно – составная часть гемоглобина крови. В организме человека содержится около 3 г железа.
Химические свойства металлического цинка (…3d 10 4s 2 ). Цинк – синевато-белый, пластичный и тягучий металл, но выше 200°С становится хрупким. Во влажном воздухе он покрывается защитной пленкой основной соли ZnCO3×3Zn(OH)2 или ZnO и дальнейшего окисления не происходит. При высоких температурах взаимодействует:
Исходя из величин стандартных электродных потенциалов, цинк вытесняет кадмий, который является его электронным аналогом, из солей: Cd 2+ + Zn ® Cd + Zn 2+ .
Благодаря амфотерности гидроокиси цинка металлический цинк способен растворяться в щелочах:
В разбавленных кислотах:
В концентрированных кислотах:
Значительная часть цинка расходуется для цинкования железных и стальных изделий. Широкое промышленное использование имеют сплавы цинка с медью (нейзильбер, латунь). Цинк широко используется при изготовлении гальванических элементов.
Химические свойства металлической меди (…3d 10 4s 1 ). Металлическая медь кристаллизуется в кубической гранецентрированной кристаллической решетке. Это ковкий мягкий, вязкий металл розового цвета с температурой плавления 1083°С. Медь находится на втором месте после серебра по электро- и теплопроводности, что обусловливает значение меди для развития науки и техники.
Медь реагирует с поверхности с кислородом воздуха при комнатной температуре, цвет поверхности становится темнее, а в присутствии CO2, SO2 и паров воды покрывается зеленоватой пленкой основных солей (CuOH)2CO3, (CuOH)2SO4.
Медь непосредственно соединяется с кислородом, галогенами, серой:
В присутствии кислорода металлическая медь взаимодействует с раствором аммиака при обычной температуре:
Находясь в ряду напряжений после водорода , медь не вытесняет его из разбавленных соляной и серной кислот. Однако в присутствии кислорода воздуха медь растворяется в этих кислотах:
Окисляющие кислоты растворяют медь с переходом ее в двухвалентное состояние:
Со щелочами медь не взаимодействует.
С солями более активных металлов медь взаимодействует, и эта окислительно-восстановительная реакция лежит в основе некоторых гальванических элементов:
Cu SO4 + Zn® Zn SO4 + Cu; E о = 1,1 B
Mg + CuCl2 ® MgCl2 + Cu; E о = 1,75 B.
Медь образует с другими металлами большое число интерметаллических соединений. Наибольшую известность и ценность имеют сплавы: латунь Cu–Zn (18 – 40% Zn), бронза Cu–Sn (колокольная – 20% Sn), инструментальная бронза Cu–Zn–Sn (11% Zn, 3 – 8% Sn), мельхиор Cu–Ni–Mn–Fe (68% Cu, 30% Ni, 1% Mn, 1% Fe).
Нахождение металлов в природе и способы получения.Вследствие высокой химической активности, металлы в природе находятся в виде различных соединений, и только малоактивные (благородные) металл – платина, золото и т.п. – встречаются в самородном (свободном) состоянии.
Наиболее распространенными природными соединениями металлов являются оксиды (гематит Fe2O3, магнетит Fe3O4, куприт Cu2O, корунд Al2O3, пиролюзит MnO2 и др.), сульфиды (галенит PbS, сфалерит ZnS, халькопирит CuFeS, киноварь HgS и т.д.), а также соли кислородосодержащих кислот (карбонаты, силикаты, фосфаты и сульфаты). Щелочные и щелочноземельные металлы встречаются преимущественно в виде галогенидов (фторидов или хлоридов).
Основная масса металлов получается путем переработки полезного ископаемого – руды. Поскольку металлы, входящие в состав руд находятся в окисленном состоянии, то их получение осуществляется путем реакции восстановления. Предварительно руду очищают от пустой породы
Образовавшийся концентрат оксида металла очищают от воды, а сульфиды, для удобства последующей переработки, переводят в оксиды путем обжига, например:
Для разделения элементов полиметаллических руд пользуются методом хлорирования. При обработке руд хлором в присутствии восстановителя образуются хлориды различных металлов, которые вследствие значительной и различной летучести могут быть легко отделены друг от друга.
Восстановление металлов в промышленности осуществляется посредством различных процессов. Процесс восстановления безводных соединений металлов при высоких температурах называют пирометаллургией. В качестве восстановителей используют металлы, более активные, чем получаемый, либо углерод. В первом случае говорят о металлотермии, во втором – карботермии, например:
Особое значение углерод приобрел как восстановитель железа. Углерод для восстановления металлов применяется обычно в виде кокса.
Процесс восстановления металлов из водных растворов их солей относится к области гидрометаллургии. Получение металлов осуществляется при обычных температурах, причем в качестве восстановителей могут быть использованы сравнительно активные металлы или электроны катода при электролизе. Электролизом водных растворов солей могут быть получены только сравнительно малоактивные металлы, расположенные в ряду напряжений (стандартных электродных потенциалов) непосредственно перед водородом или после него. Активные металлы – щелочные, щелочноземельные, алюминий и некоторые другие, получают электролизом расплава солей.
Читайте также:
