Медь мягкий металл или твердый
Обновлено: 02.05.2024
МЕДЬ – элемент 11 группы Периодической системы, плотность 8,9 г см –3 , один из первых металлов, ставших известными человеку. Считают, что медь начали использовать около 5000 до н.э. В природе медь изредка встречается в виде металла. Из медных самородков, возможно, с помощью каменных топоров, были изготовлены первые металлические орудия труда. У индейцев, живших на его берегах оз. Верхнее (Сев. Америка), где есть очень чистая самородная медь, способы ее холодной обработки были известны до времен Колумба.
Около 3500 до н.э. на Ближнем Востоке медь научились извлекать из руд, ее получали восстановлением углем. Медные рудники были и в Древнем Египте. Известно, что глыбы для знаменитой пирамиды Хеопса обрабатывали медным инструментом.
К 3000 до н.э. в Индии, Месопотамии и Греции для выплавки более твердой бронзы в медь стали добавлять олово. Открытие бронзы могло произойти случайно, однако ее преимущества по сравнению с чистой медью быстро вывели этот сплав на первое место. Так начался «бронзовый век».
Изделия из бронзы были у ассирийцев, египтян, индусов и других народов древности. Однако цельные бронзовые статуи древние мастера научились отливать не раньше 5 в. до н.э. Около 290 до н.э. Харесом в честь бога солнца Гелиоса был создан Колосс Родосский. Он имел высоту 32 м и стоял над входом во внутреннюю гавань древнего порта острова Родоса в восточной части Эгейского моря. Гигантская бронзовая статуя была разрушена землетрясением в 223 н.э. (см. также СЕМЬ ЧУДЕС СВЕТА).
Предки древних славян, жившие в бассейне Дона и в Приднепровье, применяли медь для изготовления оружия, украшений и предметов домашнего обихода. Русское слово «медь», по мнению некоторых исследователей, произошло от слова «мида», которое у древних племен, населявших Восточную Европу, обозначало металл вообще.
Символ Cu происходит от латинского aes cyproum (позднее, Cuprum), так как на Кипре (Cyprus) находились медные рудники древних римлян.
Относительное содержание меди в земной коре составляет 6,8·10 –3 %. Самородная медь встречается очень редко. Обычно элемент находится в виде сульфида, оксида или карбоната. Важнейшими рудами меди являются халькопирит CuFeS2, который, по оценкам, составляет около 50% всех месторождений этого элемента, медный блеск (халькоцит) Cu2S, куприт Cu2O и малахит Cu2CO3(OH)2. Большие месторождения медных руд найдены в различных частях Северной и Южной Америк, в Африке и на территории нашей страны. В 18–19 вв. близ Онежского озера добывали самородную медь, которую отправляли на монетный двор в Петербург. Открытие промышленных месторождений меди на Урале и в Сибири связано с именем Никиты Демидова. Именно он по указу Петра I в 1704 начал чеканить медные деньги.
Богатые месторождения меди давно выработаны. Сегодня почти весь металл добывается из низкосортных руд, содержащих не более 1% меди. Некоторые оксидные руды меди могут быть восстановлены непосредственно до металла нагреванием с коксом. Однако большая часть меди производится из железосодержащих сульфидных руд, что требует более сложной переработки. Эти руды сравнительно бедные, и экономический эффект при их эксплуатации может обеспечиваться лишь ростом масштабов добычи. Руду обычно добывают в огромных карьерах, где используются экскаваторы с ковшами до 25 м 3 и грузовики грузоподъемностью до 250 т. Сырье размалывают и концентрируют (до содержания меди 15–20%) с использованием пенной флотации, при этом серьезной проблемой является сброс многих миллионов тонн тонко измельченных отходов в окружающую среду (см. ЗАГРЯЗНЕНИЕ ОКРУЖАЮЩЕЙ СРЕДЫ). К концентрату добавляют кремнезем, а затем смесь нагревают в отражательных печах (доменные печи для тонко измельченной руды неудобны) до температуры 1400° С, при которой она плавится. Суммарное уравнение протекающих реакций можно представать в виде:
Cu +I + 1e – = Cu 0 |
Fe III + 1e – = Fe II | –10e –
2S –II – 12e – = 2S IV |
Большую часть полученной черновой меди очищают электрохимическим методом, отливая из нее аноды, которые затем подвешивают в подкисленном растворе сульфата меди CuSO4, а катоды покрывают листами очищенной меди. В процессе электролиза чистая медь осаждается на катодах, а примеси собираются около анодов в виде анодного шлама, который является ценным источником серебра, золота и других драгоценных металлов.
Около 1/3 используемой меди представляет собой вторичную медь, выплавленную из лома. Годовое производство нового металла составляет около 8 млн. т. Лидируют по производству меди Чили (22%), США (20%), СНГ (9%), Канада (7,5%), Китай (7,5%) и Замбия (5%).
Главное применение металла – в качестве проводника электрического тока. Кроме того, медь используется в монетных сплавах, поэтому ее часто называют «монетным металлом». Она также входит в состав традиционных бронзы (сплавы меди с 7–10% олова) и латуни (сплав меди с цинком) и специальных сплавов, таких как монель (сплав никеля с медью). Металлообрабатывающий инструмент из медных сплавов не искрит и может использоваться во взрывоопасных цехах. Сплавы на основе меди служат для изготовления духовых инструментов и колоколов.
В виде простого вещества медь обладает характерной красноватой окраской. Медь металл мягкий и пластичный. По электро- и теплопроводности медь уступает только серебру. Металлическая медь, как и серебро, обладает антибактериальными свойствами.
Медь устойчива в чистом сухом воздухе при комнатной температуре, однако при температуре красного каления образует оксиды. Она реагирует также с серой и галогенами. В атмосфере, содержащей соединения серы, медь покрывается зеленой пленкой основного сульфата. В электрохимическом ряду напряжений медь находится правее водорода, поэтому она практически не взаимодействует с неокисляющими кислотами. Металл растворяется в горячей концентрированной серной кислоте, а также в разбавленной и концентрированной азотной кислоте. Кроме того, медь можно перевести в раствор действием водных растворов цианидов или аммиака:
В соответствии с положением меди в Периодической системе, ее единственная устойчивая степень окисления должна быть (+I), но это не так. Медь способны принимать более высокие степени окисления, причем наиболее устойчивой, особенно в водных растворах, является степень окисления (+II). В биохимических реакциях переноса электрона, возможно, участвует медь(III). Эта степень окисления редко встречается и очень легко понижается под действием даже слабых восстановителей. Известно несколько соединений меди(+IV).
При нагревании металла на воздухе или в кислороде образуются оксиды меди: желтый или красный Cu2O и черный CuO. Повышение температуры способствует образованию преимущественно оксида меди(I) Cu2O. В лаборатории этот оксид удобно получать восстановлением щелочного раствора соли меди(II) глюкозой, гидразином или гидроксиламином:
Эта реакция – основа чувствительного теста Фелинга на сахара и другие восстановители. К испытываемому веществу добавляют раствор соли меди(II) в щелочном растворе. Если вещество является восстановителем, появляется характерный красный осадок.
Поскольку катион Cu + в водном растворе неустойчив, при действии кислот на Cu2O происходит либо дисмутация, либо комплексообразование:
Оксид Cu2O заметно взаимодействует со щелочами. При этом образуется комплекс:
Для получения оксида меди(II) CuO лучше всего использовать разложение нитрата или основного карбоната меди(II):
Оксиды меди не растворимы в воде и не реагируют с ней. Единственный гидроксид меди Cu(OH)2 обычно получают добавлением щелочи к водному раствору соли меди(II). Бледно-голубой осадок гидроксида меди(II), проявляющий амфотерные свойства (способность химических соединений проявлять либо основные, либо кислотные свойства), можно растворить не только в кислотах, но и в концентрированных щелочах. При этом образуются темно-синие растворы, содержащие частицы типа [Cu(OH)4] 2– . Гидроксид меди(II) растворяется также в растворе аммиака:
Гидроксид меди(II) термически неустойчив и при нагревании разлагается:
Есть сведения о существовании темно-красного оксида Cu2O3, образующегося при действии K2S2O8 на Cu(OH)2. Он является сильным окислителем, при нагревании до 400° С разлагается на CuO и О2.
Большой интерес к химии оксидов меди в последние два десятилетия связан с получением высокотемпературных сверхпроводников, из которых наиболее известен YBa2Cu3O7. В 1987 было показано, что при температуре жидкого азота это соединение является сверхпроводником. Главные проблемы, препятствующие его широкомасштабному практическому применению, лежат в области обработки материала. Сейчас наиболее перспективным считается изготовление тонких пленок.
Многие из халькогенидов меди – нестехиометрические соединения. Сульфид меди(I) Cu2S образуется при сильном нагревании меди в парах серы или в среде сероводорода. При пропускании сероводорода через водные растворы, содержащие катионы Cu 2+ , выделяется коллоидный осадок состава CuS. Однако, CuS – не простое соединение меди(II). Оно содержит группу S2 и лучше описывается формулой Cu I 2Cu II (S2)S. Селениды и теллуриды меди проявляют металлические свойства, а CuSe2, CuTe2, CuS и CuS2 при низких температурах являются сверхпроводниками.
При нагревании меди с галогенами можно синтезировать безводные дифторид, дихлорид и дибромид. Растворы галогенидов меди(II) удобнее получать взаимодействием металла, его оксида, гидроксида или карбоната с соответствующей галогеноводородной кислотой. Из водных растворов всегда выделяются кристаллогидраты.
Попытки получить иодид меди(II) приводят к образованию иодида меди(I) CuI:
2Cu 2+ + 4I – = 2CuI + I2
При этом раствор и осадок окрашиваются в бурый цвет за счет присутствия иода. Образовавшийся иод можно удалить действием тиосульфат-иона:
Однако при добавлении избытка тиосульфат-иона иодид меди(I) растворяется:
Точно так же попытки получить цианид меди(II) приводят к образованию CuCN. С другой стороны, с электроотрицательным фтором не удается получить соль меди(I). Три других галогенида меди(I), представляющие собой белые нерастворимые соединения, осаждаются из водных растворов при восстановлении галогенидов меди(II).
В водных растворах бесцветный ион меди(I) очень неустойчив и диспропорционирует
2Cu I Cu II + Cu(р)
Возможно, причиной этого является размер атома. Ион Cu II меньше, чем Cu I , и, имея вдвое больший заряд, намного сильнее взаимодействует с водой (теплоты гидратации составляют ~2100 и ~580 кДж моль –1 , соответственно). Разница является существенной, так как она перевешивает вторую энергию ионизации для меди. Это делает ион Cu II более стабильным в водном растворе (и ионных твердых веществах), чем Cu I , несмотря на устойчивую конфигурацию d 10 последнего. Тем не менее, Cu I может стабилизироваться в соединениях с очень низкой растворимостью или за счет комплексообразования. Комплексы легко образуются в водном растворе при взаимодействии Cu2O с соответствующими лигандами. В водных растворах хлоро- и амминкомплексы меди(I) медленно окисляются кислородом воздуха до соответствующих соединений меди(II).
Катион меди(II), напротив, в водном растворе вполне устойчив. Соли меди(II), в основном, растворимы в воде. Голубой цвет их растворов связан с образованием иона [Cu(H2O)4] 2+ . Они часто кристаллизуются в виде гидратов. Водные растворы в небольшой степени подвержены гидролизу и из них часто осаждаются основные соли. Основный карбонат есть в природе – это минерал малахит, основные сульфаты и хлориды образуются при атмосферной коррозии меди, а основный ацетат (ярь-медянка) используется в качестве пигмента.
Ярь-медянка известна со времен Плиния Старшего (23–79 н.э.). В русских аптеках ее начали получать в начале 17 в. В зависимости от способа получения она может быть зеленого или голубого цвета. Ею были окрашены стены царских палат в Коломенском в Москве.
Наиболее известную простую соль – пентагидрат сульфата меди(II) CuSO4·5H2O – часто называют медным купоросом. Слово купорос, по-видимому, происходит от латинского Cipri Rosa – роза Кипра. В Росси медный купорос называли синим, кипрским, затем турецким. То, что купорос содержит медь, было впервые установлено в 1644 Ван Гельмонтом. В 1848 Р.Глаубер впервые получил медный купорос из меди и серной кислоты. Сульфат меди широко используется в электролитических процессах, при очистке воды, для защиты растений. Он является исходным веществом для получения многих других соединений меди.
Тетрааммины легко образуются при добавлении аммиака к водным растворам меди(II) до полного растворения первоначально выпавшего осадка. Темно-синие растворы тетраамминов меди растворяют целлюлозу, которую можно вновь осадить при подкислении, что используется в одном из процессов для получения вискозы. Приливание этанола к раствору вызывает осаждение [Cu(NH3)4]SO4·H2O. Перекристаллизация тетраамминов из концентрированного раствора аммиака приводит к образованию фиолетово-синих пентаамминов, однако пятая молекула NH3 легко теряется. Гексааммины можно получить только в жидком аммиаке, и их хранят в атмосфере аммиака.
Медь(II) образует плоско-квадратный комплекс с макроциклическим лигандом фталоцианином. Его производные используются для получения ряда пигментов от синего до зеленого, которые устойчивы вплоть до 500° С и широко используются в чернилах, красках, пластиках и даже в цветных цементах.
Медь имеет важное биологическое значение. Ее окислительно-восстановительные превращения участвуют в различных биохимических процессах растительного и животного мира.
Высшие растения легко переносят сравнительно большое поступление соединений меди из внешней среды, низшие же организмы, наоборот, чрезвычайно чувствительны к этому элементу. Самые незначительные следы соединений меди их уничтожают, поэтому растворы сульфата меди или их смеси с гидроксидом кальция (бордосская жидкость) применяют как противогрибковые средства.
Из представителей животного мира наибольшие количества меди содержатся в телах осьминогов, устриц и других моллюсков. В их крови она играет ту же роль, что железо в крови других животных. В составе белка гемоцианина она участвует в переносе кислорода. Неокисленный гемоцианин бесцветен, а в окисленном состоянии он приобретает голубовато-синюю окраску. Поэтому не зря говорят, что у осьминогов – голубая кровь.
Организм взрослого человека содержит около 100 мг меди, сосредоточенной, в основном, в белках, только содержание железа и цинка выше. Ежедневная потребность человека в меди составляет около 3–5 мг. Дефицит меди проявляется в анемии, однако избыток меди также опасен для здоровья.
Медь мягкий металл или твердый

Самородная медь размером около 4 см
Медь — минерал из класса самородных элементов. В природном минерале обнаруживаются Fe, Ag, Au, As и другие элементы в виде примеси или образующие с Cu твёрдые растворы. Простое вещество медь — это пластичный переходный металл золотисто-розового цвета (розового цвета при отсутствии оксидной плёнки). Один из первых металлов, широко освоенных человеком из-за сравнительной доступности для получения из руды и малой температуры плавления. Он входит в семёрку металлов, известных человеку с очень древних времён. Медь является необходимым элементом для всех высших растений и животных.
Смотрите так же:
СТРУКТУРА
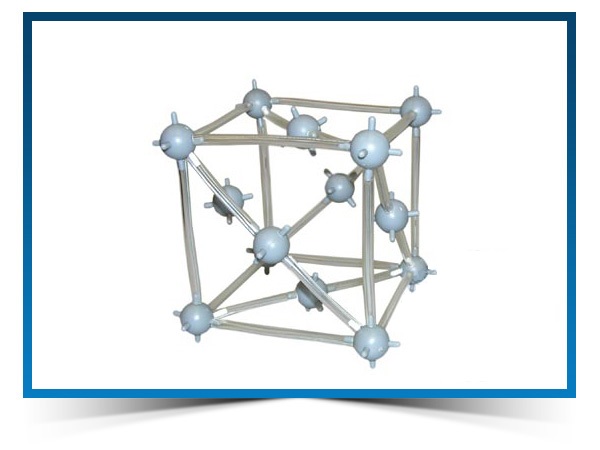
Кристаллическая структура меди
Кубическая сингония, гексаоктаэдрический вид симметрии m3m, кристаллическая структура – кубическая гранецентрированная решётка. Модель представляет собой куб из восьми атомов в углах и шести атомов , расположенных в центре граней (6 граней). Каждый атом данной кристаллической решетки имеет координационное число 12. Самородная медь встречается в виде пластинок, губчатых и сплошных масс, нитевидных и проволочных агрегатов, а также кристаллов, сложных двойников, скелетных кристаллов и дендритов. Поверхность часто покрыта плёнками “медной зелени” (малахит), “медной сини” (азурит), фосфатов меди и других продуктов её вторичного изменения.
СВОЙСТВА
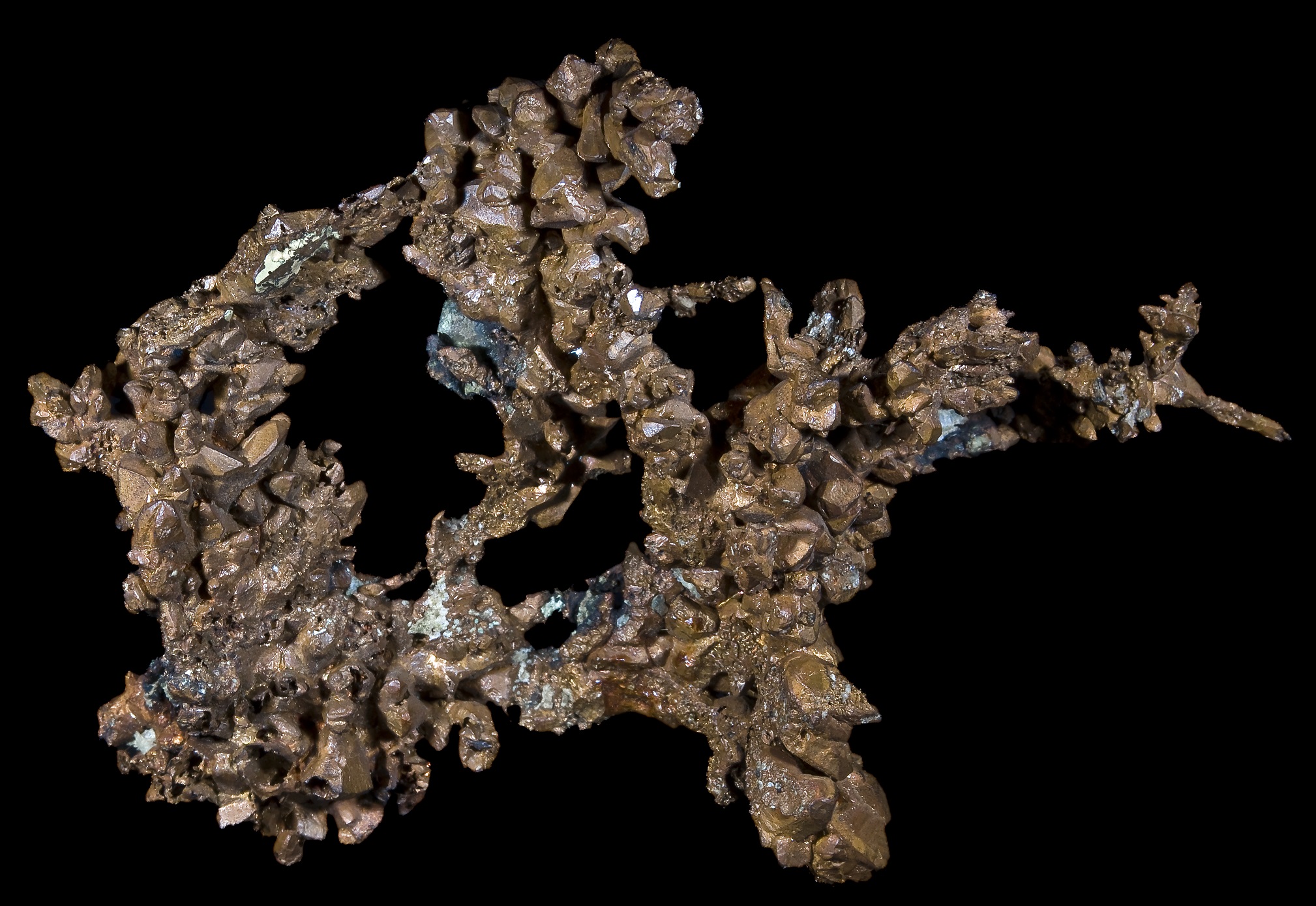
Кристаллы самородной меди, Верхнее озеро, округ Кинави, Мичиган, США. Размер 12 х 8,5 см
Медь — золотисто-розовый пластичный металл, на воздухе быстро покрывается оксидной плёнкой, которая придаёт ей характерный интенсивный желтовато-красный оттенок. Тонкие плёнки меди на просвет имеют зеленовато-голубой цвет.
Наряду с осмием, цезием и золотом, медь — один из четырёх металлов, имеющих явную цветовую окраску, отличную от серой или серебристой у прочих металлов. Этот цветовой оттенок объясняется наличием электронных переходов между заполненной третьей и полупустой четвёртой атомными орбиталями: энергетическая разница между ними соответствует длине волны оранжевого света. Тот же механизм отвечает за характерный цвет золота.
Медь обладает высокой тепло- и электропроводностью (занимает второе место по электропроводности среди металлов после серебра). Удельная электропроводность при 20 °C: 55,5-58 МСм/м. Медь имеет относительно большой температурный коэффициент сопротивления: 0,4 %/°С и в широком диапазоне температур слабо зависит от температуры. Медь является диамагнетиком.
Существует ряд сплавов меди: латуни — с цинком, бронзы — с оловом и другими элементами, мельхиор — с никелем и другие.
ЗАПАСЫ И ДОБЫЧА

Образец меди, 13,6 см. Полуостров Кинави, Мичиган, США
Среднее содержание меди в земной коре (кларк) — (4,7-5,5)·10 −3 % (по массе). В морской и речной воде содержание меди гораздо меньше: 3·10 −7 % и 10 −7 % (по массе) соответственно. Большая часть медной руды добывается открытым способом. Содержание меди в руде составляет от 0,3 до 1,0 %. Мировые запасы в 2000 году составляли, по оценке экспертов, 954 млн т, из них 687 млн т — подтверждённые запасы, на долю России приходилось 3,2 % общих и 3,1 % подтверждённых мировых запасов. Таким образом, при нынешних темпах потребления запасов меди хватит примерно на 60 лет.
Медь получают из медных руд и минералов. Основные методы получения меди — пирометаллургия, гидрометаллургия и электролиз. Пирометаллургический метод заключается в получении меди из сульфидных руд, например, халькопирита CuFeS2. Гидрометаллургический метод заключается в растворении минералов меди в разбавленной серной кислоте или в растворе аммиака; из полученных растворов медь вытесняют металлическим железом.
ПРОИСХОЖДЕНИЕ

Небольшой самородок меди
Обычно самородная медь образуется в зоне окисления некоторых медносульфидных месторождений в ассоциации с кальцитом, самородным серебром, купритом, малахитом, азуритом, брошантитом и другими минералами. Массы отдельных скоплений самородной меди достигают 400 тонн. Крупные промышленные месторождения самородной меди вместе с другими медьсодержащими минералами формируются при воздействии на вулканические породы (диабазы, мелафиры) гидротермальных растворов, вулканических паров и газов, обогащенных летучими соединениями меди (например, месторождение озера Верхнее, США).
Самородная медь встречается также в осадочных породах, преимущественно в медистых песчаниках и сланцах.
Наиболее известные месторождения самородной меди – Туринские рудники (Урал), Джезказганское (Казахстан), в США (на полуострове Кивино, в штатах Аризона и Юта).
ПРИМЕНЕНИЕ

Браслеты из меди
Из-за низкого удельного сопротивления, медь широко применяется в электротехнике для изготовления силовых кабелей, проводов или других проводников, например, при печатном монтаже. Медные провода, в свою очередь, также используются в обмотках энергосберегающих электроприводов и силовых трансформаторов.
Другое полезное качество меди — высокая теплопроводность. Это позволяет применять её в различных теплоотводных устройствах, теплообменниках, к числу которых относятся и широко известные радиаторы охлаждения, кондиционирования и отопления.
В разнообразных областях техники широко используются сплавы с использованием меди, самыми широко распространёнными из которых являются упоминавшиеся выше бронза и латунь. Оба сплава являются общими названиями для целого семейства материалов, в которые помимо олова и цинка могут входить никель, висмут и другие металлы.
В ювелирном деле часто используются сплавы меди с золотом для увеличения прочности изделий к деформациям и истиранию, так как чистое золото очень мягкий металл и нестойко к этим механическим воздействиям.
Прогнозируемым новым массовым применением меди обещает стать её применение в качестве бактерицидных поверхностей в лечебных учреждениях для снижения внутрибольничного бактериопереноса: дверей, ручек, водозапорной арматуры, перил, поручней кроватей, столешниц — всех поверхностей, к которым прикасается рука человека.
Как определить, что перед нами: латунь или медь, их основные отличия
У каждого, кто ищет и сдает цветной металл, иногда возникают сомнения по поводу вида лома и, соответственно, его истинной стоимости при сдаче.
Медь является цветным металлом, а латунь – это сплав, который обычно состоит из 70% меди, поэтому часто похож на нее.
Ошибка может обойтись довольно дорого. За медь в пунктах приема дают 285- 300 рублей, за латунь – около 150. Существует много способов, как узнать, что за металл мы видим — медь или латунь, а как отличить их друг от друга мы расскажем в этой статье.
Что такое медь и латунь
Медь – это цветной металл. Цвет у него красновато-розовый, он податливый при работе, мягкий и ковкий. Имеет высокую тепло- и электропроводимость, поэтому из меди часто производят:
- детали электроприборов;
- кабели;
- радиаторы.
Медь не закаляют, поскольку она становится твердой и после холодной ковки. Имеет свойство покрываться патиной – зеленым налетом, который возникает при высокой влажности окружающей среды.
Для повышения прочности, улучшения ряда других показателей и удешевления материала в нее добавляют примеси и получается сплав.
Одним из таких сплавов является латунь.
В классическом исполнении в ней содержится треть цинка.
Латунь – золотисто-желтая, более прочная и твердая. Она не так интенсивно окисляется, не такая пластичная.
В нее иногда, в зависимости от предназначения сплава, добавляют:
Сходства и различия
Сплав латуни по большей части состоит из меди, поэтому естественно, что они похожи не только визуально, но и некоторыми свойствами. Чем больше меди в сплаве, тем сильнее их цвета будут схожи. На этом точные совпадения заканчиваются.
Визуально легко отличаются сплавы латуни, где меди менее 80%. Они слегка похожи на золото, так как имеют выраженный желтый оттенок. Чем больше цинка, тем оттенок светлее.
Из-за этого латунь даже используют для подделки или имитации золота. У меди же главный оттенок – красноватый, который часто отливает розовым.
При сильном понижении температуры латунь не теряет своей, сравнительно ограниченной, пластичности и не становится хрупкой. Электричество и тепло проводит хуже.
Отличаются они по такому признаку, как твердость.
Медь мягче, пластичнее, а латунь, наоборот, твердая и придать ей какую-либо форму без применения отжига сложно.
Стружка также получается разная: у латуни – игольчатая, у меди – закрученная в спираль.
Рассмотрим свойства, которые имеет латунь и медь, есть ли у них отличия:
| Медь | Латунь |
| Пластичная, мягкая | Твердая |
| Красновато-коричнево -розовый оттенок | Золотистый оттенок |
| Звук ниже при ударе | Высокий звук |
| Тяжелая | Легче |
| Стружка скручивается в спираль | Стружка игольчатая |
Как отличить?
Чаще всего можно отличить по:
- виду;
- весу;
- степени твердости
без применения каких-либо инструментов или аппаратуры.
Но бывают ситуации, когда для точности необходимо задействовать:
Перед оценкой лома, который вы собираетесь отнести в пункт приема, надо очистить его от грязи, иначе «на глаз» определить точно не получится.
По цвету
Оба металла, хоть и в разной степени, могут покрыться патиной.
Поэтому не забываем хорошо очистить лом.
Если объект долго находился на открытом воздухе или в воде, слой патины снимается сложно.
Иной раз оправданной будет покупка специального средства для очистки.
Желательно осматривать лом под мощным белым светом.
Подразумевается, что можно смотреть либо под солнцем в погожий день, либо под яркой люминесцентной лампой. Лампа накаливания не подходит.
Чистая медь будет иметь красновато-коричневый оттенок, иногда с розовым отливом.Надо учитывать, что латунь может быть красной или оранжевой. Такую обычно используют для украшений и водопроводных труб.
Если материал с оранжевым, желтым или золотистым оттенком, можно быть почти уверенным, что перед вами латунь.
Она еще бывает светло-золотистой, бледно-желтой , и даже грязно-белой, но поисковикам металла встречается очень редко, так как такой сплав тяжело обрабатывать, и он используется преимущественно в украшениях.
Лучшая рекомендация – носить с собой предмет, в котором вы точно уверены, что он сделан из чистой меди. Вы сможете сравнивать ее с найденным вами ломом. Чаще всего такой метод хорошо работает.
По звуку
Еще один метод, для которого не нужны специальные навыки или приспособления. Различать металлы по звуку можно научиться после непродолжительной тренировки. Ударьте чем-то металлическим по предмету. Если он сделан из меди, то звук будет приглушенным, низким. Это происходит, так как металл мягкий.
Обычно визуального осмотра и проверки на звук и твердость достаточно для определения в полевых условиях.
Напротив, латунь будет издавать при ударе звонкий и высокий звук. Второй по значимости способ проверки для тех, кто имеет дело с металлоломом, после визуальной оценки на свету. Но, такой метод оправдан только с большими и объемными предметами – нужно, чтобы было чему издавать звук.
По твердости
Медь, как уже было сказано выше, — мягкий металл. Латунь специально создали, чтобы увеличить твердость меди при сохранении некоторых ее других характеристик. Поэтому при нанесении повреждения лому, медью будет тот материал, который легче деформируется. Латунь же стойко переносит удары.
По маркировке
Если на предмете есть метки, определение металла или сплава может стать простым и точным.
На латунь, как правило, ставят метку, которая начинается со значка «Л».
Соответственно, маркировка меди начинается с «М». Правда, медь довольно часто не имеет никакой маркировки.
Вот некоторые расшифровки, которые могут пригодиться:
- Маркировка меди начинается с одной буквы «М», за которой идут цифры. Буква «Л» на изделиях из латуни бывает не одна, за ней могут идти еще буквы, а только потом цифры.
- В Соединенных Штатах и Канаде действует система UNS, согласно которой на латуни ставится метка C2, C3, C4.
- В Европейском Союзе оба металла маркируются буквой С, все зависит от последующих букв. Для меди они будут A, B, C, D, а для латунного сплава – L, M, N, P и R.
- Еще не так давно распространенной была маркировка, состоящая из значков химических элементов. Например, Cu Zn (купрум – цинк) будет означать латунь.
По весу
Латунь легче меди благодаря добавлению в нее цинка. Но для того, чтобы определить по бесформенному куску, металл это или сплав, необходим опыт.
По стружке
Для этой проверки потребуется дрель по металлу или доступ к станку, чтобы получить стружку.
У латуни она будет, как говорят специалисты, игольчатая, так как материал твердый.
Она как бы сыпучая.
У меди стружка будет пластичнее, поэтому часто даже не разрывается и получается витиеватая, одной сплошной спиралью.
Однако существуют сорта латуни, стружки которых похожи на медные. По отзывам практиков сорт ЛС63 — очень пластичный и вязкий сплав, после его обработки остаются стружки-спиральки.
Анализ кислотой
Если вы столкнулись с латунью марки Л-96, что означает присутствие в сплаве 96% меди, отличить ее от металла без анализа сложно. Для этого можно использовать соляную кислоту. Если капнуть ею на чистую медь, она просто очистит ее от патины и в реакцию с самим металлом не вступит.
Если же нанести соляную кислоту на латунь, то в реакцию вступит цинк и на поверхности проступит окись белого цвета – хлорид цинка.
Анализатором
На нашем портале есть подробный материал про анализаторы металлов и сплавов. При помощи такого устройства можно безошибочно определить, что находится перед вами.
Такие анализаторы имеют жидкокристаллический экран, на который, после взаимодействия аппарата и металлического объекта, выводится полный список всех составляющих элементов.
Если это будет 99% меди и десятые доли процента каких-то случайных примесей – это медь. Если будут в значительных количествах другие металлы – латунь. Но способ дорогой.
По типу изделия
Некоторые изделия производят только из меди или только из латуни.
Это может стать дополнительным ориентиром.
Инструменты производят исключительно из латуни, она тверже.
Из меди делают некоторые части духовых музыкальных инструментов.
В принципе, нужно отталкиваться от назначения предмета – если он должен быть:
то для его изготовления, скорее всего, использовали латунь.
Если наоборот, нужна пластичность, высокая электро- или теплопроводность, то это – медь.
Путем нагревания
Еще один способ, при котором нужно использовать газовую горелку.
Индикатором здесь будет оксид цинка, который образуется в виде налета бледно-белого пепельного оттенка только на латуни, если ту нагреть до температуры выше 600 градусов.
Вывод
Людям, промышляющим сбором, сдачей и приемом цветного лома, необходимо знать и уметь отличать внешне похожие цветные металлы. Способность определять может хорошо окупиться, так как латунь в пунктах приема стоит почти в два раза дешевле, чем медь первого сорта.
Если найденный объект небольшой, можно определить самостоятельно. Если количество лома велико, можно прибегнуть к помощи инструментов или анализатора, который берется в аренду.
Если вы решили сдать цветной металлолом, то убедитесь, что у пункта приема есть для этого лицензия.
Как очистить данные цветные металлы перед сдачей, вы можете увидеть в данном видеоролике:
Материаловедение: медь
Чем примечательна медь, и за какие такие заслуги ее считают одним из важнейших металлов в истории человечества? Каковы ее плотность, температура плавления и прочие физико-химические свойства? Чем вызван скачок цен на медь в 2020-2021 гг., и почему это в общем-то только начало? Отвечаем на эти и другие вопросы в нашей четвертой статье из цикла «материаловедение».

Медь (Cu) – мягкий и пластичный металл золотисто-розового цвета, 29-й элемент периодической системы. Это один из главных промышленных металлов. По объемам производства среди цветметов медь вторая вслед за алюминием.
Ковкая и устойчивая к коррозии, медь используется в инженерных коммуникациях, машино- и судостроении, ювелирном деле. Однако до 60% от производимых объемов идет на электротехнику и энергетику. И это вполне логично: по тепло- и электропроводности медь впереди всех промышленных металлов и дышит в спину только серебру. Но сколько стоит медь, а сколько – серебро. Разница в цене стократная.

Медь – один из первых металлов на службе у человека. И это неспроста. Начнем с простого факта: чистая медь – химически неактивный металл, она не стремится к взаимодействию с другими элементами и веществами, как тот же алюминий. Вот почему в природе она часто встречается в самородках, даже чаще, чем железо. Кроме того, у нее умеренная температура плавления – 1 085°C, тогда как у железа 1539 °C
Одни из древнейших медных артефактов возрастом 8500 лет обнаружены на раскопках поселения Чатал-Хююк (Турция). При экскавации кургана археологи нет-нет да находили окалины и шлак – казалось бы, явные свидетельства переплавки медной руды. Впрочем, некоторые ученые воздерживаются от скоропалительных выводов. По их версии, куски руды могли образоваться случайно в попытках намешать краску для ритуальных погребений.
Тем не менее к IV тысячелетию до н. э. медь приручили если и не все цивилизации, то многие. Сперва медные самородки обрабатывали холодной ковкой: заготовки для наконечников копий и будущие лезвия топоров обстукивали камнями до нужной формы. Горючую же ковку миру явила невероятно продвинутая по тем временам кипро-минойская цивилизация. Как показывают раскопки, в III тысячелетии до н. э. на Кипре уже вовсю плавили медь из малахита, бирюзы и других окисных руд. Отсюда, между прочим, и латинское название меди Cuprum, производное от Aes Cyprium («металл Кипра»).
Сегодня медь добывают в основном из сернистых соединений CuS, Cu2S сульфидных руд: медного колчедана, медного блеска и др. В России крупнейшее медные месторождения сосредоточены в Красноярском крае и Забайкалье, а ведущим производителем считается «Норникель».

Чистая медь – мягкий и пластичный металл из семейства переходных. Она легко тянется в проволоку, хорошо обрабатывается давлением в горячем и холодном состоянии, сваривается почти всеми видами термомеханической сварки и сносно режется. К технологическим недостаткам относят низкие литейные качества. Дело в том, что расплав меди густотекучий, отливки дают большую усадку, а это требует сложных расчетов и вообще делает расход материала непомерным.
Плотность: 8933 кг/м3 (8,93 г/см3). Изделия из меди и медных сплавов увесистые. Подсчитано, что если в легковушке заменить всю медную проволоку алюминиево-циркониевой, то автомобиль «сбросит» около 12 кг.
Температура плавления: 1083°C. Это среднеплавкий металл. Для сравнения: у цинка температура плавления – 419,5°C, у алюминия – 658°C, железа – 1 539°C.
Коэффициент теплопроводности: 394 Вт/(м·К). Высокая теплопроводность делает медь эффективной в радиаторах охлаждения, отопления и кондиционирования, системах водоснабжения.
Электропроводность: 55,5—58 МСм/м. Этот показатель падает с увеличением доли примесей. По этой причине провода по нормативам изготавливают из меди с примесями не более 0,1% от состава.
Высокая стойкость к коррозии. Причем не только в пресной и морской воде, но и в различных химических средах, включая органические кислоты, едкие щелочи и галогены.
Цвет: от золотисто-розового до желто-красного. Желтоватые нотки – заслуга оксидной пленки, образующейся при взаимодействии с воздухом. Впоследствии эта пленка служит естественной защитой от коррозии. Отметим, что медь окисляется даже при комнатной температуре, чем разительно отличается от золота и серебра.

Поскольку медь отлично проводит электричество, ее активно используют в электронике, смартфонах, телевизорах, компьютерах и т. д.

В домах с медными трубами аварийные ситуации – редкость. Для сравнения: по данным ВЦИОМ за 2006 год, в первые три года использования пластиковых труб аварии случаются в 8 квартирах из 100. Кроме того, медь в отличие от пластика инертна к хлору и благодаря ионизации имеет антибактерицидные свойства. Совсем как серебро. Это, к слову, объясняет, почему поручни и дверные ручки из медесодержащих сплавов называют самоочищающимися.

От внутриквартирной разводки до перекачки мазута – медные трубы пригодятся в самом широком спектре инженерных работ. При этом срок их службы может достигать 50-100 лет.

Всего лишь одна ветряная турбина мощностью 3 МВт нуждается в более 4 т меди. Отметим, что в том числе переход на зеленую энергетику со всеми ее солнечными панелями и ветрогенераторами спровоцировал стремительный рост цен на медь, наметившийся еще с 2017 года.

Медь сплавляют с золотом, чтобы придать тому большую прочность на изгиб и стойкость к истиранию. Те же розовое и красное золото – это все сплавы меди с чистым желтым золотом в пропорции 1:3 (для пробы 750).

Первичная медь маркируется по ГОСТ 859-2014 буквой М и числом, обозначающей чистоту металла. Самая беспримесная марка однокомпонентной меди – М006, переплавляемая из катодов в вакууме, восстановительной или инертной атмосфере. Степень ее чистоты не менее 99,99%. Для сравнения: получаемая переплавкой лома М3 содержит 99,5% меди.
Иногда после числа в маркировке стоит буква: М1ф, М2р… Эта буква на конце обозначает легирующий элемент либо указывает степень раскисления. К примеру, в марке М1ф помимо собственно меди (99,9%) содержится фосфор (0,04%) и другие примеси. В марке М2р 99,7% меди, 0,01% раскисляющего кислорода и до 0,06% фосфора, а остальное – примеси.
Отметим, что примеси в составе значительно снижают характеристики меди, в первую очередь тепло- и электропроводность. Особенно критично в этом плане превышение доли мышьяка (As) и сурьмы (Sb). По этой причине как проводник используют только электролитическую медь чистых марок: М1 (99,9%), М0 (99,93%) и практически беспримесную М006 (99,99%).
Для большей прочности и улучшения технологических свойств (в первую очередь – литейных) в меди растворяют различные легирующие компоненты: Zn, Sn, Be, Ae, Mn, Ni, Si. В целом по химическому составу все сплавы на основе меди можно разделить на три большие группы: латуни, бронзы и медно-никелевые сплавы.

Медный сплав с добавлением цинка (от 5 до 45%) и иногда другими присадками. Цвет всегда с блеском и в зависимости от содержания цинка варьируется от красно-желтого или желтого (Zn ≤ 20%) до чуть зеленоватого (Zn 36-45%). Если сравнивать с медью, латунь удобнее в литье, но склонна к растрескиванию под напряжением и хуже реагирует на морскую воду. Применение: сантехника, коммутирующие устройства в электротехнике, различная фурнитура, украшения и др.

Сплав меди с оловом (~12%) и другими легирующими компонентами: алюминием, марганцем, фосфором, кремнием и др. Цвет красновато-коричневый. Будучи более хрупкими, чем медь и латунь, многие бронзы тем не менее прекрасно подходит для художественного литья, давая всего 1% усадки. Также бронза отлично противостоит морской воде и агрессивной химии, из-за чего применяется в топливной и паровой арматуре. Кому-то она известна и как подшипниковый материал – дают о себе знать отменные антифрикционные свойства.

В частности, конструкционные сплавы мельхиор (Ni 5-30%) и нейзильбер (Ni 5-35%, Zn 13-45%). Меньше на слуху электротехнические сплавы константан (Ni 39-41%, Mn 1-2%) и копель (Ni 43-44%, Fe 2-3%).
Применяются медно-никелевые сплавы в изготовлении реостатов и резисторов; в судостроении; в медицинской промышленности; в чеканке монет. В частности, до 2009 года из сплавов меди с никелем чеканились монеты Банка России в 1 и 2 рубля. В 2009 году материал поменяли: с тех пор это сталь с гальванопокрытием. Что ж, посткризисное время требует посткризисных решений.
На середину июля 2021 года цена за 1 кг меди на пунктах приема составляет от ~300 руб. за медно-никелевую трубу МНЖ5-1 до ~550 руб. за блестящий медный кабель.
Что касается цен на биржах, то после шокировавшего многих зимнего пика наметился курс на постепенную стабилизацию. На момент написания статьи на Лондонской бирже медь торгуется по стоимости $9 419,2817 за тонну.

Стабилизация – стабилизацией, но отката цен к уровню 2019 года пока не предвидится. Куда вероятнее нас ждет новый виток роста. Тому есть несколько причин. Самые очевидные – разгон мировой инфляции и дефицит металлопроката, вызванный прекращением сбора лома в первую волну коронавирусных карантинов, лавиной отложенного спроса впоследствии. В долгосрочной перспективе во все это вмешается еще и агрессивная политика озеленения энергетики. На декарбонизацию экономик согласно целям устойчивого развития, навязанных ООН и расписанных на первом этапе до 2030 года, понадобится много редкоземельных и цветных металлов. И медь в этом списке значится чуть ли не первой.

В чистом виде медь в производстве замочно-скобяных изделий не используется. Зато в ход идут медные и медесодержащие сплавы, прежде всего латунь и ЦАМ (цинковый сплав с Cu ~1%).
Если упрощенно, то чем больше меди в сплаве, тем качественнее фурнитура: точнее в размерах, дольше держит покрытие, лучше противостоит коррозии. К примеру, дверные петли Palladium отлиты из премиальной латуни Class A с Cu 54-57,4%. Отсюда эталонная геометрия, поразительная плавность хода и срок службы длиной в вечность. Также отметим латунные навесные замки Palladium и смесители Manzzaro. В последних, кстати, используется латунь ЛЦ40С с Cu 59-60%.
И в заключение о фурнитуре из медесодержащего сплава ЦАМ, прежде всего – о дверных ручках. В самом материале меди ~1%. Однако меднение является важнейшим этапом в гальванизации, от него зависит долговечность наносимого покрытия. Если производитель схитрил и недоложил адгезионный медный слой в требуемую толщину, ручка потрется или потемнеет за 1-2 года. При честном же соблюдении технологии ручка из ЦАМ должна сохранять близкий к товарному вид 5-10 лет. Даже если установлена на двери в ванной, на кухне и в других помещениях с капризной средой.
Материаловедение: латунь
Из чего состоит латунь, чем она хороша и где применяется? Каковы ее плотность, температура плавления и другие физические свойства? В этой статье мы ответим на вопросы как о самой латуни, так и об изделиях из этого материала. Особый фокус – на латунной дверной фурнитуре: ручках, петлях, навесных замках и цилиндровых механизмах. Как производитель замочно-скобяных изделий мы просто не могли обойти эту близкую нам тему стороной.

Латунь – сплав металлов на основе меди с добавлением цинка (и иногда присадками других элементов). При этом медь всегда превалирует, а содержание цинка колеблется в пределах от 5 до 45% в зависимости от марки сплава.
Податливая, стойкая к коррозии и сверкающая золотом, латунь применяется еще с античности. Считается, что одними из первых ее изловчились добывать моссинойки – племена, тысячи лет назад населявшие Причерноморье. Водилась латунь и в Древнем Риме, но по достоинству ее там толком не оценили. Возможно, виной всему уж слишком сильное и оттого разочаровывающее сходство с золотом, но вероятнее всего – дефицит на Апеннинах цинковой руды. Мало что изменилось и в эпоху Средневековья. Если латунь и использовалась, то эпизодически и по большей части в Китае и Индии, тогда как как европейцев куда больше занимало железо.
Короче говоря, латунный бум откладывался очень долго, вплоть до XVIII века. К этому времени цинк уже был описан и добывался по всей Европе, а Промышленная революция запустила гонку предпринимательского азарта. Победителем в последней стал Джеймс Эмерсон из Бристоля, в 1781 году запатентовавший технологию сплавки меди с цинком. Это событие и есть нулевая точка, определившая вектор развития латунной металлургии.

Прочность и долговечность делают латунь подходящим материалом для корпусов духовых инструментов и варганов. Не забудем и про латунные гитарные струны – может, не самые прочные, зато со звонким объемным звучанием.

Латунь исключительно стойка к водным средам, а с присадкой марганца и некоторых других металлов ее иммунитет к коррозии только возрастает.

На правах медесодержащего сплава с высокой электропроводностью латунь применяется при изготовлении токопроводящих винтов, шайб, гаек, штепсельных контактов и коммутирующих элементов.

Знаете ли вы, что начинающие ювелиры часто выбирают латунь учебным материалом? Особенно марки Л62 и Л68. Они и внешне напоминают золото, а уж по механическим свойствам вообще один в один 583 проба.

Из латуни отливают элитные дверные ручки и петли премиум-качества; корпуса навесных замков; механизмы и высокоточные детали к ним.

Отметим, что латунь с Zn ≤ 20% называют красной. Ее, в свою очередь, подразделяют на томпак (Zn <10%), полутомпак (Zn 10-20%).

Отлично подходит для тонкостенного литья, создания сложных и детализированных форм, точного воспроизведения размеров. Сравните при возможности латунные и стальные петли для деревянных дверей – разница в качестве видна ненаметанным глазом.

Те же латунные петли необязательно покрывать гальваникой. Достаточно их отполировать и пройти сверху лаком – будет вам сияющий золотистый цвет.

Основная причина: высокое содержание меди. С точки зрения электрохимии медь относится к малоактивным металлам. При окислительных реакциях она слабо вытесняется водородом и неохотно участвует в межмолекулярной диффузии. Во многом поэтому на латунь так прочно налипают гальванические покрытия: «хром», «никель», «античная бронза» и др.

Дело в основном в теплопроводности. Чем ниже теплопроводность металла – тем теплее он кажется в условиях комнатной температуры. Посмотрите таблицу выше – у латуни теплопроводность в 2 раза ниже, чем у алюминия. Неудивительно, что латунные межкомнатные ручки по ощущениям комфортней, чем алюминиевые.

Она не ржавеет (в ней нет или почти нет железа) и мало подвержена коррозии. Да, когда-нибудь на латуни проступят темная окись и зеленоватая патина. Однако: а) в обычных бытовых условиях и при наличии слоя лака этот процесс растянется на десятилетия; б) окислы можно вывести полиролем или народными средствами.
В подтверждение всему сказанному фото выше. Сложно поверить, но эта латунная ручка-скоба родом из 1950х!

Там, где существует риск вандализма, уместней использовать сплавы потверже. Есть один показательный пример из жизни – навесные замки. Если на дверь в сарай латунный замок в самый раз, то куда-нибудь в гараж берите стальной или чугунный.

С плотностью 8500–8700 кг/м3 латунь перевешивает все основные фурнитурные сплавы: и сталь Ст3 (7850 кг/м3), и ЦАМ 4-1 (6700 кг/м3), и алюминий (2700 кг/м3). Имейте это в виду, если подбираете что-то с прицелом на транспортабельность –скажем, навесной замок на противоугонную цепь для велосипеда.
Латунные петли в 3-5 раз дороже соразмерных им стальных. Похожая ситуация и с дверными ручками. Цена алюминиевой ручки – 500-1000 руб.; аналог из ЦАМ будет стоить от 1200 руб. Точно такая же по дизайну ручка из латуни обойдется минимум (!) в 4500-6000 руб.
Главный элемент сплава. Отвечает за твердость, износостойкость, электропроводящие и теплообменные свойства.
Сплавляется с медью для улучшения механических, технологических и антифрикционных свойств, влияет на цвет (см. п.3). При добавлении до 38% цинка повышается прочность, причем без существенных потерь в пластичности. В то же время, если цинка 20% и более, сплав становится восприимчивее к коррозионному растрескиванию из-за остаточных напряжений, особенно во влажной атмосфере со следами сероводорода или аммиака.
Все двухкомпонентные латуни считаются двойными (простыми). Обозначаются они буквой Л, за которой следует указание усредненного % меди. Пример: Л68 – простая обрабатываемая давлением латунь с Cu 68%, Zn 32% и примесями.
Повышает стойкость к коррозии, вместе с тем ухудшая литьевые качества (один из нежелательных эффектов – пенистость в отливках).
Добавляется для большей сопротивляемости коррозии в морской воде, атмосфере горячего пара и хлоридов. Как правило, комбинируется с другими присадками.
Уменьшает зернитость, делает сплав тверже и затрудняет кристаллизацию. Если доля железа выше 3%, изменяются магнитные свойства.
Улучшает механические и антикоррозийные качества. Если сравнивать с другими латунями, именно никелевые – самые стойкие к обесцинкованию и коррозионному растрескиванию. Ввиду этого они активно применяются в морском судостроении.
Повышает коррозионную стойкость в пресной и морской воде. Содержится в доле до ~1,5% в так называемых морских латунях (Л070-1, ЛО62-1).
Улучшает резку на станках, снижает трение. Но есть и побочные эффекты: уменьшается пластичность, возрастает риск горячеломкости латуни (особенно в сплавах с Zn 30-33%).
Отметим особый порядок маркировки многокомпонентных латуней. В названии сначала идет «Л» (латунь), а затем начальные буквы других легирующих элементов. Числа после букв обозначают долю элемента в %. Примеры: ЛАЖ60-1-1 – латунь с Cu ~60%, Al ~1%, Fe ~1%; остальное – цинк и примеси. ЛЦ23А6Ж3Мц2 – латунь с Zn ~23%, легированная Al ~6%, Fe ~3%, Mn ~2%; остальное – медь и примеси.

Бронза – сплав меди и олова (~12%); иногда с присадками алюминия, марганца, фосфора, кремния и других элементов. Главные отличия: цвет (медь обычно приглушенно-красноватая, без блеска, латунь – желтая и блестящая), зернистость (латунь в срезе мельче зерном), твердость (латунь мягче, проще обрабатывается), стойкость в агрессивных средах (бронза лучше противостоит морской воде).

Петли из латуни литые, поэтому они намного точнее и ровнее. Стальные же штампуют из рулонной ленты, а ось загибают на станке. Просто сравните качество исполнения оси на фото выше (слева латунная петля, справа – стальная).
Чем еще плохи стальные петли? На них всегда видны стыки и швы, половинки могут не совпадать по геометрии, а зазор порой достигает 2-2,5 мм. Все это сулит проблемы при врезке и, естественно, ухудшает ход петель.
ЦАМ – хороший материал, но латунь все равно лучше. Вы поймете это по прошествии времени. За 7-10 лет ручка из ЦАМ может локально протереться, покрыться пятнами – где-то больше, где-то меньше. Для ручек же из латуни 10 лет вообще не срок, тем более если это полированная латунь (без гальванического покрытия).

Да. Применение латуни в изготовлении механизмов секретности способствует большей точности и коррозионной стойкости деталей. Если вы возьмете навесные замки или цилиндры топ-брендов (Cisa, Abus, Mottura), почти наверняка пины будут из латуни или бронзы, сердечник – из латуни или нержавеющей стали. В дешевых механизмах они могут быть из цинковых сплавов.

Вообще-то да, благодаря высокому содержанию меди. Однако это больше относится к прокатной латуни. Не забудьте, что готовые изделия покрывают лаком, а иногда – еще и гальваникой или PVD-напылением (как в элитных швейцарских часах). Логично, что с каждым таким слоем антибактерицидный эффект снижается.
Мы используем разные сплавы; в основном – с 59-61% меди. В петлях в целях снижения трения и улучшения обрабатываемости применяется освинцованная латунь (Cu 54-57,4%, Pb 2,3-2,65%).
Кроме дверной и оконной фурнитуры мы продаем латунные смесители и душевые гарнитуры Manzzaro (Россия-Италия). В них использован литейный премиум-сплав ЛЦ40С – с 59-60% меди и пониженной долей свинца: 1,0-1,6% (вместо 2,5-3,5%, как у многих популярных марок сантехники).

Это значит, что изделие из чистейшей латуни. Доли вредных примесей, таких как висмут, мышьяк и сурьма, снижены до минимально возможных. К слову: дверные и оконные петли Palladium, а также корпуса наших латунных навесных замков изготовлены из латуни класса A.
Лучше всего приобрести полировочную пасту. Если не нашли – состряпайте сами из обычных столовых ингредиентов. Вот один из способов: в равных пропорциях смешайте муку с солью. Влейте к ним уксус – столько, чтобы получилась густая пастообразная смесь. Эту смесь нанесите на марлю или любую другую мягкую ткань и протрите латунь до блеска. Естественно, перед всем этим с латуни нужно удалить старый лак, а в конце – заново пролакировать.

В классических антуражах – с древесной текстурой маслянистых тонов, шелком и парчой, мрамором, зеркалами. В современных – с бетоном, темно-синим и угольно-серым цветами, элементами стиля лофт и, опять же, с зеркалами.
«Три кубика (из мрамора, льда и латуни) имеют одинаковый объем. Какой из них имеет наибольшую массу, какой – наименьшую?»
Что это? Задача из физики? Ответ: кубик из латуни будет самым тяжелым, потому что из этих трех материалов у латуни наибольшая плотность. Самый легкий кубик – ледяной (у льда наименьшая плотность).
Также в продаже: кухонные аксессуары и сантехника премиум-класса Manzzaro – латунные смесители и стойки для душа в стилях «ретро» и «хай-тек». Всё в наличии, звоните или заказывайте нужный вам товар онлайн. Доставка по всей России (от 1 дня), в Беларусь (от 4 дней) и Казахстан (от 6 дней).
Читайте также:
