Металл 62 в таблице менделеева
Обновлено: 05.07.2024
Кликнув на любой элемент таблицы Менделеева - вы перейдете на страницу с описанием выбранного химического элемента.
Щелочно земельные металлы
Периодической системой химических элементов принято называть таблицу, в которой химические элементы классифицируются по разным свойствам, определяемым зарядом атомного ядра. Называют ее периодической таблицей Менделеева, в честь российского ученого-химика Д.И. Менделеева. Именно он в 1869 году открыл периодический закон химических элементов.
В 1869-1871 был разработан самый первый вариант таблицы, в котором определялась зависимость свойств химических элементов от атомной массы. Было выдвинуто множество предложений относительно того, как изображать свойства элементов. Это были различные геометрические фигуры, графики с аналитическими кривыми.
Но ученые приняли решение, что удобнее всего двухмерная химическая таблица, где каждый столбик указывает на физико-химические свойства определенного элемента, а в строках определяются периоды элементов, максимально близких один к другому.
Значение таблицы Менделеева для науки
Развитие химии в значительной степени обязано открытию, сделанному Менделеевым, в частности, оно способствовало развитию учения про атомы и молекулы.
Благодаря этому было получено понятное представление про простые и сложные химические соединения. Человек может понять, что такое элементы, которые используются сегодня. В ХХ веке периодическая система начала играть прогнозирующую роль, когда оцениваются химические свойства трансурановых элементов, которую показал еще сам Менделеев.
Периодическая таблица позволила систематизировать типы атомов, что имела большое значение для развития физики (атом и его ядро) в ХХ веке. Так, в начале века ученые проводили исследования, в ходе которых было установлено, что порядковый номер элемента является мерой электронного заряда его атомного ядра.
Номер же периода в таблице указывает на число электронных оболочек, которыми обладает атом. На фото было установлено, что номером вертикального ряда таблицы определяется квантовая структура внешней оболочки элемента (этим обусловлен тот факт, что химические свойства у элементов, которые находятся в одном ряду, схожи между собой).
Сделанное Менделеевым открытие положило начало новой эры в мировой науке, что позволило сделать огромный прорыв в химии и ряде других направлениях науки. Таблица Менделеева в хорошем качестве стала основой сведений про элементы, ее использование позволило делать важные выводы в науке, прогнозировать открытия.
В чем особенность периодической таблицы Менделеева?
Одним из важных свойств таблицы можно назвать то, что у группы элементов (колонка) более выражена периодическая тенденция, если сравнивать с периодами или блоками.
Также можно увидеть, что по мере того, как возрастает атомная масса, стабильно изменяются свойства. Так, к примеру, фотография таблицы дает возможность увидеть, что в блоках D и F более явно выражены горизонтальные свойства, а не вертикальные.
Группам таблицы Менделеева с лева на право присвоено номера 1-18, в соответствии с международной системой названия групп. Ранее использовались римские цифры.
Вступление в силу новой системы нотации ИЮПАК (1988 г.), которой пользуются и сегодня, привело к тому, что прежние идентификаторы групп перестали существовать.
У многих групп появились травиальные несистематические названия, к примеру, «галогены», «щелочноземельные металлы» и др.
Химические элементы из одной группы периодической таблицы Менделеева проявляют тенденции по таким параметрам:электроотрицательность, атомный радиус, энергия ионизации.
Так, картинка химической таблицы показывает, что в одной группе сверху в низ возрастает радиус атома, валентные электроны элемента удаляются от ядра по мере того, как заполняются энергетические уровни. Энергия ионизации при этом снижается, связи в атоме слабеют, в результате чего изымать электроны проще. Сверху вниз у элементов снижается электроотрицательность, что объясняется увеличением расстояния между ядром и валентными электронами. Но в таблице есть и исключения из таких закономерностей, к примеру, в 11 группе данный показатель растет сверху вниз.
Таблица
Менделеева
Таблица Менделеева, (или периодическая система химических элементов) - это таблица, которая квалифицирует химические элементы по различным свойствам, зависящим от заряда атомного ядра. Эта система выражает, в виде таблицы, периодический закон химических элементов, который в 1869 году открыл Русский ученый химик Д.И. Менделеев. Самый первый вариант таблицы, был разработан Менделеевым в 1869-1871 годах, он определял зависимость свойств химических элементов, от атомной массы (в то время это называлось атомным весом). Было предложено несколько сотен различных вариантов изображения свойств химических элементов, от аналитических кривых графиков, и до различных геометрических фигур. Но ученые, в конце концов, сошлись во мнении, что самым удобным вариантом будет изображение в виде двухмерной таблицы, в которой каждый столбик будет указывать на физико-химические свойства того или иного элемента, а периоды элементов приближенных друг к другу, будут определять строки таблицы.
Открытие, сделанное Русским химиком Менделеевым, сыграло (безусловно) наиболее важную роль в развитии науки, а именно в развитии атомно-молекулярного учения. Это открытие позволило получить наиболее понятные, и простые в изучении, представления о простых и сложных химических соединениях. Только благодаря таблице мы имеем те понятия об элементах, которыми пользуемся в современном мире. В ХХ веке проявилась прогнозирующая роль периодической системы при оценке химических свойств, трансурановых элементов, показанная еще создателем таблицы.
Разработанная в ХIХ веке, периодическая таблица Менделеева в интересах науки химии, дала готовую систематизацию типов атомов, для развития ФИЗИКИ в ХХ веке (физика атома и ядра атома). В начале ХХ века, ученые физики, путем исследований установили, что порядковый номер, (он же атомный), есть и мера электрического заряда атомного ядра этого элемента. А номер периода (т.е. горизонтального ряда), определяет число электронных оболочек атома. Так же выяснилось, что номер вертикального ряда таблицы определяет квантовую структуру внешней оболочки элемента, (этим самым, элементы одного ряда, обязаны сходством химических свойств).
Открытие Русского ученого, ознаменовало собой, новую эру в истории мировой науки, это открытие позволило не только совершить огромный скачек в химии, но так же было бесценно для ряда других направлений науки. Таблица Менделеева дала стройную систему сведений об элементах, на основе её, появилась возможность делать научные выводы, и даже предвидеть некоторые открытия.

Одна из особенностей периодической таблицы Менделеева, состоит в том, что группа (колонка в таблице), имеет более существенные выражения периодической тенденции, чем для периодов или блоков. В наше время, теория квантовой механики и атомной структуры объясняет групповую сущность элементов тем, что они имеют одинаковые электронные конфигурации валентных оболочек, и как следствие, элементы которые находятся в пределах одой колонки, располагают очень схожими, (одинаковыми), особенностями электронной конфигурации, со схожими химическими особенностями. Так же наблюдается явная тенденция стабильного изменения свойств по мере возрастания атомной массы. Надо заметить, что в некоторых областях периодической таблицы, (к примеру, в блоках D и F), сходства горизонтальные, более заметны, чем вертикальные.
Таблица Менделеева содержит группы, которым присваиваются порядковые номера от 1 до 18 (с лева, на право), согласно международной системе именования групп. В былое время, для идентификации групп, использовались римские цифры. В Америке существовала практика ставить после римской цифры, литер «А» при расположении группы в блоках S и P, или литер «В» - для групп находящихся в блоке D. Идентификаторы, применявшиеся в то время, это то же самое, что и последняя цифра современных указателей в наше время (на пример наименование IVB, соответствует элементам 4 группы в наше время, а IVA – это 14 группа элементов). В Европейских странах того времени, использовалась похожая система, но тут, литера «А» относилась к группам до 10, а литера «В» - после 10 включительно. Но группы 8,9,10 имели идентификатор VIII, как одна тройная группа. Эти названия групп закончили свое существование после того как в 1988 году вступила в силу, новая система нотации ИЮПАК, которой пользуются и сейчас.
Многие группы получили несистематические названия травиального характера, (к примеру – «щелочноземельные металлы», или «галогены», и другие подобные названия). Таких названий не получили группы с 3 по 14, из за того что они в меньшей степени схожи между собой и имеют меньшее соответствие вертикальным закономерностям, их обычно, называют либо по номеру, либо по названию первого элемента группы (титановая, кобальтовая и тому подобно).
Химические элементы относящиеся к одной группе таблицы Менделеева проявляют определенные тенденции по электроотрицательности, атомному радиусу и энергии ионизации. В одной группе, по направлению сверху вниз, радиус атома возрастает, по мере заполнения энергетических уровней, удаляются, от ядра, валентные электроны элемента, при этом снижается энергия ионизации и ослабевают связи в атоме, что упрощает изъятие электронов. Снижается, так же, электроотрицательность , это следствие того, что возрастает расстояние между ядром и валентными электронами. Но из этих закономерностей так же есть исключения, на пример электроотрицательность возрастает, вместо того чтобы убывать, в группе 11, в направлении сверху вниз. В таблице Менделеева есть строка, которая называется «Период».
Среди групп, есть и такие у которых более значимыми являются горизонтальные направления (в отличии от других, у которых большее значение имеют вертикальные направления), к таким группам относится блок F, в котором лантаноиды и актиноиды формируют две важные горизонтальные последовательности.
Элементы показывают определенные закономерности в отношении атомного радиуса, электроотрицательности, энергии ионизации, и в энергии сродства к электрону. Из-за того, что у каждого следующего элемента количество заряженных частиц возрастает, а электроны притягиваются к ядру, атомный радиус уменьшается в направлении слева направо, вместе с этим увеличивается энергия ионизации, при возрастании связи в атоме - возрастает сложность изъятия электрона. Металлам, расположенным в левой части таблицы, характерен меньший показатель энергии сродства к электрону, и соответственно, в правой части показатель энергии сродства к электрону, у не металлов, этот показатель больше, (не считая благородных газов).
Разные области периодической таблицы Менделеева, в зависимости от того на какой оболочке атома, находится последний электрон, и в виду значимости электронной оболочки, принято описывать как блоки.
В S-блок, входит две первые группы элементов, (щелочные и щелочноземельные металлы, водород и гелий).
В P-блок, входят шест последних групп, с 13 по 18 (согласно ИЮПАК, или по системе принятой в Америке - с IIIA до VIIIA), этот блок так же включает в себя все металлоиды.
Блок - D, группы с 3 по 12 (ИЮПАК, или с IIIB до IIB по-американски), в этот блок включены все переходные металлы.
Блок – F, обычно выносится за пределы периодической таблицы, и включает в себя лантаноиды и актиноиды.
Самарий - 62 элемент таблицы Менделеева
В середине прошлого века на Урале был найден черный блестящий минерал. В большинстве книг по истории науки, говорится, что этот минерал открыт русским горным инженером В.Е. Самарским.
Иное утверждают авторы популярной книги «От водорода до. » П.Р. Таубе и Е.И. Руденко: «В середине прошлого века на Алтае и Урале смотрителем горного округа был инженер В.Е. Самарский. Особыми талантами он не отличался. Однажды рабочие принесли ему найденный в Ильменских горах неизвестный минерал очень красивого бархатно-черного цвета. Присутствовавший при этом угодливый чиновник предложил назвать минерал в честь смотрителя горного округа самарскитом. «Находчивость» чиновника была одобрена, минерал «окрещен» и вошел в коллекцию. По названию минерала, в котором был открыт новый элемент, Лекок де Буабодран назвал его самарием. Так было увековечено имя инженера Самарского, ничем не заслужившего такой чести».
История, как видим, забавная и – вымышленная от начала до конца. В действительности дело обстояло так (комментарий профессора С.А. Погодина), Еще в 1816 г. Берцелиус опубликовал анализ найденного в Швеции черного минерала, содержащего иттриевую землю, пятиокись тантала, окислы вольфрама, урана и некоторых других элементов. Через 23 года немецкий минералог Густав Розе описал подобный же минерал, найденный в Ильменских горах на Урале, и назвал его уранотанталом. А еще через семь лет, в 1846 г., московский химик Р.И. Герман переименовал этот минерал в иттроильменит, так как, по его мнению, в минерале был новый элемент ильмений. Однако не прошло и года, как профессор химии Берлинского университета Генрих Розе – брат Густава Розе – доказал, что, с одной стороны, в уранотантале преобладает не тантал, а похожий на него ниобий, а с другой, – что «ильмениевая кислота» Германа всего лишь смесь пятиокиси ниобия с трехокисью вольфрама. Поэтому оба предлагавшихся прежде названия минерала он считал неприемлемыми, неправильными.
Так или иначе первая глава истории элемента самария связана с Россией. Вторая – с Францией. В 1878 г. французский химик Делафонтен выделил из самарскита окись дидима. В это время основным оружием искателей новых элементов уже был спектральный анализ. В спектре дидима, полученного из самарскита, Делафонтен обнаружил две новые голубые линии. Решив, что они принадлежат новому элементу, он сразу же дал этому элементу название «деципий» – от латинского decipio, что значит обманываю.
Лекок де Буабодран назвал новый элемент самарием, как бы лишний раз подчеркивая, что тот получен из самарскита. Произошло это в 1879 г.
Годом позже швейцарский химик Мариньяк при исследовании самарскита получил две фракции, одна из которых давала точно такой же спектр, как и элемент, открытый Лекоком де Буабодраном. Так было подтверждено открытие самария. Другая же фракция, как показал спектральный анализ, содержала новый элемент. В честь одного из первых исследователей редких земель, Юхана Гадолина, этот элемент был назван гадолинием. Деципий же вскоре «закрыли»: он оказался смесью самария с другими редкоземельными элементами, прежде всего с неодимом и празеодимом.

Элементарный самарий был получен в начале XX в., но еще несколько десятилетий элемент №62 не находил применения. Сегодня этот элемент (и его соединения) довольно важен для атомной энергетики. Самарию свойственно большое поперечное сечение захвата тепловых нейтронов – около 6500 барн. Это больше, чем у традиционных материалов регулирующих стержней атомных реакторов – бора и кадмия. Керамические материалы, в которые входит окись самария (порошок бледно-кремового цвета), стали использовать в качестве защитных материалов в реакторостроении.
В последние годы особое внимание ученых и практиков привлекло интерметаллическое соединение самария с кобальтом SmCo5, оказавшееся великолепным материалом для сильных постоянных магнитов. Кроме того, самарий вводят в состав стекол, способных люминесцировать и поглощать инфракрасные лучи.
Но не всегда самарий полезен.
В заметках о лантаноидах мы уже не раз упоминали о реакторных ядах – продуктах деления урана, которые препятствуют развитию цепной ядерной реакции и даже способны ее погасить. Физики считают, что из радиоактивных изотопов наибольшую опасность в качестве реакторного яда представляет ксенон-135, а из стабильных – изотоп самария с массовым числом 149. Сечение захвата тепловых нейтронов у самария-149 огромно – 66 тыс. барн. Лишь у двух изотопов гадолиния оно еще больше. Но в реакторе образуется больше самария, чем гадолиния. В среднем на долю самария-149 (не считая других изотопов этого элемента) приходится 1,3% всех осколков, а на долю гадолиния-155 вместе с гадолинием-157 – 0,5%.
С реакторными ядами борются разными способами. Иногда приходится даже на время останавливать реактор, чтобы распались ядра радиоактивных ядов. Но в борьбе со стабильным самарием-149 остановка реактора была бы бесполезной, даже вредной. Этот изотоп продолжал бы накапливаться и в выключенном реакторе, так как в него превращался бы другой «осколок» ядерного распада – прометий-149. Напротив, в работающем реакторе происходит как бы самоочищение: при поглощении нейтрона самарий-149 превращается в самарий-150, который поглощает замедленные нейтроны намного хуже.
Для реакторов на быстрых нейтронах самарий-149 неопасен – быстрые нейтроны его ядрами не захватываются.
И чтобы покончить с разговором об изотопах, укажем, что природный самарий состоит из семи изотопов с массовыми числами 144, 147, 148, 149, 150, 152 (самый распространенный изотоп) и 154. Самарий-147 альфа-активен, период его полураспада 1011 лет.
Но не только из-за самария-147 радиоактивен красивый минерал самарскит. В его состав наряду с редкими землями, кислородом, железом, танталом и ниобием входит уран.
Из соединений самария интерес для практики (даже сугубо научной практики) пока представляют немногие. Обычные трехвалентные соединения этого элемента мало чем отличаются от соответствующих соединений других, более доступных элементов редкоземельного ряда. Исключение составляет, пожалуй, лишь трибромид самария SmBr3 – самое легкоплавкое вещество из всех редкоземельных бромидов.
Известны и такие соединения, в которых элемент №62 проявляет валентность 2+. Это, в частности, малорастворимый в воде дифторид SmF2 и кристаллический оранжевого цвета сульфат SmSO4. Последний интересен тем, что при его растворении в разбавленных кислотах из них выделяется водород.
Таким образом, можно сделать вывод: пока для техники самарий важнее, чем все его соединения, вместе взятые. Если, конечно, не считать упоминавшееся выше соединение – сплав с кобальтом.
Торий – топливо третьего тысячелетия
Этот химический элемент признан альтернативой урану как ядерному топливу. У него много плюсов, поэтому именно на торий делают ставку стратеги, курирующие сферу энергобезопасности.

Что представляет собой
Торий как элемент представлен в таблице Менделеева под номером 90. Открывает группу актиноидов. Радиоактивен незначительно.
Это серебристо-белый мягкий блестящий металл.

По составу – три десятка изотопов. Только у одного (232) период полураспада – 13,9 млрд. лет – втрое превышает возраст Земли. Время распада остальных – часы или годы.
Почти 100% тория природного происхождения – мононуклид-232.
Международное обозначение элемента – Th, Thorium.
Как был открыт
К получению тория причастны ученые нескольких стран:
- Первые крупицы вещества получил гуру европейских химиков Йенс Берцелиус (первая треть 19 века). Образцом стал минерал с сульфатом тория в составе.
- Торий как металл выделил через полвека его коллега и соотечественник швед Ларс Нильсон.
- Радиоактивность элемента обнаружили (1898 год) полька Мария Склодовска-Кюри и немец Герберт Шмидт.
Первооткрыватель назвал вещество торием в честь верховного бога скандинавского пантеона Тора. Минерал стал торитом.
Анналы науки хранят имя человека, далекого от химии. 17-летний американец, житель Детройта, соорудил в пристройке к дому ядерный реактор. Ему удалось добыть радиоактивный элемент из сеток накаливания газовых светильников. Пресса окрестила его «радиоактивным бойскаутом», феномен – «случаем с Дэвидом Ханом».
Как представлен в природе
Торий содержат магматические породы, пегматиты, редкоземельные и другие минералы (12 наименований). Главные источники вещества – редкоземельные элементы и минерал монацит. Но отдельно не добывается, только с другими элементами.

Монацит
Вместе с ураном входит примесью в граниты.

Гранит
Тонна земной коры содержит 10,5 г тория, литр морской воды – 0,05 мкг.
Месторождения ториевых минералов есть на всех континентах.
Богатые залежи у Норвегии и Индии.
Российские ресурсы сосредоточены в основном за Уралом: Омская, Томская, Новосибирская, Мурманская области, Республика Тыва, Красноярский край, Саха-Якутия.
Физико-химические характеристики
Очищенный торий
Химический элемент торий – типичный актиноид:
- С трудом растворяется в кислотах. Легко – в царской водке (азотно-соляном кислотном концентрате).
- Устойчив к агрессивным щелочам.
- Реакция с газами, галогенами, серой, кремнием, другими элементами запускается при нагреве.
Оксид вещества не окисляется, самый тугоплавкий среди оксидов.
Металл более уязвим:
- На воздухе тускнеет, темнеет (постепенно).
- Коррозия определяется температурой: на влажном холоде замедленна, в горячей воде – молниеносна.
- Нагревшись, горит ярким белым пламенем.
Порошок легко воспламеняется, поэтому хранится притопленным в керосине.
- При минус 272°С элемент становится сверхпроводником.
Структура кристаллической решетки элемента меняется с кубической на центрированную по граням. Порог перехода – 1400°С.
| Свойства атома | |
|---|---|
| Название, символ, номер | Торий / Thorium (Th), 90 |
| Атомная масса (молярная масса) | 232,03806(2) а. е. м. (г/моль) |
| Электронная конфигурация | [Rn] 6d2 7s2 |
| Радиус атома | 180 пм |
| Химические свойства | |
| Ковалентный радиус | 165 пм |
| Радиус иона | (+4e) 102 пм |
| Электроотрицательность | 1,3 (шкала Полинга) |
| Степени окисления | 4 |
| Энергия ионизации (первый электрон) | 670,4 (6,95) кДж/моль (эВ) |
| Термодинамические свойства простого вещества | |
| Плотность (при н. у.) | 11,78 г/см³ |
| Температура плавления | 2028 K |
| Температура кипения | 5060 K |
| Уд. теплота плавления | 16,11 кДж/моль |
| Уд. теплота испарения | 513,7 кДж/моль |
| Молярная теплоёмкость | 26,23 Дж/(K·моль) |
| Молярный объём | 19,8 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | кубическая, гранецентрированая |
| Параметры решётки | 5,080 Å |
| Температура Дебая | 100,00 K |
| Прочие характеристики | |
| Теплопроводность | (300 K) (54,0) Вт/(м·К) |
| Номер CAS | 7440-29-1 |
Торий причислен к тяжелым металлам: кубик с ребром 1 см весит 11,7 грамма.
Технология получения
Процесс получения вещества несложен:
- Монацитовую руду обогащают.
- На продукт воздействуют кислотами либо щелочами.
- Извлекают «редкие земли» – экстрагируя, затем сорбируя.
- Из конгломерата металлических соединений выделяют фторид, хлорид либо диоксид тория.
Металлическую форму вещества получают методом металлотермии. Процесс проходит с участием магния, кальция или натрия при 910-990°С.
Преимущества перед ураном
Торий рассматривают как альтернативу урана.

Тяжёлый серебристо-белый глянцеватый металл – уран
У элемента ряд преимуществ:
- Запасы втрое – вчетверо больше.
- Процесс безопаснее. Реактор, работающий на тории, лишен избыточной реактивности. Аварии типа Чернобыля или Фукусимы исключены.
- Новые порции топлива загружаются каждые 10 лет (а не полтора года, как у урана).
Нуклид-232 не делится. Но, прихватив нейтрон, превращается в уран-233 с делимым ядром. То есть в реакторе торий «оборачивается» топливом, пригодным для получения энергии. Реально отладить цикличность, при которой урана-233 на выходе получится больше, чем на входе.
Этим плотно занимаются США, Китай, Норвегия, Индия. Для России значение ториевой энергетики возрастает в связи с освоением Арктики.
Стоимость металла не превышает $100 за кг.
Где используется
Металл легко обрабатывать: он мягкий, ковкий, вязкий.

Металлический торий
Несмотря на слабую радиоактивность, нашел применение как мирный атом и компонент продуктов других сфер.
Атомная промышленность
Главная сфера применения вещества – атомный сектор.
Облученный в реакторе ториевый изотоп-232, через цепочку реакций, превращается в уран-233. Он легче традиционных урана-235 и плутония, но работает не хуже.
Глобальные запасы тория втрое – вчетверо превышают урановый «резерв». Энергетика на его основе решит проблему безопасного использования атома.
Другие сферы
Металлический торий приносит пользу другим отраслям промышленности:
- Металлургия. Это лигатура, улучшающая параметры сплавов (повышение порога на разрыв, жаропрочность). Оксид вещества – печной элемент-резистор. Емкости из окиси тория применяются для работ при 2550-3150°C.
- Авиастроение. Окись тория – упрочняющий элемент композитов.
- Гидроэлектростанции. Оксид вещества используется для узлов и конструкций, функционирующих в экстремальных условиях. Им выкладывают изнутри камеры сгорания и газодинамические каналы.
- Синтез. Соединения, чистое вешество – составляющая катализаторов.
Катодами с веществом, оксидом снабжены источники света: магнетроны, электронные, ксеноновые дуговые, генераторные.
Один процент оксида тория «обездвиживает» структуру вольфрамовых нитей ламп накаливания.
Влияние на живые организмы
Малотоксичный торий присутствует в растениях, организме человека и животных.
Им богаты морская флора и фауна.
Человек получает ежесуточно 3 мкг вещества с пищей и водой. Они выводятся естественным путем.
«Накопители» вещества – селезенка, печень, лимфоузлы, костный мозг, надпочечники.
Негативное влияние на человека возможно при контакте с веществом.
Ограничения
Радиоактивность элемента незначительна, однако при долгом воздействии срабатывает «накопительный» эффект. Что представляет опасность для человека.
Поэтому гранит, используемый как строительный либо декоративный материал, проверяют. Материал с некоторых месторождений использовать запрещено.
ПЕРИОДИЧЕСКАЯ ТАБЛИЦА МЕНДЕЛЕЕВА
Еще в школе, сидя на уроках химии, все мы помним таблицу на стене класса или химической лаборатории. Эта таблица содержала классификацию всех известных человечеству химических элементов, тех фундаментальных компонентов, из которых состоит Земля и вся Вселенная. Тогда мы и подумать не могли, что таблица Менделеева бесспорно является одним из величайших научных открытий, который является фундаментом нашего современного знания о химии.
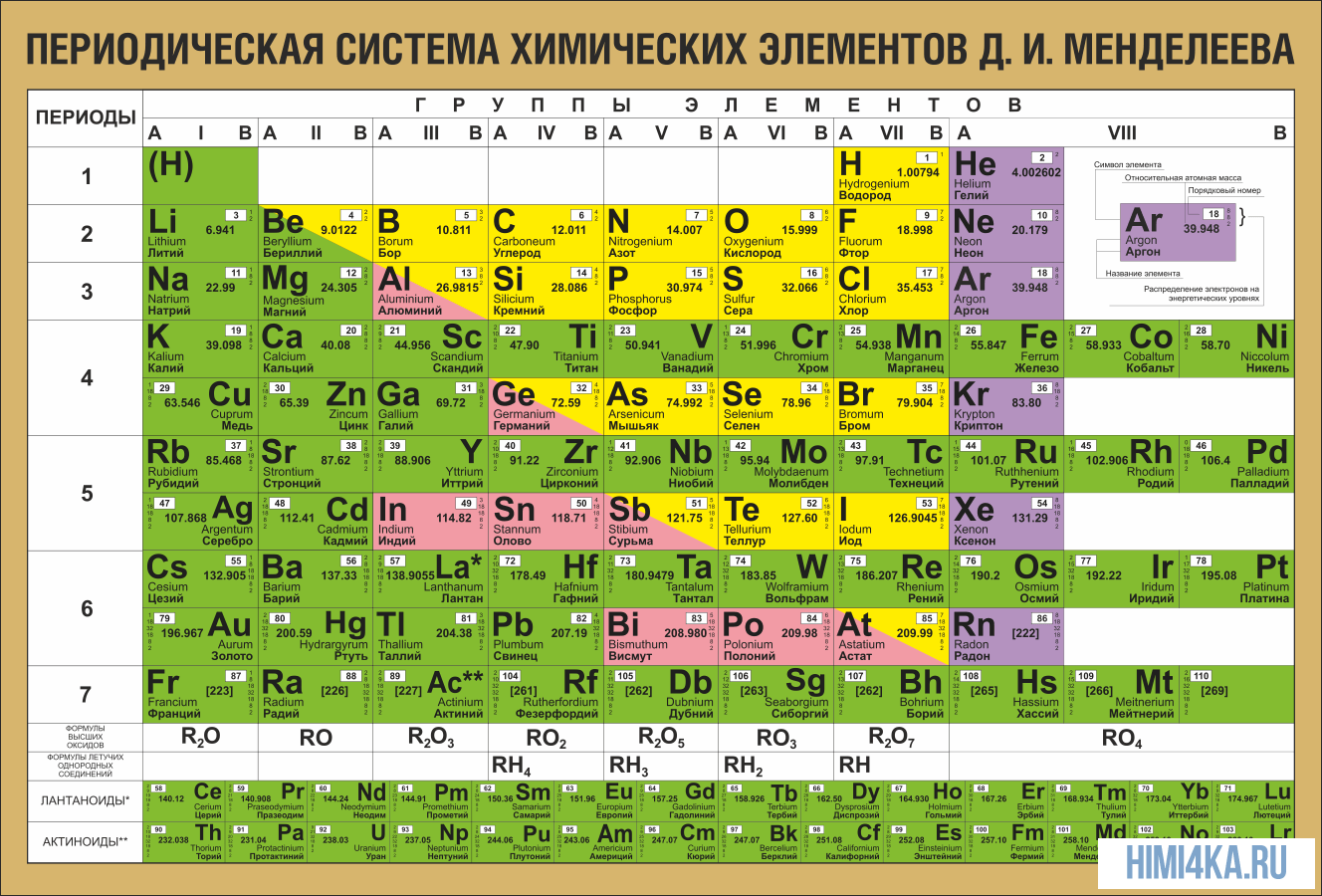
На первый взгляд, ее идея выглядит обманчиво просто: организовать химические элементы в порядке возрастания веса их атомов. Причем в большинстве случаев оказывается, что химические и физические свойства каждого элемента сходны с предыдущим ему в таблице элементом. Эта закономерность проявляется для всех элементов, кроме нескольких самых первых, просто потому что они не имеют перед собой элементов, сходных с ними по атомному весу. Именно благодаря открытию такого свойства мы можем поместить линейную последовательность элементов в таблицу, очень напоминающую настенный календарь, и таким образом объединить огромное количество видов химических элементов в четкой и связной форме. Разумеется, сегодня мы пользуемся понятием атомного числа (количества протонов) для того, чтобы упорядочить систему элементов. Это помогло решить так называемую техническую проблему «пары перестановок», однако не привело к кардинальному изменению вида периодической таблицы.
В периодической таблице Менделеева все элементы упорядочены с учетом их атомного числа, электронной конфигурации и повторяющихся химических свойств. Ряды в таблице называются периодами, а столбцы группами. В первой таблице, датируемой 1869 годом, содержалось всего 60 элементов, теперь же таблицу пришлось увеличить, чтобы поместить 118 элементов, известных нам сегодня.
Периодическая система Менделеева систематизирует не только элементы, но и самые разнообразные их свойства. Химику часто бывает достаточно иметь перед глазами Периодическую таблицу для того, чтобы правильно ответить на множество вопросов (не только экзаменационных, но и научных).
The YouTube ID of 1M7iKKVnPJE is invalid.
Периодический закон
Существуют две формулировки периодического закона химических элементов: классическая и современная.
Классическая, в изложении его первооткрывателя Д.И. Менделеева: свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величин атомных весов элементов.
Современная: свойства простых веществ, а также свойства и формы соединений элементов находятся в периодической зависимости от заряда ядра атомов элементов (порядкового номера).
Графическим изображением периодического закона является периодическая система элементов, которая представляет собой естественную классификацию химических элементов, основанную на закономерных изменениях свойств элементов от зарядов их атомов. Наиболее распространёнными изображениями периодической системы элементов Д.И. Менделеева являются короткая и длинная формы.

Группы и периоды Периодической системы
Группами называют вертикальные ряды в периодической системе. В группах элементы объединены по признаку высшей степени окисления в оксидах. Каждая группа состоит из главной и побочной подгрупп. Главные подгруппы включают в себя элементы малых периодов и одинаковые с ним по свойствам элементы больших периодов. Побочные подгруппы состоят только из элементов больших периодов. Химические свойства элементов главных и побочных подгрупп значительно различаются.
Периодом называют горизонтальный ряд элементов, расположенных в порядке возрастания порядковых (атомных) номеров. В периодической системе имеются семь периодов: первый, второй и третий периоды называют малыми, в них содержится соответственно 2, 8 и 8 элементов; остальные периоды называют большими: в четвёртом и пятом периодах расположены по 18 элементов, в шестом — 32, а в седьмом (пока незавершенном) — 31 элемент. Каждый период, кроме первого, начинается щелочным металлом, а заканчивается благородным газом.
Физический смысл порядкового номера химического элемента: число протонов в атомном ядре и число электронов, вращающихся вокруг атомного ядра, равны порядковому номеру элемента.

Свойства таблицы Менделеева
Напомним, что группами называют вертикальные ряды в периодической системе и химические свойства элементов главных и побочных подгрупп значительно различаются.
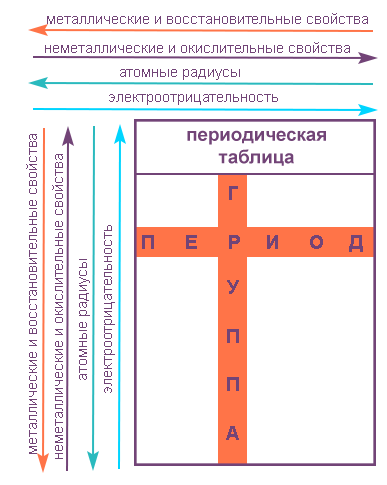
Свойства элементов в подгруппах закономерно изменяются сверху вниз:
- усиливаются металлические свойства и ослабевают неметаллические;
- возрастает атомный радиус;
- возрастает сила образованных элементом оснований и бескислородных кислот;
- электроотрицательность падает.
Все элементы, кроме гелия, неона и аргона, образуют кислородные соединения, существует всего восемь форм кислородных соединений. В периодической системе их часто изображают общими формулами, расположенными под каждой группой в порядке возрастания степени окисления элементов: R2O, RO, R2O3, RO2, R2O5, RO3, R2O7, RO4, где символом R обозначают элемент данной группы. Формулы высших оксидов относятся ко всем элементам группы, кроме исключительных случаев, когда элементы не проявляют степени окисления, равной номеру группы (например, фтор).
Оксиды состава R2O проявляют сильные основные свойства, причём их основность возрастает с увеличением порядкового номера, оксиды состава RO (за исключением BeO) проявляют основные свойства. Оксиды состава RO2, R2O5, RO3, R2O7 проявляют кислотные свойства, причём их кислотность возрастает с увеличением порядкового номера.
Элементы главных подгрупп, начиная с IV группы, образуют газообразные водородные соединения. Существуют четыре формы таких соединений. Их располагают под элементами главных подгрупп и изображают общими формулами в последовательности RH4, RH3, RH2, RH.
Соединения RH4 имеют нейтральный характер; RH3 — слабоосновный; RH2 — слабокислый; RH — сильнокислый характер.
Напомним, что периодом называют горизонтальный ряд элементов, расположенных в порядке возрастания порядковых (атомных) номеров.
В пределах периода с увеличением порядкового номера элемента:
- электроотрицательность возрастает;
- металлические свойства убывают, неметаллические возрастают;
- атомный радиус падает.
Элементы таблицы Менделеева
Щелочные и щелочноземельные элементы
К ним относятся элементы из первой и второй группы периодической таблицы. Щелочные металлы из первой группы — мягкие металлы, серебристого цвета, хорошо режутся ножом. Все они обладают одним-единственным электроном на внешней оболочке и прекрасно вступают в реакцию. Щелочноземельные металлы из второй группы также имеют серебристый оттенок. На внешнем уровне помещено по два электрона, и, соответственно, эти металлы менее охотно взаимодействуют с другими элементами. По сравнению со щелочными металлами, щелочноземельные металлы плавятся и кипят при более высоких температурах.
| Щелочные металлы | Щелочноземельные металлы |
| Литий Li 3 | Бериллий Be 4 |
| Натрий Na 11 | Магний Mg 12 |
| Калий K 19 | Кальций Ca 20 |
| Рубидий Rb 37 | Стронций Sr 38 |
| Цезий Cs 55 | Барий Ba 56 |
| Франций Fr 87 | Радий Ra 88 |
Лантаниды (редкоземельные элементы) и актиниды
Лантаниды — это группа элементов, изначально обнаруженных в редко встречающихся минералах; отсюда их название «редкоземельные» элементы. Впоследствии выяснилось, что данные элементы не столь редки, как думали вначале, и поэтому редкоземельным элементам было присвоено название лантаниды. Лантаниды и актиниды занимают два блока, которые расположены под основной таблицей элементов. Обе группы включают в себя металлы; все лантаниды (за исключением прометия) нерадиоактивны; актиниды, напротив, радиоактивны.
| Лантаниды | Актиниды |
| Лантан La 57 | Актиний Ac 89 |
| Церий Ce 58 | Торий Th 90 |
| Празеодимий Pr 59 | Протактиний Pa 91 |
| Неодимий Nd 60 | Уран U 92 |
| Прометий Pm 61 | Нептуний Np 93 |
| Самарий Sm 62 | Плутоний Pu 94 |
| Европий Eu 63 | Америций Am 95 |
| Гадолиний Gd 64 | Кюрий Cm 96 |
| Тербий Tb 65 | Берклий Bk 97 |
| Диспрозий Dy 66 | Калифорний Cf 98 |
| Гольмий Ho 67 | Эйнштейний Es 99 |
| Эрбий Er 68 | Фермий Fm 100 |
| Тулий Tm 69 | Менделевий Md 101 |
| Иттербий Yb 70 | Нобелий No 102 |
Галогены и благородные газы
Галогены и благородные газы объединены в группы 17 и 18 периодической таблицы. Галогены представляют собой неметаллические элементы, все они имеют семь электронов во внешней оболочке. В благородных газахвсе электроны находятся во внешней оболочке, таким образом с трудом участвуют в образовании соединений. Эти газы называют «благородными, потому что они редко вступают в реакцию с прочими элементами; т. е. ссылаются на представителей благородной касты, которые традиционно сторонились других людей в обществе.
| Галогены | Благородные газы |
| Фтор F 9 | Гелий He 2 |
| Хлор Cl 17 | Неон Ne 10 |
| Бром Br 35 | Аргон Ar 18 |
| Йод I 53 | Криптон Kr 36 |
| Астат At 85 | Ксенон Xe 54 |
| — | Радон Rn 86 |
Переходные металлы
Переходные металлы занимают группы 3—12 в периодической таблице. Большинство из них плотные, твердые, с хорошей электро- и теплопроводностью. Их валентные электроны (при помощи которых они соединяются с другими элементами) находятся в нескольких электронных оболочках.
| Переходные металлы |
| Скандий Sc 21 |
| Титан Ti 22 |
| Ванадий V 23 |
| Хром Cr 24 |
| Марганец Mn 25 |
| Железо Fe 26 |
| Кобальт Co 27 |
| Никель Ni 28 |
| Медь Cu 29 |
| Цинк Zn 30 |
| Иттрий Y 39 |
| Цирконий Zr 40 |
| Ниобий Nb 41 |
| Молибден Mo 42 |
| Технеций Tc 43 |
| Рутений Ru 44 |
| Родий Rh 45 |
| Палладий Pd 46 |
| Серебро Ag 47 |
| Кадмий Cd 48 |
| Лютеций Lu 71 |
| Гафний Hf 72 |
| Тантал Ta 73 |
| Вольфрам W 74 |
| Рений Re 75 |
| Осмий Os 76 |
| Иридий Ir 77 |
| Платина Pt 78 |
| Золото Au 79 |
| Ртуть Hg 80 |
| Лоуренсий Lr 103 |
| Резерфордий Rf 104 |
| Дубний Db 105 |
| Сиборгий Sg 106 |
| Борий Bh 107 |
| Хассий Hs 108 |
| Мейтнерий Mt 109 |
| Дармштадтий Ds 110 |
| Рентгений Rg 111 |
| Коперниций Cn 112 |
Металлоиды
Металлоиды занимают группы 13—16 периодической таблицы. Такие металлоиды, как бор, германий и кремний, являются полупроводниками и используются для изготовления компьютерных чипов и плат.
| Металлоиды |
| Бор B 5 |
| Кремний Si 14 |
| Германий Ge 32 |
| Мышьяк As 33 |
| Сурьма Sb 51 |
| Теллур Te 52 |
| Полоний Po 84 |
Постпереходными металлами
Элементы, называемые постпереходными металлами, относятся к группам 13—15 периодической таблицы. В отличие от металлов, они не имеют блеска, а имеют матовую окраску. В сравнении с переходными металлами постпереходные металлы более мягкие, имеют более низкую температуру плавления и кипения, более высокую электроотрицательность. Их валентные электроны, с помощью которых они присоединяют другие элементы, располагаются только на внешней электронной оболочке. Элементы группы постпереходных металлов имеют гораздо более высокую температуру кипения, чем металлоиды.
| Постпереходные металлы |
| Алюминий Al 13 |
| Галлий Ga 31 |
| Индий In 49 |
| Олово Sn 50 |
| Таллий Tl 81 |
| Свинец Pb 82 |
| Висмут Bi 83 |
Неметаллы
Из всех элементов, классифицируемых как неметаллы, водород относится к 1-й группе периодической таблицы, а остальные — к группам 13—18. Неметаллы не являются хорошими проводниками тепла и электричества. Обычно при комнатной температуре они пребывают в газообразном (водород или кислород) или твердом состоянии (углерод).
| Неметаллы |
| Водород H 1 |
| Углерод C 6 |
| Азот N 7 |
| Кислород O 8 |
| Фосфор P 15 |
| Сера S 16 |
| Селен Se 34 |
| Флеровий Fl 114 |
| Унунсептий Uus 117 |
А теперь закрепите полученные знания, посмотрев видео про таблицу Менделеева и не только.
Отлично, первый шаг на пути к знаниям сделан. Теперь вы более-менее ориентируетесь в таблице Менделеева и это вам очень даже пригодится, ведь Периодическая система Менделеева является фундаментом, на котором стоит эта удивительная наука.
Читайте также:
