Металлический натрий формула химия
Обновлено: 28.04.2024
НА́ТРИЙ -я; м. Химический элемент (Na), мягкий металл серебристо-белого цвета, быстро окисляющийся на воздухе.
(лат. Natrium), химический элемент I группы периодической системы; относится к щелочным металлам. Название (от арабского натрун) первоначально относилось к природной соде. Серебристо-белый металл, мягкий, лёгкий (плотность 0,968 г/см 3 ), легкоплавкий (tпл 97,86°C). На воздухе быстро окисляется. Взаимодействие с водой может сопровождаться взрывом. Занимает 6-е место по распространённости в земной коре (минералы галит, мирабилит и др.) и 1-е среди металлических элементов в Мировом океане. Применяют для получения чистых металлов (K, Zr, Та и др.), как теплоноситель в ядерных реакторах (сплав с калием) и источник свечения в натриевых лампах. Натрий участвует в минеральном обмене всех живых организмов.НА́ТРИЙ (лат. Natrium, от арабского натрун, греческого nitron — природная сода), Na (читается «натрий»), химический элемент с атомным номером 11, атомной массой 22,98977. В природе встречается один стабильный изотоп 23 Na. Принадлежит к числу щелочных металлов. Расположен в третьем периоде в группе IА в периодической системе элементов. Конфигурация внешнего электронного слоя 3s 1 . Степень окисления +1 (валентность I).
Рaдиус атома 0,192 нм, радиус иона Na + 0,116 нм (координационное число 6). Энергии последовательной ионизации 5,139 и 47,304 эВ. Электроотрицательность по Полингу (см. ПОЛИНГ Лайнус) 1,00.
Историческая справка
Поваренная соль (хлорид натрия NaCl), едкая щелочь (гидроксид натрия NaOH) и сода (карбонат натрия Na2CO3) находили применение еще в Древней Греции.
Металлический Na впервые получил в 1807 Г. Дэви (см. ДЭВИ Гемфри) , используя электролиз расплава каустической соды.
Нахождение в природе
Содержание в земной коре 2,64% по массе. Основные минералы: галит (см. ГАЛИТ) NaCl, мирабилит (см. МИРАБИЛИТ) Na2SO4·10H2O, тенардит (см. ТЕНАРДИТ) Na 2SO 4 , чилийская селитра NaNO3 ,трона (см. ТРОНА) NaHCO3·Na2CO 3·2H2O, бура (см. БУРА) Na2B4O7·10H2O и природные силикаты, например, нефелин (см. НЕФЕЛИН) Na[AlSiO4].
В воде Мирового океана содержится 1,5·10 16 т солей натрия.
Получение
Na получают электролизом расплава хлорида натрия NaCl, с добавлением NаСl2, КСl и NaF для снижения температуры плавления электролита до 600°C. Аноды изготовлены из графита, катоды — из меди или железа. Электролиз расплава проводят в стальном электролизере с диафрагмой. Параллельно с Na электролизом получают Cl2:
2NaCl=2Na+Cl2
Получаемый Na очищают вакуумной дистилляцией или обработкой титаном или сплавом титана и циркония.
Физические и химические свойства
Натрий — мягкий серебристо-белый металл, быстро тускнеющий на воздухе.
Na мягок, легко режется ножом, поддается прессованию и прокатке. Выше -222°C устойчива кубическая модификация, а = 0,4291 нм. Ниже — гексагональная модификация. Плотность 0,96842 кг/дм 3 . Тaмпература плавления 97,86°C, кипения 883,15°C. Пары натрия состоят из Na и Na2.
Na химически очень активен. При комнатной температуре взаимодействует с O2 воздуха, парами воды и CO2 с образованием рыхлой корки. При сгорании Na в кислороде образуются пероксид Na2О2 и оксид Na2O:
4Na+O2=2Na2O и 2Na+O2=Na2O2
При нагревании на воздухе Na сгорает желтым пламенем, в желтый цвет окрашивают пламя и многие соли натрия. Натрий бурно реагирует с водой и разбавленными кислотами:
2Na+H2O=2NaOH+H2
При взаимодействии Na и спирта выделяется H2 и образуется алкоголят натрия. Например, взаимодействуя с этанолом С2Н5ОН, Na образует этанолят натрия С2Н5ОNa:
С2Н5ОН+2Na=2С2Н5ОNa+H2
Кислородсодержащие кислоты, взаимодействуя с Na, восстанавливаются:
2Na+2Н2SO4=SO2+Na2SO4+2H2O
При нагревании до 200°C Na реагирует с H2 с образованием гидрида NaН:
2Na+H2=2NaH
Натрий самовоспламеняется в атмосфере фтора (см. ФТОР) или хлора (см. ХЛОР) , с иодом (см. ИОД) реагирует при нагревании. При перетирании в ступке Na реагирует с S с образованием сульфидов переменного состава. С N2 реакция протекает в электрическом разряде, образуются нитрид натрия Nа3N или азид NaN3. Na реагирует с жидким аммиаком с образованием голубых растворов, где Na присутствует в виде ионов Na + .
Оксид натрия Na2O проявляет ярко выраженные основные свойства, легко реагирует с водой с образованием сильного основания — гидроксида натрия NaОН:
Na2O+H2O=2NaOH
Пероксид натрия Na2O2 реагирует с водой с выделением кислорода:
2Na2O2+2H2O=4NaOH+O2
Гидроксид натрия — очень сильное основание, щелочь, (см. ЩЕЛОЧИ) хорошо растворим в воде (в 100 г воды при 20 °C растворяется 108 г NaOH). NaОН взаимодействует с кислотными и амфотерными (см. АМФОТЕРНОСТЬ) оксидами:
CO2+2NaOH=Na2CO3+H2O,
Al2O3+2NaOH+3H2O=2Na[Al(OH)4] (в растворе),
Al2O3+2NaOH=2NaAlO2+H2O (при сплавлении)
В промышленности гидроксид натрия NaOH получают электролизом водных растворов NaCl или Na2CO3 c применением ионообменных мембран и диафрагм:
2NaCl+2H2O=2NaOH+Cl2+H2
Попадание твердого NaOH или капель его раствора на кожу вызывает тяжелые ожоги. Водные растворы NaOH при хранении разрушают стекло, расплавы — фарфор.
Карбонат натрия Na2CO3 получают насыщением водного раствора NaCl аммиаком и CO2. Рaстворимость образующегося гидрокарбоната натрия NaHCO3 менее 10 г в 100 г воды при 20°C, основная часть NaHCO3 выпадает в осадок:
NaCl+NH3+CO2=NaHCO3 ,
который отделяют фильтрованием. При прокаливании NaHCO3 образуется кальцинированная сода:
2NaHCO3=Na2CO3+CO2+H2O
У большинства солей Na растворимость с ростом температуры возрастает не так сильно, у солей калия (см. КАЛИЙ) .
Na — сильный восстановитель:
TiCl4+4Na=4NaCl+Ti
Применение
Нaтрий применяется как восстановитель активных металлов, его расплав в смеси с калием является теплоносителем в ядерных реакторах, так как он плохо поглощает нейтроны. Пaры Na используются в лампах накаливания.
NaCl используется в пищевой промышленности, гидроксид натрия NaOH — в производстве бумаги, мыла, искусственных волокон, в качестве электролита. Кaрбонат натрия Na2CO3 и гидрокарбонат NaНСO3 — применяется в пищевой промышленности, является компонентом огнетушащих средств, лекарством. Фосфат натрия Na3PO4 — компонент моющих средств, применяют в производстве стекол и красок, в пищевой промышленности, в фотографии. Силикаты mNa2O·nSiO2 — компоненты шихты в производстве стекла, для получения алюмосиликатных катализаторов, жаростойких, кислотоупорных бетонов.
Физиологическая роль
Ионы натрия Na + необходимы для нормального функционирования организма, они участвуют в процессах обмена веществ. В плазме крови человека содержание ионов Na + 0,32% по массе, в костях — 0,6%, В мышечных тканях — 1,5%. Для восполнения естественной убыли человек должен ежедневно употреблять с пищей 4—5 г Na.
Особенности обращения с металлическим натрием
Хранят натрий в герметично закрытых железных контейнерах под слоем обезвоженного керосина или минерального масла. Загоревшийся Na заливают минеральным маслом или засыпают смесью талька и NaCl. Образующиеся отходы металлического Na уничтожают в емкостях с этиловым или пропиловым спиртом.
Энциклопедический словарь . 2009 .
Полезное
Смотреть что такое "натрий" в других словарях:
НАТРИЙ — НАТРИЙ. Natrium, химич. элемент, симв. Na, серебристобелый, блестящий, при обыкновенной t° восковой плотности одноатомный металл, делающийся хрупким на холоду и при ярко краснокалильном жаре перегоняющийся; открыт Де.ви (1807) электролизом… … Большая медицинская энциклопедия
НАТРИЙ — (греч. nitron, лат. natrum). Металл белого цвета, составляющий часть поваренной соли, соды, селитры и др. Словарь иностранных слов, вошедших в состав русского языка. Чудинов А.Н., 1910. НАТРИЙ белый блестящий мягкий металл, быстро окисляющийся в… … Словарь иностранных слов русского языка
Натрий-22 — Схема распада натрия 22 … Википедия
НАТРИЙ — (Natrium), Na, химический элемент I группы периодической системы, атомный номер 11, атомная масса 22,98977; мягкий щелочной металл, tпл 97,86шC. Натрий и его сплавы с калием теплоносители в ядерных реакторах. Натрий компонент сплавов для… … Современная энциклопедия
НАТРИЙ — (символ Na), распространенный серебристо белый металлический элемент, один из ЩЕЛОЧНЫХ МЕТАЛЛОВ, впервые выделенный Хэмфри Дэви (1807). Он встречается в составе солей в морской воде и во многих минералах. Главным источником его является ХЛОРИД… … Научно-технический энциклопедический словарь
Натрий — (Natrium), Na, химический элемент I группы периодической системы, атомный номер 11, атомная масса 22,98977; мягкий щелочной металл, tпл 97,86°C. Натрий и его сплавы с калием – теплоносители в ядерных реакторах. Натрий – компонент сплавов для… … Иллюстрированный энциклопедический словарь
НАТРИЙ — (лат. Natrium) Na, химический элемент I группы периодической системы Менделеева, атомный номер 11, атомная масса 22,98977; относится к щелочным металлам. Название (от араб. натрун) первоначально относилось к природной соде. Серебристо белый… … Большой Энциклопедический словарь
Натрий — Na (лат. Natrium, от араб. натрун, греч. nitron, первоначально природная сода * a. sodium, natrium; н. Natrium; ф. sodium; и. sodio), хим. элемент I группы периодич. системы Менделеева; ат.н. 11, ат. м. 22,98977; относится к щелочным… … Геологическая энциклопедия
Натрий — Na химический элемент I группы периодической системы, атомный номер 11, атомная масса 22,99; щелочной металл; благодаря высокой теплопроводности и сравнительно малому сечению захвата медленных нейтронов металлический натрий (иногда в сплаве с… … Термины атомной энергетики
НАТРИЙ — хим. элемент, символ Na (лат. Natrium), ат. н. 11, ат. м. 22,98; относится к щелочным металлам, серебристо белого цвета, плотность 968 кг/м3, t = 97,83°С, очень мягкий, обладает высокими тепло и электропроводностью. Н. легко взаимодействует со… … Большая политехническая энциклопедия
НАТРИЙ — НАТРИЙ, натрия, мн. нет, муж. (лат. natrium) (хим.). Мягкий и белый легкий щелочной металл. Поваренная соль представляет собой химическое соединение хлора с натрием. Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова
Формула металлического натрия
В обычных условиях натрий представляет собой серебристо-белый (в тонком слое — с фиолетовым оттенком), легкий, очень мягкий, низкоплавкий металл (относится к группе щелочных металлов) (рис. 1).
Пар натрия имеет темно-красный цвет и состоит из атомов Na (преобладают) и молекул Na2.
Весьма реакционноспособный; на воздухе покрывается оксидной пленкой (тускнеет), воспламеняется приумеренном нагревании. Устойчив в атмосфере аргона и азота. Сильный восстановитель; энергично реагирует с водой, кислотами, неметаллами.
Хорошо сохраняется под слоем бензина или керосина, легко суспендируется в кипящих инертных растворителях (толуол, ксилол, гептан, октан и др.). В инертной атмосфере расплавленный натрий быстро распределяется по поверхности некоторых твердых веществ (NaCl, Na2СО3, уголь, железо, Аl2О3, ZrO2), образуя серо-черные моноатомные покрытия. Окрашивает пламя газовой горелки в желтый цвет.

Рис. 1. Металлический натрий. Внешний вид.
Химическая формула металлического натрия
Химическое обозначение натрия – Na от латинского слова «natrium». Этот химический элемент расположен в третьем периоде в IА группе Периодической таблицы Д.И. Менделеева. Относится к элементамs-семейства. Металл. Относительная атомная масса натрия равна 22,9898 а.е.м.
Электронная формула металлического натрия
В ядре атома натрия содержится 11 протонов и 12 нейтронов (массовое число равно 23). В атоме натрия есть три энергетических уровня, на которых находятся 11 электронов (рис. 2).
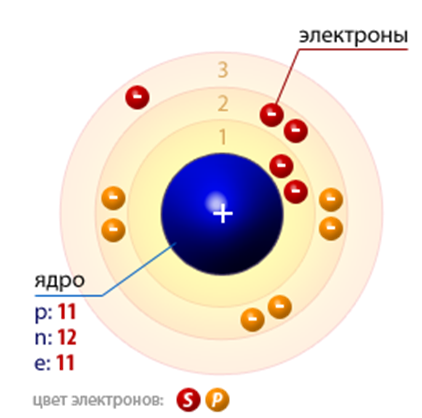
Рис. 2. Строение атома натрия.
Электронная формула атома натрия в основном состоянии имеет следующий вид:
Примеры решения задач
| Задание | Определите молекулярную формулу кальциевой селитры, в которой массовые отношения кальция, азота и кислорода равны 10:7:24. Относительная молекулярная масса кальциевой селитры 164. |
| Решение | Для того, чтобы узнать, в каких отношениях находятся химические элементы в составе молекулы необходимо найти их количество вещества. Известно, что для нахождения количества вещества следует использовать формулу: |
Найдем молярные массы кальция, азота и кислорода (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел). Известно, что M = Mr, значит M(Ca)= 40 г/моль, Ar(N)=14 г/моль, а М(O) = 32 г/моль.
Тогда, количество вещества этих элементов равно:
n (Ca) = m (Ca) / M (Ca);
n (Ca) = 10 / 40 = 0,25 моль.
n (N) = 7 / 14 = 0, 5 моль.
n (O) = 24 / 16 = 1,5 моль.
Найдем мольное отношение:
n(Ca) :n(N):n(O) = 0,25 : 0,5 : 1,5= 1 : 2 : 6,
т.е. простейшая формула соединения кальция, азота и кислорода имеет вид CaN2O6 и молярную массу 164 г/моль [M(CaN2O6) = Ar(Ca) + 2×Ar(N) + 6×Ar(O) = 40 + 2×14 + 6×16 = 40 + 28 + 96 = 164 г/моль]
Чтобы найти истинную формулу органического соединения найдем отношение полученных молярных масс:
Значит формула соединения кальция, азота и кислорода имеет вид CaN2O6или Ca(NO3)2. Это нитрат кальция.
| Задание | Установите массовую формулу вещества, содержащего 55,2% калия, 14,6% фосфора и 30,2% кислорода. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле: |
ω (Х) = n × Ar (X) / M (HX) × 100%.
Обозначим количество моль элементов, входящих в состав соединения за «х» (калий), «у» (фосфор) и «z» (кислород). Тогда, мольное отношение будет выглядеть следующим образом (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел):
x:y:z = ω(K)/Ar(K) : ω(P)/Ar(P) : ω(O)/Ar(O);
x:y:z= 55,2/39 : 14,6/31 : 30,2/16;
x:y:z= 1,4 : 0,5: 1,9 = 3 : 1: 4.
Значит формула соединения калия, фосфора и кислорода будет иметь вид K3PO4. Это фосфат калия.
Натрий

Натрий (Na, лат. natrium ) — химический элемент первой группы, третьего периода периодической системы Менделеева, с атомным номером 11. Как простое вещество представляет собой мягкий щелочной металл серебристо-белого цвета. На внешнем энергетическом уровне натрий имеет один электрон, который он легко отдаёт, превращаясь в положительно заряженный катион Na + . Единственным стабильным изотопом является 23 Na. В свободном виде не встречается, но может быть получен из различных соединений. Натрий — шестой по распространённости элемент в земной коре: он находится в составе многочисленных минералов, включая полевые шпаты, содалит и «каменную соль» (галит, хлорид натрия).
Содержание
- 1 История и происхождение названия
- 2 Нахождение в природе
- 3 Получение
- 4 Физические свойства
- 5 Химические свойства
- 6 Применение
- 7 Изотопы натрия
- 8 Биологическая роль
- 9 Меры предосторожности

История и происхождение названия
Соединения натрия известны и использовались с давних времён. В древнегреческом переводе Библии — Септуагинте — упоминается слово νίτρον (в латинском переводе — Вульгате — ему соответствует слово nitroet ) как название вещества типа соды или поташа, которое в смеси с маслом служило моющим средством(Иер. 2:22). В Танахе слову νίτρον соответствуют др.-евр. ברית — «мыло» и נתר — «щёлок»(мыльная жидкость). Сода (натрон) встречается в природе в водах натронных озёр в Египте. Природную соду древние египтяне использовали для бальзамирования, отбеливания холста, при варке пищи, изготовлении красок и глазурей. Плиний Старший пишет, что в дельте Нила соду (в ней была достаточная доля примесей) выделяли из речной воды. Она поступала в продажу в виде крупных кусков, из-за примеси угля окрашенных в серый или даже чёрный цвет.
Название «натрий» происходит от латинского слова natrium (ср. др.-греч. νίτρον ), которое было заимствовано из среднеегипетского языка (nṯr), где оно означало среди прочего: «сода», «едкий натр».
Аббревиатура «Na» и слово natrium были впервые использованы академиком, основателем шведского общества врачей Йенсом Якобсом Берцелиусом (Jöns Jakob Berzelius, 1779—1848) для обозначения природных минеральных солей, в состав которых входила сода. Ранее (а также до сих пор в английском, французском и ряде других языков) элемент именовался содий (лат. sodium ) — это название sodium, возможно, восходит к арабскому слову suda, означающему «головная боль», так как сода применялась в то время в качестве лекарства от головной боли.
Металлический натрий впервые был получен английским химиком Хемфри Дэви электролизом расплава гидроксида натрия. Дэви сообщил об этом 19 ноября 1807 года в Бейкеровской лекции (в рукописи лекции Дэви указал, что он открыл калий 6 октября 1807 года, а натрий — через несколько дней после калия).
Нахождение в природе
Кларк натрия в земной коре 25 кг/т. Содержание в морской воде в виде соединений — 10,5 г/л . Металлический натрий встречается как примесь, окрашивающая каменную соль в синий цвет. Данную окраску соль приобретает под действием радиации.
Получение

Промышленное получение натрия по способу Девилля, распространённое в 19 веке. AC — железная трубка со смесью соды, угля и мела; B — холодильник Донни и Мареска; R — приёмник с нефтью
Первым промышленным способом получения натрия была реакция восстановления карбоната натрия углем при нагревании тесной смеси этих веществ в железной ёмкости до 1000 °C (способ Девилля):
Na2CO3 + 2C → 1000oC 2Na + 3CO
Вместо угля могут быть использованы карбид кальция, алюминий, кремний, ферросилиций, силикоалюминий.
С появлением электроэнергетики более практичным стал другой способ получения натрия — электролиз расплава едкого натра или хлорида натрия:
4NaOH → электрический ток 4Na + 2H2O + O2 , 2NaCl → электрический ток 2Na + Cl2 .
В настоящее время электролиз — основной способ получения натрия.
Натрий также можно получить цирконийтермическим методом или термическим разложением азида натрия.
Физические свойства


Качественное определение натрия с помощью пламени — ярко-жёлтый цвет эмиссионного спектра «D-линии натрия», дублет 588,9950 и 589,5924 нм
Натрий — серебристо-белый металл, в тонких слоях с фиолетовым оттенком, пластичен, даже мягок (легко режется ножом), свежий срез натрия блестит. Величины электропроводности и теплопроводности натрия достаточно высоки, плотность равна 0,96842 г/см³ (при 19,7 °C ), температура плавления 97,86 °C , температура кипения 883,15 °C .
Под высоким давлением становится прозрачным и красным, как рубин.
При комнатной температуре натрий образует кристаллы кубической сингонии, пространственная группа I m3m, параметры ячейки a = 0,42820 нм , Z = 2 .
При температуре −268 °С (5 К) натрий переходит в гексагональную фазу, пространственная группа P 63/mmc , параметры ячейки a = 0,3767 нм , c = 0,6154 нм , Z = 2 .
Химические свойства
Щелочной металл на воздухе легко окисляется до оксида натрия. Для защиты от кислорода воздуха металлический натрий хранят под слоем керосина.
При горении на воздухе или в кислороде образуется пероксид натрия:
Кроме того, существует озонид натрия NaO3.
С водой натрий реагирует очень бурно, помещённый в воду кусочек натрия всплывает, из-за выделяющегося тепла плавится, превращаясь в белый шарик, который быстро движется в разных направлениях по поверхности воды, реакция идёт с выделением водорода, который может воспламениться. Уравнение реакции:
Как и все щелочные металлы, натрий является сильным восстановителем и энергично взаимодействуют со многими неметаллами (за исключением азота, йода, углерода, благородных газов):
2Na + Cl2 → 2NaCl 2Na + H2 → 250−400oC,p 2NaH
Натрий более активен, чем литий. С азотом реагирует крайне плохо в тлеющем разряде, образуя очень неустойчивое вещество — нитрид натрия (в противоположность легко образующемуся нитриду лития):
С разбавленными кислотами взаимодействует как обычный металл:
2Na + 2HCl → 2NaCl + H2↑
С концентрированными окисляющими кислотами выделяются продукты восстановления:
Растворяется в жидком аммиаке, образуя синий раствор:
С газообразным аммиаком взаимодействует при нагревании:
С ртутью образует амальгаму натрия, которая используется как более мягкий восстановитель вместо чистого металла. При сплавлении с калием даёт жидкий сплав.
Алкилгалогениды с избытком металла могут давать натрийорганические соединения — высокоактивные соединения, которые обычно самовоспламеняются на воздухе и взрываются с водой. При недостатке металла происходит реакция Вюрца.
Реагирует со спиртами, фенолами, карбоновыми кислотами с образованием солей.
Растворяется в краун-эфирах в присутствии органических растворителей, давая электрид или алкалид (в последнем у натрия необычная степень окисления −1).
Применение
Металлический натрий широко используется как сильный восстановитель в препаративной химии и промышленности, в том числе в металлургии. Используется для осушения органических растворителей, например, эфира. Натрий используется в производстве весьма энергоёмких натриево-серных аккумуляторов. Его также применяют в выпускных клапанах двигателей грузовиков как жидкий теплоотвод. Изредка металлический натрий применяется в качестве материала для электрических проводов, предназначенных для очень больших токов.
В сплаве с калием, а также с рубидием и цезием используется в качестве высокоэффективного теплоносителя. В частности, сплав состава натрий 12 %, калий 47 %, цезий 41 % имеет рекордно низкую температуру плавления −78 °C и был предложен в качестве рабочего тела ионных ракетных двигателей и теплоносителя для атомных энергоустановок.
Жидкометаллический теплоноситель в ядерных реакторах на быстрых нейтронах БН-600 и БН-800.
Натрий также используется в газоразрядных лампах высокого и низкого давления (НЛВД и НЛНД). Лампы НЛВД типа ДНаТ (Дуговая Натриевая Трубчатая) очень широко применяются в уличном освещении. Они дают ярко-жёлтый свет. Срок службы ламп ДНаТ составляет 12—24 тысяч часов. Поэтому газоразрядные лампы типа ДНаТ незаменимы для городского, архитектурного и промышленного освещения. Также существуют лампы ДНаС, ДНаМТ (Дуговая Натриевая Матовая), ДНаЗ (Дуговая Натриевая Зеркальная) и ДНаТБР (Дуговая Натриевая Трубчатая Без Ртути).
Металлический натрий применяется в качественном анализе органического вещества. Сплав натрия и исследуемого вещества нейтрализуют этанолом, добавляют несколько миллилитров дистиллированной воды и делят на 3 части, проба Ж. Лассеня (1843), направлена на определение азота, серы и галогенов (проба Бейльштейна).
Хлорид натрия (NaCl) (поваренная соль) — древнейшее применяемое вкусовое и консервирующее средство.
Азид натрия (NaN3) применяется в качестве азотирующего средства в металлургии и при получении азида свинца.
Цианид натрия (NaCN) применяется при гидрометаллургическом способе выщелачивания золота из горных пород, а также при нитроцементации стали и в гальванотехнике (серебрение, золочение).
Хлорат натрия (NaClO3) применяется для уничтожения нежелательной растительности на железнодорожном полотне.
Изотопы натрия
В настоящее время (2012 г.) известно 20 изотопов с массовыми числами от 18 до 37 и 2 ядерных изомера натрия. Единственный стабильный изотоп 23 Na. У большинства изотопов период полураспада меньше одной минуты, лишь один радиоактивный изотоп — 22 Na — имеет период полураспада больше года. 22 Na претерпевает позитронный распад с периодом полураспада 2,6027 года , его используют в качестве источника позитронов и в научных исследованиях. 24 Na, с периодом полураспада по каналу β − -распада 15 часов, используется в медицине для диагностики и для лечения некоторых форм лейкемии.
Биологическая роль
Натрий входит в состав всех живых организмов. В высших организмах натрий находится большей частью в межклеточной жидкости клеток (примерно в 15 раз больше, чем в цитоплазме клетки). Разность концентраций поддерживает встроенный в мембраны клетки натрий-калиевый насос, откачивающий ионы натрия из цитоплазмы в межклеточную жидкость.
Совместно с калием натрий выполняет следующие функции:
- Создание условий для возникновения мембранного потенциала и мышечных сокращений.
- Поддержание осмотической концентрации крови.
- Поддержание кислотно-щелочного баланса.
- Нормализация водного баланса.
- Обеспечение мембранного транспорта.
- Активация многих энзимов.
Рекомендуемая доза натрия составляет для детей от 600 до 1700 миллиграммов. Для взрослых по данным Американской Ассоциации сердечных заболеваний минимальная необходимая доза составляет меньше 500 миллиграммов, рекомендуемая до 1500 миллиграммов в день (за исключением некоторых болезней или профессий, при которых нужно повышенное количество натрия). В виде поваренной соли в 3/4 чайной ложки содержится 1725 миллиграммов натрия. По другим данным здоровым взрослым стоит ограничивать употребление натрия 2300 миллиграммами, а людям с повышенным давлением и рядом других заболеваний 1500 или меньшим количеством.
Натрий содержится практически во всех продуктах в разных количествах, хотя большую его часть организм получает из поваренной соли, в том числе в составе консервов, полуфабрикатов, соусов, колбасных изделий и т.п. В качестве источника натрия служат также такие пищевые добавки как глутамат натрия, пищевая сода (бикарбонат натрия), нитрит натрия, сахаринат натрия и бензоат натрия. Усвоение в основном происходит в желудке и тонкой кишке. Витамин Д улучшает усвоение натрия, однако чрезмерно солёная пища и пища, богатая белками, препятствуют нормальному всасыванию. Количество поступившего с едой натрия показывает содержание натрия в моче. Для богатой натрием пищи характерна ускоренная экскреция.
Дефицит натрия у питающегося сбалансированной пищей человека не встречается, однако некоторые проблемы могут возникнуть при голодании. Временный недостаток может быть вызван использованием мочегонных препаратов, поносом, обильным потением или избыточным употреблением воды.
Симптомами нехватки натрия являются потеря веса, рвота, образование газов в желудочно-кишечном тракте и нарушение усвоения аминокислот и моносахаридов. Продолжительный недостаток вызывает мышечные судороги и невралгию.
Переизбыток натрия вызывает отек ног и лица, повышенное выделение калия с мочой, у некоторых людей повышенное кровяное давление и скопление жидкости. Максимальное количество соли, которое может быть переработано почками, составляет примерно 20—30 граммов, большее количество уже опасно для жизни.
Меры предосторожности
Чистый металлический натрий огнеопасен. На воздухе склонен к самовоспламенению. Особенно опасен контакт с водой и влажными поверхностями, так как натрий очень бурно реагирует с водой, часто со взрывом, образуя едкую щёлочь (NaOH). В лабораториях небольшие количества натрия (примерно до 1 кг) хранят в закрытых стеклянных банках под слоем керосина, лигроина, бензина или вазелинового масла так, чтобы слой жидкости покрывал весь металл. Банка с натрием должна храниться в металлическом несгораемом шкафу (сейфе). Натрий берут пинцетом или щипцами, отрезают скальпелем (натрий пластичен и легко режется ножом) на сухой поверхности (не на столе, а в стеклянной чашке); необходимое количество и остаток тут же возвращают в банку под слой керосина, а отрезанный кусок либо помещают в керосин, либо тут же вводят в реакцию. Прежде чем приступить к работе с натрием, необходимо пройти инструктаж по охране труда. Лица, впервые приступающие к работе с натрием, должны производить эту работу под наблюдением сотрудников, имеющих опыт такой работы. Обычно в лабораторных условиях для реакций используют количества натрия, не превышающие нескольких десятков граммов. Для показательных опытов, например, в школе на уроках химии, следует брать не более одного грамма натрия. После работы с металлическим натрием всю посуду и остатки натрия заливают неразбавленным спиртом и полученный раствор нейтрализуют слабым раствором кислоты. Следует обратить особое внимание на то, чтобы все остатки и обрезки натрия были полностью нейтрализованы до их выбрасывания, так как натрий в мусорном ведре может вызвать пожар, а в канализационном сливе может вызвать взрыв и разрушение трубы. Все работы с натрием, как и вообще с щелочами и щелочными металлами, должны проводиться в очках или защитной маске. Хранить натрий дома и производить с ним какие-либо опыты не рекомендуется.
Воспламенение и даже взрыв металлического натрия при соприкосновении с водой и многими органическими соединениями может причинить серьёзные травмы и ожоги. Попытка взять кусочек металлического натрия голыми руками может привести к его воспламенению (иногда взрыву) из-за влажности кожи и образованию тяжелейших ожогов натрием и образующейся щёлочью. Горение натрия создает аэрозоль оксида, пероксида и гидроксида натрия, обладающий разъедающим действием. Некоторые реакции натрия протекают очень бурно (например, с серой, бромом).
Хлорид натрия

Хлорид натрия или хлористый натрий (NaCl) — натриевая соль соляной кислоты. Известен в быту под названием поваренной соли, основным компонентом которой и является. Хлорид натрия в значительном количестве содержится в морской воде. Встречается в природе в виде минерала галита (каменной соли). Чистый хлорид натрия представляет собой бесцветные кристаллы, но с различными примесями его цвет может принимать голубой, фиолетовый, розовый, жёлтый или серый оттенок.
Содержание
- 1 Нахождение в природе и производство
- 1.1 Галит
- 1.2 Каменная соль
- 1.3 Морская соль
- 1.4 Залежи
- 1.5 Производство
- 2.1 В пищевой промышленности и кулинарии
- 2.2 В медицине
- 2.3 В коммунальном хозяйстве. Техническая соль
- 2.4 Регенерация Nа-катионитовых фильтров
- 2.5 Химическая промышленность
- 2.5.1 Получение хлора и гидроксида натрия
- 2.5.2 Получение металлического натрия
- 2.5.3 Получение соляной кислоты и сульфата натрия
![Хлорид натрия]()
Нахождение в природе и производство
В природе хлорид натрия встречается в виде минерала галита, который образует залежи каменной соли среди осадочных горных пород, прослойки и линзы на берегах солёных озёр и лиманов, соляные корки в солончаках и на стенках кратеров вулканов и в сольфатарах. Огромное количество хлорида натрия растворено в морской воде. Мировой океан содержит 4 × 10 15 тонн NaCl, то есть из каждой тонны морской воды можно получить в среднем 1,3 кг хлорида натрия. Следы NaCl постоянно содержатся в атмосфере в результате испарения брызг морской воды. В облаках на высоте полтора километра 30 % капель, больших 10 мкм по размеру, содержат NaCl. Также он найден в кристаллах снега.
Наиболее вероятно, что первое знакомство человека с солью произошло в лагунах тёплых морей или на соляных озёрах, где на мелководье солёная вода интенсивно испарялась под действием высокой температуры и ветра, а в осадке накапливалась соль. По образному выражению Пифагора, «соль была рождена благородными родителями: солнцем и морем».
Галит
В природе хлорид натрия чаще всего встречается в виде минерала галита. Он имеет гранецентрированную кубическую решётку и содержит 39,34 % Na, 60,66 % Cl. Другими химическими элементами, входящими в состав примесей, являются: Br, N, H, Mn, Cu, Ga, As, I, Ag, Ba, Tl, Pb, K, Ca, S, O. Плотность 2,1—2,2 г/см³, а твёрдость по шкале Мооса — 2. Бесцветный прозрачный минерал со стеклянным блеском. Распространённый минерал соленосных толщ. Образуется при осаждении в замкнутых водоёмах, а также как продукт сгона на стенках кратеров вулканов. Составляет пласты в осадочных породах лагунных и морских фаций, штокоподобные тела в соляных куполах и тому подобных.
Каменная соль
Каменной солью называют осадочную горную породу из группы эвапоритов, состоящую более чем на 90 % из галита. Галит также часто называют каменной солью. Эта осадочная горная порода может быть бесцветной или снежно-белой, но чаще она окрашена примесями глин, талька (серый цвет), оксидами и гидроксидами железа (жёлтый, оранжевый, розовый, красный), битумами (бурая). Каменная соль содержит хлориды и сульфаты натрия, калия, магния и кальция, бромиды, йодиды, бораты, гипс, примеси карбонатно-глинистого материала, доломита, анкериту, магнезита, битумов и так далее.
По условиям формирования месторождений каменную соль подразделяют на следующие виды:
- рассолы современных соляных бассейнов
- соляные подземные воды
- залежи минеральных солей современных соляных бассейнов
- ископаемые залежи (важнейшие для промышленности).
Морская соль
Морская соль является смесью солей (хлориды, карбонаты, сульфаты и т. д.), образующейся при полном испарении морской воды. Среднее содержание солей в морской воде составляет:
Соединение Масс. доля, % NaCl 77,8 MgCl2 10,9 MgSO4 4,7 KCl 2,5 K2SO4 2,5 CaCO3 0,3 Ca(HCO3)2 0,3 другие соли 0,2 ![Хлорид натрия]()
При испарении морской воды при температуре от +20 до +35 °C в осадке сначала кристаллизуются наименее растворимые соли — карбонаты кальция и магния и сульфат кальция. Затем выпадают более растворимые сульфаты натрия и магния, хлориды натрия, калия и магния, и после них — сульфаты калия и магния. Последовательность кристаллизации солей и состав осадка может несколько варьироваться в зависимости от температуры, скорости испарения и других условий. В промышленности морскую соль получают из морской воды, в основном методом обычного выпаривания. Она отличается от каменной соли значительно большим содержанием других химических солей, минералов и различных микроэлементов, в первую очередь йода, калия, магния и марганца. Соответственно, она отличается от хлорида натрия и по вкусу — горько-солёный привкус ей придают соли магния. Она используется в медицине: при лечении кожных заболеваний, таких как псориаз. Как лечебное вещество в аптечной и обычной торговой сети, распространённым продуктом является соль из Мёртвого моря. В очищенном виде этот вид соли также предлагается в продуктовой торговой сети — как натуральная и богатая йодом пищевая.
Залежи
Залежи каменной соли найдены во всех геологических системах. Важнейшие из них сосредоточены в кембрийских, девонских, пермских и третичных отложениях. Каменная соль составляет мощные пластовые залежи и ядра сводчатых структур (соляных куполов и штоков), образует прослойки, линзы, гнезда и вкрапления в других породах. Среди озёрных месторождений России крупнейшие — Эльтонское, Баскунчак в Прикаспии, Кучукское озеро, Кулундинское озеро, Эбейты и другие озёра в Западной Сибири.
Производство
В древности технология добычи соли заключалась в том, что соляную рапу (раствор) вытаскивали лошадиным приводом из шахт, которые назывались «колодцами» или «окнами», и были достаточно глубокими — 60—90 м. Извлечённый солевой раствор выливали в особый резервуар — творило, откуда она через отверстия стекала в нижний резервуар, и системой жёлобов подавалась в деревянные башни. Там её разливали в большие чаны, на которых соль вываривали.
На Руси поморы вываривали соль на побережье Белого моря и называли её морянка. В 1137 году новгородский князь Святослав определил налог на соляные варницы.
Беломорской солью, называемой «морянкой», торговали по всей Российской империи до начала XX века, пока её не вытеснила более дешёвая поволжская соль.
Современная добыча хлорида натрия механизирована и автоматизирована. Соль массово добывается выпариванием морской воды (тогда её называют морской солью) или рассола с других ресурсов, таких как соляные источники и соляные озера, а также разработкой соляных шахт и добычей каменной соли.
Для добычи хлорида натрия из морской воды необходимы условия жаркого климата с низкой влажностью воздуха, наличие значительных низменных территорий, лежащих ниже уровня моря, или затопляемых приливом, слабая водопроницаемость почвы испарительных бассейнов, малое количество осадков в течение сезона активного испарения, отсутствие влияния пресных речных вод и наличие развитой транспортной инфраструктуры.Мировое производство соли в 2009 году оценивается в 260 миллионов тонн. Крупнейшими мировыми производителями являются Китай (60,0 млн тонн), США (46,0 млн тонн), Германия (16,5 млн тонн), Индия (15,8 млн тонн) и Канада (14 млн тонн).
Натрий
Натрий — элемент главной подгруппы первой группы, третьего периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 11. Обозначается символом Na (лат. Natrium). Простое вещество натрий (CAS-номер: 7440-23-5) — мягкий щелочной металл серебристо-белого цвета.
В воде натрий ведет себя почти так же, как литий: реакция идёт с бурным выделением водорода, в растворе образуется гидроксид натрия.
История и происхождение названия
![]()
Натрий (а точнее, его соединения) использовался с давних времён. Например, сода (натрон), встречающаяся в природе в водах натронных озёр в Египте. Природную соду древние египтяне использовали для бальзамирования, отбеливания холста, при варке пищи, изготовлении красок и глазурей. Плиний Старший пишет, что в дельте Нила соду (в ней была достаточная доля примесей) выделяли из речной воды. Она поступала в продажу в виде крупных кусков, из-за примеси угля окрашенных в серый или даже чёрный цвет.
Натрий впервые был получен английским химиком Хемфри Дэви в 1807 году электролизом твердого NaOH.
Название «натрий» (natrium) происходит от арабского натрун по-гречески — nitron и первоначально оно относилось к природной соде. Сам элемент ранее именовался содием Sodium.
Получение
Первым способом получения натрия стала реакция восстановления карбоната натрия углем при нагревании тесной смеси этих веществ в железной ёмкости до 1000°C:
Затем появился другой способ получения натрия — электролиз расплава едкого натра или хлорида натрия.
Физические свойства
![]()
![]()
![]()
Качественное определение натрия с помощью пламени — ярко-жёлтый цвет эмиссионного спектра «D-линии натрия», дублет 588,9950 и 589,5924 нм.
Натрий — серебристо-белый металл, в тонких слоях с фиолетовым оттенком, пластичен, даже мягок (легко режется ножом), свежий срез натрия блестит. Величины электропроводности и теплопроводности натрия достаточно высоки, плотность равна 0,96842 г/см³ (при 19,7° С), температура плавления 97,86° С, температура кипения 883,15° С.
Химические свойства
Щелочной металл, на воздухе легко окисляется. Для защиты от кислорода воздуха металлический натрий хранят под слоем керосина. Натрий менее активный чем литий, поэтому с азотом реагирует только при нагревании:
При большом избытке кислорода образуется пероксид натрия
Применение
Металлический натрий широко используется в препаративной химии и промышленности как сильный восстановитель, в том числе в металлургии. Натрий используется в производстве весьма энергоёмких натриево-серных аккумуляторов. Его также применяют в выпускных клапанах грузовиков как теплоотвод. Изредка металлический натрий применяется в качестве материала для электрических проводов, предназначенных для очень больших токов.
В сплаве с калием, а также с рубидием и цезием используется в качестве высокоэффективного теплоносителя. В частности, сплав состава натрий 12 %, калий 47 %, цезий 41 % имеет рекордно низкую температуру плавления −78 °C и был предложен в качестве рабочего тела ионных ракетных двигателей и теплоносителя для атомных энергоустановок.
Натрий также используется в газоразрядных лампах высокого и низкого давления (НЛВД и НЛНД). Лампы НЛВД типа ДНаТ (Дуговая Натриевая Трубчатая) очень широко применяются в уличном освещении. Они дают ярко-жёлтый свет. Срок службы ламп ДНаТ составляет 12-24 тысяч часов. Поэтому газоразрядные лампы типа ДНаТ незаменимы для городского, архитектурного и промышленного освещения. Также существуют лампы ДНаС, ДНаМТ (Дуговая Натриевая Матовая), ДНаЗ (Дуговая Натриевая Зеркальная) и ДНаТБР (Дуговая Натриевая Трубчатая Без Ртути).
Металлический натрий применяется в качественном анализе органического вещества. Сплав натрия и исследуемого вещества нейтрализуют этанолом, добавляют несколько миллилитров дистиллированной воды и делят на 3 части, проба Ж. Лассеня (1843), направлена на определение азота, серы и галогенов (проба Бейльштейна)
— Хлорид натрия (поваренная соль) — древнейшее применяемое вкусовое и консервирующее средство.
— Азид натрия (Na3N) применяется в качестве азотирующего средства в металлургии и при получении азида свинца.
— Цианид натрия (NaCN) применяется при гидрометаллургическом способе выщелачивания золота из горных пород, а также при нитроцементации стали и в гальванотехнике (серебрение, золочение).
— Хлорат натрия (NaClO3) применяется для уничтожения нежелательной растительности на железнодорожном полотне.Биологическая роль
В организме натрий находится большей частью снаружи клеток (примерно в 15 раз больше чем в цитоплазме). Это разницу поддерживает натрий-калиевый насос, который откачивает попавший внутрь клетки натрий.
Совместно с калием натрий выполняет следующие функции:
Создание условий для возникновения мембранного потенциала и мышечных сокращений.
Поддержание осмотической концентрации крови.
Поддержание кислотно-щелочного баланса.
Нормализация водного баланса.
Обеспечение мембранного транспорта.
Активация многих энзимов.Рекомендуемая доза натрия составляет для детей от 600 до 1700 миллиграмм, для взрослых от 1200 до 2300 миллиграмм. В виде поваренной соли это составляет от 3 до 6 грамм в день.
Натрий содержится практически во всех продуктах, хотя большую его часть организм получает из поваренной соли. Усвоение в основном происходит в желудке и тонкой кишке. Витамин Д улучшает усвоение натрия, однако, чрезмерно соленая пища и пища богатая белками препятствуют нормальному всасыванию. Количество поступившего с едой натрия показывает содержание натрия в моче. Для богатой натрием пищи характерна ускоренная экскреция.
Дефицит натрия у питающегося сбалансированой пищей человека не встречается, однако, некоторые проблемы могут возникнуть при вегетарианских диетах. Временный дефицит может быть вызвано использованием мочегонных, поносом, обильным потением или избыточным употреблением воды. Симптомами нехватки натрия являются потеря веса, рвота, образование газов в желудочно-кишечном тракте, и нарушение усвоения аминокислот и моносахаридов. Продолжительный дефицит вызывает мышечные судороги и невралгию.
Переизбыток натрия вызывает отек ног и лица, а так же повышеное выделение калия с мочой. Максимальное количество соли, которое может быть переработано почками составляет примерно 20-30 грамм, большее количество уже опасно для жизни.
Соединения натрия
Натрий, Natrium, Na (11)
Название натрий — sodium, natrium происходит от древнего слова, распространенного в Египте, у древних греков (vixpov) и римлян. Оно встречается у Плиния (Nitron), у других древних авторов и соответствует древнееврейскому нетер (neter). В древнем Египте натроном, или нитроном, называли вообще щелочь, получаемую не только из природных содовых озер, но и из золы растений. Ее употребляли для мытья, изготовления глазурей, при мумификации трупов. В средние века название нитрон (nitron, natron, nataron), а также борах (baurach), относилось и к селитре (Nitrum). Арабские алхимики называли щелочи alkali. С открытием пороха в Европе селитру (Sal Petrae) стали строго отличать от щелочей, и в XVII в. уже различали нелетучие, или фиксированные щелочи, и летучую щелочь (Alkali volatile). Вместе с тем было установлено различие между растительной (Alkali fixum vegetabile — поташ) и минеральной щелочью (Alkali fixum minerale — сода).В конце XVIII в. Клапрот ввел для минеральной щелочи название натрон (Natron), или натр и для растительной — кали (Kali), Лавуазье не поместил щелочи в «Таблицу простых тел», указав в примечании к ней, что это, вероятно, сложные вещества, которые когда-нибудь будут разложены. Действительно, в 1807 г. Дэви путем электролиза слегка увлажненных твердых щелочей получил свободные металлы — калий и натрий, назвав их потассий (Potassium) и содий (Sodium). В следующем году Гильберт, издатель известных «Анналов физики», предложил именовать новые металлы калием и натронием (Natronium); Берцелиус сократил последнее название до «натрий» (Natrium). В начале XIX в. в России натрий называли содием (Двигубский, 182i; Соловьев, 1824); Страхов предлагал название содь (1825). Соли натрия назывались, например, сернокислая сода, гидрохлоровая сода и одновременно уксусный натр (Двигубский, 1828). Гесс, по примеру Берцелиуса, ввел название натрий.
Периодическая система химических элементов Менделеева
Классификация хим. элементов, устанавливающая зависимость различных свойств элементов от заряда атомного ядра. Система является графическим выражением периодического закона/
198095, г.Санкт-Петербург, ул.Швецова, д.23, лит.Б, пом.7-Н, схема проезда
Читайте также:





