Металлический натрий почему так называют
Обновлено: 26.04.2024
Соединения натрия стали известны человечеству с глубокой древности.
Сейчас, также, как и раньше невозможно вообразить свою жизнь без присутствия в ней соединений натрия.
В наши дни абсолютно все люди ежедневно встречают вокруг себя огромное количество соединений натрия, даже, порой, не зная об этом. Это и обычная поваренная соль, пищевая сода, щелочные чистящие средства, мыло и средства для мытья посуды, лекарственные средства (аспирин, тетраборат натрия и другие), стекло, лампы и множество других товаров массового потребления.
Самым распространенным источником натрия на планете считается каменная соль (галит). Галит – это практически чистый NaCl.
Десятки самых разных соединений натрия используются сегодня во всех сферах нашей деятельности.
О наиболее важных соединениях натрия, а также об их использовании в промышленности и пойдет речь ниже.
• Хлорид натрия NaCl – наиболее известное всем применения получил в качестве усилителя вкуса. Ведь хлорид натрия ни что иное, как поваренная соль. Кроме улучшения вкусовых качеств хлорид натрия обладает антибактериальными свойствами, поэтому используется в качестве консерванта.
Под воздействием электрического тока из NaCl, растворенного в воде, получают сразу три важнейших для промышленности элемента. Это газообразный хлор (Cl2), гидрооксид натрия (второе название - каустическая сода) (NaOH) и газообразный водород (H2).
В свою очередь хлор применяется в производстве, красок, растворителей, пластмасс, пестицидов, используется в текстильной и фармацевтической промышленности.
• Гидрооксид натрия и раствор гидрооксида натрия нашли большое применение в металлургической, нефтеперерабатывающей, косметической, текстильной, а также пищевой промышленностях. Кроме того эти соединения успешно применяются для обработки воды.
• Карбонат натрия( Na2CO3) – всем известная сода. Это соединение натрия нашло применение в производстве стекла, бумаги и целлюлозы, мыла, чистящих и моющих средств, в легкой промышленности. Пищевая сода входит в состав продуктов питания. Также используется для очистки сточных вод, кроме того является отправной точкой для производства других соединений натрия.
• Бикарбонат натрия (NaHCO3) – при растворении в воде вызывает реакцию шипения. Например, газированные напитки, разрыхлитель для теста, аспирин в «шипучих» таблетках – здесь используется бикарбонат натрия.
• Гипохлорит натрия ( NaOCl) – используется в фармацевтической промышленности, в качестве одного из компонентов, входящих в состав бытовой химии, такой, как отбеливатели, обезжириватели , чистящие средства; применятся для обеззараживания и дезинфекции воды.
• Нитрит натрия (NaNO2) – азотосодержащее удобрение, пищевой консервант и улучшитель окраски Е250. Нитрит натрия широко используется в медицине и ветеринарии как сосудорасширяющее средство, бронхолитическое, слабительное, средство против спазмов и противоядие при отравлении цианидами. В фотографии нитрит натрия нашел применение как реагент, противоморозная добавка для бетона, применяется при изготовлении каучука и взрывчатых веществ.
• Нитрат натрия (NaNO3) - это соединение натрия также получило широчайшее применение: консервант Е251 (противомикробная добавка), удобрение. Также используется при изготовлении ракетного топлива, входит в состав взрывчатых веществ, а также в металлообрабатывающей и стекольной промышленности.
• Альгинат натрия (NaC 6 H 7 O 6 ) – производство цемента, краски на водной основе, загуститель в мороженом и других продуктах питания.
• Бифторид натрия (KHF 2 ) – антисептик, не пищевой консервант, также используется при производстве жести и травлении стекла;
• Диуранат натрия, или « желтый уран » (Na 2 U 2 O 7 ) – используется для производства оранжевой глазури для керамики;
• Фторсиликат натрия (Na 2 SiF 6 ) – используется при изготовлении зубных паст со фтором, хозяйственного мыла, также используется при изготовлении средств для борьбы с крысами и насекомыми. Кроме того фторсиликат натрия нашел применение в качестве консерванта для кожи и дерева.
• Метаборат натрия (NaBO 2 ) – гербицид, применяется для уничтожения растительности.
• Стеарат натрия (NaOOCC 17 H 35 ) – используется как добавка в косметические средства и зубные пасты. Применяется в качестве гидроизоляции и как компонент, предотвращающий разрушение пластика.
• Гликолят натрия циркония (NaZrH 3 (H 2 COCOO) 3 ) – это вещество входит в состав дезодорантов, противомикробных препаратов, также применяется при изготовлении огнестойких материалов.
• Парапериодат натрия (Na 3 H 2 IO 6 ) - это соединение помогает бумаге сохранять прочность при намокании.
• Гидрофторид натрия( NaHF2) – антисептик, используется при производстве плавиковой кислоты, также нашел применение для травления стекла.
• Вольфрамит натрия (NaWO4) – изготовление пигментов.
• Гексаметалфосфат натрия (Na6P6O18) – текстильная, кожевенная, нефтяная промышленность, смягчение воды.
• Дитионит натрия (Na2S2O4) – производство красителей
• Салицилат натрия – C7H5NaO3 – фармацевтика.
• Метасиликат натрия (Na2SiO3) – производство бетона, цементных растворов, стекла.
• Гидрид натрия (NaH) – c помощью раствора NaH в гидрооксиде натрия снимают окалину со сталей и тугоплавких металлов.
• Бисульфит натрия (NaHSO3) – фотография, бумажная, текстильная, кожевенная индустрия, очистка воды.
• Фосфат натрия (Na3PO4) – косметические препараты, зубная паста, пищевая добавка.
• Селенит натрия ( Na2SeO3) – минеральная добавка, фармацевтика, ветеринария.
• Тиосульфат натрия – фармацевтическая промышленность
• Станнит натрия (Na2SnO2) – с его помощью открывают ионы кобальта в сталях, добывают металлическое серебро, благодаря станниту натрия возможно полное восстановление органических соединений ртути.
• Метастаннат натрия Na2[Sn(OH)6] – гальваника, лужение алюминия.
• Тиоцианат натрия ( традиционное название -роданит натрия) (NaSCN) – используется в качестве реактива для фотометрического определения железа, также используется в фотографии и текстильной промышленности.
• Натрий-бутадиеновый каучук – самый востребованный из всех каучуков
• Амид натрия (NaNH2) - участвует в синтезе других химических веществ, включая витамин А.
• Ацетат натрия (C2H3O2Na) – легкая, пищевая промышленность, также используется в быту.
• Пиросульфит натрия (Na2(SO2SO3)) – пищевой консервант, также нашел применение в химической и фармацевтической отраслях.
• Кремнефтористый натрий (Na2SiO6) и Гексафторосиликат натрия (Na2[SiF6] ) – необходимы при получении берилла и марганца, используется при изготовлении цементов, стекол, эмалей, замазок.
• Метилат натрия (CH3NaO) – необходим для синтеза в при изготовлении лекарственных препаратов и химикатов.
• Перекись натрия (Na2O2) – великолепный отбеливател.ь
• Фенолят натрия используется для дезинфекции.
• Фторид натрия (NaF)- при изготовлении зубной пасты, кроме того компонент составов флюса для сварки, пайки металлов, эмалей, стекол, керамики, входит в состав средств для очистки металлов и т.д.
Радиоактивные изотопы натрия имеют как медицинское, так и не медицинское применение (например, проверят нефтепроводы на предмет утечек)
Большинство людей никогда не видели металлический натрий (Na). Да и в виде свободного элемента в природе он никогда не встречается. Он настолько активен, что обычно хранится в жидкости, с которой не реагирует, чаще всего используют керосин. Тем не менее, и в виде свободного элемента натрий нашел большое применения в различных областях промышленности. Это и теплообменная среда в атомных электростанциях, и производство других металлов, включая титан, производство аккумуляторов, электрических проводов, натриевых ламп, искусственного каучука и прочее.
Подводя итог всему вышесказанному, необходимо отметить, что переоценить роль такого химического элемента, как натрий, крайне сложно. Однако, важнейшим из всех соединений натрия, по праву может считаться обыкновенная пищевая соль. Ведь именно хлорид натрия имеет огромное влияние на ряд основных функций у растений, животных и людей. Именно хлорид натрия принимает непосредственное участие в водно-солевом обмене, одном из важнейших процессов, протекающих в организмах животных и людей.
Автор, ты хоть просматривай, что пишешь
"Бифторид натрия (KHF 2 )"
Популяризация науки - это, чаще всего, хорошо. Хотелось бы только, чтобы без ошибок ;-) В аспирине (ацетилсалицилловая кислота, на фото) натрия нет. "Реакция шипения" (так в тексте!) у бикарбоната натрия случается не при растворении, а при попадании в кислую среду, например, когда пищевую соду уксусом гасите. NaHCO3 + CH3COOH => CH3COONa + H2O + CO2. Вот этот CO2 (углекислый газ), выделяясь, шипит как раз.



Бифторид натрия (KHF2) – антисептик, .
.
Гидрофторид натрия(NaHF2) – антисептик, .
Да и все равно "ниочем" - куча фактов без объяснения ПОЧЕМУ.
Да и тег "химияпросто" - оно вообщето имеет отношение к вполне конкретному циклу научнопопулярных роликов, до уровня которых сему креативу - как до Пекина раком. Не позорьте тег.
"Всем известная сода" это гидрокарбонат натрия NaHCO3, а не карбонат Na2CO3




Спасибо ТС, очень кратко и познавательно. Будет просто прекрасно, если и про другие элементы тоже пост сделаешь)
+

Хемофобная лекция: стоит ли бояться химикатов? – химик-флейворист Сергей Белков | Научпоп
Как запрет ДДТ в США повлиял на распространение малярии? Что такое хемофобия и как с ней бороться? Может ли натуральный сельдерей с огорода навредить больше, чем удобренный химикатами? Как выбраться из Мальтузианской ловушки? Насколько опасна и полезна хлорированная вода? Как Зелёная революция повлияла на развитие сельского хозяйства в мире? Об этом и многом другом рассказывает Сергей Белков, химик, флейворист, научный журналист, член Британского сообщества флейвористов.

Учитель года

Смешивать натрий с калием-это безумие !
Ответ на пост «Как не надо экспериментировать с красным фосфором»
Ух. сколько же историй у бывалых химиков и иже сочувствующим на тему "как не надо экспериментровать".
Внесу и свои "5 копеек".
Как только в 8 классе началась химия (конец 90-х), я вдруг обнаружил, что в самом обычном учебнике есть достаточно информации для поделок в домашних условиях. Причем поделок не на уровне сода+уксус, а достаточно ярких, громких и эффектных опытов.
Особенно меня заинтересовали разделы. пожалуй, не буду уточнять какие именно, отмечу только, что элементы относились к достаточно электроположительным) А именно - восстановление одних другими из оксидов, а также, наоборот, интенсивное окисление.
Так вот, посмотрев вокруг, я обнаружил, что основные компоненты либо есть в наличии, либо можно получить из подручного сырья - удобрений, составных частей ЛКМ и т.д. Конечно же я не мог не попробовать. Бедный балкон - последующие несколько лет он был задымлен, обожжен, вонял сероводородом и заставлен подносами с сохнущими на солнце порошками от сине-зеленых до черных. Благо, эксперименты непосредственно с поджиганием я ставил в объемах "на кончике ножа" и родители не сильно подозревали грядущую опасность.
Однажды я решил проверить - а что же будет, если поджечь побольше? Намешал приблизительно полбанки из-под кофе, но в городе испытывать не решился. Взял заготовку с собой в деревню, дождался ночи и, попросив папу стать соучастником, вышел на перекресток дорог в низинке. Поджег (потом уже понял, что остаться с пальцами очень повезло). Понял, что испытывают люди, смотрящие в сторону ядерного взрыва. Когда все прогорело - не понял, куда делась банка (металлическая) и в недоумении пошел спать. А на утро, при дневном свете увидел только остатки нижнего кольца банки в земле - то есть она просто сгорела за эти несколько секунд.
Несколько последующих лет на всяких выездных мероприятиях это было моей "фишкой", помимо сине-зеленых костров, плевания огнем (керосин на вкус та еще дрянь, тройной одеколон сильно жжет слизистые, а петролейный эфир может вспыхнуть гораздо раньше, чем успеет отлететь от огнеплевателя), дымовых шашек и пр. Но каждый раз это были отдельные световые "шашечки", со своим детонатором и более-менее безопасным способом зажигания.
И вот, однажды, поехал я на открытие ролевого фестиваля (тот, где бегают эльфы, орки, рыцари и прочие дурные личности). Сначала все шло очень даже неплохо. Вспышки, фокусы, файер-шоу. Запомнился момент, когда на определенной части представления, какой-то то ли эльф, то ли друид, сыпал в костер что-то (возможно, порох), и костер отзывался вспышками, а я в какой-то раз одновременно сыпанул один из своих порошков с другой стороны. Друид этот явно не ожидал, что костер резко полыхнет зеленым, но зрителям понравилось.
И вот, все практически закончилось, кто был в силах - продолжали травить организм алкоголем, кто нет - уже окислился и спал где упал. Реактивы у меня тоже подошли к концу, но осталась одна баночка с той самой ярко вспыхивающей и высокотемпературногорящей смесью. Баночка, кстати, из-под пертуссина (для понимания объемов). И вот, в надежде потрепать людям нервы доставить людям зрелище, я начал ходить от костра к костру и исподтишка сыпать в огонь. Сыпал примерно полкрышки, но жар пламени существенно увеличивался на некоторое время, что вызывало у кого-то удивленное "ого", а у кого-то нецензурное выражение неудовольствия.
В одном месте выразились особенно грубо, что по моему мнению, должно было быть наказано и сыпнул еще, дабы проучить грубиянов. Но сыпнул не из крышки, куда предварительно отмеривал нужную порцию, а непосредственно из баночку, где оставалось меньше трети.
К моему сожалению, смесь была не только очень яркой и горячей, но и мгновенно вспыхивающей. За эти доли секунды пламя залетело в банку.
Помню треск лопающегося стекла, помню шипение пригорающей к стеклу кожи (звук примерно как от воды на оооочень раскаленной сковороде), помню, как пытался стряхнуть эту банку с руки.
Остаток ночи я провел в поисках:
1. транспорта - пешком идти километров 5 через лес. Разумеется в темноте. Разумеется не вариант, так как потом еще как-то нужно было добраться до больницы, а свое состояние я предугадать не мог, поэтому решил оставаться среди людей.
2. любых подходящих медикаментов - нашлось только полметра бинта.
3. воды - на удивление, ни у кого из неокислившихся в спиртном угаре, не нашлось воды, но, спустя пару часов, кто-то посоветовал сходить в лагерь к казакам (он был чуть поодаль) - там, как сказках, достали две пятилитровые бутыли, со словами "В одной спирт, в другой вода. Вроде, в этой - вода" - я сделал несколько глубоких глотков и понял, что они ошиблись. Водой, правда, потом таки запил. На удивление, ни опьянения, ни утренних последствий не было вообще - видимо, сказался болевой шок.
Периодически, между поисками, крутился волчком по земле, зажимая дико болящую руку и пытаясь смягчить ощущения, засовывая ее в прохладную пыль (благо, ее неплохо натоптали).
К утру я все-таки смог придремать на час-полтора, но когда рассвело - рука представляла собой достаточно противоестественное зрелище - раздуло так, что я не мог сомкнуть пальцы. А между указательным, средним и безымянным были вкрапления угля. То ли кожа так прогорела, то ли где-то прилипло - не знаю, но пришлось аккуратно соскребать.
И вот, утренний прохладный туман немного облегчил страдания, что помогло мне пройти эти пять километров до остановки. Потом был автобус, который ехал 2 часа - маршрут пролегал через весь город. И на подходе к дому, в какой-то момент, я слегка сжал (скорее, даже, просто шевельнул) пальцы - и было ощущение, что в руке была кружка воды, но без самой кружки - послышался сильный шлепок жидкости об асфальт. Посмотрев на руку, я увидел большие такие лоскуты кожи - наконец, сами лопнули волдыри. Боль, кстати, существенно утихла после этого.
Последующие пару недель были перевязки каждые 2-3 часа, ванночки с марганцовкой, намазывание "спасателем" с заматыванием в полиэтилен, но, слава Богу, зажило и почти без шрамов.
Дополнительных страданий принесло то, что в это же утро приехал заказанный ранее линолеум на всю квартиру (рулоны по 3-4 метра), и отец явно не мог затащить их один. Собственно, пришлось орудовать левой рукой и предплечьем правой, но справились.
После этого я осознал, что такое "наука на всю жизнь" и зарекся трогать пиротехнику.
P.S.: один близкий человек, работавший на "вспомогательной" должности в "органах" как-то сказал папе, что большой брат очень даже следит за "юными дарованиями", вроде меня. Это помогло взять зарок не только не связываться с пиротехникой, но и установить для себя табу на любые взрывчатые и психотропные вещества, в том смысле - что не только не делать, но даже и не знать, как оно делается.
НАТРИЙ — соль жизни
Соединения металлов натрия-калия контролируют солевой баланс в наших организмах. Нарушения этого баланса опасно для жизни. В составе крови соединения этих металлов создают своеобразный электролит, необходимый для работы любой клетки организма.
От Библии до наших дней
История героя статьи тянется с библейских времен. Именно в Библии упомянуто вещество, которым пользовались для мытья, отбеливания хлопковых тканей. В переводе слово νίτρον (нитрон) означает мыло или щелок.

Природной содой или щелоком из золы многие века люди пользовались для домашних нужд.
Свойства натрия

Натрий (natrium) относится к щелочным металлам, в таблице Менделеева имеет атомный № 11.
- Легко режется ножом.
- Чистый натрий имеет белый серебристый цвет; на воздухе быстро покрывается слоем оксида Na2O.
- Структура кристаллической решетки объемноцентрированная, кубическая.
- Natrium легче воды; если бросить кусочек в воду, он будет плавать на ее поверхности.
Металл настолько активный, что хранят его в минеральном масле или в керосине, без доступа воздуха.
- Натрий реагирует с разбавленными кислотами, как рядовой металл.
- В реакции с концентрированными кислотами образуются продукты восстановления.
- Бурная реакция с водой идет с выделением водорода, поэтому металл загорается или взрывается.
- Как все щелочные металлы, активно реагирует со многими неметаллами.
Известен один стабильный изотоп — 23-Na.
| Свойства атома | |
|---|---|
| Название, символ, номер | На́трий / Natrium (Na), 11 |
| Атомная масса (молярная масса) | 22,98976928 ± 0,00000002 а.е.м.[1] а. е. м. (г/моль) |
| Электронная конфигурация | [Ne] 3s1, 1s22s22p63s1 |
| Радиус атома | 190 пм |
| Химические свойства | |
| Ковалентный радиус | 154 пм |
| Радиус иона | 97 (+1e) пм |
| Электроотрицательность | 0,93 (шкала Полинга) |
| Электродный потенциал | -2,71 В |
| Степени окисления | −1 (в алкалидах)[2]; 0; +1 (наиболее частая) |
| Энергия ионизации (первый электрон) | 495,6(5,14) кДж/моль (эВ) |
| Термодинамические свойства простого вещества | |
| Плотность (при н. у.) | 0,971 г/см³ |
| Температура плавления | 370,96 К; 97,81 °C |
| Температура кипения | 1156,1 К; 882,95 °C |
| Уд. теплота плавления | 2,64 кДж/моль |
| Уд. теплота испарения | 97,9 кДж/моль |
| Молярная теплоёмкость | 28,23[3] Дж/(K·моль) |
| Молярный объём | 23,7 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | кубическая объёмноцентрированная |
| Параметры решётки | 4,2820 Å |
| Температура Дебая | 150 K |
| Прочие характеристики | |
| Теплопроводность | (300 K) 142,0 Вт/(м·К) |
| Номер CAS | 7440-23-5 |
Познавательно: у космонавтов в коже накапливается связанный белками Na. Тело так реагирует на чуждые условия существования. Почему соединение выводится из клеток — ученые пока не поняли.
Минералы, месторождения
В природе встречаются минералы:
- мирабилит (глауберова соль);
- галит (каменная соль);
- бура (формула Na2В4О7 • 10Н2О);
- криолит.

Месторождений металлического натрия на планете нет. В любом месте (даже в пустынях) найдется вода, с которой металл мгновенно прореагирует.
Добыча и переработка
Для производства натрия ведется добыча минералов во многих странах:

Промышленное получение натрия по способу Девилля, распространённое в 19 веке. AC — железная трубка со смесью соды, угля и мела; B — холодильник Донни и Мареска; R — приёмник с нефтью
Основной способ промышленного получения натрия — электролиз NaOH или NaCl.
Возможно получение с помощью термического разложения NaN3.

Качественное определение натрия с помощью пламени — ярко-жёлтый цвет эмиссионного спектра «D-линии натрия», спектральный дублет 588,9950 и 589,5924 нм
Плюсы и минусы
Достоинства соединений натрия не перечислить. Самое главное — без него невозможна биологическая жизнь на планете.
К недостаткам можно отнести дороговизну натриевых реакторов (необходимость промежуточного контора, усиленные системы безопасности). Реакторы на БН дороже, чем ВВЭР (водо-водяные).
Натрий вокруг нас
Применение металла и его соединений чрезвычайно широко:
- Металлический Na работает теплоносителем в реакторах на быстрых нейтронах (БН) и в ионных ракетных двигателях.

Познавательно: поваренной солью (NaCl) пользуются все жители планеты (даже животные с удовольствием приходят на солончаки полакомиться солью.
Купить металл
Цена металлического Natrium за килограмм у разных производителей колеблется от 900 до 1500 руб/кг.

Мне 42 года и я специалист в области минералогии. Здесь на сайте я делюсь информацией про камни и их свойства — задавайте вопросы и пишите комментарии!
Формула металлического натрия
В обычных условиях натрий представляет собой серебристо-белый (в тонком слое — с фиолетовым оттенком), легкий, очень мягкий, низкоплавкий металл (относится к группе щелочных металлов) (рис. 1).
Пар натрия имеет темно-красный цвет и состоит из атомов Na (преобладают) и молекул Na2.
Весьма реакционноспособный; на воздухе покрывается оксидной пленкой (тускнеет), воспламеняется приумеренном нагревании. Устойчив в атмосфере аргона и азота. Сильный восстановитель; энергично реагирует с водой, кислотами, неметаллами.
Хорошо сохраняется под слоем бензина или керосина, легко суспендируется в кипящих инертных растворителях (толуол, ксилол, гептан, октан и др.). В инертной атмосфере расплавленный натрий быстро распределяется по поверхности некоторых твердых веществ (NaCl, Na2СО3, уголь, железо, Аl2О3, ZrO2), образуя серо-черные моноатомные покрытия. Окрашивает пламя газовой горелки в желтый цвет.

Рис. 1. Металлический натрий. Внешний вид.
Химическая формула металлического натрия
Химическое обозначение натрия – Na от латинского слова «natrium». Этот химический элемент расположен в третьем периоде в IА группе Периодической таблицы Д.И. Менделеева. Относится к элементамs-семейства. Металл. Относительная атомная масса натрия равна 22,9898 а.е.м.
Электронная формула металлического натрия
В ядре атома натрия содержится 11 протонов и 12 нейтронов (массовое число равно 23). В атоме натрия есть три энергетических уровня, на которых находятся 11 электронов (рис. 2).
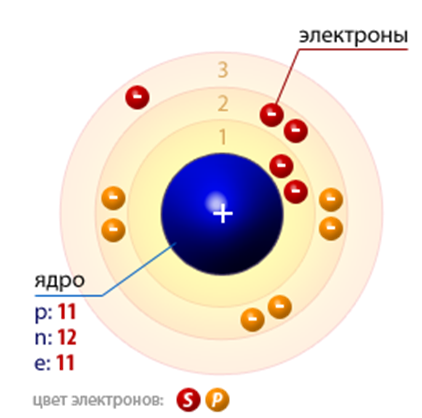
Рис. 2. Строение атома натрия.
Электронная формула атома натрия в основном состоянии имеет следующий вид:
Примеры решения задач
| Задание | Определите молекулярную формулу кальциевой селитры, в которой массовые отношения кальция, азота и кислорода равны 10:7:24. Относительная молекулярная масса кальциевой селитры 164. |
| Решение | Для того, чтобы узнать, в каких отношениях находятся химические элементы в составе молекулы необходимо найти их количество вещества. Известно, что для нахождения количества вещества следует использовать формулу: |
Найдем молярные массы кальция, азота и кислорода (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел). Известно, что M = Mr, значит M(Ca)= 40 г/моль, Ar(N)=14 г/моль, а М(O) = 32 г/моль.
Тогда, количество вещества этих элементов равно:
n (Ca) = m (Ca) / M (Ca);
n (Ca) = 10 / 40 = 0,25 моль.
n (N) = 7 / 14 = 0, 5 моль.
n (O) = 24 / 16 = 1,5 моль.
Найдем мольное отношение:
n(Ca) :n(N):n(O) = 0,25 : 0,5 : 1,5= 1 : 2 : 6,
т.е. простейшая формула соединения кальция, азота и кислорода имеет вид CaN2O6 и молярную массу 164 г/моль [M(CaN2O6) = Ar(Ca) + 2×Ar(N) + 6×Ar(O) = 40 + 2×14 + 6×16 = 40 + 28 + 96 = 164 г/моль]
Чтобы найти истинную формулу органического соединения найдем отношение полученных молярных масс:
Значит формула соединения кальция, азота и кислорода имеет вид CaN2O6или Ca(NO3)2. Это нитрат кальция.
| Задание | Установите массовую формулу вещества, содержащего 55,2% калия, 14,6% фосфора и 30,2% кислорода. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле: |
ω (Х) = n × Ar (X) / M (HX) × 100%.
Обозначим количество моль элементов, входящих в состав соединения за «х» (калий), «у» (фосфор) и «z» (кислород). Тогда, мольное отношение будет выглядеть следующим образом (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел):
x:y:z = ω(K)/Ar(K) : ω(P)/Ar(P) : ω(O)/Ar(O);
x:y:z= 55,2/39 : 14,6/31 : 30,2/16;
x:y:z= 1,4 : 0,5: 1,9 = 3 : 1: 4.
Значит формула соединения калия, фосфора и кислорода будет иметь вид K3PO4. Это фосфат калия.
Получение металлического натрия из средства для чистки труб! (Для химиков-энтузиастов)
Средство для чистки труб "Крот" - это раствор щелочи очень грязной щелочи.Можно ли получить чистый металлический натрий из этого раствора? Оказывается можно)))
В школе я с огромным интересом наблюдал за тем, как реагируют щелочные металлы с водой и мне всегда хотелось самостоятельно поэкспериментировать с такими веществами))
Если вас тоже завораживал металл плавающий по воде и выделяющий водород, то, наверное, вам будет интересно это видео)

Отлично. Теперь ждём "Кокаин из поваренной соли", "Виски из куриных потрошков" и другие полезные рецепты!
Именно таким образом сэр Хемфри Дэви и открыл натрий. Электролиз раствора едкого натра.
ну всё, теперь можешь пускаться во все тяжкие))
А, что еще можно сделать из крота?
Кстати, вопросик есть: Эта адская жидкость(крот имею ввиду) дюраль разъедает?

Реакция галлия и алюминия с прекрасной концовкой

Занимательные опыты по химии








Был бы у меня такой учитель

Ответ BabudaiAga в «Б - Баланс»
Если кого-то интересует проверка баланса своих кубиков - есть хороший способ без проведения 10000 бросков. Правда, это легко сделать только для пластиковых кубиков.
Для этого делается очень крутой солевой раствор. В простой воде кубик тонет, поэтому нужно воду сильно просолить, повысив ее плотность до того момента, что бы кубик плавал. После чего кубик кидается в этот раствор.
Куб находится во взвешенном состоянии, почти в невесомости, поэтому, если какая-то из граней перевешивает (кубик не сбалансирован), эта грань всегда будет тонуть - кубик проворачивается этой гранью вниз. И это легко увидеть, если попробовать чуть покрутить плавающий кубик пальцем. Сбалансированный куб держится любой гранью вверх, несбалансированный постоянно проворачивается в одно и то же положение. И скорость проворота в это положение показывает насколько куб несбалансирован.
Я так свои д20 кубы для настолок все проверял. Это намного быстрее и нагляднее, чем совершать 10000 бросков =)
Но с металлическими способ не канает. Ну, конечно, если у вас нет плошки с ртутью, что бы купать кубики в ней. =)

Продолжение поста «Б - Баланс»
Я уже говорил тебе, что такое безумие? Безумие — это точное повторение одного и того же действия, раз за разом, в надежде на изменение. Это и есть безумие.
(с) Ваас Монтенегро
По просьбам в комментариях под прошлым постом продолжаем тему баланса игровых костей.
Для ЛЛ: 10 000 бросков кубиков с Ozon. Потом ещё столько же бросков кубиков из магазина настолок. Потом четыре онлайн-генераторов кубов, тоже по 10 к роллов для каждого. Подведение итогов.
Объект исследования:
1) кубики из магазина настольных игр, набор 10 штук (250 р набор, по 25 р каждый);
2) самые дешёвые кубики от Ozon, набор 8 шт (на момент заказа 104 р, т.е. по 13 р каждый);
3) результаты генераторов: этого, этого, этого и вот этого (бесплатно, разумеется).
Как бросал: чтобы исключить влияние оператора, из говна и палок плотного картона сделал dice tower (благо, схему в интернете найти легко). Фотографировать этот шедевр орочьей инженерии, с вашего позволения, не буду: свою функцию выполняет, при бросках не деформируется, но выглядит неказисто.
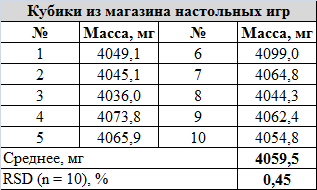
Кубики из магазина настолок: розового цвета, "для няшных варгеймов", как сказано на сайте. Не думаю, что со своими патлами и бородой я соответствую критериям няшности, но уж какие были в наличии. Размер: стандартные 16 мм. Материал: написано, что нефрит. Грани и углы хорошо сглажены: кубик катится долго, делая на столе не менее 5-6 оборотов. Матрица - правосторонняя. Материал не выглядит совершенно однородным, на гранях присутствует градиент цвета. Размер точек не отличается, сами точки залиты белой краской ниже уровня грани. Внешний вид:

Сравнение массы кубиков в наборе:
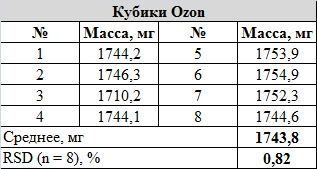
Кубики с Озона: меньше стандартных, всего 12 мм. 8 штук в наборе. Материал - АБС-пластик. Прозрачные, точки заглублены и маркированы красной, жёлтой и синей краской. Кубики, кажется, пытались сбалансировать: точка на грани 1 крупнее и глубже остальных. В толще материала 3 из 8 кубов имеют маленькие (менее 1 мм) пузырьки воздуха. Кубики с этим дефектом не исключал из выборки: проверим то, что пришло, "as is", никто ведь не будет рассматривать их так пристально во время игры. Грани и углы сглажены, куб катится хорошо. Матрица тоже правосторонняя. Внешний вид:

Т.к. в обоих случаях масса кубиков в наборе очень близка, принял решение кидать кубики каждого типа вместе, по 10 и 8 штук, для ускорения набора статистики. Иначе, думаю, к концу эксперимента кукушечка у меня отлетела бы окончательно.
Выгоняем котов (очень уж им хотелось присоединиться к новой весёлой игре) и начинаем. Результаты - в этом файле Excel (Яндекс.Диск). Далее для наглядности полученные результаты отнесены к "идеальным" 16,67% (1/6, столбец "Δ от нормы"). Для оценки полученных результатов использовал, как предложил уважаемый @fakir22, критерий хи-квадрат, только расчёт выполнил через функцию ХИ2ТЕСТ.
Результаты бросков для кубиков из магазина настолок:
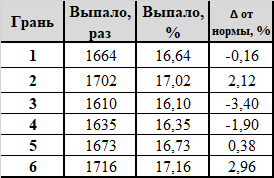
Максимальное отклонение от оптимального значения составило 3,40% (напомню, для кастомного кубика из предыдущего поста грань 6 выпадала на 9,74% чаще, а 1 - на 5,80% реже "положенного"). Для числа выпадений каждой грани RSD (n=6) 2,39%, χ^2 = 0,4451: опровергнуть гипотезу равной вероятности граней 1-6 не удалось.
Вытираем скупую мужскую слезу пот со лба, берём в руки кубики с Озона и бросаем их. правильно, ещё 10 000 раз. За окном уже брезжит рассвет и матерятся дворники. Результаты:
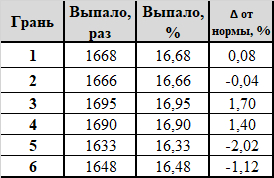
Признаться, я был удивлён. Самые дешёвые кубики, от которых не ждёшь никаких сюрпризов, показали весьма достойные результаты: RSD (n=6) 1,43%, χ^2 = 0,8891: очень. нет, ОЧЕНЬ хорошо. Очевидно, доказать неравновесность кубиков тоже не удалось. Кубики, по итогу, унёс на работу и раздарил коллегам (- Мужик, у тебя кубик есть? На, мужик, кубик).
В прошлый раз я сказал, что для нивелирования неравновесности физических дайсов стоит использовать онлайн-генераторы кубов. Чтобы не быть голословным, проверил четыре таких сайта из топа поисковика (те, что показывали полную выдачу по каждому "роллу": к этому моменту вносить результаты по одной цифре я был уже не в состоянии). Для каждого сайта делаем ещё по 10 000 "бросков" и переносим результаты в эксель.
Пикабу образовательный: теперь я знаю о возможности рассортировать данные из одной ячейки через опцию "Данные" - "Текст по столбцам" (может быть, кому-то пригодится). Полные результаты в расчётном файле по ссылке выше. Чтобы не растягивать, приведу только сводную таблицу (не реклама):
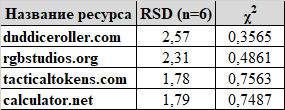
Т.о., все эти сайты дают правдоподобную картину случайного распределения результатов ролла.
Подведём итоги.
1) Если грани кубиков не имеют очевидных различий, скорее всего, распределение результатов ролла будет близко к нормальному (КАПИТАН ОЧЕВИДНОСТЬ, чёрт побери). Цена тут, вероятно, вторична.
2) При выборе кастомных костей надо быть очень осторожным. Некоторые мастера отдают предпочтение внешнему виду, по каким-то причинам (сложность ли производства, банальное попустительство или что-то ещё) забывая о балансе своих изделий.
3) Онлайн-генераторы (по крайней мере те, что я навскидку рассмотрел) дают вполне достоверную картину распределения вероятности выпадения костей. Но, разумеется, кому-то (мне, например) нравится момент бросания кубиков, в этом есть своя романтика.
Напоследок пара слов уважаемому (без сарказма) @cyberdicegames. Я ни в коем случае не ставлю под сомнение Ваше мастерство: безусловно, и кости и, особенно, коллекционные фигурки выглядят очень здорово, и я с интересом буду в дальнейшем следить за Вашими публикациями. Однако. Как там было сказано? Цитирую (орфография сохранена):
. когда мне пишут люди про баланс моих дайсов, обладая только теорией, (что у вас тут вырез на одной грани больше чем на другой и я УВЕРЕН ваши кубики НЕБАЛАНСНЫ), меня это всегда вызывает улыбку. все эти громкие заявления - пальца выделенного не стоят. . все эти люди, кто так яро выражали своё мнение про баланс - имели в своих коллекциях огромное количество дайсов просто с ужасным балансом.
Пальца выделенного, мда. Ну что же, вот я из интереса потратил своё время и теперь обладаю не только теорией, но и кучей практики (даже больше, чем хотелось бы). Самые дешёвые кубики, купленные на Озоне и в первом попавшемся магазине настолок, оказались сбалансироваными. Случайные онлайн-генераторы кубов - тоже выдают адекватные результаты. Но баланс как минимум некоторых моделей Ваших кубов, которые стоят в 69 (. ) раз дороже и которые Вы, по сути, рекламируете своими постами на Пикабу, объективно оставляет желать лучшего. Стильная, красивая, дорогая. игрушка.
Буду рад, если Вы аргументированно меня переубедите. Агрессивно отстаивая баланс своих дайсов, Вы раз за разом показываете кубик, насечки на гранях которого имеют равную длину (даже сделали, как я посмотрю, новую подпись к фото: "Perfect! Balanced Dice"). Вот только никто с этим и не спорил: например, ещё больше двух недель назад я говорил, что к этому кубику меньше всего вопросов. И даже Ваш эксперимент это подтверждает. Сомнения вызвали кубы с визуально различающейся длиной выточек, но все неудобные вопросы о них Вы игнорируете, приводите эмоциональные доводы без конкретных цифр или переходите на личности.
Вы заявляете: "самым важным элементом в моей работе является - качество", но отмахиваетесь от критики (я хотел, чтобы мои замечания были максимально обоснованными и конструктивными, сделав в общей сложности 30 000 физических роллов и 40 000 виртуальных): "мне не интересно доказывать элементарные вещи, которые каждый сам может осознать" и т.п. Это звучит инфантильно и непрофессионально.
Приглашаются: @arrraarrra (вопрос о виртуальных дайсах), @Deha4444, @ghostabv, @Whateveryouwish, @KAKAOCMETAHA, @dildus, @arigatan и остальные, спрашивавшие про баланс магазинных кубов.
НАТРИЙ — соль жизни
Соединения металлов натрия-калия контролируют солевой баланс в наших организмах. Нарушения этого баланса опасно для жизни. В составе крови соединения этих металлов создают своеобразный электролит, необходимый для работы любой клетки организма.
От Библии до наших дней
История героя статьи тянется с библейских времен. Именно в Библии упомянуто вещество, которым пользовались для мытья, отбеливания хлопковых тканей. В переводе слово νίτρον (нитрон) означает мыло или щелок.

Природной содой или щелоком из золы многие века люди пользовались для домашних нужд.
Свойства натрия

Натрий (natrium) относится к щелочным металлам, в таблице Менделеева имеет атомный № 11.
- Легко режется ножом.
- Чистый натрий имеет белый серебристый цвет; на воздухе быстро покрывается слоем оксида Na2O.
- Структура кристаллической решетки объемноцентрированная, кубическая.
- Natrium легче воды; если бросить кусочек в воду, он будет плавать на ее поверхности.
Металл настолько активный, что хранят его в минеральном масле или в керосине, без доступа воздуха.
- Натрий реагирует с разбавленными кислотами, как рядовой металл.
- В реакции с концентрированными кислотами образуются продукты восстановления.
- Бурная реакция с водой идет с выделением водорода, поэтому металл загорается или взрывается.
- Как все щелочные металлы, активно реагирует со многими неметаллами.
Известен один стабильный изотоп — 23-Na.
| Свойства атома | |
|---|---|
| Название, символ, номер | На́трий / Natrium (Na), 11 |
| Атомная масса (молярная масса) | 22,98976928 ± 0,00000002 а.е.м.[1] а. е. м. (г/моль) |
| Электронная конфигурация | [Ne] 3s1, 1s22s22p63s1 |
| Радиус атома | 190 пм |
| Химические свойства | |
| Ковалентный радиус | 154 пм |
| Радиус иона | 97 (+1e) пм |
| Электроотрицательность | 0,93 (шкала Полинга) |
| Электродный потенциал | -2,71 В |
| Степени окисления | −1 (в алкалидах)[2]; 0; +1 (наиболее частая) |
| Энергия ионизации (первый электрон) | 495,6(5,14) кДж/моль (эВ) |
| Термодинамические свойства простого вещества | |
| Плотность (при н. у.) | 0,971 г/см³ |
| Температура плавления | 370,96 К; 97,81 °C |
| Температура кипения | 1156,1 К; 882,95 °C |
| Уд. теплота плавления | 2,64 кДж/моль |
| Уд. теплота испарения | 97,9 кДж/моль |
| Молярная теплоёмкость | 28,23[3] Дж/(K·моль) |
| Молярный объём | 23,7 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | кубическая объёмноцентрированная |
| Параметры решётки | 4,2820 Å |
| Температура Дебая | 150 K |
| Прочие характеристики | |
| Теплопроводность | (300 K) 142,0 Вт/(м·К) |
| Номер CAS | 7440-23-5 |
Познавательно: у космонавтов в коже накапливается связанный белками Na. Тело так реагирует на чуждые условия существования. Почему соединение выводится из клеток — ученые пока не поняли.
Минералы, месторождения
В природе встречаются минералы:
- мирабилит (глауберова соль);
- галит (каменная соль);
- бура (формула Na2В4О7 • 10Н2О);
- криолит.

Месторождений металлического натрия на планете нет. В любом месте (даже в пустынях) найдется вода, с которой металл мгновенно прореагирует.
Добыча и переработка
Для производства натрия ведется добыча минералов во многих странах:

Промышленное получение натрия по способу Девилля, распространённое в 19 веке. AC — железная трубка со смесью соды, угля и мела; B — холодильник Донни и Мареска; R — приёмник с нефтью
Основной способ промышленного получения натрия — электролиз NaOH или NaCl.
Возможно получение с помощью термического разложения NaN3.

Качественное определение натрия с помощью пламени — ярко-жёлтый цвет эмиссионного спектра «D-линии натрия», спектральный дублет 588,9950 и 589,5924 нм
Плюсы и минусы
Достоинства соединений натрия не перечислить. Самое главное — без него невозможна биологическая жизнь на планете.
К недостаткам можно отнести дороговизну натриевых реакторов (необходимость промежуточного контора, усиленные системы безопасности). Реакторы на БН дороже, чем ВВЭР (водо-водяные).
Натрий вокруг нас
Применение металла и его соединений чрезвычайно широко:
- Металлический Na работает теплоносителем в реакторах на быстрых нейтронах (БН) и в ионных ракетных двигателях.

Познавательно: поваренной солью (NaCl) пользуются все жители планеты (даже животные с удовольствием приходят на солончаки полакомиться солью.
Купить металл
Цена металлического Natrium за килограмм у разных производителей колеблется от 900 до 1500 руб/кг.

Мне 42 года и я специалист в области минералогии. Здесь на сайте я делюсь информацией про камни и их свойства — задавайте вопросы и пишите комментарии!
Читайте также:
