Металлы антагонисты в организме
Обновлено: 28.04.2024
В данном обзоре рассматриваются витамины, минералы и микроэлементы, которые, как правило, входят в пищевые добавки. Основное внимание уделяется их способности взаимодействовать между собой при совместном приеме.
Статья опубликована
в «Международном журнале
медицинской практики», №1, 2005 г.
Литература
1. Shrimpton DH, RDAs – what do they really mean? The Pharmaceutical Journal 2002; 268:365–366.
2. Expert Group on vitamins and minerals. Safe upper levels for vitamins and minerals Food Standards Agency 2003: London UK.
3. Gregory J, Foster K, Tyler H, Wiseman M. The dietary and nutritional survey of British adults. HMSO 1990: London HK.
4. Finch S, Doyle W, Lowe C, Bates CJ, Prentice A, Smithers G, Clarke PC. Nutritional diet and nutrition survey.The Staionary Office 1998: London UK.
5. Mason J. Thiomolybdates: mediators of molybdenum toxicity and enzyme inhibitors. Toxicology 1986; 42: 99–109.
6. Brink EJ, Beynen AC. Nutrition and magnesium absorption: A review. Progress in Food and Nutrition Science 1992: 16: 125–162.
7. Ghishan FK, Said HM, Wilson PC. Intestinal transport of zinc and folic acid: a mutual inhibition effect. American Journal of Clinical Nutrition 1986; 43:258–262.
8. Agte VV, Pokniknar KM, Chiplonkar SA. Efect of riboflavin supplementation on zinc and iron absorption and growth performance in mice. Biological Trace Element Research 1998; 65: 109–115
9. Wolfe SA, Gibson RS, Gadowsky SL, O’Connor DL. Zinc status of a group of pregnant adolescents at 36 weeks gestation living in southern Ontario. Journal of the American College of Nutrition 1994; 13: 154–164
10. Agency for Toxic Substance and Disease Registry (ATSDR). Toxicological profile for selenium (update). US Department of Health and Human Services 1996: Washington DC, USA
11. AHFS Drug Information. American Hospital Formulary Service – Drug Information 94 (editor McEvoy GK). American Society of Hospital Pharmacists Inc 1994: Bethesda MD, USA
12. Herbert V, Drivas G, Foscaldi R, Manusselis C, Colman N, Kanazawa S, Das K, Gelernt M, Herzlich B, Jennings J. Multivitamin/mineral food supplements containing vitamin B12 may also contain analogues of vitamin B12. New England Journal of Medicine 1982: 255–256
13. Lynch SR. Interaction of iron with other nutrients. Nutrition Reviews 1997; 55: 102–110.
14. Hallberg L, Brune M, Evlandsson M. Calcium and iron absorption: mechanism of action and nutritional importance. European Journal of Clinical Nutrition 1991; 46: 317–327.
15. Wood RJ, Zheng JJ. High dietary calcium intakes reduce zinc absorption and balance in humans. American Journal of Clinical Nutrition 1997; 65: 1803–1809.
16. Ani M, Moshtaghie AA. The effect of chromium on parameters related to iron metabolism. Biological Trace Element Research 1992; 32: 57–64.
17. Lonnerdahl B. Bioavailability of copper. American Journal of Clinical Nutrtion 9196; 63:821S–829S.
18. Whittaker P. Iron and zinc interaction in humans. American Journal of Clinical Nutrition 1998; 68: 442S–446S.
19. Johnson MA, Murphy CL. Adverse effects of high dietary iron and ascorbic acid on copper status in copper–deficient and copper–adequate rats. American Journal of Clinical Nutrition 19898; 47: 96–101.
20. Rosander–Hulten L. Competitive absorption by manganese and zinc in humans. American Journal of Clinical Nutrition 1991: 152–156.
21. Powers HJ, Weaver LT, Austin S, Wright AJ, Fairweather–Tait SJ. Riboflavin deficiency in the rat: effects on iron utilisation and loss. British Journal of Nutrition 1991; 65: 487–496.
22. Said HM. Cellular uptake of biotin: mechanisms and regulation. Journal of Nutrition 1990; 129: 490S–493S.
23. Bloem MW. Interdependence of vitamin A and iron: an important association for programmes of anaemia control. Proceedings of the Nutrition Society 1995; 54: 501–508.
24. Matseiner JT. Mechanism of retinoic acid and squalene on vitamin K deficiency in the rat. Journal of Nutrition 1967; 91: 303–306.
25. Sakota O, Hosking D. Update on calcium and vitamin D metabolism. Current Orthopaedics 1999; 13: 53–63.
26. Hathcock JN, Hatton DG, Jemkins MY, McDonald JT, Sudaresan PR, Wilkening VL. Evaluation of vitamin A toxicity. American Journal of Clinical Nutrition 1990; 52: 183–202.
27. Kusin JA, Reddy V, Sivakumar B. Vitamin E supplements and the absorption of a massive dose of vitamin A. American Journal of Clinical Nutrition 1974; 27: 774–776.
28. Bauernfeind JC. The use of vitamin A: A Report of the International Vitamin A Consultative Group (IVACG) 1980.
29. Weir DG, Scott JM. Vitamin B1. in: Cobalamin in Modern Nutrition in Health and Disease (9th Edition); Editors Shils ME, Olson JA, Shike M, Ross AC, 1999; Williams and Wilkins: USA.
30. Gallop PM. Carboxylated calcium–binding proteins and vitamin K. New England Journal of |Medicine 1980; 302: 1460–1466.
31. Combs GF. Vitamin E in: The Vitamins. Fundamental aspects in nutrition and health 1992. Academic press Inc: London, UK.
32 Koyanagi T, Hareyama S, Kikuchi R. Effect of administration of thiamine, riboflavin, ascorbic acid and vitamin A to students on their pantothenic acid contents in serum and urine. Tohoku Journal of Experimental Medicine 1969; 98: 357–362.
33. Yacowitz H, Norris LC, Heuser GF. Evidence for an interrelationship between vitamin B12 and pantothenic acid. The Journal of Biological Chemistry 1951; 192:141–146.
34. Pudelkewicz C, Roderuk C. Pantothenic acid deficiency in the young guinea pig. Journal of Nutrition 1960; 70: 348–352.
35. Wapnick AA, Bethwell TH, Settel HC. The relationship between serum iron levels and ascorbic acid stores in siderotic Bantu. British Journal of Haematology 1970; 19:271–276.
36. Toth I, Bridges KR. Ascorbic acid modulates ferritin translation by an aconitase/IRP switch. Blood 1995; 86:127a.
37. DeLuca HF, Zierold C. Mechanisms and functions of vitamin D. Nutrition Reviews 1998; 56: S4–S10.
38. Shearer MJ. Vitamin K. The Lancet 1995; 345: 229–234.
39. Bok J, Faber JG, de Vries JA. The effect of pterylglutamic acid administration on the serum B12 concentration in pernicious anemia in relapse. Journal of laboratory and Clinical Medicine 1958; 51:667–671.
40. Norris JW, Pratt RF. A controlled study of folic acid in epilepsy. Neurology 1971; 21: 659–664.
41. Van den Berg GJ, Beynan AC. Influence of ascorbic acid supplementation on copper metabolism in rats. British Journal of Nutrition 1992; 68: 701–715.
42. Jacob RA, Skala JR, Omaye ST, Turnlund JR. Effect of varying ascorbic acid intakes on copper absorption and ceruloplasmin levels of young men. Journal of Nutrition 1987; 117:2109–2115.
43. Corrigan JJ, Marcus FI. Coagulopathy associated with vitamin E ingestion. Journal of the American Medical Association 1974; 230: 1300–1301.
44. Battger WJ, Olson R. Effect of ?–tocopherol and ?–tocopherolquinone on vitamin K dependent carboxylation in the rat. Federal Proceedings 1982; 41:344
45. Latymer EA, Coates ME. The effects of high dietary supplements of copper sulphate on pantothenic acid metabolism in the chick. British Journal of Nutrition 1980; 45: 431–439
46. Gray LF, Daniel LJ. Effects of the copper status of the rat on the copper–molybdenum–sulphate interaction. Journal of Nutrition 1964; 84: 31–37.
47. Nordic Project Group. Risk evaluation of essential trace elements – essential versus toxic levels of intake. Report of a Nordic Project Group. Nord 1995; 18.
48. Calvert H. An overview of folate metabolism: features relevant to the action and toxicities of antifolate anticancer agents. Seminars in Oncology 1999; 26: 3–10.
49. Koehler KM, Pareo–Tubbeh SL, Romero LJ. Folate nutrition and older adults:challenges and opportunities. Journal of the American Dietetic Association 1997; 97: 167–173.
50. Weir DG, Scott JM. Brain function in the elderly: role of vitamin B12 and folate. British Medical Buletin 1999; 55: 669–682.
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Влияние некоторых тяжелых металлов и микроэлементов на биохимические процессы в организме человека

библиографическое описание:
Влияние некоторых тяжелых металлов и микроэлементов на биохимические процессы в организме человека / Зинина О.Т. // Избранные вопросы судебно-медицинской экспертизы. — Хабаровск, 2001. — №4. — С. 99-105.
код для вставки на форум:
Одними из наиболее вредных для биосферы Земли загрязнений, имеющих самые разнообразные вредные последствия, как для здоровья людей, так и для жизнедеятельности живых организмов, являются загрязнения тяжелым и металлами. Наряду с пестицидами, диоксинами, нефтепродуктами, фенолами, фосфатами и нитратами тяжелые металлы ставят под угрозу саму существование цивилизации. Увеличивающийся масштаб загрязнений окружающей среды оборачивается ростом генетических мутаций, раковых, сердечно-сосудистых и профессиональных заболеваний, отравлений, дерматозов, снижением иммунитета и связанных с этим болезней. В подавляющем большинстве случаев первоисточником загрязнений является экологически безграмотная деятельность человека. Среди опасных для здоровья веществ тяжелые металлы и их соединения занимают особое место, та к как являются постоянными спутниками в жизни человека.
Очень часто многоэлементный анализ используют в медицине при выяснении причин острых и хронических отравлений, а так же при лечении профессиональных болезней, связанных с хроническим воздействием тяжелых металлов на организм в условиях реального производства и экологических особенностей.
В химико-токсикологическом анализе применяется метод минерализации при исследовании биологического материала (органов трупов, биологических жидкостей, растений, пищевых продуктов и др.) на наличие та к называемых «металлических ядов». Эти яды в виде солей, оксидов и других соединений в большинстве случаев поступают в организм через пищевой канал, в соответствующих отделах которого они всасываются в кровь и вызывают отравления.
Важнейшим и «металлическими ядами » являются соединения бария, висмута, кадмия, марганца, меди, ртути, свинца, серебра, таллия, хрома, цинка и соединения некоторых неметаллов (мышьяка, сурьмы). Ряд перечисленных выше химических элементов, соединения которых являются токсичными. В небольших количествах содержатся в тканях организма как нормальная их составная часть, В виду незначительных количеств этих химических элементов. Содержащихся в организме, их называют микроэлементами.
Установлены предельно-допустимые концентрации микроэлементов в организме.
- Каждый элемент имеет присущий ему диапазон безопасной экспозиции, который поддерживает оптимальные тканевые концентрации и функции;
- У каждого элемента имеется свой токсический диапазон, когда безопасная степень его экспозиции превышена [Mertz, 1982].
Правила Мертца особенно важны для токсикологической химии. Металлы с малыми значениями диапазона концентраций условно отнесены в разные группы по «степени опасности» (чем меньше диапазон, тем «опаснее»):
- As, Be, Cd, Hg, Pb, Tl, Zn;
- B, Co, Cr, Cu, Mo, Ni, Sb, Sc;
- Ba, Mn, Sr, V, W.
Общепризнанно, что наиболее опасными элементами для человека, да и вообще для теплокровных животных, являются кадмий, ртуть и свинец (Cd, Hg, Pb).
Кадмий вызывает отравление, описанное в Японии как болезнь «итаи-итаи» (ох-ох). Название болезни происходит от боли в спине и ногах, сопровождающей остеомаляцию (декальцификацию) костей, что приводит к ломкости костей. Хроническое отравление кадмием разрушает печень и почки, приводя к сильнейшему нарушению функции почек. Избыток кадмия нарушает метаболизм металлов, особенно железа и кальция, нарушает действие цинковых и иных металло-ферментов, блокирует сульфгидрильные группы ферментов, нарушает синтез ДНК. Кадмий легко замещает металлфлавопротеиновых комплексах, где главенствующую роль играют железо и молибден, нарушая двухстадийный процесс окисления.
Ртуть токсична в любой своей форме. Ртуть в природных условиях довольно быстро превращается в летучее токсическое соединение — хлорид метилртути. В организме ионы метилртути быстро попадают в эритроциты, печень и почки, оседают в мозге, вызывая серьезные необратимые кумулятивные нарушения ЦНС. Это приводит, к конце концов, к общему и церебральному параличу, деформации конечностей, особенно пальцев, затрудненному глотанию, конвульсиям и смерти. Ртуть блокирует активность ряда важнейших ферментов, в частности карбоангидразы, карбоксипептидазы, щелочной фосфатазы. Легко замещает кобальт в корриноидах, извращая метаболические реакции, связанные с витамином В12. Повреждение механизма биосинтеза ДНК из-за недостаточности витамина В12 является причиной мегалобластических анемий и наиболее распространенной формы - пернициозной анемии, что приводит к дегенеративным изменениям нервной системы.
Свинец известен как токсическое вещество почти 5 тысяч лет среди греческих и арабских ученых. В современных условиях наибольшим источником загрязнения свинцом среды обитания считаются выхлопы бензиновых двигателей автомашин, поскольку в бензин добавляется тетраэтилсвинец для повышения октанового числа. Свинец препятствует одной из ступеней биосинтеза гема, считается сильнейшим нейротоксином, вызывает повышенную агрессивность. Хроническое отравление свинцом постепенно приводит к нарушениям функций почек, нервной системы, анемии. Токсичность свинца увеличивается при недостатке в организме кальция и железа. Свинец блокирует SH-группы белков, образуя комплексы с фосфатными группами рибозы у нуклеотидов, особенно у цитидина, и тем самым быстро разрушает РНК, ингибирует ферменты, в частности карбоксипептидазу.
Мышьяк относится к числу наиболее сильных и опасных ядов. В присутствии кислорода быстро образует очень ядовитый мышьяковистый ангидрид. При пероральном отравлении высокая концентрация мышьяка наблюдается в желудке, кишечнике, печени, почках и поджелудочной железе, при хроническом отравлении постепенно накапливается в коже, волосах и ногтях. Из-за ингибирования различных ферментов нарушает метаболизм. В процессе отравления первыми страдают аксоны, что приводит к периферической нейропатии и параличу конечностей. Мышьяк считается канцерогенным для человека.
Таллий очень токсичен, зачастую его называют «химическим СПИДом». Таллий, проникая через клеточные мембраны, образует сильные комплексы, например, нерастворимый комплекс с рибофлавином. Это приводит к нарушению метаболизма серы и разрушению иммунной системы. Отравление таллием приводит к гастроэнтеритам, периферической нефропатии, при большой абсорбции к смерти. Через 2-3 недели после небольшого отравления у человека выпадают волосы.
Цинк в виде двухвалентного элемента входит в состав свыше 20 ферментов, включая участвующие в обмене НК. Большая часть цинка в теле человека находится в мышцах, а самая высокая концентрация — в простате. В крови он присутствует в эритроцитах как кофактор в карбоангидразе. Избыток цинка может разбалансировать метаболические равновесия других металлов. Разбалансировка отношения цинк/медь является главным причинным фактором в развитии ишемической болезни сердца. Избыточное потребление солей цинка может приводить к острым кишечным отравлениям с тошнотой. В общем, цинк не очень опасен, а возможность отравления, вероятнее всего зависит от совместного присутствия токсичного кадмия.
Медь является необходимым кофактором для нескольких важнейших ферментов, катализирующих разнообразные окислительно-восстановительные реакции, без которых нормальная жизнедеятельность невозможна. Медь входит в качестве необходимого элемента в состав цитохромоксидазы, тироназы и других белков. Их биологическая роль связана с процессами гидроксилирования, переноса кислорода, электронов и окислительного катализа. В тканях здорового организма концентрация меди в течение всей жизн и поддерживается строго постоянной. В норме существует система, препятствующая непрерывному накоплению мед и в тканях путем ограничения ее абсорбции ил и стимуляции ее выведения. Хронический избыток меди в тканях При соответствующих заболеваниях вызывают токсикоз : ведет к остановке роста, гемолизу, снижению содержания гемоглобина, к деградации тканей печени, почек, мозга. Около 95 % меди в организме присутствует в составе гликопротеина крови церулоплазмина. Известен факт недостатка этого белка При болезни Вильсона-Коновалова - врожденном дефиците метаболизма (гепатолентикулярная дегенерация). Из-за генетического дефекта в синтезе церулоплазмина его содержание в крови резко снижено. В результате медь не связывается в комплекс с нормальной для организма константой устойчивости. Это приводит к недостатк у мед и в цеп и реакций метаболизма, приводящей к естественному для здорового организма синтез у соединительной ткани. Для осуществления нормального процесса сшивки мономеров эластина и коллагена не хватает активной Си-лизолоксидазы. С другой стороны «освободившиеся» ионы меди, лишившись по сути единственного нормального потребителя, откладываются в специфических тканях (печень, ядра мозга, почки, эндокринные железы, радужная оболочка глаз), где оказывают прямой токсический эффект. Создается парадоксальная ситуация избытка меди в специфических тканях при ее недостатке в нормальной цепи метаболизма.
Хром один из наименее токсичных элементов. При острых отравлениях накапливается во внутренних органах. Считается, что трехвалентный хром в виде комплекса с никотиновой кислотой и алифатическим и аминокислотам и работает в организме в качестве «фактора толерантности к глюкозе». Его действие заключается в усилении гипогликемического действия инсулина. В обычных условиях отрицательным является недостаток хрома в организме.
Сурьма — менее токсичный элемент, чем мышьяк. При отравлении накапливается в скелете, почках, селезенке.
Барий в виде двухвалентного катиона ядовит из-за его антагонизма с калием (но не с кальцием). У обоих ионные радиусы подобны. Барий является мускульным ядом. Абсорбированный барий откладывается в костях и в пигментной оболочке глаз.
Марганец — элемент почти нетоксичен, особенно в виде двухвалентного иона. В виде перманганат-иона токсичен из-за окислительной способности. Отравление происходит в случае вдыхания оксида в промышленном производстве.
Серебро. Элемент накапливается в печени и в меньших количествах, но равномерно, в остальных органах и тканях. Отложения серебра отмечено в клубочках почек и в субэпителиальных слоях кож и («аргироз» — голубоватое окрашивание кожи).
При различных патологиях имеет место изменение содержания микроэлементов в организме. Исследование сыворотки больных острым вирусным гепатитом, а также при постгепатитном циррозе показало, что у пациентов с острым гепатитом концентрация цинка почти не менялась, концентрация кадмия значительно увеличивалась. Концентрация меди и марганца незначительно уменьшалась. При хроническом гепатите и постгепатитном циррозе содержание меди и цинка в сыворотке уменьшалось, а кадмия увеличивалось. Содержание марганца почти не менялось. Выделение с мочой меди, превышающее 115 мкг/сутки и сопровождаемое низким содержанием в крови, свидетельствует о синдроме системного заболевания, например, болезни Вильсона-Коновалова. Повышенное содержание в крови и моче алюминия, особенно у пожилых людей, может сопровождать энцефалопатию, болезнь Альцгеймера и другие формы слабоумия, а при почечной недостаточности также остеомаляцию и микроцитарную гипохромную анемию. Повышенное содержание в крови и моче лития характерно для больных с патологией мочевыделительной системы, нефропатиями.
Повышенное относительно ПДК содержание в биологических жидкостях отдельных тяжелых металлов может свидетельствовать о хроническом воздействии токсикантов на организм и перенапряжении работы почек и печени. Это требует мер по очистке организма от избытка тяжелых металлов, например, с помощью препаратов с полианионами (морская капуста) в незапущенных случаях.
Повышенное содержание в крови и моче наиболее токсичных тяжелых металлов (кадмия, ртути, свинца) требует энергичных мер по их выведению, поскольку их избыток разрушает нервную, сердечно-сосудистую и иммунную системы.
Повышенное содержание в крови и моче таллия и селена может пролить свет на причины облысения и плохое самочувствие таких больных.
Повышенное содержание в организме бора должно привлечь внимание к тяжелым металлам, содержание которых не превышает ПДК, т.к. он оказывает синергистское (усиливающее) влияние на их токсические свойства.
Токсичность «металлических ядов» объясняется связыванием их с соответствующими функциональными группами белковых и других жизненно важных соединений в организме. В результате нарушаются нормальные функции соответствующих клеток и тканей в организме, и наступает отравление, которое в ряде случае в заканчивается смертью.
похожие статьи
Анализ причин насильственной смерти в результате отравления за 2015–2019 гг. (по данным норильского отделения Красноярского краевого бюро судебно-медицинской экспертизы) / Кошак К.В., Коплатадзе И.Г., Толмачева С.К., Слащинин Г.А., Алябьев Ф.В., Фомина И.Е., Аверченко И.В., Хлуднева Н.В., Бокиев М.У., Закурдаева А.Д. // Избранные вопросы судебно-медицинской экспертизы. — Хабаровск, 2020. — №19. — С. 73-75.
Редкая ошибка / Вонгродзский В.А. // Судебно-медицинская экспертиза. — М.: Изд-во Наркомздрава, 1928. — №8. — С. 116-119.
Уголь, как противоядие при разных отравлениях / Лейбензон Е.А. // Судебно-медицинская экспертиза. — М.: Изд-во Наркомздрава, 1928. — №8. — С. 45-60.
К вопросу о химическом распознавании сероуглерода в крови при отравлениях / Кромер Н. // Судебно-медицинская экспертиза. — М.: Изд-во Наркомздрава, 1928. — №8. — С. 42-44.
Отравление депиляторием / Аджиев Б.Л. // Судебно-медицинская экспертиза. — М., 1968. — №4. — С. 43-44.
Витаминно-минеральная недостаточность
Мы намеренно объединили понятия «витаминная» и «минеральная» недостаточность в заголовке статьи, ведь, как правило, организм современного человека испытывает дефицит не отдельных витаминов или минералов, а определенных их сочетаний. Чаще всего это соче

Мы намеренно объединили понятия «витаминная» и «минеральная» недостаточность в заголовке статьи, ведь, как правило, организм современного человека испытывает дефицит не отдельных витаминов или минералов, а определенных их сочетаний. Чаще всего это сочетания синергично действующих микронутриентов. Наглядный пример — комплексная недостаточность витаминов В9 (фолиевой кислоты) и В12. Достаточное поступление в организм второго из них — необходимое условие адекватного усвоения первого. Поэтому недостаток витамина В12 может стать причиной дефицита фолиевой кислоты.
Биологические функции витаминов и минералов
Большинство витаминов участвует в метаболизме в качестве коферментов, некоторые из них являются предшественниками гормонов (витамины А и D) или антиоксидантами (витамины С и Е). Соответственно, недостаток витаминов обусловливает нарушение обменных процессов, иммунной реактивности, роста и регенерации тканей, репродуктивной функции и др.
Диагностика этих состояний, как правило, затруднена в связи с отсутствием патогномоничной клинической картины полигиповитаминоза и наличием у пациента патологии внутренних органов, симптомы которой занимают ведущее место.
Столь же велико значение для организма человека минеральных веществ. Некоторые из них считаются жизненно необходимыми — эссенциальными. Это в первую очередь такие макроэлементы (составляющие более 0,005% массы тела), как кальций, фосфор, калий, хлор, натрий; микронутриенты (менее 0,005% массы тела) — железо, медь, йод, селен и др. На сегодняшний день установлено, что клинически значимыми можно считать 32 элемента. При выраженном снижении их содержания в организме развивается более или менее характерная клиническая картина. Среди таких микроэлементов — молибден, марганец, бром и др.
Участие минеральных веществ (микро- и макроэлементов) в метаболизме связано с построением скелета (кальций, фосфор), поддержанием осмотических свойств (натрий, калий), кроветворением (железо, медь). Многие из них являются активаторами и кофакторами ферментов (магний, медь, железо, селен и др.), входят в состав гормонов и т. п. Йод, например, входящий в состав тиреоидных гормонов, оказывает анаболический эффект, стимулирует рост и формирование органов и тканей.
Выполнять свои специфические функции витамины и минеральные вещества могут только при условии их нормального усвоения, переноса в ткани, дальнейшего перехода в активное или неактивное состояние и вывода из организма. При этом синергизм или антагонизм взаимодействия некоторых микронутриентов может проявляться на стадии метаболизма.
Так, аскорбиновая кислота способствует превращению фолиевой кислоты в активные коферментные формы и восстановлению окисленной формы токоферола [1], а витамин D необходим для адекватного усвоения и утилизации кальция [2]. Известно много фактов, свидетельствующих и об антагонизме микронутриентов, например никотиновая и аскорбиновая кислоты разрушают витамин В12 [3].
Причины дефицита витаминов и минералов
Недостаток микронутриентов при обычном питании развивается практически неизбежно. Причин этого несколько. Основная состоит в том, что потребность в микронутриентах эволюционно сформировалась в условиях, когда человек в день затрачивал (и потреблял) 5000 ккал, а сейчас наши энергетические затраты в среднем составляют 2500 ккал — потребляя в 2 раза меньше пищи, мы недобираем половину необходимого количества микронутриентов.
Положение усугубляют: вредные привычки (курильщикам требуется дополнительно 35 мг витамина С); несовершенство пищевых технологий (потеря 80–90% витаминов группы В на пути от зерна до хлеба); загрязнение среды обитания (повышенный расход витаминов-антиоксидантов); геохимические особенности (низкое содержание йода в воде).
Ряд заболеваний внутренних органов приводит к снижению содержания витаминов в организме: при болезни Аддисона— Бирмера, анацидном гастрите, дифиллоботриозе, специфической мальабсорбции нарушается абсорбция витамина В12. Энтерит, сопровождающийся синдромом мальабсорбции даже на ранних стадиях способен привести к выраженному снижению содержания в организме витамина В6.
Длительный прием некоторых лекарственных препаратов может явиться причиной дефицита в организме ряда витаминов. Прием эстрогенсодержащих контрацептивов может вызвать недостаток пиридоксина. Снижение уровня последнего в организме также отмечается при длительном применении некоторых антибиотиков, сульфаниламидов, фтивазида, изониазида, циклосерина.
По данным литературы, в наибольшей мере на снижение показателей здоровья нации в настоящее время оказывает влияние дефицит витаминов А, С, Е, В1, В2, фолиевой кислоты и минеральных веществ: кальция, железа, йода, селена [4]. В связи с тем, что органы здравоохранения в настоящее время практически лишены возможности широко обследовать население на предмет выявления уровня содержания витаминов и микроэлементов в различных регионах, можно сделать вывод, что данная проблема стоит намного острее, чем это может показаться на первый взгляд.
В нынешних условиях речь идет даже не о необходимости профилактики дефицита, а о лечении полигиповитаминоза, сочетающегося с полигипомикроэлементозом. При этом повсеместному и регулярному (вне зависимости от сезона) приему витаминеральных препаратов нет альтернативы. В этой связи важно, чтобы при создании препаратов учитывался комплексный характер дефицита витаминов и минералов.
Взаимодействия микронутриентов
Биохимические и физиологические функции ряда эссенциальных микронутриентов к настоящему времени достаточно хорошо изучены. Исследования продемонстрировали, в частности, наличие связей в метаболических путях многих витаминов и минералов и привели ученых к выводу об их взаимодействии.
Это перспективное с научной и практической точки зрения направление исследований еще далеко не исчерпано, однако результаты некоторых из них уже стали общепризнанными и используются при разработке и создании витаминных препаратов.
Наиболее полные обзоры результатов таких исследований представлены в недавно опубликованных статьях [5, 6].
Современной наукой доказано более 20 фактов взаимодействия витаминов и минералов, как положительных (синергизм), так и отрицательных (антагонизм).
Синергизм микронутриентов впервые стали учитывать в лечебных витаминных препаратах направленного действия, например, для лечения остеопороза (кальций и витамин D), в антиоксидантных комплексах (витамины А и С) и т. п.
В профилактических поливитаминных препаратах, содержащих полный набор витаминов и эссенциальных микроэлементов, т. е. состоящих из десятков компонентов, требуется учитывать и антагонистические взаимодействия. Особенно много конкурентных или антагонистических взаимодействий известно в отношении минералов. Например, лечебные антианемические железосодержащие средства не рекомендуется сочетать с препаратами, содержащими кальций. По этой же причине их не следует запивать молоком [7].
Учет подобных рекомендаций необходим и при разработке составов поливитаминных комплексов, предназначенных для профилактического приема в группах риска, так как доказано, что усвоение железа из поливитамина может снизиться вдвое, если в состав того же препарата включен кальций. К сожалению, очень часто женщинам детородного возраста рекомендуют такие поливитамины именно для восполнения потерь железа.
Практическим результатом научных исследований, посвященных взаимодействию витаминов и минералов, стало разделение суточной дозы необходимых организму компонентов. Так, вещества-антагонисты включаются в разные таблетки, а синергисты объединяются в одной. Раздельный прием таблеток с интервалом несколько часов исключает возможность антагонистического взаимодействия в лекарственной форме во время хранения, на этапе высвобождения действующего начала из таблетки, в процессе всасывания, распределения и выведения из организма.
Подобный подход к разработке профилактических комплексов витаминов и минералов позволяет учесть все известные сегодня взаимосвязи между микронутриентами: в процессе производства и хранения, при усвоении в пищеварительном тракте, при включении в обменные процессы организма — и получить максимально возможный клинический эффект от применения таких препаратов.
Витаминная профилактика
Значение взаимодействий между ингредиентами поливитаминных препаратов исследователи до конца осознали относительно недавно. Но этот новый подход уже успешно реализуется производителями, которые стремятся к созданию наиболее рациональных витаминно-минеральных комплексов.
Широкая витаминная профилактика — результат развития науки о витаминах. Это направление бурно развивалось в ХХ в. и принесло исследователям четыре нобелевские премии. В 1920 г. были известны только два витамина: А и В (под витамином В подразумевались водорастворимые витамины). В 1955 г. была установлена структура последнего из общепризнанных ныне витаминов — В12, а производство его началось только в 1973 г.
Таким образом, широкое применение витаминных комплексов началось только в последней четверти ХХ в. В настоящее время, по данным исследовательской компании «Комкон-Фарма», витамины принимают 30 млн жителей России (20% населения). К большому сожалению, число потребителей витаминов не увеличивается уже несколько лет. Только треть из этих 30 млн человек использует для профилактики полноценные комплексы витаминов и минералов, остальные продолжают принимать либо монопрепараты (витамин С), либо дешевые несбалансированные комплексы, причем прием витаминов ограничивается лишь холодным временем года.
В современных условиях, когда дефицит микронутриентов носит характер сочетанной недостаточности, проявляется практически во всех группах населения и регионах и существенно не ослабевает в летний период, эффективность такой профилактики близка к нулю. Понятно, что основная причина использования устаревших препаратов — экономическая, но большую роль играет и осведомленность как специалистов, так и пациентов. Для многих людей «витамин» и «витамин С» своего рода синонимы. Некоторые до сих пор считают, что, съев за лето несколько килограммов фруктов из собственного сада, можно «зарядиться» витаминами на несколько месяцев.
Такие стереотипы ломать очень трудно. По данным компании «Комкон-Фарма», число потребителей полноценных комплексов витаминов и минералов растет приблизительно на 1 млн человек в год. При сохранении нынешних тенденций лишь через 20 лет устаревшие препараты будут вытеснены с рынка.
Современные поливитаминные препараты
Современные комплексы содержат обычно все 13 общепризнанных витаминов и основные микроэлементы в дозировках, обеспечивающих физиологические потребности.
Летом этого года введен в действие документ «Рекомендуемые уровни потребления пищевых и биологически активных веществ» [8]. В этих методических рекомендациях кроме адекватных уровней потребления витаминов и минералов устанавливаются верхние допустимые уровни потребления. В соответствии с вышеуказанными рекомендациями, для всех микронутриентов верхние допустимые уровни в несколько раз превышают адекватные уровни потребления. Это означает, что вероятность передозировки при использовании современных комплексных препаратов длительное время крайне низка. Таким образом, развенчивается миф, в который до сих пор верили даже некоторые врачи, об опасности гипервитаминозов при приеме поливитаминов на фоне якобы достаточного поступления эссенциальных микронутриентов с пищей.
По данным многочисленных исследований, в ходе которых проводились длительные наблюдения за людьми, принимавшими витамины и минералы в лечебных дозах, неблагоприятных клинических эффектов при этом не наблюдалось.
Настало время перейти от обсуждения причин и последствий гиповитаминозов к проблеме рационального выбора наиболее эффективных препаратов, учитывающих комплексный характер дефицита витаминов и минералов для данного региона.
Предпочтение, несомненно, следует отдавать средствам, которые созданы с учетом взаимодействия компонентов и состоят из нескольких таблеток, не содержащих антагонистических пар микронутриентов. Микронутриенты, образующие синергичные комбинации, должны при этом находиться в одной таблетке и, следовательно, поступать в организм одновременно. Такой принцип обеспечивает адекватное усвоение и максимальную активность всех биологически активных компонентов препарата.
Более того, при использовании такого подхода снижается вероятность развития и степень выраженности проявления некоторых реакций «аллергического типа» (индивидуальной непереносимости). Имеются в виду такие реакции, которые ярче проявляются при одновременном поступлении в организм двух определенных микронутриентов, чем в случае их раздельного приема [9]. Еще одним способом борьбы с возможными неблагоприятными реакциями является использование менее «опасных» в этом отношении форм витаминов (например, никотинамида, а не никотиновой кислоты) [10].
Синтетические витамины, входящие в состав витаминных препаратов, по своей химической структуре полностью идентичны природным аналогам, входящим в состав пищевых продуктов. При этом синтетические аналоги не только не уступают природным в эффективности физиологического воздействия на организм (что доказано многочисленными исследованиями), но и имеют ряд преимуществ. Благодаря высокой степени очистки и использованию современных технологий в производстве они менее аллергогенны. Рядом исследователей доказано, что биодоступность синтетических аналогов витамина Е значительно выше [11] .
Фармакоэкономические аспекты витаминотерапии
Поскольку, как мы уже говорили, нынешняя популярность малоэффективных профилактических средств объясняется в основном экономическими причинами, следует сказать несколько слов о слагаемых цены и качества поливитаминов.
Сегодня на рынке представлено несколько крупных западных химико-фармацевтических компаний, которые при больших объемах выпуска могут обеспечить производителей поливитаминов высококачественными ингредиентами по достаточно низкой цене. Большинство отечественных и импортных производителей поливитаминов используют именно эти субстанции.
При этом в цене препаратов стоимость активных субстанций составляет лишь 5–10% и никто из серьезных производителей не пытается экономить, внося в поливитамины дешевые и менее качественные субстанции. Большинство стоящих на аптечных полках поливитаминов по составу и качеству компонентов одинаковы. Разброс же в ценах объясняется различием в затратах на производство, упаковку, рекламу, дистрибьюцию.
Существенными для потребителя преимуществами (более выраженной эффективностью, меньшей вероятностью развития нежелательных реакций) отличаются лишь самые современные комплексные препараты, при создании которых производители учитывали принцип взаимодействия компонентов. Усвояемость некоторых витаминов и минералов из «однотаблеточных» препаратов на 30–50% ниже, чем из комплексов, представленных несколькими препаративными формами. Не менее важно и то, что потери активности при объединении всех компонентов в одной таблетке неодинаковы для разных микронутриентов и трудно предсказуемы.
Попытки решить проблему, просто разделив суточную дозу на несколько приемов (одинаковые по составу таблетки с уменьшенным содержанием всех компонентов) или принимая витамины отдельно от минералов (одна таблетка с витаминами, а другая — с минералами), несостоятельны. В первом случае взаимодействие компонентов не учитывается вовсе, а во втором — не принимаются во внимание все антагонистические пары типа витамин–витамин и минерал–минерал. Как уже говорилось выше, особенно много антагонистических взаимодействий выявлено в отношении минералов, что объясняется наличием для некоторых из них общих транспортных механизмов и, соответственно, конкуренцией за усвоение. Отличительной чертой оптимизированных по усвоению и активности витаминно-минеральных комплексов является использование принципа сочетаемости компонентов — объединение в каждой таблетке комплекса только «дружественных» витаминов и минералов, при этом антагонисты оказываются в разных таблетках.
Производство таких витаминно-минеральных комплексов, состоящих из нескольких препаративных форм с тщательно подобранными составами, естественно, является технологически более сложным и обходится дороже, по сравнению с традиционными поливитаминами, в которых все ингредиенты собраны в одну таблетку.
Тем не менее на российском рынке такие препараты уже появились. Причем отечественные и недорогие. Их состав соответствует установленным в России нормам, обеспечивающим физиологические потребности организма, а эффективность определяется не только высоким качеством компонентов (витаминов и минералов), но и достигается благодаря учету их взаимодействий.
Литература
- Sokol R. J. Vitamin E. In Ziegel E. E. and Filer L. J. (eds), Present knowledge in nutrition, 7th ed, 1996. — ILSI Press, Washington, DC. — Р. 130–136.
- Arnaud C. D. Calcium homeostasis: regulatory elements and their integration. Federation Proceedings, 1978, 37:2557–2560.
- Тутельян В. А., Спиричев В. Б., Суханов Б. П., Кудашева В. А. Микронутриенты в питании здорового и больного человека. — М.: Колос, 2002.
- Коровина Н. А., Захарова И. Н., Заплатников А. Л., Обыночная Е. Г. Дефицит витаминов и микроэлементов у детей: современные подходы к коррекции: Методическое пособие. — М.: Медпрактика-М, 2004.
- Ших Е. В. Рациональная витаминотерапия с точки зрения взамодействий// Фармацевтический вестник. — 2004. — № 11(332). — С. 8–9.
- Shrimpton D. H. Nutritional implications of micronutrients interactions. Chemist and Druggist, 2004, 15 May. — Р. 38–41.
- Yip R., Dallman P. R. Iron. In Ziegel E. E. and Filer L. J. (eds), Present knowledge in nutrition, 7th ed, 1996. ILSI Press, Washington, DC. — Р. 277–292.
- Рекомендуемые уровни потребления пищевых и биологически активных веществ: Методические рекомендации МР 2.3.1. 1915-04 (утверждены 2 июля 2004 г.). — М., 2004.
- Машковский М. Д. Лекарственные средства. — 14-е издание.- М.: Новая волна, 2000. — Т. 2.
- Mrocheck J. E., Jolley R. L., Young D. S., Turner W. J. Metabolic response of humans to ingestion of nicotinic acid and nicotinamid. Clinical Chemistry, 1976, 22:1821–1827.
- Батурин А. К. Медицинская газета, 2001, январь, № 5.
Е. В. Ших, доктор медицинских наук
Институт клинической фармакологии, Москва
Антагонизм и синергизм макро- и микроэлементов

20.12.2017
Макро- и микроэлементы, составляющие основу питания и оказывающие влияние на жизнедеятельность не только растений, но и всех живых организмов, находятся в тесном взаимодействии друг с другом. Поэтому главным фактором, обеспечивающим нормальный рост, развитие и функционирование культур, является соблюдение правильного баланса химических составляющих в питательной среде и в самом растении.
Всем культурам, в зависимости от их жизненного цикла, генотипических особенностей их биохимического состава и окружающей среды, требуется определенное соотношение питательных веществ. Этот баланс имеет более важное значение, чем фактическая концентрация отдельных элементов в питательном растворе. Ни один химический элемент в природе не действует изолированно от других.
При этом правильное соотношение микроэлементов в питании с учетом их взаимодействия между собой является не менее значимым и сложным, чем баланс макроэлементов. Чтобы обеспечить растения сбалансированным составом элементов, необходимо учитывать не только их физиологическую роль в жизни культур по отдельности, но и оказываемое влияние на растительный организм в результате их совместного действия.
Почти все элементы, входящие в состав питательных веществ, находятся между собой в одной из двух форм взаимодействия: антагонистической либо синергической. Игнорирование этого фактора приводит к несбалансированным реакциям внутри самого растения, в результате чего оно получает стресс, который может оказаться губительным.
Антагонизм между элементами возникает в том случае, если их общее участие в химических реакциях приводит к ухудшению действия одного из них. Так, избыток одного элемента может снижать уровень поглощения корневой системой растения другого элемента. Вот некоторые примеры антагонизма макро- и микроэлементов:
· чрезмерное количество N (азота) уменьшает поглощение P (фосфора), К (калия), Fe (железа ) и некоторых других элементов: Ca (кальция), Mg (магния), Mn (марганца), Zn (цинкa), Cu (меди);
· чрезмерное количество Р (фосфора) уменьшает поглощение катионов таких микроэлементов как Fe (железо), Mn (марганец), Zn (цинк) и Cu (медь);
· чрезмерное количество К (калия) уменьшает поглощение Mg (магния) в большей степени и Ca (кальция) в меньшей степени;
· чрезмерное количество Ca (кальция) снижает поглощение Fe (железа);
· чрезмерное количество Fe (железа) снижает поглощение Zn (цинка);
· избыток Zn (цинка) ухудшает доступность Mn (марганца).
В отличие от антагонизма синергизм представляет собой комплексное действие элементов (двух или более), при котором достигается усиление положительного результата их влияния на растение. С помощью практических и лабораторных исследований установлены такие примеры синергизма элементов:
· достаточное количество N (азота) обеспечивает оптимальное поглощение K (калия), а также P (фосфора), Mg (магния), Fe (железа), Mn (марганца) и Zn (цинка) из почв;
· достаточный уровень Cu (меди) и B (бора) в почве улучшает поглощение N (азота);
· oптимальнoе количество Мо (молибдена) повышает усваиваемость культурами N (азота), а также увеличивает поглощение Р (фосфора);
· достаточное количество Ca (кальция) и Zn (цинка) улучшают усвоение P (фосфорa) и K (калия);
· оптимальный уровень S (серы) повышает поглощение Mn (марганца) и Zn (цинка);
· достаточное количество Mn (марганца) увеличивает поглощение Cu (меди).
Нередко помимо этих двух групп элементов (антагонистов и синергистов) выделяют также третью группу, куда входят элементы, блокирующие действие друг друга. Например, одновременное присутствие в питательном растворе Cu (меди) и Ca (кальция) приводит к поглощению растением лишь одного из этих компонентов.
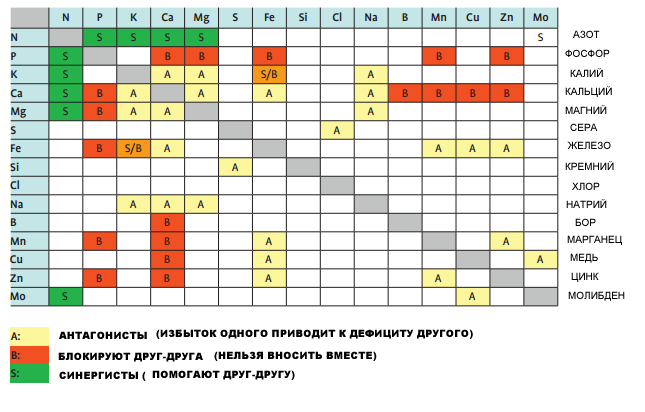
Явление, когда два или более элементов при совместном действии создают эффект улучшения физиологического состояния растения, называется синергизмом . В обратном случае, когда избыток одного из элементов уменьшает поглощение другого, наблюдается физиологический антагонизм . Эти взаимодействия зависят от типа почвы, физических свойств, рН, окружающей среды, температуры и доли участвующих питательных веществ.
Синергизм и антагонизм элементов связаны с электронным строением их атомов и ионов. Если наблюдается сходство в строении двух или более элементов, то они способны замещать друг друга в биохимических системах, что и вызывает антагонизм этих питательных веществ.
Агрономы всегда должны учитывать конкуренцию элементов, содержащих аналогичные по размеру, валентности и заряду ионы. Это очень важно при составлении сбалансированного комплекса удобрений, необходимых для прогрессирующего развития культур. Явления синергизма и антагонизма питательных веществ имеют особо критическое значение для растений, когда содержание этих элементов в почве приближено к дефициту.
Роль эссенциальных микроэлементов в жизнедеятельности человека
Минеральный состав внутриклеточной жидкости строго поддерживается на определенном уровне.
Элементы вместе с водой являются строительным материалами, кофакторами и катализаторами биохимических реакций, стабилизаторами белков и ферментов, обеспечивая постоянство осмотического давления, кислотно-щелочного баланса, процессов всасывания, секреции, кроветворения, костеобразования, свертывания крови. Благодаря присутствию элементов осуществляется процесс мышечного сокращения, нервной проводимости и внутриклеточного дыхания. Химические элементы в организме находятся в виде различных соединений и солей, их влияние на организма обусловлено дозой элемента. Для каждого элемента существует свой физиологический рабочий диапазон концентраций, обеспечивающий нормальное протекание физиологических реакций в организме.
Нарушенная экология, возросший темп жизни с неизбежным нарастанием стрессовых ситуаций, методы обработки продуктов питания, «убивающие» биологически активные вещества ведут к нарушению металло-лигандного гомеостаза и сдвигу равновесия в сторону увеличения или уменьшения концентрации элемента. Накопление элементов или их дефицит способствует активации альтернативных путей метаболизма, который в ряде случаев приводят к патологическим состояниям.
Химические элементы классифицируются в зависимости от их роли в организме. 98% тела человека состоит из органических элементов: H, C, N, O. Вместе с неорганическими элементами Na, Mg, K, Ca, P, S, Cl они составляют основу клеток и тканей, выполняя структурообразующую функцию. К эссенциальным или жизненно необходимым микроэлементам относятся Mn, Fe, Co, Ni, Cu, Zn, Mo, Se, I, при их отсутствии нарушаются базовые реакции деления и размножение клеток. К условно-эссенциальным микроэлементам относятся Li, V, Cr, B, F, Si, As, их роль до конца не определена. Существуют также «токсические металлы», которые в минимальных концентрациях способны оказывать стимулирующее воздействие на организм, но в высоких концентрациях проявляют токсические эффекты.
Микроэлементы составляют лишь 0,02% организма, но способны изменять протекание важнейших биологических реакций. Анализ волос или мочи позволяет выявить избыточное накопление микроэлементов или их дефицит. Содержание микроэлементов в волосах отражает микроэлементный статус организма в целом, поэтому пробы волос являются интегральным показателем минерального обмена. Волосы помогают диагностировать хронические заболевания, когда они себя еще ничем не проявляют.
Железо (Fe)
Железо является жизненно необходимым элементом для организма. Железо входит в состав гемсодержащих белков (гемоглобин и миоглобин) и участвует в переносе кислорода. Железо также входит в состав цитохромов (сложные белки, относящиеся к классу хромопротеидов), участвующих в процессах тканевого дыхания.
Общее содержание железа в организме человека составляет 3-5 г. Из этого количества 57% находится в гемоглобине крови, 23% — в тканях и тканевых ферментах (ферритин и гемосидерин), а остальные 20% — депонированы в печени, селезенке, костном мозге, мышцах и представляют собой "физиологический резерв" железа. Железо существует в двух формах: окисленной (Fe3+) и воcстановленной (Fe2+). Восстановленная форма лучше усваивается организмом. Только 10 % поступившего железо всасывается в кишечнике.
- мужчины: 8–10 мг/сут;
- женщины: 15–20 мг/сут;
- беременных женщины: 30–40 мг/сут;
- дети: 4–18 мг/сут.
Недостаток железа приводит к тяжелым расстройствам, наиболее важным из которых является железодефицитная анемия. Железодефицитная анемия может привести к сердечной недостаточности.
Избыточное накопление железа приводит к отложению металла в органах (печень, поджелудочная железа, суставы, сердце). Явления отравления железом выражаются рвотой, диареей, падением артериального давления, параличом ЦНС и воспалением почек. При лечении железом могут развиться запоры, так как железо связывает сероводород, что ослабляет моторику кишечника. Избыток железа в организме может привести к дефициту меди, цинка, хрома и кальция, а также к избытку кобальта.
Йод (I)
Йод необходим на всех этапах жизнедеятельности. Период младенчества и раннего детства являются критическими в отношении дефицита йода. Йод входит в состав гормонов щитовидной железы тироксина (T4) и трийодтиронина (T3). Йод необходим для роста и дифференцировки клеток всех тканей организма человека, внутриклеточного дыхания, регуляции трансмембранного транспорта натрия и гормонов.
Общее количество йода в организме составляет 25 мг, из них 15 мг аккумулирует щитовидная железа. Значительное количество йода содержится в печени, почках, коже, волосах, ногтях, яичниках и предстательной железе.
- взрослые: 100–150 мкг/сут;
- беременные: 175–200 мкг/сут;
- дети: от 60 до 150 мкг/сут.
При недостаточном поступлении йода у взрослых увеличиваются размеры щитовидной железы, замедляется основной обмен, наблюдается падение артериального давления. У детей недостаток йода сопровождается резкими изменениями всей структуры тела: ребенок отстает в умственном и физическом развитии.
Избыток йода в организме наблюдается при гипертиреозе. Развивается Базедова болезнь, сопровождающаяся экзофтальмом, тахикардией, раздражительностью, мышечной слабостью, потливостью, исхуданием, склонностью к диарее. Повышение основного обмена ведет к гипертермии, дистрофическим изменениям кожи и ее придатков, раннему поседению, депигментации кожи на ограниченных участках (витилиго), атрофии мышц.
Марганец (Mn)
Важен для репродуктивных функций и нормальной работы центральной нервной системы. Марганец участвует в синтезе нейромедиаторов, улучшает мышечные рефлексы, обеспечивает развитие соединительной и костной ткани, увеличивает утилизацию жиров, усиливает эффекты инсулина.
3–5 % поступившего марганца всасывается. Наиболее богаты марганцем трубчатые кости и печень, поджелудочная железа. Марганец содержится в клетках, богатых митохондриями.
- взрослые: 2–5 мг/сут;
- для детей в 2 раза выше.
При недостатке марганца нарушаются процессы окостенения во всем скелете, трубчатые кости утолщаются и укорачиваются, суставы деформируются. Нарушается репродуктивная функция яичников и яичек.
Избыток марганца усиливает дефицит магния и меди.
Медь (Cu)
Медь принимает участие в поддержание эластичности связок, сухожилий, кожи и стенок легочных альвеол, стенок капилляров, а также прочности костей. Медь входит в состав защитных оболочек нервных волокон, участвует в процессах пигментации, так как входит в состав меланина. Медь влияет на углеводный обмен, посредством усиления процессов окисления глюкозы и торможения распада гликогена мышц и печени. Медь обладает противовоспалительными действиями, помогает при борьбе с бактериальными агентами. Медь является кофактором ферментов антиоксидантной защиты и помогает нейтрализовать действие свободных радикалов.
Общее содержание меди в организме человека составляет примерно 100–150 мг. Лучше всего организм усваивает двухвалентную медь. В тонком кишечнике всасывается до 95% меди, поступившей с пищей. Основное "депо" меди в организме — печень, поскольку синтезирует белок-переносчик меди церулоплазмин.
- взрослые: 1 мг/сут;
- дети: от 0,5 до 1 мг/сут.
При недостатке меди в организме наблюдаются: задержка роста, анемия, дерматозы, депигментация волос, частичное облысение, потеря аппетита, сильное исхудание, понижение уровня гемоглобина, атрофия сердечной мышцы. Избыток меди приводит к дефициту цинка и мoлибдена, а также марганца.
Молибден (Мо)
Способствует метаболизму углеводов и жиров, является важной частью фермента, отвечающего за утилизацию железа, в связи с чем помогает предупредить анемию. Принимает участие в обмене мочевой кислоты, включении фтора в состав эмали зубов, гемопоэзе.
Биодоступность молибдена составляет 50%. Молибден не депонируется в организме, а распределяется между клетками крови.
- взрослые: 45–100 мкг/сут;
- дети: от 0,5 до 1 мг/сут.
Селен (Sе)
Элемент антиоксидантной защиты, хорошо сочетается с витамином Е. Селен помогает поддерживать должную эластичность тканей. Селен усиливает иммунитет, поэтому активно используется в онкологической практике, в лечении гепатитов, панкреатитов, кардиомиопатий. Селен защищает организм от тяжёлых металлов.
Всасывается в тонком кишечнике, депонируется в почках, печени, костном мозге.
- женщины: 50 мкг/сут;
- беременные: 65 мкг/сут;
- мужчины: 70 мкг/сут;
- дети: 10-50 мкг/сут.
При дефиците селена в организме усиленно накапливаются мышьяк и кадмий, которые, в свою очередь, еще больше усугубляют его дефицит.
Избыток селена приводит к гепато- и холецистопатиям, изменениям работы нервно-мышечного аппарата (боли в конечностях, судороги, чувство онемения). Избыток может привести к дефициту кальция.
Цинк (Zn)
Цинк входит в состав более 300 ферментов, чем объясняет его влияние на углеводный, жировой и белковый обмен веществ, на окислительно-восстановительные процессы, регуляцию активности генов. Цинк связан с правильным функционированием репродуктивной, неврологической, иммунной систем, ЖКТ и кожи. Присутствие микроэлемента важно для нормального сперматогенеза, органогенеза, работы нейромедиаторов и панкреатических ферментов, правильного развития тимуса, эпителизации ран в процессе заживления и ощущения вкуса.
В организме содержится около 1,5–3 г цинка. Цинк всасывается в тонком кишечнике. Медь является антагонистом цинка, и конкурирует с цинком за всасывание в кишечнике. 99% цинка находится внутриклеточно, 1% — в плазме. Цинк присутствует во всех органах и тканях, но в большей степени цинк депонируют предстательная железа, семенники, мышцы, кожа, волосы.
Физиологическая потребность в цинке составляет: 12 мг/сут для взрослых, 3–2 мг/сут для детей.
Наиболее богаты цинком дрожжи, пшеничные, рисовые и ржаные отруби, зерна злаков и бобовых, какао, морепродукты, грибы, лук, картофель.
При дефиците цинка наблюдается задержка роста, перевозбуждение нервной системы и быстрое утомление. Поражение кожи происходит с утолщением эпидермиса, отеком кожи, слизистых оболочек рта и пищевода, ослаблением и выпадением волос. Недостаточное поступление цинка приводит к бесплодию. Дефицит цинка может приводить к усиленному накоплению железа, меди, кадмия, свинца.
При цинковом отравлении наступает фиброзное перерождение поджелудочной железы. Избыток цинка задерживает рост и нарушает минерализацию костей.
Кобальт (Co)
В организме 1,5 г кобальта. Биодоступность кобальта 20%. В организм кобальт депонируется в печени, костной ткани и мышцах.
Физиологическая потребность в кобальте составляет: 10 мкг/сут для взрослых.
Кобальт содержится в печени, молоке, овощах.
Дефицит кобальта связан с В12-дефицитной анемией, вегетарианством или паразитарной инвазией. Избыток кобальта наблюдается при интоксикации кобальта (вредное производство, разрушение ортопедических имплантантов).
Никель (Ni)
Никель пролонгирует эффекты инсулина, участвует в окислении аскорбиновой кислоты, ускоряет образование дисульфидных групп.
Никель всасывается в кишечнике, биодоступность от 1 до 10 %. Запасы никеля находятся в поджелудочной железе, легких, сердце.
Физиологическая потребность в никеле составляет: 100–200 мкг/сут для взрослых.
Богаты никелем чай, гречиха, морковь и салат.
Дефицит никеля не описан. Избыток никеля наблюдается при его токсическом поступлении, злокачественных новообразованиях легких, ожогах, инсультах и инфарктах. Избыток может проявлять потерей пигментацией кожи.
Читайте также:
