Металлы платиновой группы в рудах встречаются в виде
Обновлено: 17.05.2024
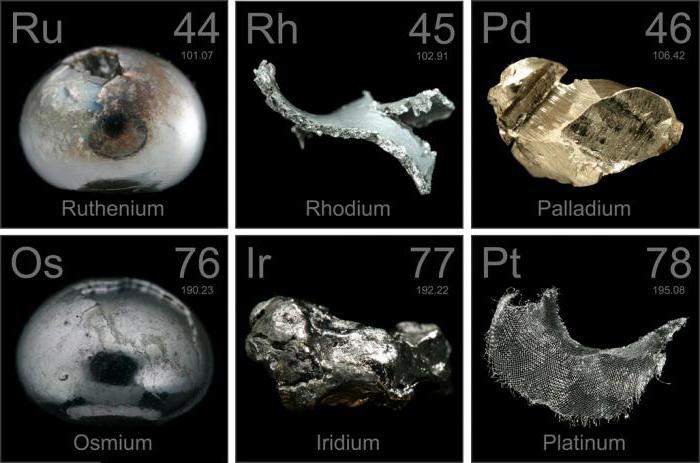
Металлы платиновой группы – это шесть благородных драгоценных химических элементов, которые расположены рядом в периодической таблице. Все они являются переходными металлами 8–10 групп 5–6 периода.
Металлы платиновой группы: список
Группа состоит из следующих шести химических элементов, расположенных в порядке возрастания атомного веса:
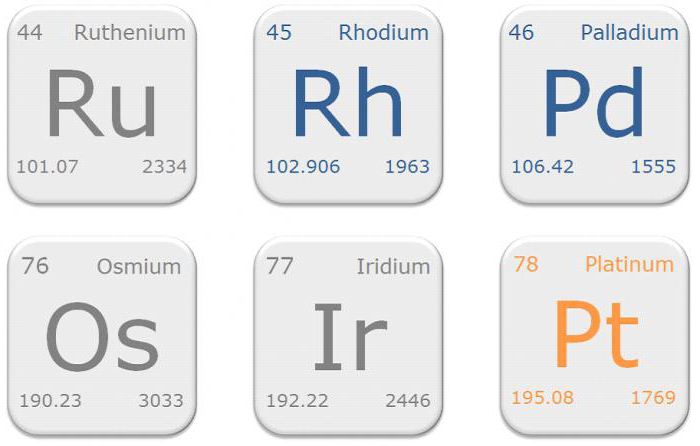
- Ru – рутений.
- Rh – родий.
- Pd – палладий.
- Os – осмий.
- Ir – иридий.
- Pt – платина.
Металлы платиновой группы обладают серебристо-белым оттенком, за исключением осмия, цвет которого голубовато-белый. Их химическое поведение парадоксально в том, что они обладают высокой устойчивостью к воздействию большинства реагентов, но используются в качестве катализаторов, легко ускоряющих или контролирующих скорость окисления, восстановления и реакций гидрирования.
Рутений и осмий кристаллизуются в гексагональную плотноупакованную систему, а другие обладают гранецентрированной кубической структурой. Это выражается в большей твердости рутения и осмия.
История открытия
Хотя платиносодержащие золотые артефакты датированы 700 г. до н. э., присутствие этого металла является, скорее, случайностью, чем закономерностью. Иезуиты в XVI веке упоминали серые плотные камешки, связанные с аллювиальными месторождениями золота. Эти камешки нельзя было расплавить, но они образовывали сплав с золотом, при этом слитки становились ломкими, и их уже было невозможно очистить. Камешки стали называть platina del Pinto – гранулы серебристого материала из реки Пинто, впадающей реку Сан-Хуан в Колумбии.
Ковкая платина, которую можно получить только после полной очистки металла, была выделена французским физиком Шабано в 1789 году. Из нее был сделан кубок, преподнесенный папе Пию VI. Об открытии палладия в 1802 году сообщил английский химик Уильям Волластон, который назвал хим. элемент группы платиновых металлов в честь астероида. Волластон впоследствии заявлял об обнаружении еще одного вещества, присутствующего в платиновой руде. Его он назвал родием из-за розового цвета солей металла. Открытия иридия (по имени богини радуги Ириды из-за пестрой окраски его солей) и осмия (от греческого слова «запах» из-за хлорного запаха его летучего окисла) были сделаны английским химиком Смитсоном Теннантом в 1803 году. Французские ученые Ипполит-Виктор Колле-Дескоти, Антуан-Франсуа Фуркруа, и Николя-Луи Воклен выделили два металла одновременно. Рутений, последний изолированный и идентифицированный элемент, получил свое название по латинскому наименованию России от русского химика Карла Карловича Клауса в 1844 году.
В отличие от таких легко выделяемых в относительно чистом состоянии путем простого огневого рафинирования веществ, как золото, серебро, металлы платиновой группы требуют сложной водно-химической обработки. Эти методы не были доступны до конца 19 века, поэтому выявление и изоляция платиновой группы отстала от серебра и золота на тысячи лет. Кроме того, высокая температура плавления этих металлов ограничивала их применение, пока исследователи в Британии, Франции, Германии и России не разработали методы преобразования платины в форму, пригодную для обработки. Как драгоценные металлы платиновой группы начали использоваться в ювелирных изделиях с 1900 года. Хотя такое применение остается актуальным и сегодня, промышленное намного его превзошло. Палладий стал очень востребованным материалом для контактов в телефонных реле и других системах проводной коммуникации, обеспечивая длительный срок службы и высокую надежность, а платина, из-за своей устойчивости к искровой эрозии, во время Второй мировой войны стала применяться в свечах зажигания боевых самолетов.
После войны расширение методов молекулярной конверсии при переработке нефти создало огромный спрос на каталитические свойства, которыми обладают металлы платиновой группы. К 1970-м годам потребление выросло еще больше, когда стандарты автомобильных выбросов в США и других странах привело к использованию данных химических элементов в каталитической конверсии выхлопных газов.
За исключением малых россыпных месторождений платины, палладия и осмистого иридия (сплава иридия и осмия), практически нет руды, в которой бы основным компонентом был химический элемент – металл платиновой группы. Минералы, как правило, содержатся в сульфидных рудах, в частности в пентландите (Ni, Fe)9S8. Наиболее распространены лаурит RuS2, ирарсит, (Ir,Ru,Rh,Pt)AsS, осмиридиум (Ir,Os), куперит, (PtS) и браггит (Pt,Pd)S.
Крупнейшее в мире месторождение металлов платиновой группы – Бушвельдский комплекс в ЮАР. Большие запасы сырья сосредоточены в месторождениях Садбери в Канаде и Норильско-Талнахском в Сибири. В США наибольшие залежи минералов платиновой группы расположены в Стилуотере, Монтана, но здесь они значительно меньше, чем в ЮАР и России. Крупнейшими в мире производителями платины являются Южная Африка, Россия, Зимбабве и Канада.

Добыча и обогащение
Основные южноафриканские и канадские месторождения эксплуатируются шахтным способом. Практически все металлы платиновой группы извлекаются из медных или никелевых сульфидных минералов с помощью флотационной сепарации. Плавка концентрата производит смесь, которая вымывается из меди и сульфидов никеля в автоклаве. Твердый остаток выщелачивания содержит от 15 до 20% металлов платиновой группы.
Иногда до флотации используется гравитационное разделение. В результате получается концентрат, содержащий до 50% платиновых металлов, что избавляет от необходимости выплавки.
Механические свойства
Металлы платиновой группы значительно отличаются механическими свойствами. Платина и палладий довольно мягкие и очень ковкие. С этими металлами и их сплавами можно работать как в горячем, так и в холодном состоянии. Родий сначала обрабатывают горячим, а позже его можно обрабатывать холодным с довольно частым отжигом. Иридий и рутений должны быть нагреты, холодной обработке они не поддаются.
Осмий – самый твердый из группы и имеет наиболее высокую температуру плавления, но его склонность к окислению накладывает свои ограничения. Иридий наиболее коррозионностойкий из платиновых металлов, а родий ценится за сохранение своих свойств при высоких температурах.

Структурные применения
Поскольку дочиста отожженная платина очень мягкая, она восприимчива к царапинам и порче. Для увеличения твердости ее сплавляют со множеством других элементов. Платиновые драгоценности очень популярны в Японии, где ее называется «хаккин» и «белое золото». Сплавы для ювелирных изделий содержат 90% Pt и 10% Pd, который легко обрабатывать и паять. Добавление рутения повышает твердость сплава, сохраняя стойкость к окислению. Сплавы платины, палладия и меди используются в кованых изделиях, так как они тверже платино-палладиевых и менее затратны.
Тигли, используемые для производства монокристаллов в полупроводниковой промышленности, требуют коррозионной устойчивости и стабильности при высоких температурах. Для этого применения лучше всего подходят платина, платина-родий и иридий. Платинородиевые сплавы используются в производстве термопар, которые предназначены для измерения повышенных температур до 1800 °C. Палладий применяют как в чистом, так и в смешанном виде в электрических устройствах (50% потребления), в стоматологических сплавах (30%). Родий, рутений и осмий редко используются в чистом виде – они служат легирующей добавкой для других металлов платиновой группы.

Катализаторы
Около 42% всей платины, произведенной на Западе, используется в качестве катализатора. Из них 90% применяется в автомобильных выхлопных системах, где тугоплавкие гранулы или сотовые конструкции с платиновым покрытием (а также палладиевым и родиевым) содействуют преобразованию несгоревших углеводородов, окиси углерода и окислов азота в воду, углекислый газ и азот.
Сплав платины и 10% родия в виде раскаленной докрасна металлической сетки служит катализатором в реакции между аммиаком и воздухом для получения окислов азота и азотной кислоты. При подаче вместе со смесью аммиака метана можно получить синильную кислоту. При переработке нефти платина на поверхности гранул оксида алюминия в реакторе является катализатором преобразования длинноцепочечных молекул нефти в разветвленные изопарафины, которые желательны в смеси высокооктановых бензинов.

Гальваника
Все металлы платиновой группы можно наносить гальванически. Из-за твердости и блеска получаемого покрытия наиболее часто применяется родий. Хотя его стоимость выше, чем платины, меньшая плотность позволяет использовать меньшую массу материала при сопоставимой толщине.
Палладий – металл платиновой группы, который проще всего использовать для нанесения покрытий. Благодаря этому прочность материала значительно повышается. Рутений нашел применение в инструментах, предназначенных для обработки трением при низком давлении.
Химические соединения
Органические комплексы металлов платиновой группы, такие как комплексы алкилплатины, используются в качестве катализаторов в процессе полимеризации олефинов, производстве полипропилена и полиэтилена, а также при окислении этилена в ацетальдегид.
Соли платины находят все более широкое применение в химиотерапии рака. Например, они входят в состав таких лекарств, как "Карбоплатин" и "Цисплатин". Покрытые оксидом рутения электроды используются в производстве хлора и хлората натрия. Сульфат и фосфат родия применяются в родиевых гальванических ваннах.
Металлы платиновой группы (МПГ)
- Платина.
- Палладий.
- Родий.
- Рутений.
- Иридий.
- Осмий.
Главными особенностями металлов платиновой группы, являются:
- серебристо-серый оттенок, кроме осмия (бело-голубой);
- кристаллические свойства, способствующие ускорению химических процессов;
- катализаторы, контролирующие скорость окисления, реакции гидрирования;
- химически стойкие металлы по отношению к действию многих реагентов;
- обладают высокой электропроводностью;
- выдерживают высокие температуры;
- тугоплавкость.
Основными источниками платиновых металлов являются минералы редких элементов. Сегодня драгоценные платиновые металлы используют в ювелирном производстве, но в разной степени, а биологически активные соединения платиновых металлов в медицине.
Платина
Платина известна издревле, а название произошло с испанского языка: «маленькое серебро». Конкистадоры, это первые европейцы, которые познакомились с платиной в середине 16 века в Южной Америке. А в 1735 году король Испании издал указ, по которому следовало топить платину в реке и не ввозить в страну. Позже речку назвали Платино-дель-Пинто. Указ был отменен только через сорок лет, для фальсифицирования золотых и серебряных монет мадридскими властями. Позже с платиной познакомились алхимики, но посчитали ее непригодной. Но во Франции она все же нашла свое применение в виде эталона метра, а затем килограмма. В России металл назвали белым золотом, найдя его в россыпном золоте.
Платина, это один из редчайших металлов, ведь в земной коре ее содержания невелико. Главными месторождениями платины являются: Россия, США (2 крупных рудника: Stillwater, East Bouder), Китай, Зимбабве (9 тонн), ЮАР (Бушвельский комплекс).
В России данный металл МПГ обладает уникальной базой, с огромным количеством месторождений, основной из которых расположен в Зареченске (Мурманской области).
Добыча платины это трудоемкий процесс, двух видов:
- Открытый способ добычи: на вторичных россыпных месторождениях. Там платина концентрируется в результате разрушений первичной породы.
- Закрытый способ добычи: на первичных месторождениях, с постройкой шахт, просверливанием отверстий в породах, закладке взрывчатки и самого взрыва.
Платина это драгоценный металл, который используют в ювелирном деле и промышленности. Свойства платины широки:
- тяжелее, чем золото и серебро;
- не окисляется;
- не вступает в реакции с другими элементами при нагреве;
- пластичный металл;
- обладает хорошей электропроводностью;
- не растворяется под воздействием кислот;
- высокая температура плавления;
- хорошая ковкость.
Область применения платины достаточно широкое и не ограничивается ювелирным производством, ведь она обладает уникальной красотой и благородством. В настоящее время рост на металл растет, так как используют ее и в промышленности. Итак, применения платины:
- ювелирное производство, для изготовления разного вида украшений;
- медицина;
- химическая индустрия;
- судостроение;
- авиастроение;
- космическая сфера;
- стекольная отрасль;
- банковское дело.
Палладий
На сегодня, палладий самый дорогой металл платиновой группы, который используется в промышленности.
В конце 17 века бразильские горнодобывающие рабочие нашли сплав, похожий на содержание золота или платины. Химик У. Волластон проработал взаимодействие неочищенной платиной с соляной и азотной кислотами, и добавкой цианида ртути. После выпал желтый осадок, который он нагрел с серой и бурой. Получив шарики из металла и, назвав металл - палладий.
Название металл получил в честь астероида. Этот металл платиновой группы встречается в природе очень редко в чистом в виде. А чаще в комплексе с другими металлами (золото, серебро, платина).
Добывают металл также двумя способами:
- на коренных (первичных) месторождениях;
- на россыпи, в виде самородка и составляют всего 2% от всей добычи металла.
Главные месторождения палладия:
В России также происходит добыча палладия, сконцентрированная на Урале. Главными свойствами палладия являются:
- низкая плотность;
- химическая инертность;
- внешне напоминает серебро;
- высокая ковкость;
- эластичность, что позволяет использовать в изготовлении украшений;
- температура плавления 1555 градусов;
- поддается обработке;
- непрочный металл при механическом воздействии;
- растворяется при воздействии смеси серной и азотной кислот;
- может образовывать соединения с иными химическими элементами ( бор, хлор, сера, кремний);
- не вступает в реакции;
- не окисляется в природе.
Области применения палладия
- Ювелирная сфера, добавляя металл в сплавы;
- производство катализаторов для автомобилей, для дожигания выхлопных газов по нормам ЕС;
- медицина: изготовление элементов для кардиостимуляторов, инструментов, посуды;
- химическая отрасль: изготавливают колбы и емкости, а также для очищения водорода;
- электронная сфера: военно-аэрокосмическая техника;
- инвестиционная деятельность: покупка слитков.
Родий
Следом за открытием палладия, Волластон открыл еще один металл платиновой группы - родий, путем растворения неочищенной платины в царской водке (смесь соляной и азотной кислот) и нейтрализации избытка кислоты едким натром. Осадив платину хлористым аммонием, палладий - цианистой ртутью. Полученный фильтрат был обработан соляной кислотой (чтобы удалить избыток цианистой ртути) и выпарен до сухого состояния. А осадок, обработанный алкоголем, выглядел как темно-красный порошок двойной натриевородиевой соли соляной кислоты. А уже в свою очередь при прокаливании порошка в токе водорода, получил металл.
Родий получил свое название с греческого языка: роза. Добыча родия производится вместе с платиной/золотом. Основными источниками родия являются золотые месторождения Мексики, залежи родиевого Невьянскита.
Родий представляет собой металл серебристо-белого оттенка и относится к благородным металлам платиновой группы.
Свойства родия
- Растворяется в перекиси водорода, серной кислоте;
- растворяется при кипячении в смеси соляной и азотной кислот;
- высокая химическая устойчивость;
- взаимодействует с неметаллами лишь при температуре красного каления;
- окисление происходит при высокой температуре;
- стойкий металл к коррозийным средам.
Так как родий, это драгоценный и уникальный металл, то и область его применения различна:
- в качестве катализатора (каталитических фильтрах для нейтрализации выхлопных газов);
- является конструкционным материалом, для изготовления зеркал, стекол;
- при сплаве родия с платиной, получается эффективный катализатор при производстве азотной кислоты по средствам окисления аммиака воздухом;
- производство термопаров (при сплаве с иридием или платиной);
- придают износостойкость и устойчивость к коррозии ювелирным изделиям.
Рутений
Рутений был открыт в Казани в 1844 году К. Клаусом. Он анализировал заводские платиновые осадки из Петербургского монетного двора. Он извлек из руды платину и некоторые платиновые металлы, после чего сплавил остатки с селитрой, извлекая растворимую в воде часть. А нерастворимый в воде осадок, взаимодействовал с царской водкой и высушил. К. Клаус обработал сухой остаток после дистилляции кипящей водой, добавил избыток поташа. Отделив осадок гидроокиси железа, он обнаружил элемент неизвестного происхождения темно-пурпурного оттенка раствора осадка в соляной кислоте. Рутений был назван в честь России (Ruthenia - Россия).
Добыча рутения всегда сопровождает добычу платины на россыпных и коренных месторождениях. Присутствует в качестве примесей в составе никелевой руды, медной руды. Также существуют искусственные источники добычи рутения, т.е. отходы ядерной промышленности. Основное месторождение данного металла платиновой группы, это ЮАР, Канада, Россия, Зимбабве.
Основные характеристики рутения:
- серебристо-белый блестящий или матовый цвет;
- обладает твердостью;
- тугоплавок;
- при сильном прокаливании на воздухе переходит в газовую фазу;
- растворяется медленно соляной кислотой при обычной температуре, при высокой температуре - быстро;
- газопоглотительная способность.
Область применения металла
- Производство катализаторов;
- защитные покрытия;
- декоративные покрытия;
- в виде добавок к украшениям;
- добавка в элитные эмали и другое.
Иридий
В начале 19 века химики были заинтересованы неочищенной платиной и всеми возможными элементами содержащиеся в ней. Тогда Дескотиль, Фуркруа и Вокелен стали изучать сырой металл, сплавив его с едким кали, получив частично растворимые в воде соединения неизвестных металлов. Теннант пошел этим же способом, и смог выделит два новых металла: иридий и осмий.
Иридий получил свое название с греческого: радуга, благодаря тому, что соединения данного металла были окрашены в разные цвета. Осмий же в связи с растворение щелочного сплава осмиридия в кислоте (или в воде) сопровождался сильным запахом. С греческого языка, получив название: запах.
Иридий очень редкий металл платиновой группы, который добыть практически невозможно. Добыча его сопровождается попутчиками: платиной или осмием и рутением или палладием. Он встречается в медных и никелевых рудах. Место добывания иридия: Канада (Британская Колумбия), США (Калифорния), ЮАР (Трансвааль), Остров Тасмания, Новая Гвинея, остров Калимантан.
- красивый металл бело-серебристого оттенка;
- твердый и долговечный металл;
- высокая плотность и прочность;
- воздействия осуществляются за счет нагревания металла;
- укрепляет любой состав, делая его износоустойчивым;
- химическая стойкость;
- стойкий к коррозиям;
- стойкость к окислению и всяческому разрушению, даже под воздействием температуры.
- химическая промышленность;
- ювелирное дело;
- вместе с иными металлами является компонентом для автомобильных свечей;
- сплавы с иридием используют в медицине, для производства инструментов;
- в научной деятельности, металл не очень востребован.
Осмий
Чистого осмия в природе нет, он находится в комплексе с родием. Месторождения осмия сконцентрированы в: Африке (юг), Тасмании, Австралии, США, Канаде, Россие, Колумбия, ЮАР (самые большие запасы).
- серебристо-голубые кристаллы;
- резкий запах, при взаимодействии с веществами;
- не растворяется в щелочах и кислотах, смеси соляной и азотной кислот;
- химическая инертность;
- порошковый осмий - сырье для продукции, медленно подвержен к растворению;
- твердый и хрупкий;
- тугоплавкий;
- высокая плотность: самый тяжелый металл.
Область применения
- Медицина: кардиостимуляторы, импланты;
- промышленность: для измерительной техники, часовые механизмы;
- тетра оксид осмия используют в электронной микроскопии.
Металлы платиновой группы, редкие и уникальные металлы, которые не так часто встречаются в природе, но широко и активно применяются в разных сферах жизни, тем самым помогая человечеству.
Платиновые металлы
Пл а тиновые мет а ллы, платиноиды, химические элементы второй и третьей триад VIII группы периодической системы Менделеева. К ним принадлежат: рутений (Ruthenium) Ru, родий (Rhodium) Rh, палладий (Palladium) Pd (лёгкие платиновые металлы, плотность ~12 г/см 3 ); осмий (Osmium) Os, иридий (Iridium) lr, платина (Platinum) Pt (тяжёлые платиновые металлы, плотность ~22 г/см 3 ). Серебристо-белые тугоплавкие металлы; благодаря красивому внешнему виду и высокой химической стойкости платиновые металлы наряду с Ag и Au называют благородными металлами.
Историческая справка. Имеются указания, что самородная платина в древности была известна в Египте, Эфиопии, Греции и Южной Америке. В 16 в. исп. конкистадоры обнаружили в Южной Америке вместе с самородным золотом очень тяжёлый белый тусклый металл, который не удавалось расплавить. Испанцы назвали его платиной — уменьшительным от исп. plata — серебро. В 1744 исп. морские офицер Антонио де Ульоа привёз образцы Pt в Лондон. Они вызвали живой интерес учёных Европы. Самостоятельным металлом Pt, которую первоначально считали белым золотом, была признана в середине 18 в.
В 1803 английский учёный У. Х. Волластон обнаружил в самородной платине палладий, получивший это название от малой планеты Паллады (открытой в 1802), и родий, названный так по розовато-красному цвету его солей (от греч. rh ó don — роза). В 1804 английский химик Смитсон Теннант в остатке после растворения самородной Pt в царской водке открыл ещё 2 металла. Один из них получил название иридий вследствие разнообразия окраски его солей (от греч. í ris, род. падеж í ridos — радуга), другой был назван осмием по резкому запаху его четырёхокиси (от греч. osm á — запах). В 1844 К. К. Клаус при исследовании остатков от аффинажа (очистки) уральской самородной Pt в Петербургском монетном дворе открыл ещё один платиновый металл — рутений (от позднелат. Ruthenia — Россия).
Распространение в природе. Платиновые металлы принадлежат к наиболее редким элементам, их среднее содержание в земной коре (кларки) точно не установлено, ориентировочные значения приведены в таблице. Самые редкие в земной коре — Rh и lr (1 × 10 -7 % по массе), наиболее распространён Os (5 × 10 -6 %). Содержание платиновых металлов повышено в ультраосновных и основных изверженных породах, происхождение которых связано с глубинными магматическими процессами. К этим породам приурочены месторождения платиновых металлов. Ещё выше среднее содержание платиновых металлов в каменных метеоритах, которые считаются аналогами средней мантии Земли (кларки платиновых металлов в каменных метеоритах составляют n × 10 -4 — n × 10 -5 % по массе). Для земной коры характерно самородное состояние платиновых металлов, а у Rh, Pd, Os и Pt известны также немногочисленные соединения с серой, мышьяком и сурьмой. Установлено около 30 минералов платиновых металлов, больше всего их у Pd (13) и Pt (9). Все минералы образовались на больших глубинах при высоких температурах и давлениях (см. Платиновые руды, Платина самородная). Платина и другие платиновые металлы встречаются в виде примеси во многих сульфидах и силикатах ультраосновных и основных пород. Геохимия платиновых металлов в биосфере почти не изучена, их содержание в гидросфере и живом веществе не установлено. Некоторые осадочные марганцевые руды обогащены Pt (до 1 × 10 -3 %), в углях наблюдалась концентрация Pt и Pd (1 × 10 -6 %); повышенное содержание платиновых металлов отмечалось в фосфоритах (вятских), в золе деревьев, растущих на месторождениях Pt.
Физические и химические свойства. Физические и механические свойства платиновых металлов сопоставлены в таблице. В дополнение необходимо указать, что Ru и Os очень тверды и хрупки (возможно вследствие присутствия примесей). Rh и lr обладают меньшими твёрдостью и хрупкостью, а Pd и Pt ковки, поддаются прокатке, волочению, штамповке при комнатной температуре. Интересна способность некоторых платиновых металлов (Ru, Pd, Pt) поглощать водород. Особенно это свойственно Pd, объём которого поглощает до 900 объёмов H2. При этом Pd сохраняет металлический вид, но растрескивается и становится хрупким. Все платиновые металлы парамагнитны. Магнитная восприимчивость c s × 10 -6 электро-магнитных единиц при 18 °С равна 0,05 у Os; 0,50 у Ru; 5,4 у Pd; у Rh, lr и Pt она несколько более 1,0.
Согласно давно установившейся традиции, платиновые металлы принято помещать в VIII группу периодической системы элементов. В соответствии с этим следовало ожидать, что все платиновые металлы должны иметь высшую степень окисления +8. Однако это наблюдается только у Ru и Os, прочие же платиновые металлы проявляют валентность не выше +6. Объясняется это тем, что у атомов Ru и Os остаются незаполненными соответственно внутренние подуровни 4f и 5f. Поэтому для атомов Ru и Os возможно возбуждение не только с подуровней 5s и 6s на подуровни 5p и 6p, но и с подуровней 4d и 5d на подуровни 4f и 5f. Вследствие этого в атомах Ru и Os появляется по 8 непарных электронов и валентность +8. Электронные конфигурации атомов Rh, lr, Pd, Pt такой возможности не допускают. Поэтому в некоторых вариантах таблицы Менделеева эти элементы (а также Со и Ni) выносят за пределы VIII группы. Все платиновые металлы легко образуют комплексные соединения, в которых имеют различные степени окисления и различные координационные числа. Комплексные соединения платиновых металлов, как правило, окрашены и очень прочны.
Химические свойства платиновых металлов имеют много общего. Все они в компактном виде (кроме Os) малоактивны. Однако в виде т. н. черни (мелкодисперсного порошка) платиновые металлы легко адсорбируют S, галогены и др. неметаллы. (Чернь обычно получают восстановлением платиновых металлов из водных растворов их соединений.) Компактные Ru, Rh, Os, lr, будучи сплавлены с Pt, Zn, Pb, Bi, переходят в раствор при действии царской водки, хотя она не действует на эти платиновые металлы, взятые отдельно.
Семейство платиновых металлов можно разделить на 3 диады (двойки), образованные двумя стоящими один под другим лёгким и тяжёлым платиновыми металлами, а именно: Ru, Os; Rh, lr; Pd, Pt.
При нагревании с O2 и сильными окислителями Ru и Os образуют легкоплавкие кристаллы — четырёхокиси (тетроксиды) — оранжевую RuO4 и желтоватую OsO4. Оба соединения летучи, пары их имеют неприятный запах и весьма ядовиты. При действии восстановителей превращаются в низшие окислы RuO2 и OsO2 или в металлы. Со щелочами RuO4 образует рутенаты, например рутенат калия K2RuO по реакции:
При действии хлора K2RuO4 превращается в перрутенат калия:
Четырёхокись OsO4 даёт с KOH комплексное соединение K2[OsO4(OH)2]. С фтором и др. галогенами Ru и Os легко реагируют при нагревании, образуя соединения типа RuF3, RuF4, RuF5, RuF6. Осмий даёт подобные же соединения, кроме OsF3; существование OsF8 не подтверждено. Весьма интересны комплексные соединения Ru с ксеноном Xe [RuF6] (канадский химик Н. Бартлетт, 1962), а также с молекулярным азотом — [(NO)(NH3)4 N2Ru (NH3)4 NO] CI (советский химик Н. М. Синицын, 1962) и [Ru (NH3)5N2] Cl2 (канадский химик А. Аллен, 1965).
На компактные Rh и lr царская водка не действует. При прокаливании в O2 образуются окислы Rh2O3 и Ir2O3, разлагающиеся при высоких температурах.
Pd легко растворяется при нагревании в HNO3 и концентрированной H2SO4 с образованием нитрата Pd (NO3)2 и сульфата PdSO4. На Pt эти кислоты не действуют. Царская водка растворяет Pd и Pt, причём образуются комплексные кислоты — тетрахлоропалладиевая кислота H2[PdCl4] и гексахлороплатиновая — коричнево-красные кристаллы состава H2[PtCl6] × 6H2O Из её солей наибольшее значение для технологии платиновых металлов имеет хлороплатинат аммония (NH4)2[PtCl6] — светло-жёлтые кристаллы, малорастворимые в воде и почти не растворимые в концентрированных растворах NH4CI. При прокаливании они разлагаются по реакции:
При этом Pt получается в мелкораздробленном виде (т. н. платиновая губка, или губчатая платина).
Получение. Разделение платиновых металлов и получение их в чистом виде очень сложно вследствие большого сходства их химических свойств; это требует большой затраты труда, времени, дорогих реактивов. Для получения чистой Pt исходные материалы — самородную платину, платиновые шлихи (тяжёлые остатки от промывки платиноносных песков), лом (негодные для употребления изделия из Pt и её сплавов) обрабатывают царской водкой при подогревании. В раствор переходят: Pt, Pd, частично Rh, lr в виде комплексных соединений H2[PtCl6], H2[PdCl4], Нз [RhCl6] и H2[IrCl6], а также Fe и Cu в виде FeClз и CuCl2. Нерастворимый в царской водке остаток состоит из осмистого иридия, хромистого железняка (FeCrO2), кварца и др. минералов.
Из раствора осаждают Pt в виде (NH4)2[PtCl6] хлористым аммонием. Но чтобы в осадок вместе с Pt не выпал lr в виде аналогичного нерастворимого соединения (NH4)2[lrCl6] (остальные платиновые металлы NH4Cl не осаждает), предварительно восстанавливают Ir (+4) до Ir (+3) (например, прибавлением сахара C12H22O11 по способу И. И. Черняева). Соединение (NH4)3[IrCl6] растворимо и не загрязняет осадка.
Хлороплатинат аммония отфильтровывают, промывают концентрированным раствором NH4CI (в котором осадок практически не растворим), высушивают и прокаливают. Полученную губчатую платину спрессовывают, а затем оплавляют в кислородно-водородном пламени или в электрической печи высокой частоты. Из фильтрата, оставшегося после осаждения (NH4)2[PtCl6], и из осмистого иридия извлекают прочие платиновые металлы путём сложных химических операций. В частности, для перевода в растворимое состояние нерастворимых в царской водке платиновых металлов и осмистого иридия используют спекание с перекисями BaO2 или Na2O2. Применяют также хлорирование — нагревание смеси Pt-концентратов с NaCl и NaOH в струе хлора.
В результате аффинажа получают труднорастворимые комплексные соединения: гексахлорорутенат аммония (NH4)3[RuCl6], дихлорид тетрамминдиоксоосмия [OsO2(NH3)4] Cl2, хлорпентамминдихлорид родия [Rh (NH3)5CI] Cl2, гексахлороиридат аммония (NH4)2[lrCl6] и дихлордиаммин палладия [Pd (NH3)2] Cl2. Прокаливанием перечисленных соединений в атмосфере H2 получают платиновые металлы в виде губки, например
Губчатые платиновые металлы сплавляют в вакуумной электрической печи высокой частоты.
Применяют и др. способы аффинажа, в частности основанные на использовании ионитов.
Основным источником получения платиновых металлов служат сульфидные медно-никелевые руды, месторождения которых находятся в СССР (Норильск, Красноярский край), Канаде (округ Садбери, провинция Онтарио), ЮАР и др. странах. В результате сложной металлургической переработки этих руд благородные металлы переходят в т. н. черновые металлы — нечистые никель и медь. Платиновые металлы собираются почти полностью в черновом Ni, a Ag и Au — в черновой Cu. При последующем электролитическом рафинировании Ag, Au и платиновые металлы осаждаются на дне электролитической ванны в виде шлама, который отправляют на аффинаж.
ПЛАТИНОВЫЕ МЕТАЛЛЫ
ПЛАТИНОВЫЕ МЕТАЛЛЫ (платиноиды), семейство из 6 хим. элементов VIII гр. периодич. системы, включающее рутений (ат. н. 44), родий (45), палладий (46), осмий (76), иридий (77), платину (78). Вместе с Au и Ag составляют группу благородных металлов. Подразделяются на легкие (Ru-Pd) и тяжелые (Os-Pt).
Распространенность в природе и природные источники. Содержание платиновых металлов в земной коре (% по массе): Pt 5·10 -7 , Pd 1·10 -6 , Ir 1·10 -7 , Rh 1·10 -7 , Os 5·10 -6 , Ru 5·10 -7 (по Виноградову). Руды платиновых металлов бывают коренные и россыпные, а по составу - собственно платиновые и комплексные (мн. коренные месторождения медных и медно-никелевых сульфидных руд, россыпные месторождения Au с Pt, а также Au с осмистым Ir). Известно более 100 минералов платиновых металлов, они бывают двух типов. В россыпях встречаются самородные Pd и Pt и разл. сплавы, в т.ч. с другими платиновыми металлами, Fe, реже-с Au (содержат также и др. металлы), капр. палладиевая платина, железистая платина (Pt, Fe), изоферроплатина Pt 3 Fe, плати-нистый палладий, осмистый иридий, иридиевая платина Pt 4 Ir 2 Fe, платинистый иридий Ir 4 Pt, осмистый иридий Ir 2 Os, ауроосмид (Ir, Os, Au) и др. Минералы второго типа-разл. соединения платиновых металлов с S, Fe, As, Bi, Pb, напр, спериллит PtAs 2 , куперит PtS, брэгтит (Pt, Pd, Ni)S, стибиопалладинит Pd 3 Sb, лаурит RuS 2 , холлингуореит (Rh, Pt, Pd, Ir)(AsS) 2 и др. Минералы этого типа встречаются в виде твердых р-ров в медно-никелевых сульфидных рудах, являющихся осн. пром. источником платиновых металлов. На долю вторичных источников платиновых металлов (лом, отработанные катализаторы и др.) приходится от 10 до 33% ежегодного мирового произ-ва этих металлов. Нек-рые изотопы Pd, Ru и Rh накапливаются в продуктах деления U и Pu в ядерных реакторах.
ХАРАКТЕРИСТИКА ПЛАТИНОВЫХ МЕТАЛЛОВ
Конфигурация внеш. электронных оболочек атома
Атомный и ионный радиусы*, нм
S 0 298 , Дж/(моль·К)
* Ионные радиусы даны по Шеннону при координац. числе 6.
** DH пл и DH исп приведены при т-рах соотв. плавления и кипения.
Мировые прогнозные ресурсы платиновых металлов (без социалистич. стран) оцениваются в 75050 т (1985), в т.ч. в ЮАР 62000, США 9300, Зимбабве 3100, Канаде 500, Колумбии 150 т. В осн. это запасы Pt (65%) и Pd (30-32%).
Свойства. Платиновые металлы-светло-серые или серебристые тугоплавкие, труднолетучие металлы (см. табл.); Rh, Pd, Ir, Pt кристаллизуются в гранецентрир. кубич. решетке, Os и Ru- в гексагональной плотноупакованной. По мех. св-вам платиновые металлы заметно различаются: Pt-мягкая, пластичная, легко вытягивается в тончайшую проволоку и прокатывается в фольгу, почти так же пластичен Pd; Os и Ru-хрупкие, Ir-твердый и прочный.
Наиб. характерные степени окисления для палладия +2, платины +2 и +4, иридия +2 и +3, осмия +4, +6 и +8, родия +3, рутения +3, +4 и +8. Платиновые металлы обладают исключительно высокой каталитич. активностью, чаще других как катализаторы используют Pt и Pd. Палладий и в меньшей степени Pt хорошо растворяют H 2 , Pd растворяет H 2 лучше всех металлов (до 800 объемов).
П латиновые металлы отличаются хим. инертностью, наиб. химически стойка Pt. Палладий раств. в горячих конц. HNO 3 и H 2 SO 4 , Pt и Pd и в меньшей степени RU- в царской водке, Ru в присут. окислителей взаимод. с H 2 SO 4 и HClO 4 , Rh медленно реагирует с конц. H 2 SO 4 , HBr, Pt медленно взаимод. с кипящей H 2 SO 4 и горячей HNO 3 , медленно раств. в конц. HBr и HI. Все платиновые металлы раств. в царской водке после оглавления с KHSO 4 или спекания с неорг. пероксидами. Платиновые металлы взаимод. при нагр. со щелочами в присут. O 2 . С O 2 воздуха платиновые металлы образуют тончайшие оксидные пленки на пов-сти: Os при 500-600 0 C, Ru выше 450 0 C, Pt при 900-1000 0 C, Ir и Rh ок. 2000 0 C. Os может гореть на воздухе, a HNO 3 окисляется до OsO 4 .
Известны сотни простых и тысячи комплексных соединений платиновых металлов. В р-рах существуют только комплексные ионы платиновых металлов. Устойчивость высоких степеней окисления платиновых металлов в комплексных соед. уменьшается в рядах Ru > Rh > Pd и Os > Ir > Pt. Платиновые металлы, особенно в низких степенях окисления, представляют собой мягкие льюисовские к-ты по Пирсону; в водных р-рах устойчивость галргенидных комплексов уменьшается в ряду F - Pt > Ru > Os > Pd.
Получение. Способ извлечения и разделения платиновых металлов существенно зависит от типа исходного сырья. Переработка россыпей сводится к добыче песка и его обогащению гравитац. методами. Переработка медно-никелевых сульфидных руд обычно включает операции мех. и флотац. обогащения, пирометаллургич. переработки концентратов и гидрометаллургич. рафинирования (аффинаж).
При переработке медно-никелевых сульфидных руд платиновые металлы концентрируются в разл. полупродуктах произ-ва; большая часть, особенно Pd и Pt, концентрируется в анодных шламах (после электролитич. рафинирования Cu и Ni); из них получают концентраты платиновых металлов, к-рые направляют на аффинажные заводы. Схемы аффинажа платиновых металлов включают после-доват. операции обработки концентрата хим. реагентами. Напр., для выделения Pd и Pt концентраты платиновых металлов обрабатывают царской водкой. К фильтрату, содержащему Pt, Pd и Au, добавляют FeSO 4 и осаждают Au. Из р-ра, содержащего Pd и Pt в виде [PtCl 6 ] 2- и [PdCl 4 ] 2- , добавлением NH 4 Cl осаждают (NH 4 ) 2 [PtCl 6 ], к-рый прокаливают до платиновой губки, затем повторяют растворение в царской водке, осаждение и прокаливание. Р-р, содержащий Pd, обрабатывают водным NH 3 и соляной к-той, при этом осаждается Pd(NH 3 ) 2 Cl 2 ; переосаждение повторяют до получения чистого в-ва, к-рое прокаливают до палладиевой губки. Из оставшегося после обработки царской водкой концентрата, используя последоват. операции сплавления, растворения и осаждения, получают чистые (NH 4 ) 3 [RhCl 6 ], (NH 4 ) 3 [RuCl 6 ], (NH 4 ) 2 [IrCl 6 ], к-рые прокаливают в атмосфере H 2 до Rh, Ru, Ir. В ряде схем аффинажа используют экстракц. методы. Высокочистые платиновые металлы получают методом зонной плавки, вытягиванием монокристаллов из расплава.
Определение. При анализе проб, содержащих от 10 -8 -10 -7 до ~10% платиновых металлов, часто необходимо предварит. кон-центрирование и разделение платиновых металлов. Чаще всего для этого используются метод пробирной плавки (см. Пробирный анализ), сорбц. и экстракц. концентрирование. Метод пробирной плавки основан на высокотемпературном извлечении платиновых металлов расплавленными Pb, Ag, Cu, сплавами Pb с Ag, Cu с Ni, NiS.
При сорбц. методах концентрирования наиб. применение находят сорбенты с комплексообразующими группами. Для разделения платиновых металлов в виде заряженных комплексов с неорг. и орг. лигандами используют хроматографич. методы. Экстракц. методы основаны на избират. извлечении орг. р-рит о-лями из водных р-ров соединений платиновых металлов с экстрагентами. Для концентрирования Ru и Os используют избират. отгонку и экстракцию оксидов MO 4 .
Для анализа проб с низким содержанием платиновых металлов (горные породы, руды и продукты их переработки, технол. р-ры, морская вода и рассолы, речная вода, сбросные воды, реактивы) используют нейтронно-активац., атомно-эмиссионный, атомно-абсорбц., ренттенофлуоресцентный, спект-рофотометрич. методы анализа. Для сплавов, концентратов платиновых металлов, отработанных катализаторов, вторичного сырья платиновых металлов применяют рентгенофлуоресцентный, кулонометрич., атомно-абсорбц., гравиметрич. методы. Примеси благородных и неблагородных металлов в платиновых металлах определяют масс-спектро-метрич., атомно-эмиссионным и атомно-абсорбционными методами.
Применение. Платиновые металлы применяют в виде индивидуальных металлов и их сплавов друг с другом, а также с Au, Ag, Со, Cu и др. Сплавы платиновых металлов обладают большей твердостью, прочностью и устойчивостью к коррозии по сравнению с индивидуальными металлами. Осн. области применения платиновых металлов и их сплавов: катализаторы гидрирования, дегидрирования, окисления, дожигания выхлопных газов автомобилей, в топливных элементах; легирующие добавки в сплавах; материалы для высокотемпературных термопар, термометров сопротивления, электрич. печей сопротивления, химически стойкой посуды, электродов, электрич. контактов, мед. инструментов, стеклоплавильных аппаратов; осн. компонентов резистивных и конденсаторных материалов; тугоплавкие припои; компоненты постоянных магнитов (напр., сплав Pt-Co); защитные покрытия на металлах; ювелирная пром-сть.
История открытия платиновых металлов началась в сер. 18 в., когда испанцы в Южной Америке обнаружили, что при промывке песка вместе с золотом отмывались тяжелые серебристые песчинки, к-рых иногда было больше золота. Такой "песок" загрязнял золото, т. к. по внеш. виду он напоминал серебро и в то же время был полностью "бесполезен", его уничижительно назвали серебришком (plata - по-испански серебро). Однако послед. исследование образцов "тяжелого песка" позволило выделить пять новых элементов. На рубеже 18 и 19 вв. в Великобритании (У. Волластон, С. Теннант), России (А. А. Мусин-Пушкин) и Франции (Л. Воклен, А. Фуркруа) разработаны методы получения ковкой платины, в 1803 Волластон получил Pd, в 1804 он же выделил Rh, а Теннант -Ir и Os. Значительно позднее, в 1844, после четырех лет исследований уральской руды профессор Казанского университета К. К. Клаус выделил новый металл, к-рый он назвал рутением в честь России (ср.-век. лат. Ruthenia-Россия).
Лит.: Аналитическая химия платиновых металлов, M., 1972; Ливинг-стон С., Химия рутения, родия, палладия, осмия, иридия, платины, пер. с англ., M., 1978; Пробоотбирание и анализ благородных металлов. Справочник, 2 изд., M., 1978; Платина, ее сплавы и композиционные материалы, M., 1980; Юделевич И. Г., Старцевa E. А., Атомно-абсорбционное определение благородных металлов, Новосиб., 1981; Благородные металлы. Справочник, M., 1984; Металлургия благородных металлов, 2 изд., M., 1987; Griffith W. R., The chemistry of the rares platinum metals (Os, Ru, Ir and Rh), ed. by A. Cotton, G. Wilkinson, L., 1967. O. M. Петрухин.
§ 2. Платиновые металлы
Все платиновые металлы относятся к числу мало распространенных элементов. Содержание каждого из них в земной коре оценивается следующими величинами (в %):
Скопления платиновых металлов встречаются очень редко и содержат их почти исключительно в самородном состоянии, как незначительную примесь к другим продуктам выветривания горных пород. Количество самой платины в подобных россыпях (аналогичных золотым) обычно бывает гораздо больше, чем остальных металлов платиновой группы. Отделение последних от платины и друг от друга представляет значительные трудности, чем отчасти и обусловлена высокая стоимость рассматриваемых элементов.
1) Ежегодная мировая добыча платиновых металлов составляет около 25 т. Значительные количества палладия (и платины) получают не из платиновых месторождений, а как побочный продукт при переработке никелевых руд. Размеры добычи платины и палладия гораздо больше, чем остальных платиновых металлов.
В свободном состоянии элементы платиновой группы представляют собой тугоплавкие и труднолетучие металлы, по плотности разделяемые иногда на легкие (Ru, Rh, Pd) и тяжелые (Os, Ir, Pt). Их важнейшие константы сопоставлены ниже:
Палладий и платина хорошо поддаются механической обработке, тогда как Ru, Rh, Os и Ir более тверды и хрупки. Для большинства элементов платиновой группы характерна способность поглощать некоторые газы, в частности водород.
2) Наименее активен по отношению к водороду осмий, в компактном состоянии практически не поглощающий этого газа. Наиболее активен палладий, один объем которого способен при обычной температуре поглотить более 700 объемов водорода. Металл при этом вспучивается, становится хрупким и покрывается трещинками. Растворимость водорода в платине гораздо меньше, чем в палладии (причем заметна лишь при повышенных –температурах). Напротив, кислород платина растворяет лучше палладия: при 450 °С один объем платины может поглотить около 70 объемов кислорода, а один объем палладия – 0,07 объема.
По отношению к химическим воздействиям элементы платиновой группы чрезвычайно устойчивы. В виде компактных металлов большинство из них (кроме Pd и Pt) нерастворимо не только в обычных кислотах, но и в царской водке. Последняя легко растворяет платину, а палладий растворим также в HNO3 .
Даже наиболее активные металлоиды при обычных температурах на компактные платиновые металлы не действуют. Более или менее энергичное взаимодействие может быть вызвано нагреванием, причем наблюдаются интересные индивидуальные особенности отдельных элементов: по отношению к кислороду устойчивее других металлов платина, по отношению к сере – рутений, по отношению к хлору – иридий, по отношению к фтору – родий. Наиболее энергично реакции протекают у осмия, тонкий порошок которого медленно окисляется на воздухе (до OsO4 ) даже при обычных условиях. Меньшая химическая устойчивость в очень мелко раздробленном состоянии
Наибольшее практическое значение из элементов платиновой группы имеет сама платина. Она служит для выработки отдельных частей аппаратуры химических заводов, нагревательной обмотки электрических печей, приборов для измерения высоких температур и т. д. Весьма важное применение находит она также в качестве катализатора при различных производственных процессах химической промышленности. Однако около половины всей мировой добычи платины тратится малопроизводительно путем использования ее в ювелирном и зубоврачебном деле.
Соединения элементов платиновой группы сколько–нибудь значительного практического применения пока не находят. Они весьма многочисленны и разнообразны по типам, так как у отдельных металлов известны производные, отвечающие самым различным валентностям – от I до VIII. Однако некоторые из последних малохарактерны и встречаются лишь как исключения. Все элементы платиновой группы отличаются чрезвычайно сильно выражений тенденцией к комплексообразованию.
Производные двухвалентных элементов особенно характерны для палладия и отчасти платины. Последняя образует очень большое число комплексных соединений, но лишь немного простых. Напротив, для палладия двухвалентное состояние является наиболее устойчивым и в том и в другом случае.
Из простых соединений Pd 2+ наиболее важны его соли, большая часть которых легкорастворима. В растворе уже при обычной температуре PdCl2 легко восстанавливается до металла под действием окиси углерода:
На этом основано его применение для открытия СО.
Комплексные производные двухвалентных палладия и платины весьма многочисленны и разнообразны по составу. Наиболее устойчивым из них является платиносинеродистая кислота – H2 [Pt(CN)4 ]. Весьма характерны для платины также хлороплатиниты – соли комплексной кислоты H2 [PtCl4 ].
Соединения трехвалентных элементов наиболее характерны для родия и иридия. Их гидроокиси – желтая Rh(OH)3 и зеленая Ir(ОН)3 – практически нерастворимы в воде. Обе они характеризуются слабо выраженными основными свойствами, а при нагревании легко теряют воду, переходя в черные окислы Э2 О3 . Помимо обычных солей, для обоих элементов известно очень много разнообразных комплексных соединений.
Отвечающие четырехвалентным элементам двуокиси ЭО2 известны для всех платиновых металлов (частично – лишь в форме гидратов). Другие производные этой валентности особенно характерны для самой платины. Красно–коричневая Pt(OH)4 растворима ив кислотах и в сильных щелочах, причем продуктами взаимодействия являются, как правило, не простые соли, а комплексные соединения. Например, взаимодействие с NaOH и НСl протекает по схемам:
Образование комплексных аммиакатов характерно лишь для платины, причем большинство их отвечает типам [Pt(NH3 )6 ]X4 и [Pt(NH3) 4X2 ]X2 . Напротив, анионные комплексы общей формулы М2 [ЭХ6 ] (где X большей частью галоид) известны для всех металлов платиновой группы. Устойчивость их наибольшая у производных платины.
Являющаяся обычным продажным препаратом этого элемента свободная платинохлористоводородная кислота (H2 [PtCl6 ]) может быть получена растворением платины в насыщенной хлором соляной кислоте:
Образованием желтых осадков труднорастворимых хлороплатинатов NH4 + , K + , Rb + и Cs + пользуются иногда для открытия перечисленных катионов.
Производные шестивалентных элементов наиболее характерны для осмия и рутения. Оба металла при сплавлении их со щелочами в присутствии окислителей образуют соли осмиевой или рутениевой кислоты общей формулы М2 ЭО4 по схеме, например:
Как осматы, так и рутенаты в обычных условиях довольно неустойчивы, однако типичный для них характер изменений существенно различен. Рутенаты легко восстанавливаются до RuO2 , которая является наиболее устойчивым кислородным соединением рутения. Напротив, осматы легко окисляются до OsO4 .
Соединения восьмивалентных элементов известны только для осмия и рутения. Взаимодействие порошка металлического осмия с фтором около 250°С ведет к образованию бесцветных паров OsF4 , при охлаждении сгущающихся в лимонно–желтые кристаллы (т. пл. 34 °С, т. кип. 48 °С). С химической стороны восьми–фтористый осмий характеризуется резко выраженными окислительными свойствами. Водой он постепенно разлагается по уравнению:
Четырехокись осмия является наиболее устойчивым при обычных условиях окислом этого элемента и медленно образуется из мелко раздробленного металла и его соединений уже при хранении на воздухе. Четырехокись рутения может быть получена обработкой раствора K2 RuO4 избытком хлора (K2 RuO4 + Cl2 = 2KCl + RuO4 ). Обе четырехокиси представляют собой легколетучие кристаллические вещества бледно–желтого (OsO4 ) или золотисто–желтого (RuO4 ) цвета. В воде они довольно хорошо растворимы, причем растворы не показывают кислой реакции на лакмус.
Хотя сильными окислителями являются обе четырехокиси, однако различие их устойчивости проявляется довольно отчетливо. В то время как OsO4 кипит при 131 °С без разложения, четырехокись рутения при нагревании до 108 °С со взрывом распадается на RuO2 и кислород. При обычных условиях и без соприкосновения с восстановителями OsO4 изменениям не подвергается, тогда как RuO4 может сохраняться только в отсутствие света и влаги. Четырехокись осмия хорошо растворима в спирте, причем восстанавливается им до OsO2 лишь медленно, a RuO4 при соприкосновении со спиртом взрывает. В общем, следовательно, RuO4 значительно менее устойчива, чем OsO4 , и ее окислительные свойства выражены резче. Пары обеих четырехокисей весьма ядовиты.
При всем многообразии образуемых элементами платиновойгруппы соединений основное для химии их практическое использование связано с каталитическими свойствами самих металлов. Ускоряя разнообразные химические процессы, они иногдаособенно способствуют реакциям, протекающим при участии газообразного водорода. Наиболее интересен с этой стороны палладий, в присутствии которого водород уже на холоду и в темноте восстанавливает хлор, бром, иод и кислород, переводит SO2 в H2 S, СlO3 в Cl – , FeCl3 в FeCl2 и т. д. При одновременном наличии кислорода и воды насыщенный водородом палладий способен превращать N2 в NH4 NO2 , т. е. осуществлять связывание свободного азота в обычных условиях температуры и давления.
3) Так как каталитическая активность металла тем больше, чем сильнее развита его поверхность, при изготовлении катализаторов стараются по возможности ее увеличить. С этой целью металл часто осаждают на каком–нибудь индифферентном пористом материале, например асбесте. В частности, платинированный асбест может быть получен пропиткой асбеста разбавленным (1–2%) раствором H2 [PtCl6 ] с последующим его прокаливанием (что вызывает распад по уравнению:
Однако металлические катализаторы часто готовят и без индифферентной основы. Та или иная наиболее удобная для каждого конкретного случая степень дробления металла достигается при этом применением различных методов его выделения. Например, губчатая платина может быть получена слабым прокаливанием (NH4 )2 [PtCl6 ], содержащая более мелко раздробленный металл платиновая чернь – восстановлением раствора H2 [PtCl6 ] металлическим цинком
а еще более раздробленная коллоидная платина – восстановлением того же раствора хлористым оловом
Несмотря на многие отдельные различия, платиновые металлы в общем похожи на элементы семейства железа. И те и другие являются серебристо–белыми или серыми металлами, характеризующимися трудной летучестью, причем их температуры плавления в группе изменяются довольно закономерно, уменьшаясь при переходе снизу вверх и слева направо (наиболее тугоплавок осмий, наименее – никель) Для всех металлов VIII группы характерна высокая каталитическая активность. Их ионы проявляют сильно выраженную тенденцию к комплексообразованию. Производящиеся от них соединения в подавляющем большинстве окрашены.
Почти все элементы VIII группы образуют соединения, отвечающие нескольким различным валентностям, причем изменение последних осуществляется сравнительно легко. При переходе в группе снизу вверх и слева направо наиболее типичная для того или иного элемента валентность в общем, как это видно из приводимого сопоставления, понижается:
Между элементами вертикальных столбцов проявляются отдельные черты и более близкого сходства. Например, для всехкленов ряда Со, Rh, Ir (в противоположность остальным элементам группы) характерно образование аммиакатов типа [Э(NН3 )6 ]Х3 . Члены ряда Fe, Ru, Os являются особенно активными катализаторами при синтезе аммиака из элементов, a Ni, Pd и Pt – при реакциях присоединения водорода к органическим соединениям. Для Fe, Ru и Os кислородные соединения характернее сернистых, тогда как в ряду Ni, Pd, Pt наблюдается обратное. В этом, равно как и в некоторых других отношениях, Fe, Ru и Os похожи на Мn, Тс и Re, a Ni, Pd и Pt – на Cu, Ag и Au. По своим химическим свойствам члены VIII группы являются таким образом переходными между примыкающими к ним элементами подгруппы марганца, с одной стороны, и подгруппы меди – с другой.
Читайте также:
