Металлы с объемно центрированной кубической решеткой
Обновлено: 02.07.2024
Все тела в зависимости от расположения атомов делятся на аморфные и кристаллические. В отличие от аморфных тел, атомы в которых расположены хаотично, металлы в твердом состоянии являются телами кристаллическими. Кристаллическое строение характеризуется закономерным расположением атомов.
Атомы металлов образуют кристаллическую решетку или ячейку. Каждый металл имеет определенный тип кристаллической решетки, чаще всего встречаются три типа решеток: кубическая объемноцентрированная – ОЦК (рис. 16, а), кубическая гранецентрированная – ГЦК (рис. 16, б) и гексагональная – ГПУ (рис. 16, в).
В кубической объемноцентрированной решетке атомы расположены в узлах ячейки и один атом в центре куба. Такие решетки имеют металлы: Feα, Сг, W, Mo, Tiβ, Nb, Та, Li n др.
В кубической гранецентрированной решетке атомы расположены в узлах ячейки и в центре каждой грани. Этот тип решетки имеют металлы: Feγ, Ni, Ag, Au, Pb, Сu, Соβ и др.
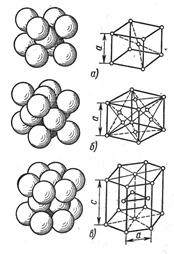
Рис. 16. Типы кристаллических решеток:
а – кубическая объемноцентрированная;
б – кубическая гранецентрированная;
В гексагональной решетке атомы расположены в узлах и центре шестигранных оснований призмы и три атома в средней плоскости призмы. Такую решетку имеют металлы: Zn, Cd, Be, Re, Coα, Tiα и др. Индексы α, β, γ обозначают, что у соответствующих металлов различные кристаллические решетки при различных температурах.
Типы кристаллических ячеек определяются при помощи рентгеноструктурного анализа.
Расстояния между центрами соседних атомов в кристаллической решетке называется периодом (а, b, с). Расстояния между атомами измеряются в ангстремах - , 1 = 1•10 -8 см.
Базис кристаллической решетки - это число атомов, принадлежащих одной элементарной кристаллической ячейке; для ОЦК базис равен 2, для ГЦК – 4, ГПУ – 6.
Плотность упаковки – это отношение объема занимаемого атомами к объему всей ячейки. Плотность упаковки для ОЦК составляет 68%, для ГЦК и ГПУ – 74%. Плотность упаковки характеризуется координационным числом, т. е. числом атомов, находящихся на равном и наименьшем расстоянии от данного атома. Координационное число для ОЦК – 8, для ГЦК и ГПУ – 12.
2.1. Полиморфизм металлов.
Полиморфизмом или аллотропией называют способность металла в твердом состоянии при изменении температуры перестраивать свою кристаллическую решетку. Полиморфные превращения сопровождаются выделением или поглощением теплоты, а также изменением свойств металла. Различные аллотропические состояния называют модификациями. Каждой модификации свойственно оставаться устойчивой лишь в пределах определенного для данного металла интервала температур. Аллотропические формы обозначаются греческими буквами α, β, γ и т. д. На кривых охлаждения и нагрева переход из одного состояния в другое характеризуется остановкой (для чистых металлов) или изменением характера кривой (для сплавов). При аллотропических превращениях кроме изменения свойств (теплопроводности, электропроводности, механических, магнитных и др.) наблюдают изменения объема металла и растворимости (например, углерода в железе). Аллотропические превращения свойственны многим металлам (железу, олову, титану и др.).
Железо известно в двух полиморфных модификациях — α и γ. На рис. 17 приведена кривая охлаждения, характеризующая его аллотропические превращения. Как видно, в интервале температур 911. 1392 °С железо имеет кубическую гранецентрированную решетку γ-железа (γFe), а в интервале от 0 до 911 °С и от 1392 до 1539 °С— объемноцентрированную решетку α-железа (αFe). Железо меняет свои магнитные свойства: выше 768 °С железо немагнитно, а ниже — магнитно.
Кристаллическая структура металлов
Изучение металлов в соответствии с периодической системой элементов Менделеева показывает, что за исключением Mn и Hg элементы подгруппы А, в том числе переходные металлы и большинство редкоземельных элементов, а также металлы подгрупп IB и IIB и некоторые элементы группы IIIB, в том числе Al образуют одну из следующих типичных металлических структур:
А1 – кубическая гранецентрированная решетка (ГЦК)
Кубической гранецентрированной решеткой обладают следующие металлы: g - Fe, Al, Cu, Ni, a - Co, Pb, Ag, Au, Pt и др.
В кубической гранецентрированной решетке атомы располагаются по вершинам элементарной ячейки и в центрах ее граней (рис.1.5).
Каждый атом в этой решетке окружен 12-ю ближайшими соседями, располагающихся на одинаковых расстояниях, равных = 0,707×а, где а – ребро элементарной ячейки. Число ближайших соседей, равное 12-ти называется координационным числом кристаллической решетки. Кроме этих ближайших атомов, в кристаллической решетке имеется 6 атомов, удаленных на значительно большие расстояния, равные а.
Рассматриваемая кристаллическая решетка имеет два вида пустот, (междоузлий, в которых могут располагаться более мелкие атомы других элементов в сплавах) образующих твердые растворы внедрения.
Наибольшие междоузлия или пустоты находятся в центре куба и посередине его ребер. Каждая из этих пустот окружена шестью атомами ГЦК решетки, занимающими места в вершинах правильного октаэдра. В связи с этим, они называются октаэдрическими пустотами (рисунок 1.5, б). Такие положения различных элементов в гранецентрированной кубической решетке занимают атомы Na и Cl в решетке NaCl. Такие же положения занимает углерод в решетке g - Fe.
Кроме этих пустот в ГЦК решетке имеются более мелкие пустоты, называемые тетраэдрическими, в связи с тем, что их окружают 4 атома. Всего в ГЦК решетке 8 тетраэдрических пустот (рисунок 1.5, в).
Размеры тетраэдрических и октаэдрических пустот можно ощутить, если предположить, что решетка построена из жестких шаров, радиусом r, соприкасающихся друг с другом; в этом случае в имеющиеся промежутки можно было бы поместить сферы, радиусом 0,41 r и 0,225 r соответственно для октаэдрической и тетраэдрической пустот.
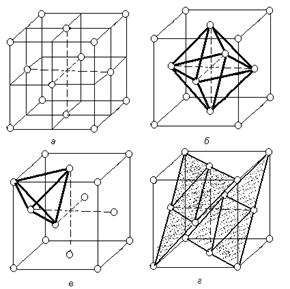 |
| Рисунок 1.5. Гранецентрированная кубическая решетка (а), размещение в ней октаэдрических (б) и октаэдрических (в) пустот; г - расположение плотноупакованных плоскостей (111) |
Наиболее плотноупакованными плоскостями в структуре гранецентрированного куба являются плоскости изображенные на рисунке. Их условное обозначение (рисунок 1.5., г).
Объемно-центрированную кубическую решетку А2 (ОЦК) имеют металлы a - Fe, хром, вольфрам, молибден, ванадий, натрий, литий и другие. Структура А2 является менее плотноупакованной.
Атомы в решетке ОЦК располагаются в вершинах и в центре элементарной ячейки (рисунок 1.6).
Каждый атом в этой ячейке имеет 8 ближайших соседей, располагающихся на расстоянии где, а – длина ребра куба. Следовательно, координационное число решетки равно 8. Иногда его обозначают (8 + 6), т.к. следующие по удаленности атомы расположено на расстоянии а, число их равно 6.
В структуре ОЦК также имеются 2 типа пустот. Крупные занимают положения на гранях куба (рисунок 1.6, в). Они окружены 4 атомами, располагающимися в вершинах тетраэдра, ребра которых попарно равны. Более мелкие пустоты, окруженные 6 атомами, занимающими места в вершинах неправильного октаэдра, располагаются посередине ребер и граней ячейки (рисунок 1.6, г). Если структуру ОЦК решетки построить из жестких шаров, то в тетраэдрические пустоты можно поместить сферы радиусом 0,292 r, а в октаэдрические - 0,154 r.
 |
| Рисунок 1.6. Объемноцентрированная кубическая решетка (а), размещение в ней наиболее плотной системы плоскостей (110) б; тетраэдрических (в) и октаэдрических (г) |
Таким образом, максимальный размер сферы, которую можно поместить в пустоты более плотно упакованной решетки ГЦК оказывается большим, чем в решетку ОЦК.
Внедрение других атомов в октаэдрическую пору ОЦК решетки вызывает смещение двух атомов в направлении параллельными ребру куба, что вызывает расширение решетки в этом направлении. В структуре мартенсита, где атомы углерода внедряются в октаэдрические пустоты, расположенные только на ребрах, параллельных оси С и в центрах граней, перпендикулярных этой оси, это приводит к тетрагональному искажению решетки a - Fe.
Наиболее плотноупакованными плоскостями ОЦК являются 12 плоскостей семейства (рисунок 1.6.б). В этих плоскостях имеются 2 направления, в которых жесткие шары могут соприкасаться.
Гексагональной плотноупакованной решеткой А3 (ГПУ) обладают такие металлы, как Zn, b - Co, Cd, Mg, a - Ti, a - Zr.
Гексагональная решета построена из отдельных слоев, причем таким образом, что каждый атом любого слоя окружен 6 расположенными на равных расстояиях соседями, принадлежащими этому же слою, и, кроме того, имеет по три ближайших соседа в слоях, расположенных выше и ниже данного слоя (рисунок 1.7).
 |
| Рисунок 1.7. Гексагональная плотноупакованная решетка (ГПУ): а - расположение атомов; б - выделенные типы пустот в решетке: октаэдрическая (вверху) и тетраэдрическая (внизу) |
Расстояние между атомами в гексагональных слоях обозначается через а, высота ячейки через с. Шесть ближайших соседей, расположенных в смежных слоях будут также находиться на расстоянии, а от данного атома, если отношение осей с/а составит, то такая структура называется идеальной плотноупакованной. Причем координационное число в этом случае, также как и в ГЦК решетке, равно 12.
Большинство металлов с гексагональной плотноупакованной решеткой имеет отношение осей с/а = 1,56 – 1,63. Исключения составляют Zn и Cd (1,86; 1,89). Это связано с тем, что электронные облака атомов Zn и Cd не обладают сферической симметрией и вытянуты вдоль оси С. В гексагональной плотноупакованной решетке, также как и в ГЦК, имеется 2 вида пустот: октаэдрические и тетраэдрические (рисунок 1.7, б).
Диаметры жестких сфер, которые могут быть помещены в эти пустоты также как и для ГЦК равны 0,41 r и 0,225 r.
Достаточно взглянуть на построение плотноупакованных плоскостей ГЦК решетки (рисунок 1.8, а), чтобы найти полную аналогию в построении атомов в этих двух решетках. Разница этих решеток состоит в чередовании слоев. Если в гексагональной решетке происходит чередование слоев АВАВ и т.д., то в ГЦК решетке: АВСАВС (рисунок 1.8, б), т.е. при этом используется третье возможное положение плотноупакованного слоя.
Разница в энергетическом отношении между этими двумя решетками незначительна и, в связи с этим, последовательность чередования слоев может легко нарушиться при пластической деформации, а также в результате возникновения дефектов кристалла во время его роста, так называемых дефектов упаковки.
Таким образом, кажущаяся разница в построении ГПУ и ГЦК решетки совсем не велика (рисунок 1.8).
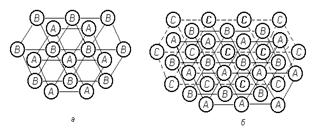 |
| Рисунок 1.8. Схема расположения плотноупакованных атомных слоев в решетках: а - ГПУ; б - ГЦК |
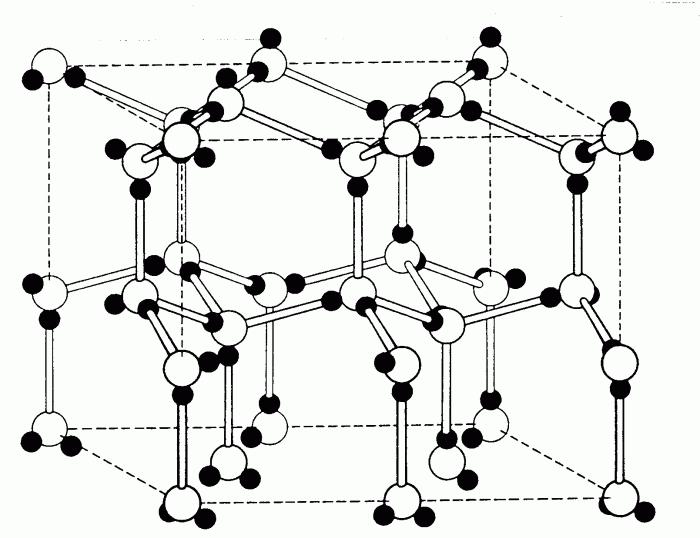
Углерод в виде алмаза, кремний, германий, a - олово (серое) имеют двойную кубическую решетку типа алмаза (рисунок 1.9). Она отличается от ГЦК решетки наличием в четырех из восьми тетраэдрических пустот дополнительно четырех атомов. В результате, структура оказывается более рыхлой.
Каждый атом алмаза окружен лишь четырьмя ближайшими соседями, располагающимися в углах правильного тетраэдра. Координационное число такой структуры равно 4.
Как было показано выше, одни и те же металлы при разных температурах могут иметь разное кристаллическое строение, что вызвано их аллотропией.
Аллотропическим (полиморфным) превращением называют изменение пространственной решетки кристаллического тела.
| Рисунок 1.9. Кристаллическая решетка алмаза |
В качестве примеров аллотропических превращений можно привести превращение низкотемпературной аллотропической формы a - Fe с объемно-центрированной кубической решеткой в высокотемпературную форму g - Fe с гранецентрированной кубической решеткой, при температуре 910 °С и последующее превращение при температуре 1392 °С g - Fe в d - Fe с объемно-центрированной кубической решеткой, аналогичной a - Fe. Аналогичные превращения можно наблюдать в титане, цирконии и т.д. В титане и цирконии низкотемпературной аллотропической формой являются a - Ti, a - Zr с гексагональной плотноупакованной решеткой. При температуре выше 882 °С для титана и 862 °С для циркония образуются b - Ti и b - Zr, обладающие объемно-центрированной решеткой.
Как вы видели, аллотропическое превращение заключается в том, что атомное строение кристаллического тела изменяется при нагреве и охлаждении. Сам процесс перестройки кристаллической решетки происходит изотермически при постоянной температуре, кривая охлаждения сплава претерпевающего аллотропические превращения, аналогична кривой, наблюдаемой при затвердевании жидкого металла. Температура перехода называется критической точкой превращения. При температуре (Т0) наблюдается фазовое равновесие двух аллотропических разновидностей.
Аналогично процессу кристаллизации аллотропическое превращение идет с поглощением тепла при нагреве и выделением его при охлаждении. Аллотропическое превращение (также по аналогии с процессом кристаллизации) происходит путем образования зародышей и их последующего роста, в связи с чем оно протекает всегда с наличием переохлаждения (при охлаждении) и перенагрева при нагреве.
Аллотропическое превращение происходит, так же как и процесс кристаллизации, в связи со стремлением системы к уменьшению свободной энергии.
Основные типы кристаллических решеток
Все металлы являются кристаллическими телами, имеющими определенный тип кристаллической решетки, состоящей из малоподвижных положительно заряженных ионов, между которыми движутся свободные электроны (так называемый электронный газ). Такой тип структуры называется металлической связью.
Тип решетки определяется формой элементарного геометрического тела, многократное повторение которого по трем пространственным осям образует решетку данного кристаллического тела.
| кубическая (1 атом на ячейку) а) | объемно-центрированная кубическая (ОЦК) (2 атома на ячейку) б) | гранецентрированная кубическая (ГЦК) (4 атома на ячейку) в) | гексагональная плотноупакованная (ГП) (6 атомов на ячейку) г) |
Рис. 1.2. Основные типы кристаллических решеток металлов
Металлы имеют относительно сложные типы кубических решеток - объемно центрированная (ОЦК) и гранецентрированная (ГЦК) кубические решетки.
Основу ОЦК-решетки составляет элементарная кубическая ячейка (рис. 1.2,б), в которой положительно заряженные ионы металла находятся в вершинах куба, и еще один атом в центре его объема, т. е. на пересечении его диагоналей. Такой тип решетки в определенных диапазонах температур имеют железо, хром, ванадий, вольфрам, молибден и др. металлы.
У ГЦК-решетки (рис. 1.2, в) элементарной ячейкой служит куб с центрированными гранями. Подобную решетку имеют железо, алюминий, медь, никель, свинец и др. металлы.
Третьей распространенной разновидностью плотноупакованных решеток является гексагональная плотноупакованная (ГПУ, рис. 1.2, г). ГПУ-ячейка состоит из отстоящих друг от друга на параметр с параллельных центрированных гексагональных оснований. Три иона (атома) находятся на средней плоскости между основаниями.
У гексагональных решеток отношение параметра с/а всегда больше единицы. Такую решетку имеют магний, цинк, кадмий, берилий, титан и др.
Компактностькристаллической решетки или степень заполненности ее объема атомами является важной характеристикой. Она определяется такими показателями как параметр решетки, число атомов в каждой элементарной ячейке, координационное число и плотность упаковки.
Параметр решетки - это расстояние между атомами по ребру элементарной ячейки. Параметры решетки измеряется в нанометрах (1 нм = 10 -9 м = 10 Å). Параметры кубических решеток характеризуются длиной ребра куба и обозначаются буквой а.
Для характеристики гексагональной решетки принимают два параметра - сторону шестигранника а и высоту призмы с. Когда отношение с/а = 1,633, то атомы упакованы наиболее плотно, и решетка называется гексагональной плотноупакованной (рис. 1.2 г). Некоторые металлы имеют гексагональную решетку с менее плотной упаковкой атомов (с/а > 1,633). Например, для цинка с/а = 1,86, для кадмия с/а = 1,88.
Параметры кристаллических решеток металлов могут быть измерены с помощью рентгеноструктурного анализа.
При подсчете числа атомов в каждой элементарной ячейке следует иметь в виду, что каждый атом входит одновременно в несколько ячеек. Например, для ГЦК-решетки, каждый атом, находящийся в вершине куба, принадлежит 8 ячейкам, а атом, центрирующий грань, двум. И лишь атом, находящийся в центре куба, полностью принадлежит данной ячейке.
Таким образом, ОЦК- и ГЦК-ячейки содержат соответственно 2 и 4 атома.
Под координационным числом понимается количество ближайших соседей данного атома.
Рис. 1.3. Координационное число в различных кристаллических решетках для атома А:
а) - объемноцентрированная кубическая (К8); б) - гранецентрированная кубическая (К12); в) - гексагональная плотноупакованная (Г12)
В ОЦК решетке (рис. 1.3, а)атом А (в центре) находится на наиболее близком равном расстоянии от восьми атомов, расположенных в вершинах куба, т. е. координационное число этой решетки равно 8 (К8).
В ГЦК решетке (рис. 1.3, б) атом А (на грани куба) находится на наиболее близком равном расстоянии от четырех атомов /, 2, 3, 4, расположенных в вершинах куба, от четырех атомов 5, 6, 7, 8, расположенных на гранях куба, и, кроме того, от четырех атомов 9, 10, 11, 12, принадлежащих расположенной рядом кристаллической ячейке. Атомы 9, 10, 11, 12 симметричны атомам 5, 6, 7, 8. Таким образом, ГЦК решетки координационное число равно 12 (К12).
В ГПУ решетке при с/а = 1,633 (рис. 1.3, в) атом А в центре шестигранного основания призмы находится на наиболее близком равном расстоянии от шести атомов /, 2, 3, 4, 5, 6, размещенных в вершинах шестигранника, и от трех атомов 7, 8, 9, расположенных в средней плоскости призмы. Кроме того, атом А оказывается на таком же расстоянии еще от трех атомов 10, 11, 12, принадлежащих кристаллической ячейке, лежащей ниже основания. Атомы 10, 11, 12 симметричны атомам 7, 8, 9.
Следовательно, для ГПУ решетки координационное число равно 12 (Г12).
Плотность упаковки представляет собой отношение суммарного объема, занимаемого собственно атомами в кристаллической решетке, к ее полному объему. Различные типы кристаллических решеток имеют разную плотность упаковки атомов. В ГЦК решетке атомы занимают 74 % всего объема кристаллической решетки, а межатомные промежутки («поры») 26 %. В ОЦК решетке атомы занимают 68 % всего объема, а «поры» 32 %. Компактность решетки зависит от особенностей электронной структуры металлов и характера связи между их атомами.
От типа кристаллической решетки сильно зависят свойства металла.
1.3. Кристаллографические направления и плоскости
Упорядоченность кристаллического строения в пространственной решетке позволяет выделить отдельные кристаллографические направления и плоскости.
Кристаллографические направления - это характерные прямые линии, выходящие из точки отсчета, вдоль которых в кристаллической решетке располагаются атомы. Точками отсчета, могут служить вершины куба, а кристаллографическими направлениями - его ребра и диагонали, а также диагонали граней (рис. 1.4, а).
Рис. 1.4. Кристаллографические направления и плоскости в кристаллической решетке: а) - основные направления и их обозначение; б), в), г) - основные плоскости и их обозначение
Кристаллографическими плоскостями являются, например, плоскости граней кубов (рис. 1.4, б), а также их различные диагональные плоскости вместе с находящимися на них атомами (рис. 1.4, в, г). Для ГПУ-решеток кристаллографическими плоскостями могут быть плоскости оснований (рис. 1.2, г).
Для определения индекса какого-либо направления необходимо найти индекс ближайшего к данной точке отсчета атома, находящегося на данном направлении. Например, индекс ближайшего атома вдоль оси ОХ обозначается цифрами 100 (рис. 1.4,а). Эти цифры представляют собой координаты упомянутого атома относительно точки О, выраженные через количество параметров вдоль осей OX, OY и OZ соответственно.
Индексы направления ОХ и параллельных ему направлений обозначаются [100]. Соответственно направления OY и OZ обозначаются [010] и [001]. Кристаллографические направления вдоль диагоналей граней XOZ, XOY и YOZ обозначают [101], [110] и [011]. Пользуясь указанной методикой, можно определить индекс любого направления. Например, индекс направления вдоль диагонали куба выразится так: [111].
Для определения индекса кристаллографической плоскости необходимо вначале найти координаты ближайших точек ее пересечения с осями координат, проведенными из точки отсчета О. Затем взять обратные им величины и записать их в круглых скобках в обычной последовательности. Например, координатами точек пересечения с осями координат ближайшей плоскости, параллельной плоскости XOY, выраженными через параметры решеток, являются числа Ґ, Ґ, 1 (см. рис. 1.4, б). Поэтому индекс этой плоскости можно записать в виде (001).
Индексами плоскостей, параллельных плоскостям XOZ и YOZ, окажутся выражения (010) и (100) (рис. 1.4, б). Индекс вертикальной диагональной плоскости куба выразится через (110), (рис. 1.2, в), а индекс наклонной плоскости, пересекающейся со всеми тремя осями координат на удалении одного параметра, примет вид (111) (см. рис. 1.4, г).
1.4. Анизотропия в кристаллах
Под анизотропией понимается неодинаковость механических и других свойств в кристаллических телах вдоль различных кристаллографических направлений. Она является естественным следствием кристаллического строения, так как на различных кристаллографических плоскостях и вдоль различных направлений плотность атомов различна.
Например, в кубических решетках (см. рис. 1.2, б, в) по направлениям вдоль ребер насчитывается меньше атомов, чем вдоль диагоналей куба в ОЦК-решетке или диагоналей граней в ГЦК-решетке. На плоскостях, проходящих через грани ОЦК- и ГЦК-решеток, находится меньше атомов, чем на диагональных плоскостях.
Поскольку механические, физические и химические свойства вдоль различных направлений зависят от плотности находящихся на них атомов, то перечисленные свойства вдоль различных направлений в кристаллических телах должны быть неодинаковыми.
Анизотропия проявляется только в пределах одного монокристалла или зерна-кристаллита. В поликристаллических телах она не наблюдается из-за усреднения свойств по каждому направлению для огромного количества произвольно ориентированных друг относительно друга зерен. Поэтому реальные металлы являются квазиизотропными телами, т. е. псевдоизотропными.
| Рис. 1.5. Элементарная ячейка решетки ОЦК | Сдвиг в кристалле происходит наиболее легко вдоль атомных плоскостей с наиболее плотной упаковкой атомов. Рассмотрим объемно-центрическую кубическую решетку (ОЦК) (рис. 1.5): |
| а) | 1) Плоскость ABCD (рис 1.6 а). Количество атомов в плоскости ABCD – 1; площадьABCD = a 2 ; площадь, приходящаяся на 1 атом – удельная площадь: – мера плотности упаковки. |
| б) Рис. 1.6. Плоскости решетки ОЦК а) - базисная плоскость; б) - плоскость с максимальной упаковкой атомов | 2) Плоскость ABGH (рис 1.6 б). Количество атомов в плоскости ABGH – 2; площадьABGH = a 2 ; |
В плоскости ABGH плотность упаковки больше чем в AB С D . Наиболее вероятен сдвиг вдоль диагональных плоскостей.
1.5. Аллотропия металлов
Некоторые металлы, например, железо, титан, олово и др. способны по достижении определенных температур изменять кристаллическое строение, т. е. изменять тип элементарной ячейки своей кристаллической решетки. Это явление получило название аллотропии или полиморфизма , а сами переходы от одного кристаллического строения к другому называются аллотропическими или полиморфными.
На рис. 1.7 показано изменение свободной энергии F от температуры t для двух вариантов кристаллического строения железа: ОЦК (кривая 1) и ГЦК (кривая 2).
В интервале температур 911-1392оC железо имеет решетку ГЦК, так как при этом его свободная энергия меньше. При t1392°С, у него должна быть решетка ОЦК, обладающая меньшей свободной энергией.
Рис. 1.7. Изменение свободной энергии (F св ) в зависимости от температуры (T) и типа кристаллической решетки: 1 - для ОЦК-решетки; 2 - для ГЦК-решетки
Разные аллотропические формы металлов обозначаются буквами греческого алфавита, при этом низкотемпературные модификации обозначаются буквой a, а последующие в порядке роста температур - буквами b, g ,d ит. д. Аллотропическими формами железа являются: до 911°С - альфа-железо (a-Fe), имеющее ОЦК-решетку, от 911°С до 1392 °С -гамма-железо (g -Fe) с решеткой ГЦК и от 1392°С до 1539 °С т. е. до температуры плавления - снова a-Fe с решеткой OЦK, однако, чтобы отличить его от низкотемпературной модификации, его принято называть дельта-железом (d -Fе).
Известное в практике так называемое немагнитное бета-железо (b -Fe) самостоятельной аллотропической формой не является, так как имеет такую же, как у a-Fe ОЦК-решетку и отличается от него только отсутствием магнитных свойств, которые оно теряет при 768°С (точка Кюри).
1.6. Дефекты кристаллической решетки металла
Кристаллическая решетка, в которой отсутствуют нарушения сплошности и все узлы заполнены однородными атомами называется идеальной кристаллической решеткой металла.
В решетке реального металла могут находиться различные дефекты.
Все дефекты кристаллической решетки принято делить на точечные, линейные, поверхностные и объемные.
Точечные дефекты соизмеримы с размерами атомов. К ним относятся вакансии, т. е. незаполненные узлы решетки, межузельные атомы данного металла (рис 1.8), примесные атомы замещения, т. е. атомы, по диаметру соизмеримые с атомами данного металла и примесные атомы внедрения, имеющие очень малые размеры и поэтому находящиеся в междоузлиях (рис 1.9). Влияние этих дефектов на прочность металла может быть различным в зависимости от их количества в единице объема и характера.
Рис. 1.8. Схема образования пары вакансия-внедренный атом
Рис. 1.9. Примесные атомы внедрения и замещения
Линейные дефекты имеют длину, значительно превышающую их поперечные размеры. К ним относятся дислокации , т. е. дефекты, образующиеся в решетке в результате смещений кристаллографических плоскостей.
Дислокации бывают двух видов.
Наиболее характерной является краевая дислокация (рис. 1.10). Она образуется в результате возникновения в решетке так называемой полуплоскости или экстраплоскости.
Рис. 1.10. Схема краевой дислокации в идеальном кристалле
Нижний ряд экстраплоскости собственно и принято называть дислокацией.
Другим типом дислокации является винтовая дислокация, которая представляет собой некоторую условную ось внутри кристалла, вокруг которой закручены атомные плоскости (рис.1.11).
Рис. 1.11. Схема винтовой дислокация
В винтовой дислокации, так же как в краевой, существенные искажения кристаллической решетки наблюдаются только вблизи оси, поэтому такой дефект может быть отнесен к линейным.
Дислокации обладают высокой подвижностью, поэтому существенно уменьшают прочность металла, так как облегчают образование сдвигов в зернах-кристаллитах под действием приложенных напряжений.
Дислокационный механизм сдвиговой пластической деформации внутри кристаллов может привести к разрушению изделия. Таким образом, дислокации непосредственно влияют на прочностные характеристики металла.
Для оценки этого влияния используется плотность дислокаций, под которой принято понимать отношение суммарной длины дислокаций к объему содержащего их металла. Плотности дислокаций измеряется в см-2 или м-2.
На рис. 1.12 в виде кривой ABC схематически показана зависимость прочности металла от плотности дислокаций. Точка А соответствует теоретической прочности металла, обусловленной необходимостью одновременного разрыва всех межатомных связей, проходящих через плоскость сдвига, в случае отсутствия дислокаций.
При увеличении количества дислокаций (см. участок АВ) прочность резко снижается, так как на несколько порядков уменьшаются усилия, необходимые для осуществления сдвигов в зернах металла при его деформировании и разрушении.
Рис. 1.12. Зависимость предела прочности кристалла от плотности линейных дефектов(дислокаций). Кривая Одинга
При плотности дислокаций 106-107 см-2 (точка В на кривой), прочности минимальна, и на участке ВС происходит ее рост. Это объясняется тем, что с ростом плотности дислокаций их передвижение происходит не только по параллельным, но и по пересекающимся плоскостям, что существенно затрудняет процесс деформирования зерен.
Поэтому начиная с точки В прочность металла возрастает.
Максимальная плотность дислокаций, может составить 1013 см-2. При дальнейшем росте плотности дислокаций происходит разрушение металла.
Поверхностные дефекты включают в себя главным образом границы зерен (рис.1.13). На границах кристаллическая решетка сильно искажена. В них скапливаются перемещающиеся изнутри зерен дислокации.
Из практики известно, что мелкозернистый металл прочнее крупнозернистого. Так как у последнего меньше суммарная протяженность (площадь) границ. То можно сделать вывод, что поверхностные дефекты способствуют повышению прочности металла. Поэтому создано несколько технологических способов получения мелкозернистых сплавов.
Рис.1.13. Структура границы двух соседних кристаллических зерен
Объемные дефекты кристаллической решетки включают трещины и поры. Наличие данных дефектов, уменьшая плотность металла, снижает его прочность.
Кроме того, трещины являются сильными концентраторами напряжений, в десятки и более раз повышающими напряжения создаваемые в металле рабочими нагрузками. Последнее обстоятельство наиболее существенно влияет на прочность металла.
Контрольные вопросы по лекции №1
В чем состоит существенная разница между строением аморфных и кристаллических тел? Что такое кристаллическая решетка?
Перечислите основные типы ячеек кристаллических решеток металлов. Что такое параметры решеток?
Что понимается под кристаллографическими направлениями и плоскостями и как они обозначаются?
Что такое анизотропия свойств в кристаллах, чем она обусловлена? Привести пример.
Почему поликристаллические тела являются изотропными? Что такое квазиизотропия (псевдоизотропия)?
Что такое аллотропия (полиморфизм) металлов и каково ее практическое значение?
Что представляют собой краевые дислокации, какова их роль в протекании пластической деформации металла и как они влияют на его прочность?
Что такое плотность дислокаций и как она влияет на характер изменения прочности металла?
Кубическая гранецентрированная решетка — координационное число, структура и геометрия

Координационное число (в химии и кристаллографии) — характеристика, которая определяет число ближайших частиц (ионов или атомов) в молекуле или кристалле.
Структура решетки
Атомы расположены в центрах граней и вершинах простой кубической решетки. Соответствует одной из возможных плотных упаковок шаров в пространстве. Ближайшие друг к другу атомы формируют тетраэдры и октаэдры, полностью заполняющие пространство. Область пространства, лежащая ближе к данному атому, чем к остальным атомам, для ГЦК решетки представляет собой ромбододекаэдр. Атомы, ближайшие к данному, лежат на вершинах кубооктаэдра.
А) объемноцентрированная кубическая
б) гранецентрированная кубическая
в) гексагональная плотноупакованная
Некоторые металлы, в зависимости от температуры, могут иметь различный тип кристаллической решётки, т.е. могут существовать в различных кристаллических модификаций.
Полиморфизм (аллотропия) – когда металл имеет разную кристаллическую решётку в зависимости от условия образования. Переход одной решётки в другую называется полиморфное или аллотропическое состояние. Полиморфные превращения в металлах происходят при изменении температуры. Так, при температуре свыше 723°С железо переходит из α – модификации в γ – модификацию, при этом изменяются физико-механические свойства металла.
Чтобы отличить одну кристаллическую решётку железа Fe от другой ставят значок α или γ
В монокристаллах свойства металла по различным направлениям различны – это явление носит название анизотропией.
В реальных поликристаллических металлах свойства по любому направлению одинаково – это явление называется изотропией.
Металлы обладают целым рядом общих свойств:
Высокая электо- и теплопроводимость
Характерный металлический блеск
Положительный коэффициент электросопротивления
Способность к значительной пластической деформации
Одним из самых распространенных материалов, с которым всегда предпочитали работать люди, был металл. В каждую эпоху предпочтение отдавалось разным видам этих удивительных веществ. Так, IV-III тысячелетия до нашей эры считаются веком хальколита, или медным. Позже его сменяет бронзовый, а затем в силу вступает тот, что и по сей день является актуальным — железный.
Сегодня вообще сложно представить, что когда-то можно было обходиться без металлических изделий, ведь практически все, начиная от предметов быта, медицинских инструментов и заканчивая тяжелой и легкой техникой, состоит из этого материала или включает в свой состав отдельные части из него. Почему же металлы сумели завоевать такую популярность? В чем проявляются особенности и как это заложено в их строении, попробуем разобраться далее.
Распространенность в природе
Этой решеткой обладает ряд металлов (алюминий, золото, медь, серебро, никель, платина и др.), ее образуют при конденсации инертные газы.
Общее понятие о металлах
«Химия. 9 класс» — это учебник, по которому проходят обучение школьники. Именно в нем подробно изучаются металлы. Рассмотрению их физических и химических свойств отведена большая глава, ведь разнообразие их чрезвычайно велико.
Именно с этого возраста рекомендуют давать детям представление о данных атомах и их свойствах, ведь подростки уже вполне могут оценить значение подобных знаний. Они прекрасно видят, что окружающее их разнообразие предметов, машин и прочих вещей имеет в своей основе как раз металлическую природу.
Что же такое металл? С точки зрения химии, к данным атомам принято относить те, что имеют:
- малое число электронов на внешнем уровне;
- проявляют сильные восстановительные свойства;
- имеют большой атомный радиус;
- как простые вещества обладают рядом специфических физических свойств.
Основу знаний об этих веществах можно получить, если рассмотреть атомно-кристаллическое строение металлов. Именно оно объясняет все особенности и свойства данных соединений.
В периодической системе для металлов отводится большая часть всей таблицы, ведь они образуют все побочные подгруппы и главные с первой по третью группу. Поэтому их численное превосходство очевидно. Самыми распространенными являются:
Все металлы имеют ряд свойств, которые позволяют объединять их в одну большую группу веществ. В свою очередь, эти свойства объясняет именно кристаллическое строение металлов.

Геометрия решетки
Орты (единичные векторы) , задающие направление от некоторого атома кристаллической решетки к его ближайшим соседям, могут быть представлены в виде:
где — орты Декартовой системы координат.
Безразмерные параметры координационного тензора
Свойства металлов
В чем же заключается такое строение, чем характеризуется? Само название говорит о том, что все металлы представляют собой кристаллы в твердом состоянии, то есть при обычных условиях (кроме ртути, которая является жидкостью). А что такое кристалл?
Это условное графическое изображение, построенное путем пересечения воображаемых линий через атомы, которые выстраивают тело. Другими словами, каждый металл состоит из атомов. Они располагаются в нем не хаотично, а очень правильно и последовательно. Так вот, если мысленно соединить все эти частицы в одну структуру, то получится красивое изображение в виде правильного геометрического тела какой-либо формы.
Это и принято называть кристаллической решеткой металла. Она очень сложная и пространственно объемная, поэтому для упрощения показывают не всю ее, а лишь часть, элементарную ячейку. Совокупность таких ячеек, собранная вместе и отраженная в трехмерном пространстве, и образует кристаллические решетки. Химия, физика и металловедение — это науки, которые занимаются изучением особенностей строения таких структур.
Сама элементарная ячейка — это набор атомов, которые располагаются на определенном расстоянии друг от друга и координируют вокруг себя строго фиксированное число других частиц. Она характеризуется плотностью упаковки, расстоянием между составными структурами, координационным числом. В целом все эти параметры являются характеристикой и всего кристалла, а значит, отражают и проявляемые металлом свойства.
Существует несколько разновидностей кристаллических решеток. Объединяет их все одна особенность — в узлах находятся атомы, а внутри располагается облако электронного газа, которое формируется путем свободного передвижения электронов внутри кристалла.
Типы кристаллических решеток
Четырнадцать вариантов строения решетки принято объединять в три основных типа. Они следующие:
- Объемно-центрированная кубическая.
- Гексагональная плотноупакованная.
- Гранецентрированная кубическая.
Кристаллическое строение металлов было изучено только благодаря электронной микроскопии, когда стало возможным получать большие увеличения изображений. А классификацию типов решеток впервые привел французский ученый Браве, по фамилии которого их иногда называют.

Объемно-центрированная решетка
Строение кристаллической решетки металлов данного типа представляет собой следующую структуру. Это куб, в узлах которого находится восемь атомов. Еще один располагается в центре свободного внутреннего пространства ячейки, что и объясняет название «объемно-центрированная».
Это один из вариантов наиболее простого строения элементарной ячейки, а значит, и всей решетки в целом. Такой тип имеют следующие металлы:
- молибден;
- ванадий;
- хром;
- марганец;
- альфа-железо;
- бетта-железо и другие.
Основные свойства таких представителей — высокая степень ковкости и пластичности, твердость и прочность.
Гранецентрированная решетка
Кристаллическое строение металлов, имеющих гранецентрированную кубическую решетку, представляет собой следующую структуру. Это куб, который включает в свой состав четырнадцать атомов. Восемь из них формируют узлы решетки, а еще шесть расположены по одному на каждой грани.
Подобную структуру имеют:
Основные отличительные свойства — блеск разного цвета, легкость, прочность, ковкость, повышенная устойчивость к коррозии.

Гексагональная решетка
Кристаллическое строение металлов, обладающих данным типом решетки, следующее. В основе элементарной ячейки лежит шестигранная призма. В ее узлах располагается 12 атомов, еще два по основаниям и три атома свободно лежат внутри пространства в центре структуры. Всего семнадцать атомов.
Подобную сложную конфигурацию имеют такие металлы, как:
Основные свойства — высокая степень прочности, сильный серебристый блеск.
Дефекты кристаллического строения металлов
Однако все рассмотренные типы ячеек могут иметь и естественные недостатки, или так называемые дефекты. Это может быть связано с разными причинами: посторонними атомами и примесями в металлах, внешними воздействиями и прочим.
Поэтому существует классификация, отражающая дефекты, которые могут иметь кристаллические решетки. Химия как наука изучает каждый из них с целью выявления причины и способа устранения, чтобы свойства материала не были изменены. Итак, дефекты следующие.
- Точечные. Они бывают трех основных видов: вакансии, примеси или дислоцированные атомы. Приводят к ухудшению магнитных свойств металла, электро- и теплопроводности его.
- Линейные, или дислокационные. Выделяют краевые и винтовые. Ухудшают прочность и качество материала.
- Поверхностные дефекты. Влияют на внешний вид и структуру металлов.
В настоящее время разработаны методики устранения дефектов и получения чистых кристаллов. Однако совсем искоренить их не удается, идеальной кристаллической решетки не существует.

Значение знаний о кристаллическом строении металлов
Из вышеизложенного материала очевидно, что знания о тонкой структуре и строении позволяют спрогнозировать свойства материала и повлиять на них. И это позволяет делать наука химия. 9 класс общеобразовательной школы делает в процессе обучения упор на то, чтобы сформировать у учащихся четкое понятие о важном значении основополагающей логической цепочки: состав — строение — свойства — применение.
Сведения о кристаллическом строении металлов очень четко иллюстрирует эту зависимость и позволяет учителю наглядно объяснить и показать детям, насколько важно знать тонкую структуру, чтобы правильно и грамотно использовать все свойства.
Кол-во блоков: 18 | Общее кол-во символов: 12839
Количество использованных доноров: 3
Информация по каждому донору:
Параметры решетки, базис, координационное число

Металлы – особая группа элементов в периодической таблице Менделеева. В отличие от неметаллов элементы этой группы являются исключительно восстановителями с положительной степенью окисления, а также обладают пластичностью, твёрдостью, упругостью, что обусловлено кристаллическим строением металлов.
Общее строение
Металлы – твёрдые вещества, имеющие кристаллическое строение. Исключение составляет ртуть – жидкий металл. Кристаллические решётки представляют собой упорядоченные определённым образом атомы металла. Каждый атом состоит из положительно заряженного ядра и нескольких отрицательно заряженных электронов. В атомах металлов недостаточно электронов, поэтому они являются ионами.
Единица кристаллической решётки – элементарная кристаллическая ячейка, в условных узлах и на гранях которой находятся положительно заряженные ионы. Их удерживают вместе металлические связи, возникающие за счёт беспорядочного движения отделившихся от атомов электронов (благодаря чему атомы превратились в ионы).
Отрицательно заряженные электроны держат на равном расстоянии положительно заряженные электроны, предавая кристаллической решётке правильную геометрическую форму.

Рис. 1. Схема металлической связи.
Свободное движение электронов обусловливает электро- и теплопроводность металлов.
Примеры материалов
Все металлы характеризуются кристаллическим строением. Они отличаются наличием малоподвижных ионов с положительным зарядом и движущимися между ними электронами. Данные структуры именуют металлическими связями.
Объемно-центрированная кубическая решетка свойственна для Fe при комнатной температуре, W, V, Cr, Mo и прочих металлов.

Гранецентрированная кубическая решетка встречается на Mg, Ti, Zn, Zr и прочих металлах.
Виды решёток
Элементарные кристаллические ячейки могут иметь различную конфигурацию. В связи с этим выделяют три типа кристаллических решёток:
- объемно-центрированная (ОЦК) кубическая – состоит из 9 ионов;
- гранецентрированная (ГЦК) кубическая – включает 14 ионов;
- гексагональная плотноупакованная (ГПУ) – состоит из 17 ионов.
ОЦК представляет собой куб, в узлах которого находится по атому. В центре куба, на пересечении диагоналей располагается девятый ион. Этот тип характерен для железа, молибдена, хрома, вольфрама, ванадия.
Элементарной кристаллической ячейкой типа ГЦК является куб с ионами в узлах и в середине каждой грани – на пересечении диагоналей. Такое строение имеют медь, серебро, алюминий, свинец, никель.
Третий тип имеет вид гексагональной призмы, в узлах которой находится по шесть ионов с каждой стороны. Посередине между шестью узлами располагается по одному иону. В середине призмы между шестиугольными гранями находится равносторонний треугольник, который составляют три иона.

Рис. 2. Типы решёток.
Металл может содержать большое количество дефектов атомного строения. Дефекты влияют на свойства металла.
Структура и геометрия
Кристаллические решетки представляют совокупность кристаллитов. В ближних зернах они взаимно расположены под некоторым углом. Атомы, представляющие собой микроскопические частицы вещества и наименьшие части химических элементов, в кристаллитах размещены в соответствии с ближним и дальним порядком. Первый подразумевает определенный порядок размещения и стабильности ближайших друг к другу микрочастиц, второй – самых отдаленных. Возможно покидание отдельными атомами мест расположения вследствие диффузии, однако это не приводит к нарушению упорядоченности строения.

Тип решетки определяют формой простейшего геометрического тела, образующего ее. Кубические решетки дифференцируют на четыре вида:
- кубическая с микрочастицами в углах;
- объемно-центрированный вариант имеет восемь атомов, расположенных по углам, и один в центре;
- гранецентрированная кубическая решетка отличается размещением атомов в центрах граней и вершинах;
- гексагональная плотноупакованная с нахождением микрочастиц в углах шестигранной призмы, в центре оснований и трех в центральной плоскости.
К основным параметрам решеток относят компактность, под которой понимают степень заполнения объема атомами. Ее определяют тремя прочими показателями:
- параметр решетки – значение межатомного расстояния в нм по ребру простейшей ячейки (характеризуется для кубических вариантов длиной ребра);
- координационное число, под которым понимают количество ближайших соседних микрочастиц;
- плотность упаковки, представленная отношением общего атомного объема решетки и ее общего объема.

Для измерения параметра решеток применяют рентгеноструктурный метод анализа. При подсчете количества атомов учитывают, что каждый из них принадлежит к нескольким ячейкам сразу. Для кубических решеток исключение представляет размещенная в центре куба микрочастица.
Для объемно-центрированного типа координационное число составляет 8 по числу ближайших атомов к центральному. Для гранецентрированного варианта микрочастица на кубической грани размещена на одинаковом расстоянии от четырех в углах, четырех на гранях, четырех ближайшей кристаллической ячейки. То есть, координационное число составляет 12.
Различные варианты кристаллических решеток характеризуются разной плотностью упаковки. Для простой кубической решетки координационное число равно 6, для ОЦК — 8, ГЦК и ГП (гексагональной плотноупакованной) — 12.
Для объемно-центрированного варианта объемы микрочастиц и межатомных промежутков соотносятся в пропорции 68/32%, для ГЦК значения соответствующих параметров равны 74 и 26% соответственно. Компактность решетки определяется особенностями металлической электронной структуры и характером атомной связи.
Ввиду упорядоченности решетки возможно выделение кристаллографических плоскостей и направлений.
Под направлениями понимают прямые, вдоль которых находятся атомы. То есть они представлены ребрами, диагоналями и гранями.
Плоскости подразделяют на диагональные и плоскости кубических граней.
Для обозначения данных категорий применяют трехзначные индексы. Для направлений их определяют путем нахождения ближайшего атома и использования его координат относительно точки O. Для плоскостей находят координаты точек их пересечения с осями координат и меняют на обратные.
Следует отметить, что в кристаллических телах наблюдается изменение механических свойств вдоль направлений. Данная особенность, называемая анизотропией, объясняется различной атомной плотностью. Так, для кубических решеток вдоль диагоналей и на диагональных плоскостях данный показатель больше, чем вдоль ребер и на проходящих сквозь грани плоскостях. При этом анизотропия наблюдается в пределах кристаллита либо монокристалла. Для поликристаллических тел она нехарактерна ввиду усреднения параметров по всем направлениям для большого числа произвольно взаимно ориентированных зерен. Ввиду этого металлы относят к псевдо- или квазиизотропным телам.
Кроме того, для некоторых металлов (Ti, Fe, Sn) характерна аллотропия, под которой понимают изменение кристаллического строения путем изменения типа простейшей ячейки. Также данное свойство называют полиморфизмом.
Так, у железа в температурном интервале 911-1392 °C кубическая решетка гранецентрированного типа, а при температурах за пределами приведенного диапазона – отдельно-центрированная (до плавления при 1539 °C). Для дифференциации аллотропических форм применяют греческие буквы.
Возможно наличие дефектов решетки. Их классифицируют на несколько типов.
- Точечные, по размеру близкие к атомам, представлены вакансиями (пустые узлы, межузельные микрочастицы), примесными атомами замещения (того же размера, что и исходные) и внедрения (маленькие микрочастицы в междоузлиях).
- Линейные (протяженные) представлены дислокациями (плоскостные смещения). Их классифицируют на наиболее распространенные краевые (экстраплоскость или полуплоскость) и винтовые (закручивание плоскостей).
- Поверхностные – искажения на границах зерен ввиду передвигающихся зерен дислокации.
- Объемные – поры и трещины.

Названные дефекты по-разному сказываются на прочности. Для точечных степень влияния на данный показатель определяется их характером и числом в конкретном объеме. Линейные дефекты ввиду большой подвижности значительно сказываются на прочности, упрощая сдвиги кристаллитов под влиянием напряжений. Воздействие линейных дефектов на прочность оценивают по их плотности (отношение их общей длины к объему материала). Ее предельное значение – 1013 см-2 (при большем происходит разрушение). На основе того, что мелкозернистые материалы более прочны в сравнении с крупнозернистыми при большей общей протяженности границ, поверхностные дефекты наоборот повышают прочность. Объемные, помимо непосредственного снижения прочности, значительно повышают напряжения от рабочих нагрузок, концентрируя их.
Характеристика решётки
Кристаллические решётки характеризуются компактностью или степенью наполненности. Компактность определяют показатели:
- параметр решётки – расстояние между атомами;
- число атомов;
- координационное число – количество соседних ячеек;
- плотность упаковки – отношение объёма, занимаемого атомами, к полному объёму решётки.
При подсчёте количества атомов следует помнить, что атомы в узлах и на гранях входят в состав соседних ячеек.

Рис. 3. Кристаллические ячейки составляют решётку.
В огромном ряду материалов, с незапамятных времен известных человеку и широко используемых им в своей жизни и деятельности, металлы всегда занимали особое место. Причина этого — в особых свойствах металлов, выгодно отличающих их от других материалов и делающих во многих случаях незаменимыми.
– один из классов конструкционных материалов, характеризующийся определенным набором свойств:
· «металлический блеск» (хорошая отражательная способность);
Данные свойства обусловлены особенностями строения металлов. Согласно теории металлического состояния, металл представляет собой вещество, состоящее из положительных ядер, вокруг которых по орбиталям вращаются электроны. На последнем уровне число электронов невелико и они слабо связаны с ядром. Эти электроны имеют возможность перемещаться по всему объему металла, т.е. принадлежать целой совокупности атомов. Таким образом, пластичность, теплопроводность и электропроводность обеспечиваются наличием «электронного газа».
Все металлы, затвердевающие в нормальных условиях, представляют собой кристаллические вещества, то есть укладка атомов в них характеризуется определенным порядком – периодичностью, как по различным направлениям, так и по различным плоскостям. Этот порядок определяется понятием кристаллическая решетка.
Элементарная ячейка
– элемент объема из минимального числа атомов, многократным переносом которого в пространстве можно построить весь кристалл.
Все металлы и металлические сплавы – тела кристаллические. Атомы (ионы) расположены в металлах закономерно, в геометрически правильном порядке и образуют пространственную кристаллическую решетку.
Решетка характеризуется наличием каркаса из малоподвижных заряженных ионов, в промежутках которого с огромной скоростью движутся свободные электроны. Если через атомы в кристаллических решетках провести плоскости, то атомы в них будут располагаться в геометрически правильном порядке, образуя кристаллографические плоскости. Наименьший объем металла, который характеризует атомно–кристаллическое строение всего объема, называется элементарной кристаллической решеткой.
Пространственные кристаллические решетки полностью определяют строение кристалла.
Различают простые и сложные кристаллические решетки. В простой решетке атомы (ионы) расположены только в вершинах, а в сложных – они могут находиться также внутри многогранника или на его гранях.
Металлы имеют сложные кристаллические решетки. Всего существует четырнадцать типов решеток, но основными являются три — это:
— Объемно-центрированная кубическая решетка (ОЦК);
— Гранецентрированная кубическая решетка (ГЦК);
— Гексагональная плотноупакованная решетка (ГПУ).
1) В элементарной ячейке ОЦК атомы находятся в вершинах куба и в центре на пересечении пространственных диагоналей. Всего 9 атомов (рис.1).
2) В гранецентрированной кубической решетке атомы расположены в вершинах куба и в центрах каждой грани куба. Всего 14 атомов (рис.2).
3) Гексагональная плотноупакованная решетка. Элементарная ячейка – шестигранная призма, в которой атомы находятся в вершинах и в центре оснований призмы, а также внутри призмы — 3 атома. ГПУ содержит 17 ионов (рис.3).
Кристаллические решетки характеризуют следующие основные параметры: период решетки, атомный радиус, координационное число, базис и коэффициент компактности решетки.
- Периодом решетки называется расстояние между центрами двух соседних частиц (атомов, ионов) в элементарной ячейке решетки (a,b,с). Периоды решетки выражаются в ангстремах – А (1А=10-8 см).
- Под атомным радиусом понимают половину межатомного расстояния между центрами ближайших атомов в кристаллической решетке элемента при нормальной температуре и атмосферном давлении. Однако атомный радиус не является неизменной величиной, а изменяется в зависимости от ряда факторов, важнейшим из которых являются координационное число и тип химической связи между атомами в кристалле.
- Координационное число Кпоказывает количество атомов, находящихся на наиболее близком и равном расстоянии от любого выбранного атома в решетке. Чет выше координационное число, тем плотнее пространственная кристаллическая решетка материала.
- Базисом решетки называется количество атомов, приходящихся на одну элементарную ячейку решетки.
- Коэффициент компактности η решетки определяется отношением объема, занимаемого атомами Va, ко всему объему решетки Vp, т.е. η = Va / Vp.
Рассмотрим эти параметры для основных типов кристаллических решеток.

ОЦК решетка
Период решетки – а = 0,286 — 0,607 нм.
Координационное число К
Каждый угловой атом входит в восемь соединительных ячеек, следовательно, одной ячейке принадлежит от угловых атомов только 1/8 атома; только внутренний атом целиком принадлежит данной ячейки. Таким образом, на одну ячейку объемно-центрированной кристаллической решетки приходится 8 * 1/8 + 1 = 2 атома.
Объемно-центрированную кубическую решетку имеют металлы: Li, Na, K, V, Cr, Feα, Rb, Nb, Mo, W и др.
ГЦК решетка
Период решетки – а.
Каждый угловой атом входит в восемь ячеек, а находящийся в центре грани – в две соседние ячейки; в центре атома нет. Следовательно, на одну ячейку приходится 8*1/8+6*1/2 = 4 атома.
Гранецентрированную кубическую решетку имеют металлы: AI, Ca, Feγ, Ni, Cu, Pb, Ag, Pt, Au, Pd и др.
ГПУ решетка
Период решетки а и с (а = 0,228 — 0,398 нм; с = 0,357 — 0,652 нм), причем с/а = 1,633 (если с/а > 1,633, то данная решетка будет гексагональной, но не плотноупакованная, характерная для Mg, Zn).
Базис решетки – 6 атомов.
На одну ячейку кристаллической решетки приходится 6 атомов: 2 атома, лежащие в центре шестиугольника, входят в две соседние ячейки (2*1/2) = 1атом, а 12 атомов, образующие вершины призмы, — в 6 соседних ячеек (12*16/) = 2 атома, 3 атома, лежащие внутри призмы, целиком принадлежат данной ячейке (3*1 = 3 атома).
В гексагональной системе кристаллизуются Be, Мg, Cd, Ti, Co, Zn и другие металлы.
Многие металлы при разных температурах имеют неодинаковые кристаллические решетки. Это явление называется полиформизмом или аллотропией (например Fe, имеет α и γ решетки).
Читайте также:
