Методы изолирования металлических ядов
Обновлено: 02.05.2024
доктор фарм. наук Камаева С.С., доцент кафедры Фармация ФПК и ППС, к.фарм.н. Воробьева Н.В.
Учебно-методическое пособие по токсикологической химии для студентов 4 курса очного отделения фармацевтического факультета / И.К. Петрова, Р.И.Мустафин – Казань: КГМУ, 2013 – 80 с.
Учебно-методическое пособие по токсикологической химии для студентов 4 курса очного отделения фармацевтического факультета соответствует федеральному государственному образовательному стандарту по специальности «Фармация» от 2011 года.
© Казанский государственный медицинский университет, 2013
Оглавление
1. Изолирование соединений, содержащих «металлические» яды из биологического материала _______________________________________5
1.1. Разрушение биоматериала азотной и серной кислотами ___________6
1.2. Разрушение биоматериала хлорной, азотной и серной кислотами___7
1.3. Разрушение биоматериала пергидролем и серной кислотой________8
1.4. Разрушение биоматериала методом сухого озоления_____________9
2. Дробный метод анализа минерализата________________________10
2.1. Исследование осадка _______________________________________17
2.1.1. Соединения свинца _______________________________________17
2.1.2. Соединения бария ________________________________________21
2.2. Исследование фильтрата ____________________________________23
2.2.1. Соединения марганца _____________________________________23
2.2.2. Соединения хрома________________________________________25
2.2.3. Соединения серебра ______________________________________27
2.2.4. Соединения меди_________________________________________30
2.2.5. Соединения сурьмы_______________________________________32
2.2.6. Соединения таллия _______________________________________34
2.2.7. Соединения мышьяка _____________________________________36
2.2.8. Соединения висмута ______________________________________41
2.2.9. Соединения цинка ________________________________________43
2.2.10. Соединения кадмия ______________________________________46
2.2.11. Соединения ртути________________________________________48
3. Методы количественного определения «металлических» ядов в минерализате _________________________________________________52
3.1. Гравиметрический метод____________________________________52
3.2. Титриметрические методы___________________________________53
3.3. Фотоколориметрический метод_______________________________54
3.4. Атомно-абсорбционная спектроскопия ________________________59
3.5. Эмиссионный спектральный анализ___________________________59
3.6 Рентгено-флуоресцентный метод______________________________59
Вопросы для самоконтроля______________________________________60
Ситуационные задачи __________________________________________76
Введение
Группа веществ, изолируемых минерализацией, включает так называемые «металлические» яды. В настоящее время одной из актуальнейших проблем является ухудшение здоровья населения в связи с различными вредными факторами окружающей среды. Постоянно ухудшающаяся экологическая обстановка приводит к увеличению суммарной токсигенной нагрузки на человека. Определенное количество «тяжелых» металлов поступает в пищевые продукты из воздуха, загрязненной почвы, питьевой воды, переработанного сырья и из металлических деталей и изделий, в которых проводится переработка и хранение сырья. Широкое распространение лекарственных препаратов, в составе которых также нормируется содержание «тяжелых» металлов, ввиду возможного их присутствия, создаются условия для возникновения острых отравлений в результате их неправильного применения в целях самолечения и суицида. Правилами судебно-химического исследования при проведении ненаправленного анализа предусмотрено обязательное исследование на «металлические» яды.
В учебно-методическом пособии приводятся сведения по методам изолирования «металлических» ядов, химического анализа минерализата с использованием дробного метода. Пособие разработано с целью оказания помощи студентам 4 курса очного отделения при освоении ПК-39 (способность и готовность к участию в проведении химико-токсикологического исследования с целью диагностики отравлений, наркотических и алкогольных опьянений); ПК-35 (способность и готовность проводить анализ лекарственных средств с помощью химических, биологических, хроматографических и физико-химических методов в соответствии с требованиями ГФ).
По результатам освоения данной дисциплины решаются следующие задачи: студенты овладевают профессиональными умениями и навыками практического определения «металлических» ядов в различных объектах исследования с использованием приемов и методов, принятых в химико-токсикологическом анализе.
Учебно-методическое пособие по токсикологической химии для студентов 4 курса очного отделения фармацевтического факультета составлено в соответствии с федеральным государственным образовательным стандартом 3 поколения по специальности «Фармация», с учетом требований приказов МЗ РФ, а также в связи с отсутствием современного учебника по курсу токсикологической химии.
Пособие, несомненно, будет полезно для студентов 4 курса фармацевтического факультета при изучении большого раздела курса токсикологической химии: «Группа веществ, изолируемых минерализацией («металлические» яды)».
1. Изолирование соединений, содержащих «металлические» яды из биологического материала
В судебно-химическом и химико-токсикологическом анализе при исследовании биологического материала (органов трупов, биологических жидкостей, растений, пищевых продуктов и др.) на наличие «металлических» ядов применяется метод минерализации. Эти яды в виде солей, оксидов и других соединений в большинстве случаев, поступают в организм перорально, всасываются в кровь и вызывают отравления. «Металлические» яды будут находиться в организме в виде соединений с белками, пептидами, аминокислотами и некоторыми другими веществами, выполняющими важную роль в жизненных процессах. Связи металлов с большинством указанных веществ являются прочными (ковалентными). Поэтому для исследования биологического материала на наличие «металлических» ядов необходимо разрушить органические вещества, с которыми связаны металлы, и перевести их в ионное состояние. Выбор метода минерализации органических веществ зависит от свойств исследуемых элементов, количества биологического материала, поступившего на анализ.
Минерализация – это окисление (сжигание) органического вещества (объекта) для высвобождения металлов из их комплексов с белками и другими соединениями. Наиболее широко распространённые методы минерализации можно разделить на 2 большие группы:
1. Общие методы (методы «мокрой» минерализации) применяются при общем исследовании на группу «металлических ядов», пригодны для изолирования всех катионов металлов. Кроме ртути. Для минерализации используют смеси кислот-окислителей: серной и азотной, серной, азотной и хлорной.
2. Частные методы (методы «сухого озоления») – метод простого сжигания, метод сплавления со смесью нитратов и карбонатов щелочных металлов. К числу частных методов относится и метод частичной минерализации (деструкции), служащий для изолирования соединений неорганической ртути из биологических материалов.
Методичка металлические яды. Учебнометодическое пособие по токсикологической химии для студентов 4 курса очного отделения

Единственный в мире Музей Смайликов
Самая яркая достопримечательность Крыма
Государственное бюджетное образовательное учреждение
высшего профессионального образования
«Казанский государственный медицинский университет»
Министерства здравоохранения Российской Федерации
Кафедра фармацевтической химии
с курсами аналитической и токсикологической химии
Группа веществ, изолируемых минерализацией
(«металлические» яды)
Учебно-методическое пособие по токсикологической химии
для студентов 4 курса очного отделения
УДК 615.07 (075ю8)
ББК 52.81.012
Печатается по решению Центрального координационно-методического совета Казанского государственного медицинского университета
Составители:
старший преподаватель, к.фарм.н. Петрова И.К.
зав. кафедрой, доцент, к.фарм.н. Мустафин Р.И.,
Доцент кафедры фармацевтической технологии,
Учебно-методическое пособие по токсикологической химии для студентов 4 курса очного отделения фармацевтического факультета соответствует федеральному государственному образовательному стандарту по специальности «Фармация» от 2011 года.
© Казанский государственный медицинский университет, 2013
Пособие, несомненно, будет полезно для студентов 4 курса фармацевтического факультета при изучении большого раздела курса токсикологической химии: «Группа веществ, изолируемых минерализацией («металлические» яды)».
1. Изолирование соединений, содержащих «металлические» яды из биологического материала
Общие методы (методы «мокрой» минерализации) применяются при общем исследовании на группу «металлических ядов», пригодны для изолирования всех катионов металлов. Кроме ртути. Для минерализации используют смеси кислот-окислителей: серной и азотной, серной, азотной и хлорной.
Частные методы (методы «сухого озоления») – метод простого сжигания, метод сплавления со смесью нитратов и карбонатов щелочных металлов. К числу частных методов относится и метод частичной минерализации (деструкции), служащий для изолирования соединений неорганической ртути из биологических материалов.
1.1. Разрушение биологического материала
азотной и серной кислотами
В колбу Кьельдаля вместимостью 500—800 мл вносят 100 г измельченного биологического материала, прибавляют 75 мл смеси, состоящей из равных объемов концентрированных азотной и серной кислот и воды очищенной. Колбу с содержимым в вертикальном положении закрепляют в штативе так, чтобы дно ее находилось над асбестовой сеткой на расстоянии 1—2 см. Над колбой Кьельдаля в штативе закрепляют делительную воронку, в которой содержится кислота азотная концентрированная, разбавленная равным объемом воды. Далее начинают осторожно нагревать колбу. В течение 30—40 мин происходит деструкция, разрушение форменных элементов биологического материала. По окончании деструкции получается полупрозрачная жидкость, окрашенная в желтый или бурый цвет.
Затем колбу Кьельдаля с содержимым опускают на асбестовую сетку и усиливают нагрев — начинается стадия глубокого жидкофазного окисления. Для разрушения органических веществ, находящихся в колбе, из капельной воронки по капле прибавляют концентрированную азотную кислоту, разбавленную равным объемом воды. Минерализация считается законченной тогда, когда прозрачная жидкость (минерализат) при нагревании без добавления азотной кислоты в течение 30 мин перестает темнеть, а над жидкостью будут выделяться белые пары ангидрида серной кислоты.
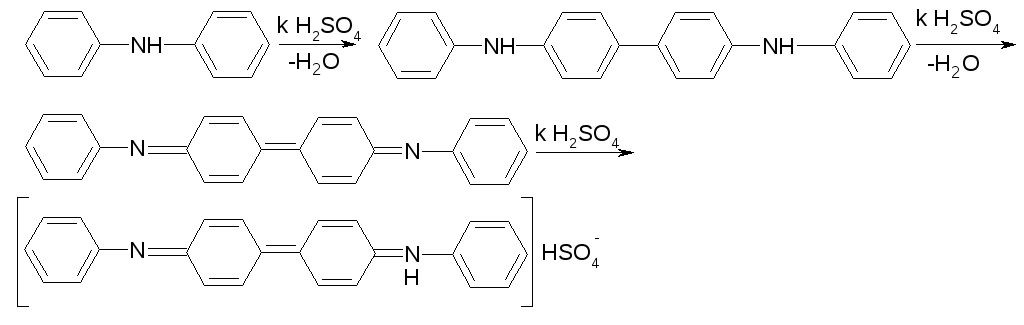
Полученный минерализат подвергают денитрации: охлаждают, прибавляют 10—15 мл воды очищенной и нагревают до 110-130°С, а затем осторожно по каплям, избегая избытка, прибавляют раствор формальдегида. При этом отмечают обильное выделение бурых, иногда оранжевых, паров. После окончания выделения этих паров жидкость еще нагревают в течение 5—10 мин, а затем 1—2 капли охлажденной жидкости (минерализата) наносят на предметное стекло или на фарфоровую пластину и прибавляют каплю раствора дифениламина в концентрированной серной кислоте. Эффект реакции — характерное синее окрашивание.
Отрицательная реакция минерализата с дифениламином на азотную, азотистую кислоты, а также на окислы азота указывает на окончание процесса денитрации. При положительной реакции минерализата с дифениламином денитрацию проводят повторно.
Метод минерализации биологического материала концентрированными азотной и серной кислотами имеет ряд достоинств. Минерализация этим методом происходит быстрее, получается относительно небольшой объем минерализата, чем с использованием других методов. Однако минерализация смесью серной и азотной кислотой непригодна для изолирования ртути из биологического материала, так как значительное количество ее улетучивается при нагревании биологического материала на стадии глубокого жидкофазного окисления.
1.2. Разрушение биологического материала хлорной,
В колбу Кьельдаля вместимостью 500 мл вносят измельченный биологический материал, прибавляют по 25 мл концентрированных азотной и серной кислот и 35 мл 37 % -го или 42 % -го раствора кислоты хлорной. Колбу с содержимым устанавливают на асбестированную сетку и постепенно усиливают нагрев. При нагревании может происходить обугливание. В этом случае в колбу по капле прибавляют концентрированную азотную кислоту. Если и при этом будет продолжаться обугливание, и над жидкостью будут появляться пары ангидрида хлорной кислоты Сl2O7, то нагревание колбы прекращают или ослабляют. Окисление биологического материала продолжают, прибавляя по капле 35—45 % раствора кислоты азотной. Когда жидкость в колбе становится прозрачной, тогда прекращают нагревание и проверяют полноту окисления органических веществ в минерализате. С этой целью к капле охлажденного, разбавленного водой минерализата, прибавляют 25 % раствор аммония гидроксида. Появление слабо желтой окраски свидетельствует об окончании процесса минерализации. Появление оранжевой окраски указывает на наличие в минерализате некоторых еще не разрушенных аминокислот: фенилаланина, тирозина, триптофана и др.
Данным методом достигается почти полное разрушение биологического материала и в 2—3 раза сокращается время разрушения по сравнению со временем, необходимым для минерализации объектов биологического происхождения азотной и серной кислотами. При использовании этого метода требуется особая осторожность ввиду взрывоопасности оксида хлора (VII). Метод не пригоден для разрушения биологического материала, подлежащего исследованию на наличие ртути, которая улетучивается в процессе минерализации.
1.3. Разрушение биологического материала
пергидролем и серной кислотой
Исследуемый объект по возможности освобождают от воды выпариванием, измельчают и вносят в фарфоровую чашку, в которую небольшими порциями, при помешивании стеклянной палочкой, прибавляют пятикратное количество кислоты серной концентрированной и нагревают на водяной бане. При этом происходит обугливание исследуемого объекта с выделением оксида углерода (II). После заметного уменьшения скорости выделения углекислого газа содержимое фарфоровой чашки переносят в колбу Кьельдаля, которую устанавливают на асбестовую сетку. При слабом нагревании колбы в нее вносят небольшими порциями пергидроль. Прибавление новых небольших порций пергидроля производят до тех пор, пока жидкость не станет бесцветной или слегка желтоватой от наличия солей железа. После этого колбу с жидкостью охлаждают, а содержимое разбавляют десятикратным количеством воды. Для удаления избытка пергидроля в колбу Кьельдаля небольшими порциями прибавляют насыщенный водный раствор сульфата натрия или сульфата гидразина и кипятят в течение 5—10 мин.
Данный метод пригоден при исследовании малых навесок объектов биологического происхождения, поступивших на исследование.
1.4. Разрушение биологического материала
методом сухого озоления
Сжигание. Исследуемые объекты (овощные консервы или части органов) измельчают, вносят в фарфоровую чашку, которую помещают на песчаную баню, и высушивают. Затем при дальнейшем осторожном нагревании песчаной бани пробу обугливают. Обуглившийся или превращенный в пепел биологический материал охлаждают, смачивают концентрированным раствором нитрата аммония или концентрированной азотной кислотой. Фарфоровую чашку помещают на кипящую водяную баню и выпаривают ее содержимое, которое переносят в фарфоровый тигель вместимостью 30—50 мл, и осторожно нагревают на слабом пламени. При этом пламя не должно соприкасаться с дном тигля. Нагревание тигля производят таким образом, чтобы его содержимое постепенно превращалось в золу (без вспышки). При неполном сгорании органических веществ зола в тигле имеет черный или серый цвет.
Для полноты сгорания содержимое тигля, смачивают концентрированным раствором нитрата аммония, высушивают на водяной бане и прокаливают. После этого тигель охлаждают и прибавляют раствор кислоты хлористоводородной (при исследовании на марганец) или азотной (при исследовании на медь), фильтруют. Полученный фильтрат выпаривают на кипящей водяной бане досуха. Сухой остаток растворяют в 3—5 мл воды очищенной, полученные растворы исследуют на наличие катионов соответствующих металлов.
Метод может также использоваться при анализе биологического материала на наличие ионов цинка и висмута. При разрушении органических веществ с помощью этого метода для исследования берут небольшие навески исследуемых объектов (1—10 г). Возможно улетучивание некоторых металлов (ртути и таллия) или их соединений (хлориды кадмия, свинца, серебра, цинка, марганца, мышьяка) в процессе нагревания. При высоких температурах возможно также взаимодействие цинка, серебра, свинца со стенками кварцевого или фарфорового тиглей.
Сплавление: 1—2 г исследуемого объекта вносят в фарфоровую чашку, прибавляют 4— 6 г смеси, состоящей из двух частей натрия карбоната и одной части калия нитрата, перемешивают, промывают водой и при нагревании на водяной бане высушивают досуха. В фарфоровый тигель вместимостью 30—50 мл вносят 5—6г калия нитрата. Тигель осторожно нагревают до полного расплавления калия нитрата. Затем уменьшают пламя и в тигель небольшими порциями вносят указанную выше высушенную в фарфоровой чашке смесь исследуемого объекта, калия нитрата и натрия карбоната. Каждую новую порцию этой смеси вносят в тигель после сгорания предыдущей и перехода ее в расплавленное состояние.
После сжигания последней порции смеси к ней добавляют 2—3 г натрия карбоната, хорошо перемешивают, чтобы остатки исследуемого объекта на стенках фарфоровой чашки хорошо смешались с натрия карбонатом. При сплавлении смеси пламя горелки регулируют так, чтобы в тигле не вспыхивало пламя и с выделяющимися газами не удалялось исследуемое вещество. После сжигания всей смеси тигель охлаждают, а его содержимое обрабатывают кипящей водой.
Метод применяется при специальных заданиях. Исследуются органические и лекарственные вещества, содержащие металлы, остатки после выпаривания мочи, волосы, ногти и другие объекты на наличие мышьяка, серебра и некоторых других металлов. Метод непригоден для исследования объектов биологического происхождения на наличие соединений ртути, так как они улетучиваются при нагревании с калия нитратом и натрия карбонатом.
1. Дробный метод анализа минерализата
В химико-токсикологическом анализе для обнаружения ионов металлов в минерализатах используется дробный метод анализа, основоположником которого является Н. А. Тананаев. Большой вклад в разработку метода и внедрение его в практику судебно-химических лабораторий внесла А. Н. Крылова. Метод основан на применении реакций, с помощью которых в любой последовательности можно обнаружить ионы в отдельных небольших порциях исследуемого раствора. Для обнаружения соответствующих ионов дробным методом необходимо применять специфические реактивы, позволяющие обнаружить искомый ион в присутствии посторонних ионов. В качестве реакций идентификации избраны наиболее чувствительные и специфичные. Предпочтение отдано жидкофазным реакциям, что позволяет исключить процессы фильтрования, промывания, упаривания и приводит не только к ускорению процесса анализа, но и к повышению его чувствительности. Доказательность и надежность метода достигается применением основной (специфичной) и дополнительной (подтверждающей) реакций.
Обнаружение искомых ионов дробным методом производится в два этапа. Вначале устраняют влияние мешающих ионов с помощью соответствующих реактивов или их смесей, а затем прибавляют реактив, дающий окраску или осадок с искомым ионом.
Дробный метод анализа особенно удобен в тех случаях, когда задача эксперта-токсиколога ограничена заданием провести исследование только на определенные ионы или исключить тот или иной ион. Таким образом, дробный метод анализа подходит для решения практических задач судебно-химической экспертизы.
1. Изолирование соединений, содержащих «металлические» яды из биологического материала
Общие методы (методы «мокрой» минерализации) применяются при общем исследовании на группу «металлических ядов», пригодны для изолирования всех катионов металлов. Кроме ртути. Для минерализации используют смеси кислот-окислителей: серной и азотной, серной, азотной и хлорной.
Частные методы (методы «сухого озоления») – метод простого сжигания, метод сплавления со смесью нитратов и карбонатов щелочных металлов. К числу частных методов относится и метод частичной минерализации (деструкции), служащий для изолирования соединений неорганической ртути из биологических материалов.
1.1. Разрушение биологического материала азотной и серной кислотами
Метод минерализации биологического материала концентрированными азотной и серной кислотами имеет ряд достоинств. Минерализация этим методом происходит быстрее, получается относительно небольшой объем минерализата, чем с использованием других методов. Однако минерализация смесью серной и азотной кислотой непригодна для изолирования ртути из биологического материала, так как значительное количество ее улетучивается при нагревании биологического материала на стадии глубокого жидкофазного окисления.
Группа веществ, изолируемых минерализацией («металлические» яды)
Оглавление Введение
Методика изолирования металлических ядов из биологического материала общим методом минерализации
100 г биологического объекта в колбе Къельдаля заливают 75 мл окислительной смеси (кислоты серной концентрированной, кислоты азотной концентрированной, воды дистиллированной в соотношении 1:1:1). Колбу закрепляют в штативе вертикально на расстоянии 1-2 см от асбестовой сетки. Над колбой помещают капельную воронку с разбавленной азотной кислотой (1:1). Колбу осторожно нагревают на плитке, добавляя при необходимости (потемнение жидкости) разбавленную азотную кислоту (1:1) по каплям до просветления жидкости. Концом минерализации считается момент, когда в колбе остается 15-20 мл бесцветной или окрашенной жидкости, которая не темнеет в течение 30 минут при постоянном нагревании, без добавления азотной кислоты. Охлажденный минерализат осторожно выливают в химический стакан, содержащий 30 мл дистиллированной воды, колбу Къельдаля ополаскивают два раза дистиллированной водой по 10 мл и присоединяют промывные воды к разбавленному минерализату. Разбавление минерализата способствует затем более легкому протеканию процесса денитрации.
В маленькой фарфоровой чашке в 2-3 каплях концентрированной серной кислоты растворяют 2-3 кристалла дифениламина и к полученному бесцветному раствору прибавляют одну каплю разбавленного минерализата. В случае появления сине-голубого окрашивания проводят денитрацию раствора.

Стакан с содержимым ставят на плитку, нагревают до кипения и вносят одну каплю формалина; кипятят 10 минут и вновь проделывают реакцию с дифениламином.

2 2 + H2O HNO2 + HNO3
4 2 + 2 H2CO 2 NO + N2 + 2 CO2 + 4 H2O
4 3 + 3 H2CO 4 NO + 3 CO2 + 5 H2O
4 3 + 5 H2CO 2 N2 + 5 CO2 + 7 H2O
В случае отсутствия голубого окрашивания в результате реакции с дифениламином жидкость кипятят до исчезновения запаха формалина, охлаждают, количественно переносят в мерную колбу на 200 мл и доводят дистиллированной водой до метки. Жидкость из мерной колбы переносят в чистую сухую склянку и используют для обнаружения катионов (100 мл) и количественного определения (100 мл). Если при разбавлении минерализата водой выпадает осадок, то независимо от того, проводилась денитрация или нет, жидкость в стакане нагревают до кипения, кипятят 10 минут и оставляют стоять на сутки для получения более плотного осадка. На второй день белый кристаллический осадок отфильтровывают через маленький плотный фильтр (фильтрат используют для проведения дробных реакций на катионы по схеме), промывают несколько раз холодной дистиллированной водой, промывные воды присоединяют к фильтрату и доводят его водой до 200 мл в мерной колбе.
4 + 2 CH 3COONH4 (CH3 COO)2 Pb + (NH4)2 SO4
Осадок на фильтре еще раз промывают водой, подкисленной 1% раствором серной кислоты (эти промывные воды отбрасывают). Затем осадок на фильтре обрабатывают 5 мл горячего раствора ацетата аммония. Полученный раствор используют для проведения качественных реакций на катион свинца, а оставшуюся часть – для количественного определения свинца. Осадок на фильтре после обработки ацетатом аммония исследуют на катион бария сначала количественно (по указанию преподавателя), а затем проводят качественные реакции.
Читайте также:
