Наиболее частый метод стерилизации металлических изделий медицинского назначения
Обновлено: 04.10.2024
Типичные ошибки при стерилизации изделий медицинского назначения
Н.С. ВАСИЛЬЕВ, ведущий научный сотрудник научно-производственной фирмы "Винар", О.Д. ЛЯМКИНА, инженер-испытатель научно-производственной фирмы "Винар", СМ. САВЕНКО, заведующий ЦСО ФГУ КБ УД Президента РФ, член Технического комитета № 283 "Стерилизация медицинских изделий" Госстандарта РФ, г. Москва
В течение последних двух лет в результате внедрения системы контроля паровой стерилизации ИМН с использованием "внутренних" индикаторов "Стеритест-П-120/45" и "Стеритест-П-132/20" во многих ЛПУ выявлены случаи получения нестерильных ИМН, прошедших цикл стерилизации. Для выяснения причин и помощи персоналу стерилизационных и ЦСО сотрудники НПФ "Винар" неоднократно выезжали в областные и районные центры России. В этой статье обобщен накопленный опыт и представлена информация, которая может быть полезна многим специалистам.
В текущем году журнал опубликовал серию статьей о стерилизации изделий медицинского назначения: статья "Производственный контроль паровой стерилизации изделий медицинского назначения в ЛПУ" посвящена проблеме качества, статья "Паровая стерилизация изделий медицинского назначения в ЛПУ" - стерилизационному оборудованию. Названные публикации носят больше теоретический характер. В предлагаемой статье авторы анализируют конкретные примеры типичных ошибок при стерилизации, выявленных специалистами НПФ "Винар".
Монтажные испытания
В настоящее время в России идет интенсивное обновление парка стерилизационного оборудования. При этом во всех ЛПУ совершают одну типичную ошибку: принимают стерилизационное оборудование в эксплуатацию без проведения комплекса проверок при монтаже. Проверкой при монтаже в соответствии с ГОСТ Р 51935-2002 называется последовательность проверок и испытаний, выполняемых после монтажа стерилизационного оборудования на месте использования. Стерилизационное оборудование - это стерилизатор с контрольно-измерительным комплексом, программами стерилизации изделий медицинского назначения, методами поверок и средств контроля процесса стерилизации. Успех стерилизации зависит от правильного сочетания и исправности каждого из всех перечисленных компонентов.
В ГОСТ Р 51935-2002 приведены категории испытаний (раздел 15), программа испытаний (раздел 16), методы испытаний (разделы 17-22), которые должны выполнять в обязательном порядке специалисты, установившие стерилизационное оборудование:
- биологические испытания - испытания реального стерилизационного цикла с полной загрузкой камеры текстильными изделиями. Пять биологических индикаторов закладывают в середину стандартной контрольной упаковки из текстиля, которую помещают в самую холодную точку стерилизационной камеры (Тест-ИБ по МУК 4.2.1990-05 [2]);
- термометрирование пустой стерилизационной камеры с контрольной тестовой упаковкой (текстиль) с термодатчиками по контрольным точкам и в центре упаковки;
- термометрирование загруженной текстильными изделиями стерилизационной камеры с контрольной тестовой упаковкой (текстиль) с термодатчиками по контрольным точкам и в центре упаковки;
- контроль удаления воздуха и проникновение пара (Бови-Дик тест или Тест-ИХ по МУК 4.2.1990-05);
- контроль герметичности стерилизационной камеры по вакуум-тесту;
- контроль утечки воздуха по детектору воздуха;
- контроль увлажненности загрузки с использованием контрольной упаковки из текстиля;
- контроль увлажненности загрузки с использованием металлической загрузки.
В обязательном порядке необходимо проверять наличие сетчатого фильтра на дренажную систему, который должен предохранять ее от засорения. Если стерилизатор не укомплектован фильтром, его необходимо приобрести отдельно. В инструкциях к отечественным стерилизаторам не указана периодичность проверки и очистки дренажной системы, хотя этот узел в стерилизаторе так же важен, как и парогенератор. Поэтому при эксплуатации стерилизатора мы рекомендуем работникам сервисной службы проверять эту систему не реже 1 раза в месяц.
Все результаты монтажных испытаний должны быть зафиксированы в документах всех программ стерилизации (стерилизационных циклов), которые будут использоваться на этом оборудовании в данном ЛПУ. Только после получения положительных результатов испытаний подписывают акт приемки оборудования между ЛПУ и монтажной организацией. Все документы монтажных испытаний являются приложениями к этому акту.
Таким образом, после установления оборудования на месте использования монтажные испытания подтверждают, что стерилизационное оборудование обеспечивает надежную стерилизацию.
К сожалению, ни в одном ЛПУ не удалось найти аналогичный акт, ни в одной организации после монтажа не проводят полный комплекс испытаний. В результате сотрудники ЦСО и стерилизационной остаются одни с проблемным оборудованием.
Типичные примеры неисправного стерилизационного оборудования
Пример 1. Крупное областное медицинское учреждение в июне 2005 г. закупило и смонтировало в ЦСО гравитационный паровой стерилизатор ГК-100-3, выпущенный в августе 2004 г., несмотря на то, что во всех нормативных документах указано, что для стерилизации ИМН следует использовать только форвакуумные стерилизаторы. Имеется заключение сервисной службы об исправности стерилизатора, но отсутствуют документы, подтверждающие проведение полноценных монтажных испытаний. В процессе эксплуатации контроль "внутренними" индикаторами нового поколения выявил нарушение условий стерилизации.
По просьбе руководства ЛПУ сотрудники НПФ "Винар" провели тестирование процесса стерилизации на данном оборудовании в реальном стерилизационном цикле "132 ± 2°С, 20 мин", принятом в данном учреждении. Термометрирование проводили с помощью контрольно-измерительной системы, соответствующей требованиям ГОСТ Р ИСО 11140-2 и ГОСТ Р 51935-2002, контроль удаления воздуха - с помощью Тест-ИХ (МУК 4.2.1990-05). Стерилизационный цикл в ЛПУ состоял из следующих последовательно выполняемых операций: подача пара в камеру, подъем и достижение рабочего давления в стерилизационной камере без предварительной продувки; в течение 20-минутной стерилизационной выдержки трижды по 2 мин проводили продувку камеры насыщенным паром путем сброса пара в дренаж, при этом время стерилизационной выдержки не увеличивали на общее время нарушения режима. Время сушки изделий составляло 10 мин.
В процессе тестирования установлено, что во время стерилизационной выдержки в камере стерилизатора температура держалась на уровне 131-134°С и полностью соответствовала нормам. Химические индикаторы снаружи упаковок достигли конечного состояния, Тест-ИХ показал неудовлетворительное удаление воздуха. По результатам термометрирования температура в центре стандартной тестовой упаковки (наиболее трудностерилизуемая загрузка) к концу стерилизационной выдержки достигла только 35°С. Эти условия являются наилучшими для инкубации патогенных микроорганизмов, но не для стерилизации.
Причиной получения таких результатов явилось нарушение технологии (программы) стерилизации. Причем нарушение технологии произошло не по вине специалистов стерилизационного отделения, а в результате неквалифицированного преподавания на цикле повышения квалификаций. К сожалению, это не единичный случай неправильного обучения.
Специалисты фирмы "Винар" изменили стерилизационную программу в ГК-100-3 и провели второй цикл стерилизации "132±2°С, 20 мин" со следующей последовательностью операций (правильной):
- после загрузки камеры и закрытия двери провели 15-минутную продувку камеры насыщенным паром при открытом наполовину вентиле "пар в камеру" и открытом полностью - "слив конденсата";
- через 15 мин вентиль "слив конденсата" закрыли и после достижения в камере заданного давления обеспечили стерилизационную выдержку 23 мин. В течение этого времени дважды открывали вентиль "слив конденсата" на 15 с для удаления конденсата из камеры. В процессе слива конденсата происходило небольшое снижение давления (и температуры), которое восстанавливалось через 1 мин. Фактически дважды параметры стерилизационной выдержки нарушались на общее время 3 мин, поэтому время стерилизационной выдержки увеличили на 3 мин;
- закрыли вентиль "пар в камеру" и открыли "слив конденсата" для сброса пара из камеры и снижения давления до атмосферного;
- после выравнивания давления в камере с атмосферным давлением закрыли вентиль "слив конденсата" и открыли вентиль "вакуум" для сушки простерилизованных изделий (сушка осуществляется испарением влаги с горячих изделий и конденсацией в холодном конденсаторе), длительность сушки - 10 мин;
- после окончания сушки закрыли вентиль "вакуум" и открыли "воздух в камеру".
Проведенный цикл показал, что в процессе удаления воздуха продувкой в камере давление возрастало до 0,11 МПа, а температура - до 120°С. При исправной дренажной системе давление не должно превышать 0,04 МПа, а температура - 110°С. Обнаружено, что дренажная система засорена обрывками бумаги, нитками и кусочками тряпок. Такая неисправность привела к неудовлетворительному удалению воздуха (подтверждено Тест-ИХ). И хотя "наружные" индикаторы достигли конечного состояния (температура в камере соответствовала нормам - 131 - 134°С), стандартная упаковка к концу стерилизационной выдержки прогрелась только до 127°С. Пористые изделия плохо прогрелись из-за плохого удаления воздуха при продувке камеры паром.
В результате проведенных испытаний специалистам ЦСО были даны рекомендации: очистить дренажную систему и установить сетчатый фильтр, предотвращающий попадание посторонних предметов и грязи в дренаж; правильно выполнять программу стерилизации.
Все эти неисправности можно было выявить и предотвратить при монтажных испытаниях.
Пример 2. В ЦСО медсанчасти крупного предприятия в 2004 г. была установлена и запущена стерилизационная установка ЦСУ-1000,0 с программой стерилизации, использующей однократную вакуумную откачку воздуха из стерилизационной камеры. Организация, проводящая профилактику и ремонт оборудования, выдала заключение об исправности стерилизатора, хотя документы, подтверждающие проведение полноценных монтажных испытаний, отсутствуют.
В процессе эксплуатации установки индикаторы "Стеритест-П-132/20" и "Стеритест-П-120/45", закладываемые внутрь изделий и упаковок, показали нарушение условий стерилизации.
По просьбе ЛПУ сотрудники НПФ "Винар" провели тестирование загруженного стерилизатора в реальном стерилизационном цикле "132°С, 20 мин" в соответствии с ГОСТ Р 51935-2002. Цикл стерилизации выполняли в автоматическом режиме с однократной откачкой воздуха вакуумным насосом в течение 10 мин, стерилизационной выдержкой 20 мин при 132°С и 20-минутной вакуумной сушкой.
Результаты контроля показали, что все наружные индикаторы достигли конечного состояния, температура в камере даже превышала норму - 134-136°С, Тест-ИХ выявил неудовлетворительное удаление воздуха, а стандартная контрольная упаковка к концу стерилизационной выдержки прогрелась только до 80°С.
Для определения причин плохой стерилизации в этом стерилизаторе с полностью загруженной камерой в ручном режиме были проведены два цикла стерилизации:
- цикл 1 стерилизации "132°С, 20 мин" (гравитационный) с удалением воздуха продувкой паром в течение 15 мин, с вакуумной сушкой 20 мин (цикл проводили для оценки состояния дренажной системы);
- цикл 2 стерилизации "132°С, 20 мин" с форвакуумной трехкратной откачкой воздуха. Каждая откачка состояла из следующих операций: в камеру подавали пар до 1,1 атм и откачивали паровоздушную смесь насосом до -0,5 атм; послестерилизационную вакуумную сушку изделий осуществляли в течение 20 мин. В процессе стерилизации проводили контроль в соответствии с ГОСТ 51935-2002.
Результаты контроля цикла 1 с удалением воздуха продувкой паром: во время продувки давление в камере возросло до рабочего (2,0 МПа), наружные индикаторы достигли конечного состояния, температура в камере в течение всей 20-минутной стерилизационной выдержки даже превышала норму - 134-137°С. Однако за счет неудовлетворительного удаления воздуха стандартная контрольная упаковка к концу стерилизационной выдержки прогрелась только до 112 °С (температура не менее 130°С должна удержаться не менее 7 мин). Было выявлено засорение дренажной системы и отсутствие сетчатого фильтра.
Результаты контроля цикла 2 с форвакуумной откачкой воздуха показали: наружные индикаторы достигли конечного состояния, Тест-ИХ показал хорошее удаление воздуха, в течение 20 мин стерилизационной выдержки в камере температура составляла 135- 138°С, стандартная контрольная упаковка прогрелась до температуры стерилизации уже на этапе подъема давления в камере до заданного после трехкратной форвакуумной откачки воздуха и держалась в течение 20 мин 135-138 °С. Изделия считаются стерильными и могут использоваться в клинических отделениях по назначению.
В результате исследований для данной ЦСУ-1000,0 рекомендовано установить автоматическую программу стерилизации с трехкратной форвакуумной откачкой воздуха из камеры и параметрами стерилизационной выдержки "134+3°С, 5 мин", очистить дренажную систему и поставить сетчатый фильтр. Засорение дренажа в форвакуумном цикле препятствует сливу конденсата из камеры и не позволяет эффективно сушить медицинские инструменты после стерилизации.
Пример 3. В ЦСО крупного московского медицинского научно-исследовательского института в 2003 г. установили большой стерилизатор "AMSKO Series 3051" (США). Стерилизатор рассчитан на использование для стерилизации как ИМН, так и растворов. Объем стерилизационной камеры составляет 1500 л. По документам в ЦСО стерилизацию ИМН проводили в гравитационных циклах "120°С, 45 мин" и "132°С, 20 мин", хотя стерилизатор позволяет использовать более надежные форвакуумные циклы стерилизации. Протоколы полноценных монтажных испытаний обнаружить не удалось.
Все документы контроля стерилизации, имеющиеся в ЦСО, указывали на соблюдение всех норм и правил: "наружные" индикаторы достигали конечного состояния, распечатки показаний термодатчиков и давления во время всего цикла стерилизации показывали соблюдение режима (температура 136-138 °С), имелось заключение сервисной службы об исправности стерилизатора, еженедельно проводили контроль Бови-Дик тестами с положительным результатом.
Контроль "внутренними" индикаторами "Стеритест-П-132/20" и "Стеритест-П-120/45" показал нарушение условий стерилизации.
По просьбе заведующего ЦСО сотрудники НПФ "Винар" провели тестирование стерилизатора в цикле стерилизации "132 °С, 20 мин" с загруженной камерой с "наружными" индикаторами по всем контрольным точкам, с использованием Тест-ИХ и термометрирования условий внутри стандартной контрольной упаковки по ГОСТ Р 51935-2002. При этом выяснилось: все "наружные" индикаторы достигли конечного состояния, температура снаружи упаковок в течение 20 мин составляла 132-134 °С, Тест-ИХ показал плохое удаление воздуха в отличие от Бови-Дик теста, стандартная контрольная упаковка к концу стерилизационной выдержки прогрелась только до 33 °С.
Причину такого явления выяснили после анализа стерилизационной программы: воздух из стерилизационной камеры удаляли продувкой паром только в течение 3 мин. Для стерилизации ИМН использовали программу стерилизации растворов с измененными параметрами температуры (132 °С) и времени (20 мин) выдержки.
Причиной получения разных результатов по Бови-Дик тесту и Тест-ИХ является то, что Бови-Дик тестом исследуют только специальный тестовый форвакуумный цикл в пустой камере, а стерилизацию проводят в загруженной камере в гравитационном цикле. С помощью Тест-ИХ стерилизатор тестируют с загруженной камерой в процессе стерилизации изделий в реальном цикле стерилизации, что позволяет исключить такие ошибки.
В результате исследований было установлено, что все узлы стерилизатора исправны, неисправна программа стерилизации.
Для данного стерилизатора рекомендовано установить программу стерилизации для изделий медицинского назначения (пористых изделий) вместо программы стерилизации растворов.
Выводы
Приведенные примеры показывают, что только внедрение современных средств контроля паровой стерилизации позволяет выявлять все нарушения условий стерилизации и исключить использование нестерильных изделий.
Основным нарушением является неудовлетворительное удаление воздуха из камеры и стерилизуемых изделий, которое возникает в результате:
- неправильно выбранного стерилизационного цикла или программы стерилизации (вакуумный вместо форвакуумного, или гравитационный для стерилизации растворов вместо форвакуумного для стерилизации ИМН);
- засорения дренажной системы, через которую удаляется воздух и сливается конденсат, или использования труб для дренажа с уменьшенной площадью сечения;
- отсутствия сетчатого фильтра в дренажном отверстии, что приводит к его засорению; - нарушения стерилизационного цикла в гравитационных стерилизаторах
- уменьшают время продувки при удалении воздуха или вообще не продувают; время, ушедшее на слив конденсата, не компенсируют увеличением стерилизационной выдержки.
Во всех трех приведенных примерах использовались стерилизаторы, введенные в эксплуатацию в 2003-2005 гг. Многие недостатки и неисправности имели место на стадии сдачи оборудования в эксплуатацию. Чтобы избежать вышеперечисленных ошибок, необходимо проводить полный комплекс монтажных испытаний по ГОСТ Р 51935-2002. Акт сдачи в эксплуатацию стерилизационного оборудования необходимо подписывать только после проведения всего комплекса монтажных испытаний.
Стерилизация хирургических инструментов
Обработка всех инструментов включает в себя последовательное выполнение двух этапов: предстерилизационной обработки и непосредственно стерилизации.
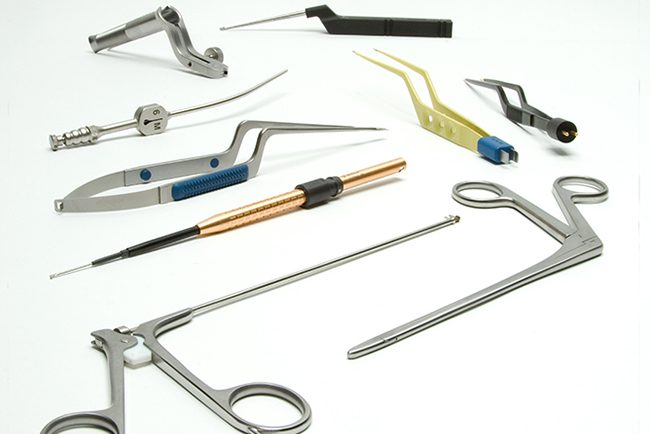
Вид и объем предстерилизационной обработки определяется степенью инфицированности инструментов, а способ стерилизации прежде всего зависит от вида инструментов.
Этапы стерилизации:
Предстерилизационная подготовка
Предстерилизационная подготовка складывается из обеззараживания, мытья и высушивания. Ей подвергаются все виды инструментов.
Вид и объем предстерилизационной обработки в недавнем прошлом определялся степенью инфицированности инструментов.
Обеззараживание
![]()
Непосредственно после использования инструменты погружаются в емкость с дезинфицирующими средствами (накопитель). При этом они должны быть полностью погружены в раствор. В качестве дезинфицирующих
средств используется 3% раствор хлорамина (экспозиция 40-60 минут) или 6% раствор перекиси водорода (экспозиция 90 минут). После обеззараживания инструменты промываются проточной водой.
Мытье
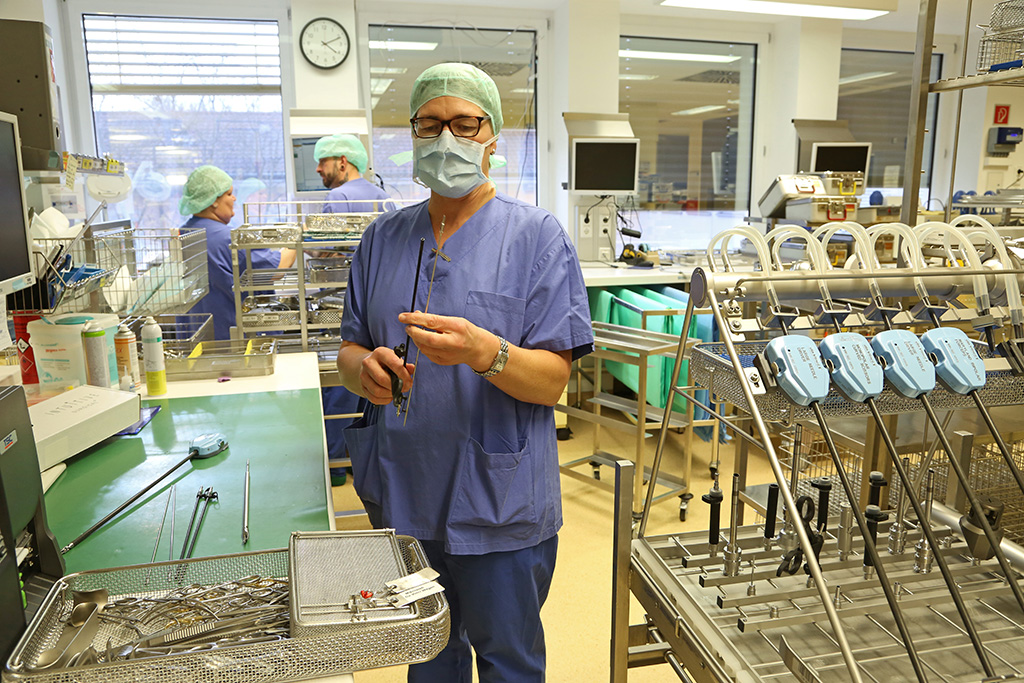
Инструменты погружаются в специальный моющий (щелочной) раствор, в состав которого входит моющее средство (стиральный порошок), перекись водорода и вода. Температура раствора 50-60°С, экспозиция 20 минут. После этого инструменты моют щетками в том же растворе, а затем в проточной воде.
Высушивание
Высушивание может осуществляться естественным путем. В последнее время, особенно при последующей стерилизации горячим воздухом, инструменты сушат в сухожаровом шкафу при 80°С в течение 30 минут. После высушивания инструменты готовы к стерилизации.
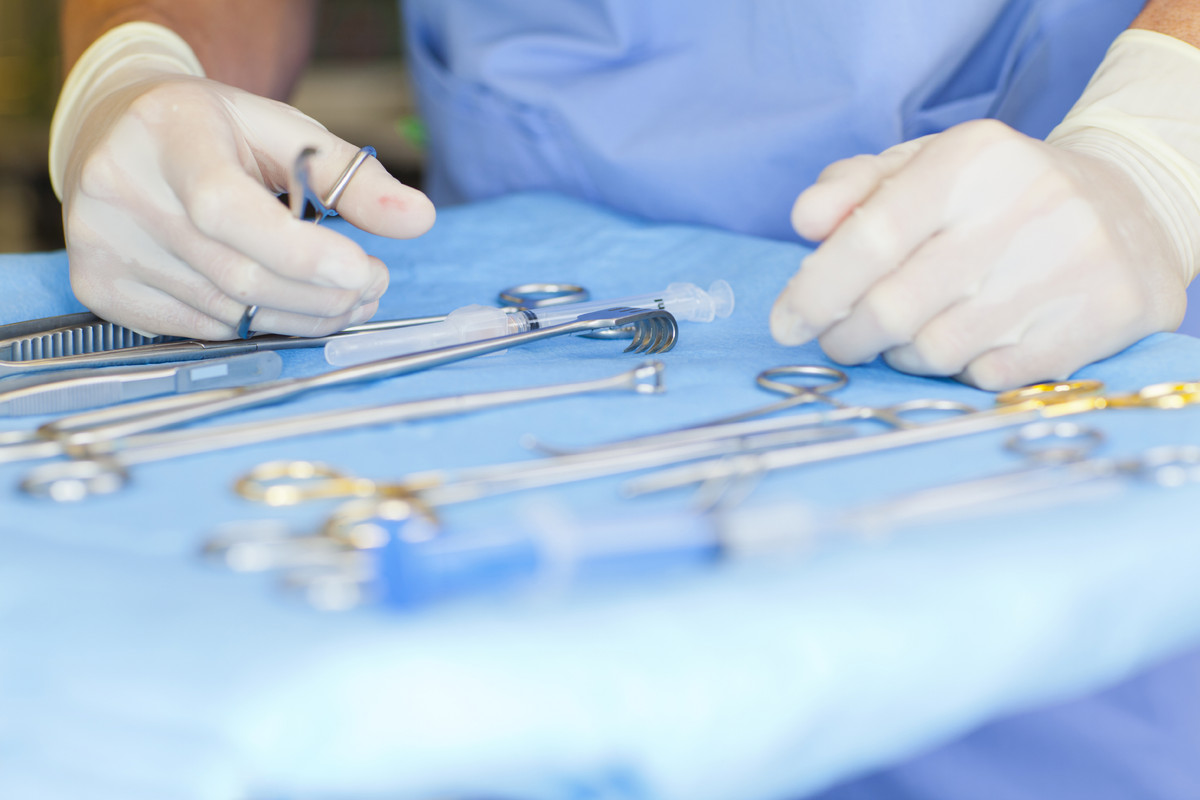
Рис. Инструменты хирургические
Выбор метода стерилизации в первую очередь зависит от вида хирургических инструментов.
Собственно стерилизация
Все хирургические инструменты по особенностям использованных материалов и других качеств можно условно разделить на три группы:
- металлические (режущие и нережущие),
- резиновые и пластмассовые,
- оптические

Рис. Стерилизация инструментов
Стерилизация нережущих металлических инструментов

Рис. Сухожаровой стерилизатор
Основным методом стерилизации является стерилизация горячим воздухом в сухожаровом шкафу или в автоклаве при стандартных режимах. Возможно также использование кипячения. Однако инструменты после операций по поводу анаэробной инфекции и в группе риска по гепатиту кипятить не рекомендуется. Некоторые виды простых инструментов (пинцеты, зажимы, зонды и др.), предназначенные для одноразового использования, могут стерилизоваться лучевым способом.
Стерилизация режущих металлических инструментов
Проведение стерилизации режущих инструментов с помощью термических методов приводит к их затуплению и потере необходимых для хирурга свойств.
Основным методом стерилизации режущих инструментов является холодный химический способ с применением растворов антисептиков.

Рис. Химический стерилизатор
В последнее время в перевязочных режущие инструменты, как и нережущие, стерилизуются в сухожаровом шкафу, что приводит к некоторому снижению их остроты, но обеспечивает абсолютную стерильность.
Самыми лучшими способами стерилизации являются газовая стерилизация и особенно лучевая стерилизация в заводских условиях.

Стерилизация резиновых и пластмассовых инструментов
Основным методом стерилизации резиновых изделий является авто- клавирование.
При многократной стерилизации резина теряет свои эластические свойства, трескается, что является некоторым недостатком метода. Допустимо также кипячение резиновых изделий в течение 15 минут.
Пластмассовые изделия разового использования, а также катетеры и зонды подвергаются лучевой заводской стерилизации.
Особо следует сказать о стерилизации перчаток. В последнее время наиболее часто используются одноразовые перчатки, подвергшиеся лучевой заводской стерилизации. При многократном использовании основным методом стерилизации является автоклавирование в щадящем режиме: после предстерилизационной обработки перчатки высушивают, пересыпают тальком (предупреждает слипание), заворачивают в марлю, укладывают в бикс и автоклавируют.

Стерилизация оптических инструментов
Основным методом стерилизации оптических инструментов, требующих наиболее щадящей обработки с исключением нагревания, является газовая стерилизация.
Этим способом обрабатываются все инструменты для проведения лапароскопических и торакоскопических вмешательств, что связано с их сложным устройством и дороговизной.
При стерилизации фиброгастроскопов, холедохоскопов, колоноскопов возможно применение и холодной стерилизации с использованием химических антисептиков.
Дезинфекция и стерилизация медицинских изделий
Цель дезинфекции и стерилизации медицинских приспособлений – нейтрализация и уничтожение микроорганизмов. В стремлении сэкономить некоторые руководители клиник пренебрегают соблюдением санитарных норм. Результатом становится повышение риска распространения инфекционных болезней среди пациентов и персонала. Правильное обеззараживание медицинских изделий важно для поддержания здоровой атмосферы.
Оценка качества дезинфекции проводится путем смывов на выявление инфекционных возбудителей. Выполняется контроль 1% из партии изделий, прошедших обработку, но не менее трех штук. При отсутствии увеличения числа микроорганизмов очистка признается успешной.
- Дезинфекция.
- Предстерилизационная очистка.
- Стерилизация.
Организация этих мероприятий проводится в соответствии с действующими нормативными актами.
Дезинфекционная обработка
Подразумевает ликвидацию условно-патогенной и патогенной флоры на предметах интерьера, поверхностях помещения, приспособлениях и расходных материалах, используемых в работе медицинского учреждения.
Задача дезинфекционной очистки – предупреждение и устранение накопления, репродукции и распространения болезнетворных микроорганизмов. Существует два вида обработки.
Минимизирует риск инфицирования. Заключается процедура в проведении регулярной влажной уборки и еженедельной генеральной уборки помещений с высокими требованиями к стерильности.
Выполняется при подозрении и выявлении инфекционного очага.
Препараты для дезинфекции
Вид и концентрация препарата определяются возбудителем инфекции. Исходя из вида медицинского предмета, проводится дезинфекция высокого, промежуточного или низкого уровня.
Классификация обрабатываемых изделий:
- «Некритические». Находятся в контакте с неповрежденными кожными покровами.
- «Полукритические». Взаимодействуют с кожей и слизистыми оболочками, имеющими повреждения.
- «Критические». Погружаются в стерильные ткани, сосуды. Взаимодействуют с кровью и растворами для инъекций.
ДВУ применяется для «критических» изделий. Уничтожает микробы, но не бактериальные споры.
ДПУ провоцирует гибель вегетативных форм бактерий, грибов, вирусов. Не воздействует на споры бактерий. Устойчивость к методу демонстрируют мелкие нелипидные вирусы. Обрабатываются «полукритические» инструменты.
ДНУ применяется против вегетативных форм микроорганизмов. Обрабатывается часть «полукритических» и «некритических» изделий.
Методы дезинфекционной обработки:
- Механический. Мойка поверхностей, уборка пылесосом, вентиляция, проветривание.
- Физический. Кипячение, автоклав, сухожаровый шкаф.
- Химический. Погружение в дезраствор.
- Бактериологический. Применяются узкоспецифичные бактериофаги.
Классификация химических средств дезинфекции
Чаще всего применяются в клиниках. По химическому составу средства подразделяются на группы:
- Галогеносодержащие. Активное вещество – йод, бром или хлор.
- Кислородосодержащие. Действующий компонент – кислород, который выделяется из перекиси водорода, надкислот и перекисных соединений.
- ПАВы. Обеспечивают возможность совмещения дезинфекционной и предстерилизационной обработки.
- Гуанидсодержащие. Сложные органические соединения, воздействующие на широкий спектр микроорганизмов.
- Альдегидсодержащие. Янтарный и глутаровый альдегид. Оказывают бактерицидное, спороцидное, фунгицидное и вирулоцидное действие. Негативно действуют на макроорганизмы.
- Спирты. Предназначены для очищения оборудования и поверхностей.
- Фенолсодержащие. Амоцид и Амоцид 2000 - предназначены для дезинфекционной обработки очагов туберкулеза.

Правила проведения
Инструменты помещаются в дезраствор после применения, так чтобы жидкость покрывала изделия на 1 см над поверхностью. Предметы сложной конструкции обрабатываются в разобранном виде. В полостях не должно быть пузырьков воздуха. При сильных загрязнениях проводится двукратная процедура.
Обработка приспособлений из стекла, пластмассы, резины выполняется хлорсодержащими средствами. Запрещено использовать ерш для изделий из резины.
Металлический инструментарий длительного применения обрабатывается веществами, не вызывающими коррозии.
По завершению процедуры приспособления промываются водой.
- рабочие растворы готовятся в местах с хорошей вентиляцией;
- применяются перчатки, очки и респираторы;
- хранение растворов в герметичных емкостях;
- концентрат запрещено разводить водой повышенной температуры;
- не разрешена промывка предметов проточной водой до дезинфекционной обработки.
Обязанности дезинфекции возлагаются на средний медицинский персонал.
Предстерилизационная обработка
Инструменты, контактирующие с ранами и слизистыми оболочками, требуют проведения стерилизации. На предварительном этапе удаляются мелкие частицы и белковые соединения. Применяются дезинфектанты или специальные растворы.
Качество очистки каждый день оценивается путем биологических и химических проб.
Стерилизация
«Критические» предметы подвергаются абсолютной стерилизации для уничтожения микроорганизмов и бактериальных спор.
- Химический. Плазменный способ или воздействие химическими растворами.
- Физический. Подразумевает воздействие паром, нагретым воздухом, УФ излучением. В стоматологии применяется гласперленовый способ.
- Газовый. Воздействие смесью окиси этилена и углекислого газа.
Успешная стерилизация возможна при соблюдении условий: подача пара под напором, режим температуры, период воздействия.
Виды стерилизаторов
Приборы, принцип действия которых основан на УФ излучении. Инструменты обрабатываются 25 минут.
Доступны разные модели аппаратуры для обработки мелких инструментов. Например, гласперленовый стерилизатор – камера с шариками из стекла, нагревающимися до 240 градусов. Применяется в стоматологии.
Некоторые ЛПУ применяют газовые стерилизаторы. Подобные устройства предусматривают возможность стерилизации упакованных материалов. Недостатки: дороговизна и длительная экспозиция.
Плазменные стерилизаторы SPS – современная методика обработки инструментов и оборудования, чувствительных к влажности и повышенному температурному режиму.

Главный санитарный врач РФ об изменениях в требованиях к помещениям и зданиям, где размещаются медучреждения
01.01.2021 г. вступило в силу Постановление главврача (по санитарной части) Российской Федерации от 24.12.2020 г. В…

Текущий 2022 год начался для сегмента коммерческой медицины достаточно оптимистично. Однако с конца февраля в…

"Доктор Питер – Частная медицина" – гипермаркет "МЕДМАРТ" в качестве партнера городской премии подарил 10 сертификатов победителям
16.06.2021 г. прошла I церемония вручения специализированной премии "Доктор Питер – Частная медицина". Владельцы…
Методы стерилизации хирургических инструментов
Стерилизация – это процесс устранения всех форм жизни, в том числе и инфекционных агентов (грибы, бактерии, споры, вирусы), которые присутствуют на поверхностях, содержатся в жидкостях.
Подвергаться обязательной стерилизации должны:
- предметы, которые соприкасаются с поверхностью ран, имеют контакт с кровью и инъекционными препаратами
- диагностическая аппаратура, которая соприкасается со слизистыми оболочками и может вызвать их повреждение.
Выделяют три основных этапа стерилизации:
- дезинфекция
- предстерилизационная очистка
- стерилизация
Стерилизация достигается путем применения термической, химической или радиоактивной обработки.
Качество стерилизации во многом зависит от контакта стерилизующего агента с поверхностью стерилизуемого инструмента. Выбор агента связан с природой инструмента, который необходимо стерилизовать.
Процесс стерилизации происходит в специальном устройстве, которое называется стерилизатор.
Методы стерилизации
1) Термический метод стерилизации
- Паровая стерилизация (автоклавирование)
При термической обработке гибнут живые организмы. Этот процесс ускоряется при добавлении влаги, но обычного пара недостаточно для стерилизации. Необходимо давление, больше атмосферного, что позволит повысить температуру пара для термического разрушения микробной жизни. Пар под давлением вызывает денатурацию и коагуляцию белка и его ферментов в клетках.
Устройство, в котором происходит стерилизация паром, называется автоклав. Весь цикл стерилизации в автоклаве может занять от 15 до 60 минут, в зависимости от давления, температуры и материала стерилизуемых инструментов.
Автоклавирование подходит для предметов, которые переносят влажность, высокое давление (от 1 до 3,5 атмосфер выше внешней среды), а также высокую температуру (от + 121°С до + 148 °C). Например, хирургические инструменты.
Отличным представителем устройств для паровой стерилизации является серия автоклавов Statim. Компактные кассетные стерилизаторы продлевают срок службы хрупких инструментов.
- Воздушная стерилизация (сухожаровой шкаф)
Сухое тепло в виде горячего воздуха используется в основном для стерилизации объектов на основе безводных масел, нефтепродуктов и порошков, что не может быть стерилизовано посредством пара и газа. Гибель микробных организмов происходит за счет окисления и медленного процесса сжигания белка в клетках. При отсутствии влаги в процессе стерилизации требуются более высокие температуры.
- Микроволновая стерилизация
Под действием не ионизирующих излучение микроволн, создаются гипертермические условия, которые нарушают жизненные процессы микроорганизмов. Температура цикла ниже, чем при стерилизации паром. Время цикла гораздо меньше – 30 секунд. Металлические инструменты могут быть стерилизованы, если их поместить в условия частичного вакуума, в стеклянной емкости. Стерилизатор такого типа отлично подойдет для небольших объемов стерилизации.
2) Химический метод стерилизации
- Стерилизация газом
Окись этилена.Основной цикл стерилизации состоит из пяти этапов и занимает около 2,5 часов, за исключением времени аэрации. Газ вступает в химическую реакцию с аминокислотами, белками, ДНК и предотвращает размножение микробных организмов.
Такой метод стерилизации подходит для предметов, которые не могут выдержать высокую температуру и влажность, необходимую для паровой стерилизации. Благодаря низким температурным условиям (+ 30 ° до + 60 ° C), данный метод стерилизации хорошо подходит для медицинских устройств со встроенной электроникой. Недостаток метода – легкая воспламеняемость.
Формальдегид. Газ убивает микроорганизмы путем коагуляции белка в клетках. Данный метод стерилизации является сложным и менее эффективным, чем другие методы стерилизации. От его использования для стерилизации почти отказались в Соединенных Штатах, Канаде и Австралии, но он до сих пор используется в некоторых странах Европы и Азии.
- Плазменная стерилизация
Плазма представляет собой состояние вещества отличное от твердого, жидкого или газообразного состояния. Это состояние достигается за счет создания сильного электрического или магнитного поля. Свободные радикалы перекиси водорода взаимодействуют с клеточными мембранами, ферментами, нуклеиновыми кислотами и нарушают жизненные функции микроорганизмов.
Основной цикл плазменной стерилизация состоит из четырех этапов (создание вакуума, Н2О2 инъекция, диффузия, плазменный разряд). Процесс занимает от 1 до 3 часов.
Данный метод стерилизации подходит для объектов, которые не могут выдержать высокую температуру и влажность, необходимую для паровой стерилизации.
- Стерилизация озоном
Озон является формой кислорода. Процесс стерилизации происходит посредством окисления, разрушения органических и неорганические веществ. Озон проникает в мембрану клетки, вызывая ее взрыв. Озон является нестабильным газом, но может быть легко генерирован из кислорода. Время цикла - до 60 минут в зависимости от размера камеры или нагрузки.
3) Радиационный метод стерилизации
Является наиболее эффективным методом стерилизации, но ограничивается только использованием в коммерческих целях.
Ионизирующее излучение производит ионы, которые выбивают электроны из атомов. Эти электроны ударяют смежный атом и либо присоединяются, либо выбивают электрон из второго атома. Ионная энергия преобразуется в тепловую и химическую энергию. Эта энергия вызывает гибель микроорганизмов путем разрушения молекулы ДНК, что предотвращает клеточное деление и распространение биологической жизни. Основными источниками ионизирующего излучения являются бета-частицы и гамма-лучи.
Каждый метод стерилизации имеет свои особенности. При выборе того или иного метода, следует учитывать возможные побочные эффекты, особенно когда речь идет о стерилизации различных электронных устройств.
Читайте также:
