Осаждение белков солями тяжелых металлов механизм
Обновлено: 21.09.2024
При действии небольших концентраций солей тяжелых металлов (Рb +2 , Аg +1 , Аs +3 , Нg +2 , Сd +2 , Вi +3 и т.д.) на растворы белка происходит денатурация белковых молекул. Осаждение денатурированного белка обусловлено адсорбцией иона тяжелого металла на поверхности белковой молекулы и образованием нерастворимых в воде комплексных соединений. Кроме того, тяжелые металлы нейтрализуют электрический заряд и изменяют четвертичную, третичную и вторичную структуры макромолекул белка, образуя связи между функциональными группами молекул.
Существуют определенные границы концентраций солей тяжелых металлов, при которых комплекс белка с солью тяжелого металла переходит в осадок либо находится в растворимом состоянии.
Ход работы. К 2 мл раствора яичного альбумина добавляют 5 капель 1 %-ного раствора сульфата меди. Выпадает осадок, который растворяется в избытке (7-10 мл) раствора этой соли.
Результаты наблюдений заносят в таблицу 5.
Таблица 5 Результаты наблюдений
Денатурирующий фактор и его воздействие
Материалы и реактивы: раствор яичного альбумина (см. приложение Б, п.4); 1 %, 10 %-ный раствор уксусной кислоты; 10 %-ный раствор NаОН; 96 %-ный этиловый спирт; 80 %-ный ацетон; концентрированные кислоты Н2SO4, НСl, НNО3; 1 %-ный раствор сульфата меди; 10 %-ный раствор ТХУ; насыщенный раствор NаСI.
Оборудование: пробирки обыкновенные; пипетки на 1–2 мл; спиртовка.
Контрольные вопросы
1.Что такое денатурация белка?
2. Какие Вы знаете денатурирующие факторы и каков механизм их действия?
3. Какие структуры белковых молекул изменяются при денатурации?
4. Является ли денатурация обратимым процессом?
5.4 Разделение и очистка белков методом диализа
Диализом называется процесс разделения высокомолекулярных и низкомолекулярных веществ с помощью полупронецаемых мембран. Белковые молекулы, обладая большой молекулярной массой, не способны проникать через полупронецаемые перегородки (искусственные и естественные мембраны). При этом низкомолекулярные частицы (органические и неорганические) легко проходят через поры полупроницаемых мембран.
Диализ широко используется для очистки белков от низкомолекулярных примесей (соли, сахара и других), которые легко проходят через поры полупроницаемых мембран. Прибор, в котором проводят диализ, называется диализатором. Целлофановый или коллодиевый мешочек, опущенный в сосуд с водой, представляет простейший диализатор (рис.1). Белок, помещенный в мешочек, остается в нем, а низкомолекулярные вещества диффундируют через мембрану в воду.
(NН4)2SО4
2О
Рисунок 1Схема диализатора
Методом диализа можно разделить альбумины и глобулины. При переходе солей из белкового раствора в окружающую среду глобулины будут выпадать в осадок, т.к. они не растворимы в водной среде, а альбумины будут оставаться в растворе.
Простейшим диализатором может служить целлофановый мешочек, опущенный в стакан с водой. Солевой раствор белка помещают в мешочек, при этом молекулы низкомолекулярных веществ (ионы соли) диффундируют через стенку мешочка, а крупные молекулы белка остаются внутри мешочка.
Ход работы. 10–15 мл раствора яичного белка, содержащего альбумины, глобулины и сульфат аммония, помещают в целлофановый мешочек и погружают в стакан с дистиллированной водой так, чтобы уровень жидкости в мешочке совпадал с уровнем воды. Для ускорения диализа необходимо менять воду в сосуде. Через 1 час анализируют воду из стакана: в одной пробирке проводят биуретовую реакцию и убеждаются, что белки через мембрану не проходят; в другой пробирке проводят реакцию на ион SO4 2- , добавлением нескольких капель 10%-ного раствора ВаСI2 для установления проникновения соли через стенку целлофанового мешочка. Через 2–3 часа отмечают появление осадка глобулинов внутри мешочка, который отфильтровывают. В фильтрате остаются белки альбуминовой фракции.
Глобулиновую природу белков осадка доказывают растворением его в растворах солей (10 %-ный раствор хлористого аммония, хлористого натрия и др.) При разбавлении раствора водой вновь выпадает осадок.
Альбуминовую природу белков фильтрата подтверждают разбавлением водой с отсутствием осадка или полным насыщением сернокислым аммонием (выпадает осадок).
Материалы и реактивы: раствор яичного белка, содержащего альбумины, глобулины и сульфат аммония (см. приложение Б, п.5); 10 %-ный раствор хлористого бария; 10 %-ный раствор едкого натра; 1%-ный раствор медного купороса; 10 %-ный раствор хлористого аммония; сернокислый аммоний, тонко измельченный.
Оборудование: пробирки обыкновенные; целлофановый или коллодиевый мешочек; химический стакан или сосуд на 1–2 мл; пипетки мерные на 10 мл; пипетки.
Процесс необратимого осаждения белков. Денатурация, обратимость процесса.
Необратимое осаждение белков связано с глубокими нарушениями структуры белков (вторичной и третичной) и потерей ими нативных свойств. Такие изменения белков можно вызвать кипячением, действием концентрированных растворов минеральных и органических кислот, солями тяжелых металлов.
(При действии солей тяжелых металлов происходит денатурация белковой молекулы. Осаждение денатурированного белка происходит из-за адсорбции частиц металла на поверхности белковой частицы. Свойства белков осаждаться солями тяжелых металлов используется в медицинской практике. Белки (в составе молока, яйца) применяют в качестве противоядия при отравлении солями тяжелых металлов. Белок ограничивает всасывание ионов металла, образуя с ними нерастворимые комплексы.)
Денатурация белков (лат. denaturatus — лишенный природных свойств; от de- — приставка, означающая отделение, удаление + natura — природа, естество) — термин биологической химии, означающий потерю белками их естественных свойств (растворимости, гидрофильности и др.) вследствие нарушения пространственной структуры их молекул.
Ренатурация — процесс, обратный денатурации, при котором белки возвращают свою природную структуру.(При нагревании двухцепочечных молекул ДНК до темп-ры ок. 100°С водородные связи между основаниями разрываются, и комплементарные цепи расходятся — ДНК денатурирует. Однако при медленном охлаждении комплементарные цепи могут вновь соединяться в регулярную двойную спираль. Эта способность ДНК к Р. используется для получения искусств, гибридных молекул ДНК (т. н. молекулярная гибридизация)
Нативная структура белка и ее разрушения. Признаки денатурации.
Функционально активную конформацию белка называют "нативная структура".
Денатурация белков - это разрушение их нативной конформации, вызванное разрывом слабых связей, стабилизирующих пространственные структуры, при действии денатурирующих агентов. Денатурация сопровождается потерей биологической активности белка.
Признаки денатурации:
1.Уникальная трехмерная структура каждого белка разрушается, и все молекулы одного белка приобретают случайную конформацию, т. е. отличную от других таких же молекул.
2. Радикалы аминокислот, формирующие активный центр белка, оказываются пространственно удаленными друг от друга, т. е. разрушается специфический центр связывания белка с лигандом.
3. Гидрофобные радикалы, обычно находящиеся в гидрофобном ядре глобулярных белков, при денатурации оказываются на поверхности молекулы, тем самым создаются условия для агрегации белков. Агрегаты белков выпадают в осадок.
4. При денатурации белков не происходит разрушения их первичной структуры. Вспомните условия, в которых происходит гидролиз пептидных связей.
Осаждение белков солями тяжелых металлов, механизм, особенности, значение для клиники.
При действии солей тяжелых металлов происходит денатурация белковой молекулы. Осаждение денатурированного белка происходит из-за адсорбции частиц металла (свинца, меди, ртути, серебра и других) на поверхности белковой частицы.
Особенности:Однако при избытке некоторых солей наблюдается растворение первоначально образовавшегося осадка. Это связано с накоплением ионов металла на поверхности денатурированного белка и появлением положительного заряда на белковой молекуле.
В клинике:свойства белков осаждаться солями тяжелых металлов используется в медицинской практике. Белки (в составе молока, яйца) применяют в качестве противоядия при отравлении солями тяжелых металлов. Белок ограничивает всасывание ионов металла, образуя с ними нерастворимые комплексы.
Осаждение белков минеральными и органическими кислотами, особенности процесса, значение для клиники.
Принцип:концентрированные кислоты (серная, хлористоводородная, азотная и др.) вызывают денатурацию белка за счет удаления факторов устойчивости белка в растворе (заряда и гидратной оболочки). Однако при избытке хлористоводородной и серной кислот выпавший осадок денатурированного белка вновь растворяется. По-видимому, это происходит в результате перезарядки молекул белка и частичного гидролиза. При добавлении избытка азотной кислоты растворение осадка не происходит (точный механизм этого явления не установлен).
Клиника:для определения малых количеств белка в моче в клинических лабораториях пользуются азотной кислотой.
Осаждение органическими кислотами
Принцип: трихлоруксусная кислота осаждает только белки, а сульфосалициловая осаждает не только белки, но и высокомолекулярные полипептиды. ТХУ кислота осаждает только белки и не осаждает продукты распада белка и аминокислоты, поэтому ею пользуются часто для полного удаления белков из биологических жидкостей (например, сыворотки крови).
Клиника: Сульфосалициловой кислотой (как самой чувствительной) широко пользуются для обнаружения белка в моче.
Уровни структурной организации белков.
4 уровня структурной организации: первичная, вторичная, третичная и четвертичная.
Линейную последовательность аминокислотных остатков в полипептидной цепи называют "первичная структура белка". Пептидная связь образуется за счет -карбоксильной группы одной аминокислоты и -аминной группы другой. Типы связей: ковалентные пептидные связи, дисульфидные мостики. Первичная структура задана генетически. Примеры: инсулин, пепсин, химотрипсин.
1) Первичной структурой белков называется линейная полипептидная цепь из аминокислот, соединенных между собой пептидными связями.
2) Вторичная структура представляет собой способ укладки полипептидной цепи в упорядоченную структуру благодаря образованию водородных связей между пептидными группами одной цепи или смежными полипептидными цепями.
3) Третичной структурой белка называется способ укладки полипептидной цепи в пространстве. По форме третичной структуры белки делятся в основном на глобулярные и фибриллярные. Глобулярные белки чаще всего имеют эллипсовидную форму, а фибриллярные (нитевидные) белки — вытянутую (форма палочки, веретена).
4) Белки, состоящие из одной полипептидной цепи, имеют только третичную структуру. К ним относятся миоглобин — белок мышечной ткани.
Первичная структура белка, понятия и типы связей первичной структуры.
Первичной структурой белков называется линейная полипептидная цепь из аминокислот, соединенных между собой пептидными связями. Линейную последовательность аминокислотных остатков в полипептидной цепи называют "первичная структура белка". Пептидная связь образуется за счет -карбоксильной группы одной аминокислоты и -аминной группы другой. Типы связей: ковалентные пептидные связи, дисульфидные мостики. Первичная структура задана генетически. Примеры: инсулин, пепсин, химотрипсин.
Зависимость физико-химических и биологических свойств белков от первичной структуры.
1. Первичная структура белков уникальна и детерминирована генетически. Каждый индивидуальный гомогенный белок характеризуется уникальной последовательностью аминокислот: частота замены аминокислот приводит не только к структурным перестройкам, но и к изменениям физико-химических свойств и биологических функций.
2. В первичной структуре полипептидной цепи детерминированы вторичная, третичная и четвертичная структуры белковой молекулы, определяющие ее общую пространственную конформацию.
Осаждение белка солями тяжелых металлов.
Белки при взаимодействии с солями свинца, меди, ртути, серебра и других тяжелых металлов денатурируются и выпадают в осадок. Однако при избытке некоторых солей наблюдается растворение первоначально образовавшегося осадка. Это связано с накоплением ионов металла на поверхности денатурированного белка и появлением положительного заряда на белковой молекуле.
1) яичный белок, 1% раствор;
2) сульфат меди, 10% раствор;
3) ацетат свинца, 5% раствор;
4) нитрат серебра, 5% раствор.
Классификация белков в зависимости от выполняемых функций:
- ферменты – (от лат. «fermentum» - брожение, закваска) – группа специфических белков, увеличивающих скорость протекания химических реакций в клетках всех живых организмов.
- транспортные – группа белков, выполняющих функцию переноса различных атомов, молекул, ионов как внутри клетки, так и между клетками в многоклеточных организмах.
- структурные – группа белков, отвечающих за поддержание формы и стабильности клеток и тканей.
- регуляторные (гормональные) – группа белков, осуществляющих функции сигнальных веществ (гормонов).
- защитные – группа белков, предохраняющих организм от вторжения других организмов и повреждений.
- запасающие (резервные, пищевые) – группа белков, являющихся ценными пищевыми веществами. У животных – мышечные белки служат резервными питательными веществами, которые мобилизируются при крайней необходимости.
- сократительные (дигательные) – группа белков, ответственных за мышечное сокращение и другие формы биологической подвижности.
16.
Каждый индивидуальный белок, имеющий уникальную первичную структуру и конформацию, обладает и уникальной функцией, отличающей его от bqcx остальных белков. Набор индивидуальных белков выполняет в клетке множество разнообразных и сложных функций.
Необходимое условие для функционирования белков - присоединение к нему другого вещества, которое называют "лиганд". Лигандами могут быть как низкомолекулярные вещества, так и макромолекулы. Взаимодействие белка с лигандомвысокоспецифично, что определяется строением участка белка, называемого центром связывания белка с лигандом или активным центром.
А. Активный центр белков и избирательность связывания его с лигандом
Активный центр белков - определённый участок белковой молекулы, как правило, находящийся в её углублении ("кармане"), сформированный радикалами аминокислот, собранных на определённом пространственном участке при формировании третичной структуры и способный комплементарно связываться с лигандом. В линейной последовательности полипептидной цепи радикалы, формирующие активный центр, могут находиться на значительном расстоянии друг от друга.
Высокая специфичность связывания белка с лигандом обеспечивается комплементарностью структуры активного центра белка структуре лиганда (рис. 1-25).
Под комплементарностью понимают пространственное и химическое соответствие взаимодействующих молекул. Лиганд должен обладать способностью входить и пространственно совпадать с конформацией активного центра. Это совпадение может быть неполным, но благодаря конформационной лабильности белка активный центр способен к небольшим изменениям и "подгоняется" под лиганд. Кроме того, между функциональными группами лиганда и радикалами аминокислот, образующих активный центр, должны возникать связи, удерживающие лиганд в активном центре. Связи между лигандом и активным центром белка могут быть как нековалентными (ионными, водородными, гидрофобными), так и ковалентными.

Рис. 1-25. Взаимодействие белка с лигандом. А и Б - некомплементарное взаимодействие и разрушение связей между белком и лигандом; В - комплементарное взаимодействие белка с лигандом.
1. Характеристика активного центра
Активный центр белка - относительно изолированный от окружающей белок среды участок, сформированный аминокислотными остатками. В этом участке каждый остаток благодаря своему индивидуальному размеру и функциональным группам формирует "рельеф" активного центра.
Объединение таких аминокислот в единый функциональный комплекс изменяет реакционную способность их радикалов, подобно тому, как меняется звучание музыкального инструмента в ансамбле. Поэтому аминокислотные остатки, входящие в состав активного центра, часто называют "ансамблем" аминокислот.
Уникальные свойства активного центра зависят не только от химических свойств формирующих его аминокислот, но и от их точной взаимной ориентации в пространстве. Поэтому даже незначительные нарушения общей конформации белка в результате точечных изменений его первичной структуры или условий окружающей среды могут привести к изменению химических и функциональных свойств радикалов, формирующих активный центр, нарушать связывание белка с лигандом и его функцию. При денатурации активный центр белков разрушается, и происходит утрата их биологической активности.
Часто активный центр формируется таким образом, что доступ воды к функциональным группам его радикалов ограничен, т.е. создаются условия для связывания лиганда с радикалами аминокислот.
В некоторых случаях лиганд присоединяется только к одному из атомов, обладающему определённой реакционной способностью, например присоединение О2 к железу миоглобина или гемоглобина. Однако свойства данного атома избирательно взаимодействовать с О2 определяются свойствами радикалов, окружающих атом железа в составе тема. Гем содержится и в других белках, таких как цитохромы. Однако функция атома железа в цитохромах иная, он служит посредником для передачи электронов от одного вещества другому, при этом железо становится то двух-, то трёхвалентным.
Центр связывания белка с лигандом часто располагается между доменами. Например, протеолитический фермент трипсин, участвующий в гидролизе пептидных связей пищевых белков в кишечнике, имеет 2 домена, разделённых бороздкой. Внутренняя поверхность бороздки формируется аминокислотными радикалами этих доменов, стоящими в полипептидной цепи далеко друг от друга (Сер177, Гис40, Асп85).
Разные домены в белке могут перемещаться друг относительно друга при взаимодействии с лигандом, что облегчает дальнейшее функционирование белка. В качестве примера можно рассмотреть работу гексокиназы, фермента, катализирующего перенос фосфорного остатка с АТФ на молекулу глюкозы (при её фосфорилировании). Активный центр гексокиназы располагается в расщелине между двумя доменами (рис. 1-26) При связывании гексокиназы с глюкозой окружающие её домены сближаются, и субстрат оказывается в "ловушке", что облегчает его дальнейшее фосфорилирование.
Основное свойство белков, лежащее в основе их функций, - избирательность присоединения к определённым участкам белковой молекулы специфических лигандов.
2. Многообразие лигандов
- Лигандами могут быть неорганические (часто ионы металлов) и органические вещества, низкомолекулярные и высокомолекулярные вещества;
- существуют лиганды, которые изменяют свою химическую структуру при присоединении к активному центру белка (изменения субстрата в активном центре фермента);
- существуют лиганды, присоединяющиеся к белку только в момент функционирования (например, О2, транспортируемый гемоглобином), и лиганды, постоянно связанные с белком, выполняющие вспомогательную роль при функционировании белков (например, железо, входящее в состав гемоглобина).
В тех случаях, когда аминокислотные остатки, формирующие активный центр, не могут обеспечить функционирование данного белка, к определённым участкам активного центра могут присоединяться небелковые молекулы. Так, в активном центре многих ферментов присутствует ион металла (кофактор) или органическая небелковая молекула (кофермент). Небелковую часть, прочно связанную с активным центром белка и необходимую для его функционирования, называют "простатическая группа". Миоглобин, гемоглобин и цитохромы имеют в активном центре простетическую группу - гем, содержащий железо (более подробно гемсодержащие белки описаны в разделе 4, а кофакторы и коферменты - в разделе 2).
Соединение протомеров в олигомерном белке - пример взаимодействия высокомолекулярныхлигандов. Каждый протомер, соединённый с другими протомерами, служит для них лигандом, так же как они для него.
Иногда присоединение какого-либо лиганда изменяет конформацию белка, в результате чего формируется центр связывания с другими лигандами. Например, белок кальмодулин после связывания с четырьмя ионами Са 2+ в специфических участках приобретает способность взаимодействовать с некоторыми ферментами, меняя их активность.

Рис. 1-26. Связывание гексокиназы с глюкозой.
3. Сродство активного центра лиганду
Скорость взаимодействия белка с лигандом определяется концентрациями белка и лиганда в растворе, а также степенью комплементарности белка и лиганда.
Константа диссоциации - характеристика сродства активного центра лиганду.
· Так как взаимодействие белка с лигандом - обратимый процесс, то его можно описать следующим уравнением:
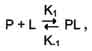
где Р - белок, L - лиганд, PL - комплекс белка с лигандом, К1 - константа скорости связывания белка с лигандом, К-1 - константа скорости распада комплекса PL.
Когда скорости образования и распада комплекса равны, говорят о том, что система находится в состоянии равновесия:
Соотношение констант распада [PL] комплекса и его образования называется константой диссоциации (Кдисс) комплекса [PL]. Чем меньше Кдисс , тем больше молекул лиганда связано с белком, тем больше комплементарность между Р и L и тем больше сродство лиганда к белку. То есть между Кдисс и сродством лиганда к белку имеется обратно пропорциональная связь.
Иногда при описании процесса связывания белка с лигандом используют величину, обратную Кдисс, называемую константой связывания (Ксв) или ассоциации.
Между Ксв. и сродством лиганда к белку существует прямо пропорциональная зависимость.
Зависимость насыщения белка лигандом от концентрации лиганда при постоянной концентрации белка
· При постоянной концентрации белка увеличение концентрации лиганда приводит к росту концентрации комплекса [PL]. Эта зависимость носит характер гиперболической кривой (рис. 1-27). Кривая стремится к максимуму, когда при некоторой концентрации лиганда все молекулы белка находятся в связанном с лигандом состоянии (происходит насыщение белка лигандом). Степень насыщения белка лигандом можно выразить следующим уравнением: степень насыщения = [PL]/[P0]?100 (где Р0 - концентрация белка до добавления лиганда).
· При полунасыщении белка лигандом концентрации [PL] и [Р] равны, и из уравнения Кдисс, приведённого выше, следует, что Кдисс = [L], т.е. Кдисс численно равна концентрации лиганда, при которой 50% белка находится в комплексе с лигандом. Поэтому по кривой насыщения можно найти Кдисс и оценить сродство данного белка лиганду.
Зависимость между образованием комплекса [PL] и концентрацией белка при избытке лиганда
· Как было сказано выше, при возрастающей концентрации лиганда насыщение белка ограничено его концентрацией. При избытке лиганда все молекулы белка находятся в составе комплекса [PL]. Однако, если увеличивать концентрацию белка, то количество [PL] начнёт увеличиваться пропорционально концентрации белка. Концентрацию комплекса [PL] можно регистрировать, например

Рис. 1-27. График насыщения белка лигандом.
· с помощью измерения поглощения света. Учитывая, что его количество пропорционально концентрации белка, можно на основании построенного графика определять концентрацию белка в растворе (рис. 1-28).
В основе функционирования любого белка лежит его способность к избирательному взаимодействию с каким-либо другим веществом — лигандом. Лигандом может быть как низкомолекулярное вещество, так и макромолекула, в том числе другой белок. Лиганд присоединяется к определенному участку на поверхности белковой молекулы — центру связывания (активный центр).
Активный центр белков – определённый участок белковой молекулы, как правило, находящийся в её углублении, сформированный радикалами аминокислот, собранных на определённом пространственном участке при формировании третичной структуры и способный комплементарно связываться с лигандом. В линейной последовательности полипептидной цепи радикалы, формирующие активный центр, могут находиться на значительном расстоянии друг от друга.
Высокая специфичность связывания белка с лигандом обеспечивается комплементарностью структуры активного центра белка и структуры лиганда.
Под комплементарностью понимают пространственное и химическое соответствие взаимодействующих молекул. Лиганд должен обладать способностью входить и пространственно совпадать с конформацией активного центра. Это совпадение может быть неполным, но благодаря конформационной лабильности белка, активный центр способен к небольшим изменениям и «подгоняется» под лиганд. Кроме того, между функциональными группами лиганда и радикалами аминокислот, образующих активный центр, должны возникать связи, удерживающие лиганд в активном центре. Связи между лигандом и активным центром белка могут быть как нековалентными (ионными, водородными, гидрофобными), так и ковалентными.
Тот факт, что ферменты обладают высокой специфичностью, позволил в 1890 г. выдвинуть гипотезу, согласно которой активный центр фермента комплементарен субстрату, т.е. соответствует ему как "ключ замку". После взаимодействия субстрата ("ключ") с активным центром ("замок") происходят химические превращения субстрата в продукт. Активный центр при этом рассматривался как стабильная, жёстко детерминированная структура.
В 1959 г. был предложен другой вариант гипотезы "ключ-замок", объясняющий события в активном центре фермента. По этой гипотезе активный центр является гибкой структуройпо отношению к субстрату. Субстрат, взаимодействуя с активным центром фермента, вызывает изменение его конформации, приводя к формированию фермент-субстратного комплекса, благоприятного для химических модификаций субстрата. При этом молекула субстрата также изменяет свою конформацию, что обеспечивает более высокую эффективность ферментативной реакции. Эта "гипотеза индуцированного соответствия" впоследствии получила экспериментальное подтверждение.
19.Четвертичная структура белков
Количество и взаиморасположение полипептидных цепей в пространстве называют "четвертичная структура белков".Отдельные полипептидные цепи в таком белке носят название протомеров, или субъединиц. Белок, содержащий в своём составе несколько протомеров, называют олигомерным.
1. Количество протомеров в структуре
олигомерных белков
В состав олигомерных белков может входить от двух до нескольких десятков протомеров, хотя наиболее часто встречают белки, содержащие от двух до четырёх полипептидных цепей (димерные, тетрамерные белки).Так, фермент гексокиназа содержит в своём составе 2 протомера; белок эритроцитов гемоглобин и фермент лактатдегидрогеназа - 4 протомера; Некоторые олигомерные белки содержат идентичные протомеры (например, гексокиназа), другие состоят из разных протомеров. Олигомерные белки имеют большую молекулярную массу. Белки с молекулярной массой более 50 000 Д практически всегда содержат несколько мономерных полипептидных цепей. По сравнению с индивидуальными мономерными белками олигомеры выполняют более сложные функции.
2. Сборка протомеров в олигомерный белок.
Комплементарность протомеров
"Узнавание" и присоединение отдельных протомеров олигомерного белка происходят благодаря формированию на их поверхности контактных участков. Последние состоят из радикалов аминокислот, собранных в данном месте в процессе образования третичной структуры белка. Совокупность этих радикалов формирует уникальные поверхности, способные с высокой специфичностью объединяться друг с другом. Таким образом, взаимодействие протомеров осуществляется во многих точках контактирующих поверхностей, с образованием десятков слабых связей. Благодаря этому контактные поверхности соединяются с высокой специфичностью, и ошибки формирования четвертичной структуры белков практически исключены. Комплементарность - универсальный принцип, свойственный живой природе и лежащий в основе узнавания и соединения не только протомеров, но и других (не обязательно белковых) молекул.
Кооперативность
Кооперативное связывание
Когда субстрат связывается с активным центром одной субъединицы фермента, остальные субъединицы активируются. Лиганды могут иметь некооперативный, положительный или отрицательный кооперативный эффект.(Примером положительной кооперативности может служить связывание кислорода гемоглобином.)Отрицательная кооперативность означает противоположное — в момент связывания лиганда белком, сродство белка к лиганду снижается. Примером может служить взаимодействие между глицеральдегид-3-фосфатом и ферментом глицеральдегид-3-фосфат дегидрогеназой.
Кооперативность, явление кооперативности — это такие изменения состояния системы, взаимодействие элементов которой усиливается с течением процесса изменения так, что существенно ускоряет его ход в целом (положительная кооперативность). Таким образом, сила взаимодействия атомов или молекул возрастает по мере нарастания изменений в системе, делая их коллективно согласованными
3. ОСОБЕННОСТИ ФУНКЦИОНИРОВАНИЯ ОЛИГОМЕРНЫХ БЕЛКОВ НА ПРИМЕРЕ ГЕМОГЛОБИНА.
Олигомерные белки проявляют свойства, отсутствующие у мономерных белков. Влияние четвертичной структуры на функциональные свойства белка можно рассмотреть, сравнивая строение и функции двух родственных гемсодержащих белков: миоглобина и гемоглобина. Оба белка имеют общее эволюционное происхождение, сходную конформацию отдельных полипептидных цепей и сходную функцию (участвуют в транспорте кислорода), но миоглобин - мономерный белок, а гемоглобин - тетрамер. Наличие четвертичной структуры у гемоглобина придаёт этому белку свойства, отсутствующие у миоглобина.
Реакции осаждения белков
Известно, что белки в растворе сохраняются в природном состоянии за счёт факторов устойчивости, к которым относятся заряд белковой молекулы и гидратная (водная) оболочка вокруг нее. Удаление этих факторов приводит к склеиванию этих молекул белка и выпадению в осадок. Осаждение белков может быть обратимым и необратимым в зависимости от природы используемых реактивов.
Обратимое осаждение – при этом процессе под воздействием факторов осаждения белки выпадают в осадок, но после прекращения действия этих факторов белки вновь переходят в растворимое состояние и приобретают свои нативные свойства. Одним из видов обратимого осаждения белков является высаливание.
Необратимое осаждение белков связано с глубокими нарушениями структуры белков (вторичной и третичной) и потерей ими нативных свойств. Такие изменения белков можно вызвать кипячением, действием концентрированных растворов минеральных и органических кислот, солями тяжелых металлов.
Для высаливания белков используют соли щелочных и щелочноземельных металлов (наиболее часто в практике используют сульфат натрия и аммония). Эти соли удаляют водную оболочку (вызывают обезвоживание) и снимают заряд. Между величиной водной оболочки белковых молекул и концентрацией солей существует прямая зависимость: чем меньше гидратная оболочка, тем меньше требуется солей. Так, глобулины, имеющие крупные и тяжелые молекулы и небольшую водную оболочку, выпадают в осадок при неполном насыщении раствора солями, а альбумины как более мелкие молекулы, окруженные большой водной оболочкой, – при полном насыщении.
Денатурация белка (необратимое осаждение) сводится к разрушению третичной и частично вторичной структуры белковой молекулы врезультате разрыва водородных связей и потере им биологических или нативных свойств. При необратимых реакциях осаждения белки претерпевают глубокие изменения и не могут быть растворимы в первоначальном растворителе. К необратимым реакциям относятся осаждение белка солями тяжелых металлов, минеральными и органическими кислотами, алкалоидными реактивами и осаждение при кипячении.
Опыт 1. Высаливание белков сульфатом аммония.
Принцип метода. Высаливание – это добавление к раствору белка нейтральных солей (Na2SO4, (NH4)2SO4). Механизм высаливания заключается во взаимодействии анионов (SO4 2– ) и катионов (Na + , NH4 + ) с зарядами белка (группы NH4 + и COO – ). В результате заряд исчезает, и соответственно, исчезает взаимоотталкивание молекул. Одновременно резко уменьшается гидратная оболочка. Все это приводит к «слипанию» молекул и осаждению.
Насыщенным раствором сульфата аммония осаждается альбуминовая фракция белков, полунасыщенным раствором – глобулиновая фракция.
Сущность реакции заключается в дегидратации молекул белка.
Порядок выполнения работы.
В пробирку наливают 30 капель неразведённого яичного белка и добавляют равное количество насыщенного раствора сульфата аммония. Содержимое пробирки перемешивают. При этом осаждается альбуминовая фракция белков.
Получают полунасыщенный раствор сульфата аммония и также смешивают (1:1) с яичным белком, при этом глобулиновая фракция осаждается, а альбуминовая остается в растворе. Последнюю отфильтровывают, затем смешивают с порошком сульфата аммония до тех пор, пока не прекратится растворение соли, при этом выпадает осадок – альбумины.
К образовавшимся осадкам (глобулинов и альбуминов) добавляют воду и наблюдают их растворение. Это доказывает, что высаливание – процесс обратимый.
Оформление опыта: полученные результаты опыта записать в тетрадь и сделать вывод.
Опыт 2. Высаливание белков хлоридом натрия и сульфатом магния.
Принцип метода. Для высаливания белков из растворов применяются хлорид натрия, сульфат натрия, ацетат натрия, сульфат магния, ацетат калия, хлорид кальция, нитрат кальция и сульфат аммония. Некоторые из перечисленных солей высаливают белки не только при насыщении ими раствора; определенные белки высаливаются и при достаточно низких концентрациях солей. К таким солям относится сульфат аммония. Условия, при которых происходит осаждение сульфатом аммония, настолько характерны для отдельных белков (за редкими исключениями), что это свойство белков можно сравнить с растворимостью, характеризующей кристаллические вещества.
Белки состоят из аминокислот и поэтому обладают амфотерными свойствами. При растворении белков в воде ион водорода,появляющийся в результате диссоциации карбоксильной группы, присоединяется к аминогруппе. Поэтому белковые молекулы несут как положительные, так и отрицательные заряды. Величина заряда определяется количеством ионогенных групп. При определённом значении рН суммарный электрический заряд молекулы белка становится равным нулю. Такое значение рН называется изоэлектрической точкой (рJ). В изоэлектрической точке растворы белков имеют минимальную устойчивость, поскольку они лишены основного стабилизирующего фактора – заряда и поэтому легко выпадают в осадок. Определить изоэлектрическую точку белка можно, определив рН, при котором раствор белка имеет наибольшее помутнение. У большинства белков изоэлектрическая точка лежит в слабокислой среде.
Осаждение белков NaCl и MgSO4 - Хлорид натрия и сульфат магния в отличие от сульфата аммония осаждают глобулины из насыщенного раствора. В изоэлектрической точке глобулины этими же солями осаждаются при более низкой концентрации.
В 2 пробирки наливают по 5 мл 1% раствора белка, прибавляют при перемешивании до полного насыщения (когда часть кристаллов остается нерастворённой, несмотря на взбалтывание) в одну пробирку тонко измельченного хлорида натрия, в другую – сульфата магния. Через несколько минут в двух пробирках появляется осадок глобулинов. Осадки отфильтровывают и к фильтрату добавляют несколько капель разбавленной уксусной кислоты (СН3СООН) – в слабокислой среде выпадают альбумины, поскольку рН раствора альбуминов приблизится к изоэлектрической точке.
В водном растворе белков их частицы являются заряженными и сильно гидратированными, что обуславливает устойчивость белковых растворов. Но при высокой концентрации солей, ионы которых тоже сильно гидратированы, происходит разрушение водных оболочек белковых молекул и снимается заряд с белковой молекулы адсорбирующимися на ней ионами соли.
В результате этих двух процессов белковые растворы теряют устойчивость, частицы белка слипаются друг с другом, укрупняются и, наконец, выпадает осадок.
Опыт 3. Свертывание белков при нагревании.
Принцип метода. Выпадение белков в осадок при нагревании характерно почти для всех белков (исключение составляет желатина, не свёртывающаяся при нагревании). Особенно легко и более полно происходит осаждение белка в слабокислой среде, вблизи от изоэлектрической точки. В нейтральной и сильнокислой средах осаждение белков идёт значительно хуже, а в щелочной среде вовсе не наблюдается.
В щелочной среде понижается диссоциация белка по радикалам диаминокислот, молекулы его приобретают отрицательный заряд, вследствие чего остаются в растворе даже при нагревании до кипения.
Добавление к раствору белка нейтральных солей (NaCl) облегчает и ускоряет свёртывание белков при кипячении вследствие наступающего дегидратирования белковых частиц.
В 5 пробирок наливают по 2 мл. белка: первую пробирку нагревают, осадок появляется еще до того, как жидкость закипит. Во вторую пробирку добавляют 1 каплю 1%-ного раствора уксусной кислоты (СН3СООН) и нагревают. Хлопьевидный осадок белка выпадает скорее и полнее, чем в первой пробирке вследствие того, что при подкислении рН раствора приблизится к изоэлектрической точке белка (заряд белка = 0). В третью пробирку добавляют 0,5 мл. 10%-ной уксусной кислоты (СН3СООН) и нагревают. Осадка не образуется даже при кипении. В четвертую пробирку добавляют 0,5 мл. 10%-ной уксусной кислоты (СН3СООН) и несколько капель насыщенного раствора хлорида натрия и нагревают. Осадок есть. В пятую пробирку добавляют 0,5 мл. 10% раствора щелочи и нагревают. Осадок не образуется даже при кипячении. Оформление работы.
Читайте также:
