Плавление металлов и сплавов
Обновлено: 04.10.2024
Металлы и сплавы — это незаменимая основа для литейного и ювелирного производства, ковки и многих других сфер. Что бы ни делал человек из металла (какой бы это ни был процесс), для правильной работы ему нужно знать, при какой температуре плавится тот или иной металл. Мы подробно рассмотрим процесс плавления, его отличие от кипения, а также сравним температуры в таблицах.
Таблица температур плавления
Что такое температура плавления
Каждый металл имеет неповторимые свойства, и в этот список входит температура плавления. При плавке металл уходит из одного состояния в другое, а именно из твёрдого превращается в жидкое. Чтобы сплавить металл, нужно приблизить к нему тепло и нагреть до необходимой температуры – этот процесс и называется температурой плавления. В момент, когда температура доходит до нужной отметки, он ещё может пребывать в твёрдом состоянии. Если продолжать воздействие – металл или сплав начнет плавиться.
Плавление и кипение – это не одно и то же. Точкой перехода вещества из твердого состояния в жидкое, зачастую называют температуру плавления металла. В расплавленном состоянии у молекул нет определенного расположения, но притяжение сдерживает их рядом, в жидком виде кристаллическое тело оставляет объем, но форма теряется.
При кипении объем теряется, молекулы между собой очень слабо взаимодействуют, движутся хаотично в разных направлениях, совершают отрыв от поверхности. Температура кипения – это процесс, при котором давление металлического пара приравнивается к давлению внешней среды.
Для того, чтобы упростить разницу между критическими точками нагрева мы подготовили для вас простую таблицу:
| Свойство | Температура плавки | Температура кипения |
|---|---|---|
| Физическое состояние | Сплав переходит в расплав, разрушается кристаллическая структура, проходит зернистость | Переходит в состояние газа, некоторые молекулы могут улетать за пределы расплава |
| Фазовый переход | Равновесие между твердым состоянием и жидким | Равновесие давления между парами металла и воздухом |
| Влияние внешнего давления | Нет изменений | Изменения есть, температура уменьшается при разряжении |
При какой температуре плавится
Металлические элементы, какими бы они ни были — плавятся почти один в один. Этот процесс происходит при нагреве. Оно может быть, как внешнее, так и внутреннее. Первое проходит в печи, а для второго используют резистивный нагрев, пропуская электричество либо индукционный нагрев. Воздействие выходит практически схожее. При нагреве, увеличивается амплитуда колебаний молекул. Образуются структурные дефекты решётки, которые сопровождаются обрывом межатомных связей. Под процессом разрушения решётки и скоплением подобных дефектов и подразумевается плавление.
У разных веществ разные температуры плавления. Теоретически, металлы делят на:
- Легкоплавкие – достаточно температуры до 600 градусов Цельсия, для получения жидкого вещества.
- Среднеплавкие – необходима температура от 600 до 1600 ⁰С.
- Тугоплавкие – это металлы, для плавления которых требуется температура выше 1600 ⁰С.
Плавление железа
Температура плавления железа достаточно высока. Для технически чистого элемента требуется температура +1539 °C. В этом веществе имеется примесь — сера, а извлечь ее допустимо лишь в жидком виде.
Без примесей чистый материал можно получить при электролизе солей металла.
Плавление чугуна
Чугун – это лучший металл для плавки. Высокий показатель жидкотекучести и низкий показатель усадки дают возможность эффективнее пользоваться им при литье. Далее рассмотрим показатели температуры кипения чугуна в градусах Цельсия:
- Серый — температурный режим может достигать отметки 1260 градусов. При заливке в формы температура может подниматься до 1400.
- Белый — температура достигает отметки 1350 градусов. В формы заливается при показателе 1450.
Важно! Показатели плавления такого металла, как чугун – на 400 градусов ниже, по сравнению со сталью. Это значительно снижает затраты энергии при обработке.
Плавление стали

Плавления стали при температуре 1400 °C
Сталь — это сплав железа с примесью углерода. Её главная польза — прочность, поскольку это вещество способно на протяжении длительного времени сохранять свой объем и форму. Связано это с тем, что частицы находятся в положении равновесия. Таким образом силы притяжения и отталкивания между частицами равны.
Справка! Сталь плавится при 1400 °C.
Плавление алюминия и меди
Температура плавления алюминия равна 660 градусам, это означает то, что расплавить его можно в домашних условиях.
Чистой меди – 1083 градусов, а для медных сплавов составляет от 930 до 1140 градусов.
От чего зависит температура плавления
Для разных веществ температура, при которой полностью перестраивается структура до жидкого состояния – разная. Если взять во внимание металлы и сплавы, то стоит подметить такие моменты:
- В чистом виде не часто можно встретить металлы. Температура напрямую зависит от его состава. В качестве примера укажем олово, к которому могут добавлять другие вещества (например, серебро). Примеси позволяют делать материал более либо менее устойчивым к нагреву.
- Бывают сплавы, которые благодаря своему химическому составу могут переходить в жидкое состояние при температуре свыше ста пятидесяти градусов. Также бывают сплавы, которые могут «держаться» при нагреве до трех тысяч градусов и выше. С учетом того, что при изменении кристаллической решетки меняются физические и механические качества, а условия эксплуатации могут определяться температурой нагрева. Стоит отметить, что точка плавления металла — важное свойство вещества. Пример этому – авиационное оборудование.
Термообработка, в большинстве случаев, почти не изменяет устойчивость к нагреву. Единственно верным способом увеличения устойчивости к нагреванию можно назвать внесение изменений в химический состав, для этого и проводят легирование стали.
У какого металла самая высокая температура плавления

Вольфрам – самый тугоплавкий металл, 3422 °C (6170 °F).
Твердый, тугоплавкий, достаточно тяжелый материал светло-серого цвета, который имеет металлический блеск. Механической обработке поддается с трудом. При комнатной температуре достаточно хрупок и ломается. Ломкость металла связана с загрязнением примесями углерода и кислорода.
Примечание! Технически, чистый металл при температуре выше 400 °C становится очень пластичным. Демонстрирует химическую инертность, неохотно вступает в реакции с другими элементами. В природе встречается в виде таких сложных минералов, как: гюбнерит, шеелит, ферберит и вольфрамит.
Вольфрам можно получить из руды, благодаря сложным химическим переработкам, в качестве порошка. Используя прессование и спекание, из него создают детали обычной формы и бруски.
Вольфрам — крайне стойкий элемент к любым температурным воздействиям. По этой причине размягчить вольфрам не могли более сотни лет. Не существовало такой печи, которая смогла бы нагреться до нескольких тысяч градусов по Цельсию. Ученым удалось доказать, что это самый тугоплавкий металл. Хотя бытует мнение, что сиборгий, по некоторым теоретическим данным, имеет большую тугоплавкость, но это лишь предположение, поскольку он является радиоактивным элементом и у него небольшой срок существования.
8. Плавление металлов и строение расплавов
Плавление – это физический процесс перехода металла из твердого состояния в жидкое расплавленное. Плавление – процесс, обратный кристаллизации, происходит при температуре выше равновесной, т. е. при перегреве. Поскольку жидкий металл обладает большей внутренней энергией, чем твердый, при кристаллизации выделяется теплота. Между теплотой Q и температурой кристаллизации Тк существует определенная связь. Степень перегрева при плавлении металлов не превышает нескольких градусов.
В жидком состоянии атомы вещества из-за теплового движения перемещаются беспорядочно, в жидкости имеются группировки атомов небольшого объема, в их пределах расположение атомов аналогично расположению в решетке кристалла. Эти группировки неустойчивы, они рассасываются и снова появляются в жидкости. При переохлаждении жидкости некоторые крупные группировки становятся устойчивыми и способными к росту. Эти устойчивые группировки атомов называют центрами кристаллизации (зародышами). Для осуществления процесса плавления необходимо наличие некоторого перегрева над равновесной температурой, т. е. термодинамического потенциала. Выше равновесной температуры более устойчив жидкий металл, он имеет меньший запас свободной энергии. Ниже этой температуры более устойчив твердый металл. При равновесной температуре свободные энергии жидкого и твердого состояния одинаковы, поэтому при этой температуре обе фазы (жидкая и твердая) могут сосуществовать одновременно и притом бесконечно долго. Равновесная температура очень близка к температуре плавления Тпл, с которой ее часто сравнивают. При охлаждении переход из жидкого состояния в твердое сопровождается образованием кристаллической решетки, т. е. кристаллизацией. Чтобы вызвать кристаллизацию, жидкий металл нужно переохладить до температуры ниже температуры плавления.
Жидкости, находящиеся при температуре, близкой к температуре плавления называются расплавами. Расплавы бывают металлическими, ионными, полупроводниковыми, органическими и высокополимерными. В зависимости от того, какие химические соединения образуют расплавы, выделяют солевые, оксидные, оксидно-силикатные и другие расплавы.
Большинство расплавов имеют в составе искосаэдрические частицы.
В процессе плавления химические связи в расплавах подвергаются видоизменению. В полупроводниках наблюдается образование металлической проводимости, у некоторых галогенидов вместо ионной проводимости происходит снижение электрической проводимости из-за образования расплава с молекулярным составом. Уровень температуры также влияет на тип связи в расплавах.
Среднее координационное число и межатомные расстояния также являются характеристиками расплавов. В процессе плавления металлов происходит уменьшение координационного числа примерно на 10–15 %. В тоже время межатомные расстояния остаются прежними. При плавлении полупроводников происходит увеличение их координационного числа в 1,5 раза, расстояние между атомами также увеличивается. Многокомпонентные расплавы характеризуются неравновесными, метастабильными состояниями, которые имеют взаимосвязь со структурой первоначальных твердых фаз.
Во многих случаях встречается отставание (гистерезис) свойств расплавов в процессе изменения температуры. На свойства и строения расплавов оказывают влияние следующие факторы: температура, время выдержки, скорость колебания температуры, тот материал, из которого создан контейнер, а также наличие примесей.
Состав расплавов отличается своей сложностью. В ионных расплавах могут содержаться простые или комплексные ионы, недиссоциированные и полимерные молекулы, а также свободные объемы. Силикатные расплавы могут содержать изолированные кремнекислородные тетраэдры и образуемые ими цепи, кольца, сетки и каркасы.
Однозначная модель структуры расплавов формируется достаточно сложно, т. к. расплавы содержат разные виды частиц и связи. Основная функция моделей: определение и интерпретация свойств расплавов, а также расчет свойств.
Расплавы в металлургической области подразделяются на промежуточные, побочные и конечные продукты. Используя расплавы в качестве электролитов, в металлургии производят и рафинируют металлы, а также осуществляют нанесение покрытий. Многие сплавы образуются в виде расплавов. Монокристаллы и эпитаксиальные пленки выращиваются из расплавов. В качестве катализаторов принято использовать металлические, солевые и оксидные расплавы. Солевые расплавы применяют в отжиговых и закалочных ваннах, высокотемпературных топливных элементах, в качестве теплоносителей, флюсов в процессе пайки и сварки металлов, реакционных сред в неорганическом и органическом синтезе, а также как поглотители, экстрагенты и т. д. Некоторые расплавы используются для получения силикатных, фторидных и иных специальных стеков и аморфных металлов.
Данный текст является ознакомительным фрагментом.
Продолжение на ЛитРес
Строение древесины
Строение древесины Сделав только поперечный срез, можно четко рассмотреть строение древесины. Каждый брусок необтесанного дерева имеет кору – это кожа дерева, которая не используется в работе, ее обязательно снимают. Под корой располагается зона роста дерева, которая
ЛЕКЦИЯ № 1. Строение древесины
ЛЕКЦИЯ № 1. Строение древесины 1. Виды древесных пород и части дерева Растущие деревья имеют следующие составные части: корни, ствол, ветви, листья. Корневая система деревьев выполняет функции поставщика влаги и питательных веществ из почвы по стволу и ветвям к листьям.
2. Макроскопическое строение древесины
2. Макроскопическое строение древесины При поперечном разрезе ствола дерева можно установить главные макроскопические признаки: заболонь, ядро, годичные слои, сердцевинные лучи, сосуды, смоляные ходы и сердцевинные повторения.У молодых деревьев всех пород древесина
1. Строение металлов
1. Строение металлов Металлы и их сплавы – основной материал в машиностроении. Они обладают многими ценными свойствами, обусловленными в основном их внутренним строением. Мягкий и пластичный металл или сплав можно сделать твердым, хрупким, и наоборот. Для того чтобы
Свойства расплавов стекол
Свойства расплавов стекол К свойствам расплавов стекломассы относятся вязкость, связанная с ней скорость твердения, поверхностное натяжение и кристаллизация, а также теплоемкость, теплопроводность, электрическая проводимость. Значение этих свойств при производстве
§ 3.3 Строение атомов и периодический закон Менделеева
§ 3.3 Строение атомов и периодический закон Менделеева Свойства простых тел, а также формы и свойства соединений элементов, находятся в периодической зависимости (или, выражаясь алгебраически, образуют периодическую функцию) от их атомных весов. Д.И. Менделеев Считается,
§ 3.6 Строение ядер
§ 3.6 Строение ядер Чем больше в ядре должно поместиться нуклонов, тем больше должна быть площадь поверхности ядра, где происходят присоединения то протонов, то нейтронов… Этим особенностям лучше всего отвечает форма ядра в виде двух пирамид Хеопса, соединённых
§ 4.14 Строение вещества и химическая связь
§ 4.14 Строение вещества и химическая связь Что, наконец, представляется нам затверделым и плотным, То состоять из начал крючковатых должно несомненно, Сцепленных между собой наподобие веток сплетённых. В этом разряде вещей, занимая в нём первое место, Будут алмазы
Глава 32 Строение Пространства – Времени
Глава 32 Строение Пространства – Времени «Действие есть кривизна Мира» Павел Дмитриевич Успенский, 1911 год Мы уже предполагали аналогии квантового строения микромира и макромира, при определенных условиях. Далее, будет показаны законы резонансного строения нашего
2. Зеренное строение металлов. Границы зерен и субзерен
2. Зеренное строение металлов. Границы зерен и субзерен Металлы – это поликристаллические тела, они состоят из мелких кристаллов. Характеризуются металлическими свойствами и составляют 50 % всех химических элементов. Строение металлов и их сплавов кристаллическое.В
10. Строение слитка и аморфные сплавы
10. Строение слитка и аморфные сплавы Строение стального слитка впервые дано в 1878 г. Д.К. Черновым. Структура литого слитка состоит из трех основных зон. Первая зона – наружная мелкозернистая корка, которая состоит из дезориентированных мелких кристаллов –
Температура плавления разных металлов в таблице
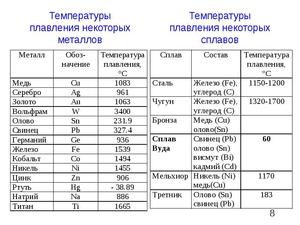
Каждый металл и сплав имеет собственный уникальный набор физических и химических свойств, среди которых не последнее место занимает температура плавления. Сам процесс означает переход тела из одного агрегатного состояния в другое, в данном случае, из твердого кристаллического состояния в жидкое. Чтобы расплавить металл, необходимо подводить к нему тепло до достижения температуры плавления. При ней он все еще может оставаться в твердом состоянии, но при дальнейшем воздействии и повышении тепла металл начинает плавиться. Если температуру понизить, то есть отвести часть тепла, элемент затвердеет.
Самая высокая температура плавления среди металлов принадлежит вольфраму: она составляет 3422С о , самая низкая — у ртути: элемент плавится уже при — 39С о . Определить точное значение для сплавов, как правило, не представляет возможности: оно может значительно колебаться в зависимости от процентного соотношения компонентов. Их обычно записывают в виде числового промежутка.
Как происходит

Плавление всех металлов происходит примерно одинаково — при помощи внешнего или внутреннего нагревания. Первый осуществляется в термической печи, для второго используют резистивный нагрев при пропускании электрического тока или индукционный нагрев в высокочастотном электромагнитном поле. Оба варианта воздействуют на металл примерно одинаково.
При увеличении температуры увеличивается и амплитуда тепловых колебаний молекул, возникают структурные дефекты решетки, выражающиеся в росте дислокаций, перескоке атомов и других нарушениях. Это сопровождается разрывом межатомных связей и требует определенного количества энергии. В это же время происходит образование квази-жидкого слоя на поверхности тела. Период разрушения решетки и накопления дефектов называется плавлением.
Разделение металлов
В зависимости от температуры плавления металлы делятся на:

- Легкоплавкие: им необходимо не более 600С о . Это цинк, свинец, виснут, олово.
- Среднеплавкие: температура плавления колеблется от 600С о до 1600С о . Это золото, медь, алюминий, магний, железо, никель и большая половина всех элементов.
- Тугоплавкие: требуется температура свыше 1600С о , чтобы сделать металл жидким. Сюда относятся хром, вольфрам, молибден, титан.
В зависимости от температуры плавления выбирают и плавильный аппарат. Чем выше показатель, тем прочнее он должен быть. Узнать температуру нужного вам элемента можно из таблицы.
Еще одной немаловажной величиной является температура кипения. Это величина, при которой начинается процесс кипения жидкостей, она соответствует температуре насыщенного пара, который образуется над плоской поверхностью кипящей жидкости. Обычно она почти в два раза больше, чем температура плавления.
Обе величины принято приводить при нормальном давлении. Между собой они прямопропорциональны.
Температура плавления металлов: таблица и понятие
При сварке происходит воздействие высокой температуры на детали, поэтому очень важно придавать значение температуре плавления металлов, учитывая её в процессе работы, так как данные показатели играют немаловажную роль в параметрах тока. В горелке, при сгорании газа в момент действия электрической дуги, создается тепловая мощь для того, чтобы подвергнуть разрушению кристаллическую решетку металла. Характеристикам плавления металлов уделяют внимание при подборе материала для сооружения узлов, подвергающихся силе трения или же конструкций из металла, которые испытывают воздействие температур.
Что такое температура плавления?
Чтобы узнать при какой температуре плавится металл, в лабораторных условиях, точку старта в начале процесса плавления вычисляют до сотой градусной доли. При этом данный показатель не находится в зависимости от усилия при давлении на деталь.
При создании определенного давления в условиях вакуума, заготовки из металла имеют одинаковую температуру плавления. Данное явление можно объяснить накоплением энергии внутри вещества, при которой разрушаются связи между молекулами.
Разница между температурой плавления и кипения
Температурой плавления металлов называют точку перехода твердокристаллического вещества в жидкое состояние. В составе расплава у молекул нет собственного места расположения, они удерживаются за счет силы притяжения, поэтому в разжиженном состоянии сохраняется объем, но теряется форма.
В процессе кипения происходит потеря молекулярного объема, а молекулы вяло взаимодействуют друг с другом, двигаясь хаотично в разных направлениях, отставая от поверхности. Температурой кипения называется процесс, при котором уровень давления металлического пара уравновешивается с давлением внешней среды.

Кристаллические решетки металла
Под воздействием высокой температуры на металлическую деталь, возникают изменения в ее кристаллической решетке на молекулярном уровне. Это увеличивает скорость движения молекул. При критической температуре происходит распад молекулярной структуры металла, потому что межмолекулярные связи не в состоянии производить удержание в узловой структуре решетки. И вместо колеблющихся движений в узле возникают хаотичные, разнонаправленные движения, образуя ванну расплава в точках плавления.
Температура плавления различных металлов
Согласно знаниям из раздела физики, процесс превращения твердого вещества в жидкое имеется лишь у тел с кристаллической решеткой. Температура плавления металлов и сплавов возникает в различном диапазоне значений. Но, с точностью высчитать пограничную температуру фазовых состояний у сплавов весьма проблематично. У чистых элементов имеет значимость каждый градус, если это составы с легкой плавкостью.
Железо
Температура плавления железных составов должна быть высокой. Если элемент обладает технической чистотой, то он плавится при температуре 1 539 °C. В составе его вещества присутствуют включения серы, поэтому для её извлечения необходимо жидкое состояние. Также очищенное железо получается в процессе электролиза солей металла.
Чугун
Чугун считается самым лучшим материалом для плавления. Он имеет хорошие показатели жидкой текучести и усадки, поэтому его эффективно использовать в процессе литья. Ниже будут приведены показатели температурного кипения чугуна:
Серая разновидность чугуна, у которой температурный режим доходит до отметки 1 260 °C. А при разливе его в формы, увеличивается до 1 400 °C.
Белая разновидность чугуна, у которого температура поднимается до 1 350 °C.
Одним из немаловажных моментов является то, что температура, которой обладает чугун, на 400 единиц меньше той же стали. Поэтому процесс обработки данного материала менее энергозатратен.
Сталь, температура плавления
Средняя температура плавления стали составляет 1400 °C.
Сталью называется железосодержащий сплав с включением углерода. Её основной характеристикой является прочность. Это достигается за счет того, что она долгое время сохраняет параметры объема и формы. При этом расположение молекул в веществе находится в сбалансированном состоянии. Именно поэтому достигается равновесие между силой притяжения и силой отталкивания.
Диапазон плавления стали выше, чем у чугуна, поэтому она более энергозатратна.
Нержавеющая сталь
Температура плавления нержавеющей стали колеблется в среднем диапазоне между чугуном и сталью. Нержавеющей сталью называется вещество из легированной стали, обладающее антикоррозийными свойствами за счет содержания хрома в своем составе от 11% процентов и больше.
Показатели температуры плавления нержавейки составляют от 1 300 до 15 000 °C.
Алюминий и медь
Температура плавления алюминия составляет 6 600 °C, поэтому он зарекомендовал себя в качестве одного из среднеплавких металлов. Плавление чистых медных составов происходит при температуре 10 830 °C, а сплавов – 930 — 11 400 °C.
Серебро и золото
Серебро в чистом виде плавится при температуре 9 620 °C. При этом при температуре плавления серебра, оно может сравниться с температурой плавления в градусах со сплавами из меди.
Золото плавится при температуре в 10 640 °C.
Ртуть
Ртуть обладает самой низкой температурой плавления с отрицательным значением. Она составляет — 38,80 °C.
Какой металл обладает самой высокой температурой плавления?
У вольфрама самая высокая температура плавления, которая составляет 34 220 °C. Он относится к самым тугоплавким металлам. Очень тяжел, с виду серых оттенков, имеет характерный блеск и практически не поддается стандартной обработке. В помещениях с комнатной температурой быстро ломается и крошится. И ломается из-за того, что содержит включения кислорода и углерода.
| Легкоплавкие металлы | |
| Литий | + 180 °C |
| Калий | + 63,60 °C |
| Индий | + 156,60 °C |
| Олово | + 2 320 °C |
| Таллий | + 3 040 °C |
| Кадмий | + 3 210 °C |
| Свинец | + 3 270 °C |
| Цинк | + 4 200 °C |
| Среднеплавкие металлы | |
| Магний | + 6 500 °C |
| Алюминий | + 6 600 °C |
| Барий | + 7 270 °C |
| Серебро | + 9 600 °C |
| Золото | +10 630 °C |
| Марганец | + 12 460 °C |
| Медь | + 10 830 °C |
| Никель | + 14 550 °C |
| Кобальт | + 14 950 °C |
| Железо | + 15 390 °C |
| Дюралей | + 6 500 °C |
| Латунь | + 950 – 10 500 °C |
| Чугун | + 1 100 – 13 000 °C |
| Тугоплавкие металлы | |
| Титан | + 16 800 °C |
| Платина | + 17 690 °C |
| Хром | + 19 070 °C |
| Цирконий | + 18 550 °C |
| Ванадий | + 19 100 °C |
| Иридий | + 24 470 °C |
| Молибден | + 26 230 °C |
| Тантал | + 30 170 °C |
| Вольфрам | + 34 200 °C |
От чего зависит температура плавления?
У различных материалов различается, и температура их плавления, при которой происходит коренное перестраивание решетки до состояния жидкости. Металлические изделия и изделия из сплавов имеют следующие особенности:
- У различных материалов различается, и температура их плавления, при которой происходит коренное перестраивание решетки до состояния жидкости. Металлические изделия и изделия из сплавов имеют следующие особенности:
- Они редко встречаются в натуральном виде, т.е. без примесей. Именно состав определяет, какой должна быть температура плавки. В пример можно взять олово, в которое добавляют включения серебра. Благодаря примесям материал начинает становится устойчивым к воздействию температуры.
- Существуют такие сплавы, которые из-за химического состава трансформируются в жидкое состояние, когда столбик термометра поднимается чуть выше отметки в + 1 500 °C. Есть и такие сплавы, которые «держатся», если их нагревать до 30 000 °C.
- Стоит учитывать тот факт, что одним из наиболее важных свойств веществ является их точка плавления. В качестве примера можно привести авиационную технику.
Процесс плавления
Плавление любого металла осуществляется по одинаковой схеме с помощью нагрева внешнего или внутреннего типа. В первом варианте материал подвергается плавке в специальной печи, во втором применяется резистивная методика нагрева. При данной методике через вещество пропускается ток, либо он может быть индукционным нагревом в электромагнитном поле высокой частоты. В обоих случаях достигается одинаковый результат.
Типы сплавов металлов
Типы металлических сплавов различаются на основе температуры плавления, поэтому выделяют следующие варианты сплава:
- Легкоплавкий (олово, цинк, свинец, висмут) с температурой плавления не больше 600 °C.
- Среднеплавкий (алюминий, магний, никель, железо) с температурой 600 — 1 600 °C.
- Тугоплавкий (молибден, вольфрам, титан) с температурой более 1 600 °C.
Далее расскажем немного о разновидностях сталей, о сплаве вуда и припоях.
Особенности углеродистой стали
В данном материале содержится примесь углерода, примерно 2,13 %. При этом он лишен легирующих добавок, но есть примеси кремния, марганца и магния.
Особенности легированной стали
Помимо содержания углерода и железа в неё добавляют дополнительные элементы, улучшающие её свойства.
Особенности нержавейки
Нержавеющая сталь отлична от углеродистой из-за содержания элемента хрома в своем составе, благодаря свойствам которого она не подвержена окислению, а, следовательно, покрытию ржавчиной.
Особенности инструментальной стали
Также обладает углеродистым составом (0,8 – 0,9 %). Демонстрирует твердость, прочность, хорошо поддаются обработке. Используется в изготовлении инструментов, например, медицинских.
Сплав Вуда
Представляет собой материал, применяемый при паянии деталей для радиоприемников, а также в гальванической пластике, при работе в лабораторных условиях с ядохимикатами.
Сплавы для пайки
Другое их название – припои. Материалы для припоев бывают различными. Все зависит от того, что входит в состав материалов, которые необходимо соединить. К примеру, алюминий требует один сплав припоя, а вот медь уже совершенно другой.
Температура плавления неметаллов
У неметаллов также существует свой диапазон плавления, который колеблется от температуры в 38 000°C, которой обладает графит до температуры в — 2 100 °C у азота. Это потому, что неметаллы способны к образованию кристаллических решеток двух вариантов: молекулярной (у кислорода, азота, фосфора и т.д.) и атомной (графит, алмаз, бор, кремний и т.д.).
Надеемся, что статья была полезной, если остались вопросы — задавайте в комментарии!
Читайте также:
