Почему металлы не вытесняют водород из азотной кислоты
Обновлено: 15.05.2024
Азотная кислота реагирует практически со всеми металлами, кроме золота, но при этом образуются другие продукты реакции.
Контрольные задания III
Выписать из раздела II формулы приведенных в таблице 1 кислот, составить следующую таблицу и заполнить ее согласно примеру.
| Формула кислоты | Название | Тип кислоты | Основность | Тип элек-тролита | Соответству-ющий оксид |
| HCl | соляная | бескислородная | одноосновная | сильный | - |
| угольная | кислородосодержащая | двухосновная | слабый | ||
| …… | ……. | ………………… | …………….. | …………. | ……. |
С какими из приведенных веществ будет реагировать данная кислота? Написать уравнения реакций
49. При взаимодействии соляной кислоты с карбонатом натрия выделилось 5,6 л углекислого газа (нормальные условия). Сколько граммов соли при этом образовалось?
50. Сколько граммов серного ангидрида потребуется для получения 4,9 г серной кислоты?
51. Сколько литров сероводорода (нормальные условия) выделится при действии серной кислоты на 43,5 г сульфида цинка?
52. При взаимодействии цинка с соляной кислотой выделилось 5,6 л газа (нормальные условия). Сколько граммов соли при этом образовалось?
53. Сколько литров газообразного хлора (нормальные условия) необходимо для получения раствора соляной кислоты, содержащего 146 г ?
54. Какое количество нитрата меди (II) образуется при взаимодействии 20 г оксида меди (II) с азотной кислотой? Какое количество азотной кислоты будет израсходовано?
55. Какую массу магния надо растворить в соляной кислоте, чтобы образовалось 47,5 г хлорида магния? Сколько литров водорода (нормальные условия) при этом выделится?
56. Определить массу сульфата железа (II), полученного при растворении в серной кислоте 11,2 г железа, и объем полученного выделившегося водорода (нормальные условия)?
57. Сколько граммов соляной кислоты потребуется для превращения 40 г оксида меди(II) в хлорид меди (II)? Какая масса соли при этом образуется?
58. Сколько граммов воды выделится при нейтрализации 10 г гидроксида натрия серной кислотой? Сколько молей соли при этом образуется?
59. Сколько литров оксида углерода(IV) (нормальные условия) выделится при действии соляной кислоты на 25 г карбоната кальция?
60. Сколько граммов цинка необходимо взять, чтобы при растворении его в соляной кислоте выделилось 5,6 л водорода (нормальные условия)? Сколько граммов соли при этом образуется?
61. Сколько литров водорода (нормальные условия) выделится при растворении 9 г алюминия в серной кислоте? Сколько граммов соли при этом образуется?
62. Сколько граммов нитрата меди(II) образуется при взаимодействии 24,5 г гидроксида меди(II) с азотной кислотой? Сколько граммов азотной кислоты будет израсходовано?
63. Сколько граммов нитрата кальция получится при нейтрализации раствора, содержащего 31,5 г азотной кислоты, гидроксидом кальция?
64. При растворении алюминия в соляной кислоте выделилось 5,6 л водорода (нормальные условия). Сколько граммов хлорида алюминия при этом образовалось?
В данной работе рассматривается три типа солей – средние, кислые и основные.
Главной реакцией получения солей является реакция нейтрализации – взаимодействие кислоты с основанием. Любую соль можно рассматривать как продукт замещения ионов водорода в кислоте на катионы основания, или как продукт замещения гидроксо-ионов основания на анионы – кислотные остатки кислоты. При этом происходит соединение ионов водорода кислоты с гидроксо-ионами основания, т.е. эти ионы нейтрализуют друг друга – отсюда название “реакция нейтрализации”.
Если происходит полное замещение ионов по указанным схемам и при этом все ионы водорода кислоты соединяются со всеми гидроксо-ионами основания, то образуется средняя соль. Если водород в кислоте замещен не полностью, то образуется кислая соль, а если гидроксо-ионы в основании замещены не полностью, то образуется основная соль.
Рассмотрим в качестве примера реакцию между серной кислотой и гидроксидом кальция. Реакция может происходить по трем направлениям:
В этой реакции кислота взята в избытке, а основание – в недостатке. Получилась кислая соль.
В этой реакции наоборот, основание взято в избытке, а кислота – в недостатке. Получена основная соль.
В этой реакции кислоты и основания взято столько, чтобы все ионы водорода кислоты соединились со всеми гидроксо-ионами основания, и в результате образовалась средняя соль.
Таким образом, при реакции нейтрализации в зависимости от условий проведения процесса могут быть получены все три типа солей.
Представляется очевидным, что одноосновные кислоты не могут образовывать кислые соли, а однокислотные основания – основные соли.
Для того, чтобы из средней соли получить кислую, надо добавить к ней соответствующую кислоту
А чтобы получить основную – добавить основание
И наоборот, чтобы перевести кислую соль в среднюю, надо добавить основание, а чтобы перевести основную в среднюю – добавить кислоту
С точки зрения электролитической диссоциации все соли являются сильными электролитами.
Методы получения солей
1. Реакция нейтрализации
2. Взаимодействие метала с неметаллом
3. Взаимодействие метала с кислотой
4. Взаимодействие основного оксида с кислотным
5. Взаимодействие основного оксида с кислотой
6. Взаимодействие кислотного оксида с основанием
7. Взаимодействие аммиака с кислотами с образованием солей аммония
Химические свойства солей
1. Многие соли способны разлагаться при нагревании. Разложение солей различного состава происходит по-разному и является предметом рассмотрения в курсе неорганической химии.
Некоторые соли (карбонаты, сульфаты) разлагаются при нагревании на кислотный и основной оксиды
Соли щелочных металлов обычно устойчивы при нагревании.
Перечисленные ниже химические свойства солей являются одновременно методами получения одной соли из другой.
2. Взаимодействие металла с солью
Эти реакции протекают в том случае, если реагирующий металл стоит в ряду напряжений левее металла, входящего в состав соли. Иными словами, более активный металл вытеснят менее активный из соли.
Щелочные и щелочно-земельные металлы не вытесняют друг друга из солей.
Большинство реакций, отражающих химические свойства солей, приведенные в пунктах 1-5, происходят в растворах и протекают необратимо (или как принято говорить – “до конца”), если в результате процесса образуется: а) осадок, б) газ, в) слабый электролит. Если эти правила не выполняются, реакция до конца не идет. Например, реакция
существует только на бумаге.
При написании реакций в растворах следует указывать, почему эта реакция идет до конца.
3. Взаимодействие соли со щелочью
4. Взаимодействие соли с кислотой
Последняя реакция, на первый взгляд, противоречит правилу, указанному в химических свойствах кислот, а именно, что сильные кислоты вытесняют слабые из их солей. В приведенном примере, наоборот, слабая кислота вытесняет сильную ( ). Однако вторым продуктом реакции является нерастворимая соль, , выпадающая в осадок. Поэтому данная реакция идет до конца.
5. Взаимодействие в растворе двух солей между собой
Контрольные задания IV
Получите всеми возможными способами следующие соли (№№1-24)
1. Карбонат натрия
- Сульфат бария
- Нитрат калия
- Хлорид цинка
- Хлорид серебра
- Карбонат кальция
- Фосфат натрия
- Сульфат аммония
- Нитрат бария
- Сульфат железа(III)
- Сульфат ртути(II)
- Силикат калия
- Нитрит магния
- Сульфит натрия
- Нитрат меди(II)
- Хлорид аммония
- Фосфат кальция
- Бромид серебра
- Нитрат железа(III)
- Сульфид натрия
- Силикат натрия
- Сульфид меди(II)
- Хлорид натрия
- Сульфат железа(III).
Назвать все вещества в цепочках и осуществить указанные превращения (№№25-40)
Урок 24. Выделение водорода в реакциях кислот с металлами
В уроке 24 «Выделение водорода в реакциях кислот с металлами» из курса «Химия для чайников» познакомимся с рядом активности металлов, а также больше узнаем о кислотах в химических реакциях.

Характерное химическое свойство кислот — выделение из них водорода в реакциях с некоторыми металлами. Атомы металлов замещают атомы водорода в молекулах кислот, в результате чего водород выделяется в виде газа. В пробирку с хлороводородной кислотой опустим кусочек цинка. На поверхности металла образуются, а затем выделяются из раствора пузырьки газа. Соберем этот газ в пробирку и поднесем ее к пламени спиртовки (рис. 100). Мы услышим хлопок. Это свидетельствует о наличии в пробирке водорода.
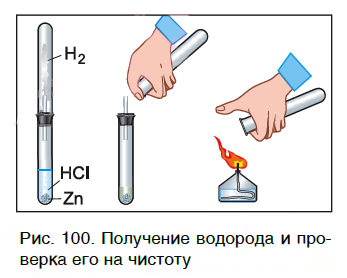
Каплю образовавшегося раствора поместим на стеклянную пластинку и подогреем ее в пламени спиртовки. После испарения воды на пластинке остается вещество белого цвета. Опытным путем можно установить, что состав этого вещества выражается формулой ZnCl2.
Теперь мы можем записать уравнение реакции цинка с кислотой:
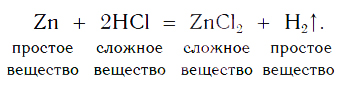
На рисунке 101 дана схема этой реакции. Из уравнения и поясняющей его схемы видим, что атомы цинка замещают атомы водорода в кислоте. В результате из простого вещества цинка и сложного вещества хлороводородной кислоты образуются два новых: сложное вещество ZnCl2 и простое вещество водород Н2.
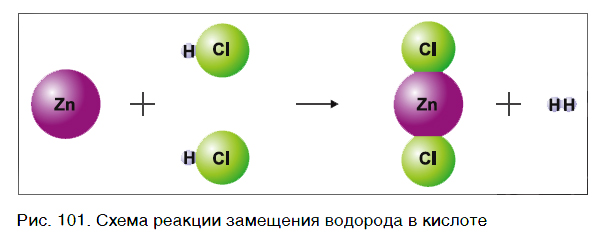
Так же протекают реакции алюминия, железа, других металлов и с раствором серной кислоты:
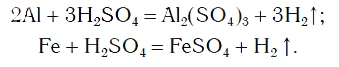
Эти химические реакции подтверждают, что кислоты являются сложными веществами, состоящими из атомов водорода,
способных замещаться на атомы металла, и кислотных остатков.
Вытеснительный ряд металлов
При проведении опыта вы убедились, что алюминий энергично вытесняет водород из раствора хлороводородной кислоты. С железом реакция вытеснения водорода протекает менее энергично, а с медью вовсе не идет.
По интенсивности вытеснения водорода из кислот металлы можно разместить в ряд:
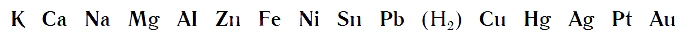
Его называют рядом активности или вытеснительным рядом металлов.
Чем левее расположен металл в вытеснительном ряду до водорода (Н2), тем активнее он вытесняет водород из кислот. Металлы, стоящие в ряду правее водорода, из кислот водород не вытесняют.
Зная расположение металлов в вытеснительном ряду, заранее можно предсказать:
- Будут ли реагировать металлы с кислотами с выделением водорода;
- Насколько активно будут протекать эти реакции.
Для получения водорода из кислот в лаборатории или школьном кабинете химии необходимо брать металлы, которые в вытеснительном ряду стоят до водорода. Но не каждый металл подходит для этих целей. Активные металлы натрий и калий реагируют с кислотами со взрывом, а реакции кислот с оловом и свинцом протекают медленно. Наиболее подходящими металлами для практического получения водорода являются цинк и алюминий. Как вы убедились, при проведении реакций этих металлов с раствором хлороводородной кислоты они протекают спокойно и достаточно быстро.
Краткие выводы урока:
- Кислоты — сложные вещества, состоящие из атомов водорода, способных замещаться на атомы металлов, и кислотных остатков.
- Металлы, стоящие в вытеснительном ряду до водорода, вытесняют его из кислот.
- В лаборатории водород получают в реакции металлов с кислотами.
Надеюсь урок 24 «Выделение водорода в реакциях кислот с металлами» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Почему металлы не вытесняют водород из азотной кислоты

пятница, 20 февраля 2015 г.
Взаимодействие металлов с кислотами
С разбавленными кислотами, которые проявляют окислительные свойства за счет ионов водорода (разбавленные серная, фосфорная, сернистая, все бескислородные и органические кислоты и др.)

реагируют металлы:
• расположенные в ряду напряжений до водорода (эти металлы способны вытеснять водород из кислоты);
• образующие с этими кислотами растворимые соли (на поверхности этих металлов не образуется защитная солевая
пленка).
В результате реакции образуются растворимые соли и выделяется водород:
2А1 + 6НСI = 2А1С13 + ЗН2↑
М g + Н2 SO 4 = М gS О4 + Н2↑
разб.
С u + Н2 SO 4 → X (так как С u стоит после Н2)
разб.
РЬ + Н2 SO 4 → X (так как РЬ SO 4 нерастворим в воде)
разб.
Некоторые кислоты являются окислителями за счет элемента, образующего кислотный остаток, К ним относятся концентрированная серная, а также азотная кислота любой концентрации. Такие кислоты называют кислотами-окислителями.

Окислительные свойства кислотных остатков и значительно сильнее, чем нона водорода Н, поэтому азотная и концентрированная серная кислоты взаимодействуют практически со всеми металлами, расположенными в ряду напряжений как до водорода, так и после него, кроме золота и платины. Так как окислителями в этих случаях являются ноны кислотных остатков (за счет атомов серы и азота в высших степенях окисления), а не ноны водорода Н, то при взаимодействии азотной, а концентрированной серной кислот с металлами не выделяется водород. Металл под действием данных кислот окисляется до характерной (устойчивой) степени окисления и образует соль, а продукт восстановления кислоты зависит от активности металла и степени разбавления кислоты

Разбавленная и концентрированная серные кислоты ведут себя по-разному. Разбавленная серная кислота ведет себя, как обычная кислота. Активные металлы, стоящие в ряду напряжений левее водорода
вытесняют водород из разбавленной серной кислоты. Мы видим пузырьки водорода при добавлении разбавленной серной кислоты в пробирку с цинком.
Медь стоит в ряду напряжений после водорода – поэтому разбавленная серная кислота не действует на медь. А в концентрированной серной кислоты, цинк и медь, ведут себя таким образом…
Цинк, как активный металл, может образовывать с концентрированной серной кислотой сернистый газ, элементарную серу, и даже сероводород.
Медь - менее активный металл. При взаимодействии с концентрированно серной кислотой восстанавливает ее до сернистого газа.
Следует иметь в виду, что на схемах указаны продукты, содержание которых максимально среди возможных продуктов восстановления кислот.
На основании приведенных схем составим уравнения конкретных реакций — взаимодействия меди и магния с концентрированной серной кислотой:
0 +6 +2 +4
С u + 2Н2 SO 4 = С uSO 4 + SO 2 + 2Н2 O
конц.
0 +6 +2 -2
4М g + 5Н2 SO 4 = 4М gSO 4 + Н2 S + 4Н2 O
конц.
Некоторые металлы ( Fe . АI, С r ) не взаимодействуют с концентрированной серной и азотной кислотами при обычной температуре, так как происходит пассивации металла. Это явление связано с образованием на поверхности металла тонкой, но очень плотной оксидной пленки, которая и защищает металл. По этой причине азотную и концентрированную серную кислоты транспортируют в железных емкостях.
Если металл проявляет переменные степени окисления, то с кислотами, являющимися окислителями за счет ионов Н + , он образует соли, в которых его степень окисления ниже устойчивой, а с кислотами-окислителями — соли, в которых его степень окисления более устойчива:
0 +2
F е+Н2 SO 4 = F е SO 4 +Н2
0 разб. + 3
F е+Н2 SO 4 = F е2( SO4 )3 + 3 SO2 + 6Н2 O
конц
Азотная кислота
Азотная кислота HNO3 – это сильная одноосновная кислота-гидроксид. При обычных условиях бесцветная, дымящая на воздухе жидкость, температура плавления −41,59 °C, кипения +82,6 °C ( при нормальном атмосферном давлении). Азотная кислота смешивается с водой во всех соотношениях. На свету частично разлагается.
Валентность азота в азотной кислоте равна IV, так как валентность V у азота отсутствует. При этом степень окисления атома азота равна +5. Так происходит потому, что атом азота образует 3 обменные связи и одну донорно-акцепторную, является донором электронной пары.
Поэтому строение молекулы азотной кислоты можно описать резонансными структурами:


Обозначим дополнительные связи между азотом и кислородом пунктиром. Этот пунктир по сути обозначает делокализованные электроны. Получается формула:

Способы получения
В лаборатории азотную кислоту можно получить разными способами:
1. Азотная кислота образуется при действии концентрированной серной кислоты на твердые нитраты металлов. При этом менее летучая серная кислота вытесняет более летучую азотную.
Например , концентрированная серная кислота вытесняет азотную из кристаллического нитрата калия:
2. В промышленности азотную кислоту получают из аммиака . Процесс осуществляется постадийно.
1 стадия. Каталитическое окисление аммиака.
2 стадия. Окисление оксида азота (II) до оксида азота (IV) кислородом воздуха.
3 стадия. Поглощение оксида азота (IV) водой в присутствии избытка кислорода.
Химические свойства
Азотная кислота – это сильная кислота . За счет азота со степенью окисления +5 азотная кислота проявляет сильные окислительные свойства .
1. Азотная кислота практически полностью диссоциирует в водном растворе.
2. Азотная кислота реагирует с основными оксидами, основаниями, амфотерными оксидами и амфотерными гидроксидами.
Например , азотная кислота взаимодействует с оксидом меди (II):
Еще пример : азотная кислота реагирует с гидроксидом натрия:
3. Азотная кислота вытесняет более слабые кислоты из их солей (карбонатов, сульфидов, сульфитов).
Например , азотная кислота взаимодействует с карбонатом натрия:
4. Азотная кислота частично разлагается при кипении или под действием света:
5. Азотная кислота активно взаимодействует с металлами. При этом никогда не выделяется водород! При взаимодействии азотной кислоты с металлами окислителем всегда выступает азот +5. Азот в степени окисления +5 может восстанавливаться до степеней окисления -3, 0, +1, +2 или +4 в зависимости от концентрации кислоты и активности металла.
металл + HNO3 → нитрат металла + вода + газ (или соль аммония)
С алюминием, хромом и железом на холоду концентрированная HNO3 не реагирует – кислота «пассивирует» металлы, т.к. на их поверхности образуется пленка оксидов, непроницаемая для концентрированной азотной кислоты. При нагревании реакция идет. При этом азот восстанавливается до степени окисления +4:
Золото и платина не реагируют с азотной кислотой, но растворяются в «царской водке» – смеси концентрированных азотной и соляной кислот в соотношении 1 : 3 (по объему):
HNO3 + 3HCl + Au → AuCl3 + NO + 2H2O
Концентрированная азотная кислота взаимодействует с неактивными металлами и металлами средней активности (в ряду электрохимической активности после алюминия). При этом образуется оксид азота (IV), азот восстанавливается минимально:
С активными металлами (щелочными и щелочноземельными) концентрированная азотная кислота реагирует с образованием оксида азота (I):
Разбавленная азотная кислота взаимодействует с неактивными металлами и металлами средней активности (в ряду электрохимической активности после алюминия). При этом образуется оксид азота (II).
С активными металлами (щелочными и щелочноземельными), а также оловом и железом разбавленная азотная кислота реагирует с образованием молекулярного азота:
При взаимодействии кальция и магния с азотной кислотой любой концентрации (кроме очень разбавленной) образуется оксид азота (I):
Очень разбавленная азотная кислота реагирует с металлами с образованием нитрата аммония:
Таблица . Взаимодействие азотной кислоты с металлами.
| Азотная кислота | ||||
| Концентрированная | Разбавленная | |||
| с Fe, Al, Cr | с неактивными металлами и металлами средней активности (после Al) | с щелочными и щелочноземельными металлами | с неактивными металлами и металлами средней активности (после Al) | с металлами до Al в ряду активности, Sn, Fe |
| пассивация при низкой Т | образуется NO2 | образуется N2O | образуется NO | образуется N2 |
6. Азотная кислота окисляет и неметаллы (кроме кислорода, водорода, хлора, фтора и некоторых других). При взаимодействии с неметаллами HNO3 обычно восстанавливается до NO или NO2, неметаллы окисляются до соответствующих кислот, либо оксидов (если кислота неустойчива).
Например , азотная кислота окисляет серу, фосфор, углерод, йод:
Безводная азотная кислота – сильный окислитель. Поэтому она легко взаимодействует с красным и белым фосфором . Реакция с белым фосфором протекает очень бурно. Иногда она сопровождается взрывом.
Видеоопыт взаимодействия фосфора с безводной азотной кислотой можно посмотреть здесь.
Видеоопыт взаимодействия угля с безводной азотной кислотой можно посмотреть здесь.
7. Концентрированная а зотная кислота окисляет сложные вещества (в которых есть элементы в отрицательной, либо промежуточной степени окисления): сульфиды металлов, сероводород, фосфиды, йодиды, соединения железа (II) и др. При этом азот восстанавливается до NO2, неметаллы окисляются до соответствующих кислот (или оксидов), а металлы окисляются до устойчивых степеней окисления.
Например , азотная кислота окисляет оксид серы (IV):
Еще пример : азотная кислота окисляет иодоводород:
Сера в степени окисления -2 окисляется без нагревания до простого вещества, при нагревании до серной кислоты.
Например , сероводород окисляется азотной кислотой без нагревания до молекулярной серы:
При нагревании до серной кислоты:
Соединения железа (II) азотная кислота окисляет до соединений железа (III):
8. Азотная кислота окрашивает белки в оранжево-желтый цвет («ксантопротеиновая реакция«).
Ксантопротеиновую реакцию проводят для обнаружения белков, содержащих в своем составе ароматические аминокислоты. К раствору белка прибавляем концентрированную азотную кислоту. Белок свертывается. При нагревании белок желтеет. При добавлении избытка аммиака окраска переходит в оранжевую.

Видеоопыт обнаружения белков с помощью азотной кислоты можно посмотреть здесь.
Кислоты. Химические свойства и способы получения

Перед изучением этого раздела рекомендую прочитать следующую статью:
Кислоты – сложные вещества, которые при взаимодействии с водой образуют в качестве катионов только ионы Н + (или Н3О + ).
По растворимости в воде кислоты можно поделить на растворимые и нерастворимые . Некоторые кислоты самопроизвольно разлагаются и в водном растворе практически не существуют (неустойчивые) . Подробно про классификацию кислот можно прочитать здесь.


Получение кислот
1. Взаимодействие кислотных оксидов с водой. При этом с водой реагируют при обычных условиях только те оксиды, которым соответствует кислородсодержащая растворимая кислота.
кислотный оксид + вода = кислота
Например , оксид серы (VI) реагирует с водой с образованием серной кислоты:
При этом оксид кремния (IV) с водой не реагирует:
2. Взаимодействие неметаллов с водородом. Таким образом получают только бескислородные кислоты.
Неметалл + водород = бескислородная кислота
Например , хлор реагирует с водородом:
H2 0 + Cl2 0 → 2 H + Cl —
3. Электролиз растворов солей. Как правило, для получения кислот электролизу подвергают растворы солей, образованных кислотным остатком кислородсодержащих кислот. Более подробно этот вопрос рассмотрен в статье Электролиз.
Например , электролиз раствора сульфата меди (II):
4. Кислоты образуются при взаимодействии других кислот с солями. При этом более сильная кислота вытесняет менее сильную.
Например: карбонат кальция CaCO3 (нерастворимая соль угольной кислоты) может реагировать с более сильной серной кислотой.
5. Кислоты можно получить окислением оксидов, других кислот и неметаллов в водном растворе кислородом или другими окислителями.
Например , концентрированная азотная кислота окисляет фосфор до фосфорной кислоты:
Химические свойства кислот
1. В водных растворах кислоты диссоциируют на катионы водорода Н + и анионы кислотных остатков. При этом сильные кислоты диссоциируют почти полностью, а слабые кислоты диссоциируют частично.
Например , соляная кислота диссоциирует почти полностью:
HCl → H + + Cl –
Если говорить точнее, происходит протолиз воды, и в растворе образуются ионы гидроксония:
HCl + H2O → H3O + + Cl –
Многоосновные кислоты диссоциируют cтупенчато.
Например , сернистая кислота диссоциирует в две ступени:
HSO3 – ↔ H + + SO3 2–
2. Кислоты изменяют окраску индикатора. Водный раствор кислот окрашивает лакмус в красный цвет, метилоранж в красный цвет. Фенолфталеин не изменяет окраску в присутствии кислот.
3. Кислоты реагируют с основаниями и основными оксидами .
С нерастворимыми основаниями и соответствующими им оксидами взаимодействуют только растворимые кислоты.
нерастворимое основание + растворимая кислота = соль + вода
основный оксид + растворимая кислота = соль + вода
Например , гидроксид меди (II) взаимодействует с растворимой бромоводородной кислотой:
При этом гидроксид меди (II) не взаимодействует с нерастворимой кремниевой кислотой.
С сильными основаниями (щелочами) и соответствующими им оксидами реагируют любые кислотами.

Щёлочи взаимодействуют с любыми кислотами — и сильными, и слабыми . При этом образуются средняя соль и вода. Эти реакции называются реакциями нейтрализации . Возможно и образование кислой соли, если кислота многоосновная, при определенном соотношении реагентов, либо в избытке кислоты. В избытке щёлочи образуется средняя соль и вода:
щёлочь(избыток)+ кислота = средняя соль + вода
щёлочь + многоосновная кислота(избыток) = кислая соль + вода
Например , гидроксид натрия при взаимодействии с трёхосновной фосфорной кислотой может образовывать 3 типа солей: дигидрофосфаты, фосфаты или гидрофосфаты.
При этом дигидрофосфаты образуются в избытке кислоты, либо при мольном соотношении (соотношении количеств веществ) реагентов 1:1.
При мольном соотношении количества щелочи и кислоты 1:2 образуются гидрофосфаты:
В избытке щелочи, либо при мольном соотношении количества щелочи и кислоты 3:1 образуется фосфат щелочного металла.

4. Растворимые кислоты взаимодействуют с амфотерными оксидами и гидроксидами.
Растворимая кислота + амфотерный оксид = соль + вода
Растворимая кислота + амфотерный гидроксид = соль + вода
Например , уксусная кислота взаимодействует с гидроксидом алюминия:

5. Некоторые кислоты являются сильными восстановителями. Восстановителями являются кислоты, образованные неметаллами в минимальной или промежуточной степени окисления, которые могут повысить свою степень окисления (йодоводород HI, сернистая кислота H2SO3 и др.).
Например , йодоводород можно окислить хлоридом меди (II):
4H I — + 2 Cu +2 Cl2 → 4HCl + 2 Cu + I + I2 0
6. Кислоты взаимодействуют с солями.
Кислоты реагируют с растворимыми солями только при условии, что в продуктах реакции присутствует газ, вода, осадок или другой слабый электролит . Такие реакции протекают по механизму ионного обмена.
Кислота1 + растворимая соль1 = соль2 + кислота2/оксид + вода

Например , соляная кислота взаимодействует с нитратом серебра в растворе:
Ag + NO3 — + H + Cl — → Ag + Cl — ↓ + H + NO3 —
Кислоты реагируют и с нерастворимыми солями. При этом более сильные кислоты вытесняют менее сильные кислоты из солей .
Например , карбонат кальция (соль угольной кислоты), реагирует с соляной кислотой (более сильной, чем угольная):
7. Кислоты взаимодействуют с кислыми и основными солями. При этом более сильные кислоты вытесняют менее сильные из кислых солей. Либо кислые соли реагируют с кислотами с образованием более кислых солей.
кислая соль1 + кислота1 = средняя соль2 + кислота2/оксид + вода
Например , гидрокарбонат калия реагирует с соляной кислотой с образованием хлорида калия, углекислого газа и воды:
KHCO3 + HCl → KCl + CO2 + H2O
Ещё пример : гидрофосфат калия взаимодействует с фосфорной кислотой с образованием дигидрофосфата калия:
При взаимодействии основных солей с кислотами образуются средние соли. Более сильные кислоты также вытесняют менее сильные из солей.
Например , гидроксокарбонат меди (II) растворяется в серной кислоте:
Основные соли могут взаимодействовать с собственными кислотами. При этом вытеснения кислоты из соли не происходит, а просто образуются более средние соли.
Например , гидроксохлорид алюминия взаимодействует с соляной кислотой:
Al (OH) Cl2 + HCl → AlCl3 + H2O
8. Кислоты взаимодействуют с металлами.
При этом протекает окислительно-восстановительная реакция. Однако минеральные кислоты и кислоты-окислители взаимодействуют по-разному.
К минеральным кислотам относятся соляная кислота HCl, разбавленная серная кислота H2SO4, фосфорная кислота H3PO4, плавиковая кислота HF, бромоводородная HBr и йодоводородная кислоты HI и др.
Такие кислоты взаимодействуют только с металлами, расположенными в ряду активности до водорода:

При взаимодействии минеральных кислот с металлами образуются соль и водород:
минеральная кислота + металл = соль + H2↑
Например , железо взаимодействует с соляной кислотой с образованием хлорида железа (II):
Fe + 2 H + Cl → Fe +2 Cl2 + H2 0
Кислоты-окислители (азотная кислота HNO3 любой концентрации и серная концентрированная кислота H2SO4(конц)) при взаимодействии с металлами водород не образуют, т.к. окислителем выступает не водород, а азот или сера. Продукты восстановления азотной или серной кислот бывают различными. Определять их лучше по специальным правилам. Эти правила подробно разобраны в статье Окислительно-восстановительные реакции . Я настоятельно рекомендую выучить их наизусть.
9. Некоторые кислоты разлагаются при нагревании.
Угольная H2CO3, сернистая H2SO3 и азотистая HNO2 кислоты разлагаются самопроизвольно, без нагревания:
Кремниевая H2SiO3, йодоводородная HI кислоты разлагаются при нагревании:
Читайте также:
