Полупроводник диэлектрик полупроводник металл
Обновлено: 17.05.2024
Зонная теория позволила с единой точки зрения истолковать существование металлов, диэлектриков и полупроводников, объясняя различие в их электрических свойствах, во-первых, неодинаковым заселением электронами разрешенных зон, и во-вторых, шириной запрещенных зон.
Рассматривая заполнение электронами разрешенных зон необходимо использовать два правила: 1) Электроны стремятся занять самые низкие энергетические уровни. 2) Принцип Паули: на одном энергетическом уровне не может быть более двух электронов. Эти электроны должны иметь разные спины.
Степень заполнения электронами энергетических уровней в зоне определяется заполнением соответствующего атомного уровня. Если уровень атома полностью заполнен, то и зона полностью заполнена. Из незанятых уровней образуются свободные зоны, из частично заполненных – частично заполненные зоны. В общем случае можно говорить о валентной зоне, которая полностью заполнена и образовалась из энергетических уровней внутренних электронов свободных атомов и о зоне проводимости (свободной зоне), которая либо частично заполнена, либо свободна и образована из энергетических уровней внешних коллективизированных электронов изолированных атомов (рис.2).
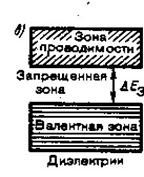 | Самая верхняя зона целиком занятая электронами (при Т=0 К) называется валентной. Зона, заполненная электронами частично (при Т = 0 К), называется зоной проводимости. Определим изменение энергии электрона, находящегося на некотором уровне в разрешенной зоне, под действием внешнего поля с напряженностью . Энергия приобретаемая электроном на длине свободного пробега , где - средняя длина свободного пробега электрона в кристалле равная примерно 10 -8 м в электрическом поле с напряженностью В/м, которая соответствует обычным источникам тока, эВ. |
| Рис.2. |
Это означает, что возможны только внутризонные переходы, так как междузонные переходы имеют много большую энергию. Необходимым условием электрической проводимости является наличие в разрешенной зоне свободных энергетических уровней на которые электрическое поле сторонних сил могло бы перевести электроны. В зависимости от степени заполнения зон электронами и ширины запрещенной зоны возможны три случая, изображенных на рис.3.
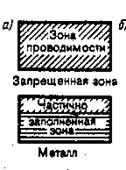   |
| (а) (б) (в) |
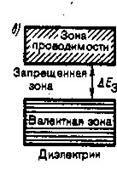
| Рис.3 |
3а). Зона проводимости заполнена лишь частично., то есть в ней имеются вакантные уровни. В этом случае электроны, получив сколь угодно малую энергетическую добавку (от поля или теплового движения) переходят на более высокий энергетический уровень той же зоны, то есть они участвуют в проводимости. Такой переход возможен, так как 1 К = 10 -4 эВ, что много больше расстояния между уровнями равному 10 -22 эВ. Таким образом, если в твердом теле имеется зона, лишь частично заполненная электронами, то это тело всегда будет проводником электрического тока. Именно это свойственно металлам.
3б). Возможно также такое перераспределение электронов между зонами, возникающими из уровней различных атомов, которое привело к тому, что вместо двух частично заполненных зон кристалла окажется одна целиком заполненная (валентная) зона и одна свободная зона (зона проводимости). Твердые тела, у которых энергетический спектр электронных состояний состоит только из валентной зоны и зоны проводимости, являются диэлектриками или полупроводниками в зависимости от ширины запрещенной зоны. Если ширина запрещенной зоны кристалла порядка нескольких электрон –вольт, то тепловое движение не может перебросить электроны из валентной зоны в зону проводимости и кристалл является диэлектриком, оставаясь им при всех реальных температурах.
3в). Если запрещенная зона достаточно узка ( эВ), то переход электронов из валентной зоны в зону проводимости может быть осуществлен сравнительно легко путем теплового возбуждения, либо за счет внешнего источника, способного передать электронам энергию , и кристалл является полупроводником.
Различие между металлами и диэлектриками с точки зрения зонной теории состоит в том, что при 0 К в зоне проводимости металлов имеются электроны, а в зоне проводимости диэлектриков они отсутствуют. Различие же между диэлектриками и полупроводниками определяется шириной запрещенных зон: для диэлектриков она довольно широка (например для NaCl =6 эВ), а для полупроводников достаточно узка (для германия =0,72 эВ). При температурах близких к 0 К полупроводники ведут себя как диэлектрики, то есть переброс электронов в зону проводимости не происходит.
Сущность зонной теории проводимости заключается в следующем:
1). При объединении атомов в кристалл твердого тела возникают энергетические зоны.
2). Ширина запрещенных зон и характер заполнения электронами разрешенных зон обуславливают электрические свойства твердого тела – оно может быть или металлом, или полупроводником, или диэлектриком.
Металлы, полупроводники и диэлектрики
В зависимости от ширины запрещенной зоны (Eg) все твердые тела подразделяются на металлы (Eg < 0,08 эВ), диэлектрики (Eg > 3 эВ), полупроводники (0,08 эВ < Eg < 3 эВ).
Металл – кристалл, в котором либо имеется зона проводимости, в которой не все энергетические уровни заняты электронами, либо зона проводимости и валентная зона перекрываются. Ширина запрещенной зоны равна нулю, или ее величина меньше тепловой энергии кристалла, которая составляет величину порядка 3kT, что при T=300К примерно равно 0,08 эВ. В металлах число свободных электронов сравнимо с числом атомов в том же объеме (~10 22 атом/см 3 ), при этом концентрация электронов не зависит от температуры. Электропроводность при T»300K велика. Металлами являются кристаллические вещества с металлическим типом химической связи.
Диэлектрик и полупроводник имеют ширину запрещенной зоны больше, чем энергия тепловых колебаний решетки. Если ширина запрещенной зоны не слишком велика, то существует вероятность перехода электронов из валентной зоны в зону проводимости за счет тепловых колебаний решетки, либо за счет поглощения кванта света. Условной границей подразделения кристаллов на полупроводники и диэлектрики является ширина запрещенной зоны, при которой возможен переход электрона из валентной зоны в зону проводимости при поглощении кванта видимого света. Энергия кванта, соответствующего коротковолновой границе видимой области света (l ~ 400 нм), составляет величину hn ~ 3 эВ.
В полупроводниковых кристаллических веществах химическая связь относится к ковалентному или смешанному ионно-ковалентному типу.
Диэлектрик – кристалл, имеющий ширину запрещенной зоны много больше, чем энергия тепловых колебаний (Е>>kT), концентрация свободных электронов равна нулю. Электропроводность незначительна, слабо зависит от температуры. Как правило, это молекулярные кристаллы и вещества с ионным или ион-ковалентным типом химической связи.
Пример 1. Металлический кристалл Li. Валентные электроны 2s 1 . 2s-атомные орбитали образуют зону, которая заполнена только наполовину.
Пример 2. Металлический кристалл Mg. Валентные электроны 3s 2 . Валентная зона магния заполнена электронами полностью, свободные уровни, которые могли бы обеспечить перемещение электронов в валентной зоне, отсутствуют. Ближайшая по энергии зона, зона проводимости, образованная свободными 3p атомными орбиталями, перекрывается с валентной зоной.
Пример 3. Кристалл Si. Валентные электроны 3s 2 3p 2 . Кремний – ковалентный кристалл, связи осуществляются электронами, располагающимися на sp 3 -гибридных орбиталях, которые образуют как валентную зону, так и зону проводимости. Каждый атом кремния имеет 4 sp 3 -гибридные орбитали, то есть в кристалле, состоящем из N атомов, имеется 8N энергетических состояний электронов. Нижняя по энергии половина из них при Т=0 К полностью заселена, образуя валентную зону, а верхняя свободна, образуя зону проводимости. В отличие от магния, в кристалле кремния валентная зона и зона проводимости не перекрываются. Ширина запрещенной зоны составляет величину Eg=1,12 эВ. Кристалл кремния – полупроводник.
Пример 4. Кристалл NaCl. Химическая связь в этом кристалле относится к ионному типу. Валентную зону образуют заполненные орбитали Cl - – 3s 2 3p 6 , а зону проводимости свободные орбитали Na + – 3s 0 . В кристалле хлорида натрия, так же как и в случае с кристаллом кремния, валентная зона и зона проводимости не перекрываются. Но ширина запрещенной зоны много больше, чем у кремния, Eg = 7,7 эВ, хлорид натрия – диэлектрик.
Кристаллические материалы
Наиболее близким к идеальному понятию кристалл является монокристаллический материал. Монокристалл (монос – один) – твердое вещество с непрерывной кристаллической решеткой во всем объеме физического тела. Линейные размеры монокристаллов могут составлять доли микрометра и доходить до ~1 м. Монокристаллы, в силу своего внутреннего строения, обладают анизотропными свойствами. Анизотропия (анизос – неравный, тропос – направление) – зависимость физических и физико-химических свойств тела от направления в кристалле. Если в рассматриваемом физическом теле имеется несколько различным образом ориентированных, связанных между собой сильными химическими связями монокристаллов, то данное тело представляет собою блочный монокристалл. Границы отдельных блоков (монокристаллов) – дефекты кристаллической структуры.
Гораздо более распространены в природе твердые тела, состоящие из большого числа произвольно ориентированных относительно друг друга мелких монокристаллов, сцепленных как сильными, так и слабыми химическими связями. Такие тела называются поликристаллами (полис – многочисленный). Поликристаллические тела, вследствие усреднения анизотропных свойств отдельных произвольно ориентированных монокристаллов, обладают изотропией физических и физико-химических свойств.
Дефекты кристаллической решетки.
Другим типом дефектов являются нарушения регулярности решетки, связанные с примесями, которые появились в кристалле случайно (химические примеси) или были введены в него преднамеренно (легирующие добавки). С дефектами связаны многие физические и химические свойства кристаллов (электропроводность, прочность, оптические свойства, коррозионная стойкость и др.).
Различают точечные дефекты, одномерные (дислокации) и двумерные (поверхности, границы кристаллических зерен), объемные (пузыри). Дефекты возникают как в процессе кристаллизации, так и в результате внешних воздействий на кристалл. Создание дефектов связано с разрывом имеющихся химических связей между атомами кристалла или образованием дополнительных связей.
Точечные дефекты.
Простейшими из точечных дефектов в полупроводниках являются электроны проводимости и дырки. Электронно-дырочная пара образуются в результате асимметричного разрыва химической связи между атомами кристалла при поглощении тепловой энергии. При этом один из атомов приобретает избыточный отрицательный заряд за счет дополнительного валентного электрона (электрон проводимости), а другой – избыточный положительный заряд (дырка). Оба дефекта могут перемещаться по кристаллу независимо друг от друга. Электрон проводимости перемещается путем эстафетной передачи избыточного электрона от атома к атому, а дырка – путем эстафетного захвата электрона от атома к атому.
В процессе образования электронно-дырочных пар большую роль играют примесные атомы, находящиеся в узлах кристаллической решетки. Атомы примеси, имеющие число валентных электронов большее, чем число связей с ближайшими соседями (электронно-избыточные примеси), являются источником электронов проводимости. Образующиеся при этом дырки локализованы на примесном атоме и не могут мигрировать по кристаллу. Атомы примеси, имеющие число валентных электронов меньше, чем число связей с ближайшими соседями (электронно-дефицитные примеси), являются источником дырок, а электрон будет локализован на атоме примеси.
Энергия, необходимая для образования электронно-дырочных пар, может быть сообщена кристаллу не только нагреванием, но и при поглощении электромагнитного излучения. Причем энергия кванта электромагнитного излучения должна быть больше, чем ширина запрещенной зоны (энергии ионизации химической связи).
Необходимо отметить, что в кристаллах диэлектриков электронно-дырочные пары не образуются при подводе тепловой энергии из-за большой величины ширины запрещенной зоны. Они могут быть образованы при поглощении электромагнитного излучения достаточной энергии или ионизирующего излучения.
В кристаллах могут быть дефекты, образованные без разрыва химической связи, напримерэкситоны(от лат. excito – возбуждаю) – квазичастицы, представляющие собою возбужденные состояния атомов кристаллической решетки. Возбуждения могут передаваться от атома к атому, мигрируя по кристаллу.
Точечные дефекты, связанные с нарушением регулярности расположения частиц в кристалле, могут быть собственными – разупорядочение решетки, и примесными – присутствие в кристалле посторонних атомов (рис. 4.14).
Рис. 4‑14 Точечные дефекты в решетке ионного кристалла: A + G – катионы в узлах решетки; B - G − анионы в узлах решетки; вакансии: Vc – катионные; Va – анионные; межузельные ионы: A + I – катион; B - I − анион; примесные ионы в узле решетки: катион (P + G) или анион (P - G); примесный атом или ион в межузельном положении (PI)
Собственные дефекты: вакансия – отсутствие в узле решетки частицы, образующей кристалл; межузельные атомы или ионы.
В ионных кристаллах отсутствие в узле решетки катиона или аниона (катионные и анионные вакансии) нарушает баланс электрических зарядов в кристалле. Поэтому в кристалле должно быть либо равное количество катионных и анионных вакансий (дефекты Шоттки), либо на каждую ионную вакансию необходимо равное количество межузельных частиц того же знака (дефекты Френкеля).
Собственные дефекты образуются в кристалле в результате теплового движения частиц при температурах выше 0 К. Для создания собственного дефекта частица должна перейти из узла решетки в междоузлие, для этого частице необходимо преодолеть потенциальный барьер, который называется энергией образования дефекта (Ед). Вероятность преодоления потенциального барьера и образования дефекта определяется количеством частиц, имеющих энергию большую, чем энергия Ед. Из молекулярно-кинетической теории известно, что доля таких частиц зависит от температуры и пропорциональна множителю . Таким образом, каждой температуре соответствует равновесная концентрация собственных дефектов (n), которая экспоненциально увеличивается с ростом температуры:
где А – предэкспоненциальный множитель, k – константа Больцмана; T – температура, К.
Точечные примесные дефекты связаны с присутствием в твердом веществе химических примесей. Примесный атом или ион может находиться в узле решетки или в межузельном положении. Где будет находиться примесная частица, как правило, зависит от соотношения ее размеров и размеров частиц, образующих решетку.
Точечные дефекты вызывают нарушение регулярного расположения частиц кристалла в их ближайшем окружении (искажение кристаллической решетки), тем самым увеличивая энергию кристаллической решетки (рис. 4.15).
Рис. 4‑15. Искажение кристаллической решетки точечными дефектами. Электронные возбуждения: электроны (e - ) A+ē®A - , дырки (p + ) A-ē®A + , экситоны (ex 0 ) A * . Собственные точечные дефекты: вакансии (V), межузельные атомы (I) Примесный точечный дефект: решеточный примесный атом (PG), межузельный примесный атом (PI)
Дефекты могут захватывать электрон или отдавать его (захватывать дырки), могут взаимодействовать друг с другом, образовывая более сложные структуры (ассоциаты). Например, в щелочно-галоидных кристаллах (А + В - ) анионная вакансия может захватить электрон Vaē (электрон располагается на орбиталях катионов, окружающих анионную вакансию), и образуется так называемый F-центр. Если межузельный анион отдает электрон (захватывает дырку), то образуется H-центр (В 0 ), который может с ближайшим решеточным анионом образовать молекулярный ион В2 - (Vк-центр).
Линейные дефекты кристаллической решетки – дислокации.
Дислокации – дефекты кристаллической решетки, представляющие собой линии, вдоль которых нарушено правильное чередование атомных плоскостей. Дислокации появляются в кристалле в результате пластической деформации или в процессе роста кристалла. Простейшими типами дислокаций являются краевые и винтовые дислокации (рис. 4.16).
Рис. 4‑16 Краевая (а) и винтовая (б) дислокации.
Кристаллическая решетка в непосредственной близости от дислокации находится в искаженном состоянии, поскольку в ней размещается дополнительное число атомов. Нормальный порядок расположения атомов восстанавливается в обоих направлениях от дислокации на расстоянии нескольких постоянных решетки.
Плотность дислокаций (концентрация дислокаций) в кристалле бывает очень велика, достигая 10 6 дислокаций на 1 см 2 .
Аморфные твердые тела
В аморфных твердых телах, в отличие от кристаллов, в которых существует пространственная периодичность в равновесных положениях атомов, атомы колеблются около хаотически расположенных точек. Основные отличия свойств аморфных веществ от кристаллических связаны именно с нерегулярностью расположения частиц. Хотя в аморфных веществах отсутствует дальний порядок, на расстояниях, сравнимых с длиной химических связей, пространственное расположение ближайших соседних частиц сохраняется, то есть имеется ближний порядок.
Такая разупорядоченность структуры является следствием недостаточной подвижности частиц при кристаллизации. Частицы при достаточно быстром охлаждении теряют подвижность и не успевают образовать кристаллическую решетку, то есть занять места в пространстве, отвечающие минимуму энергии. Таким образом, аморфное состояние вещества является нестабильным, обладающим избыточной энергией, и при определенных условиях может самопроизвольно переходить в кристаллическое состояние. В отличие от кристаллов, для которых существует фиксированная температура плавления, переход аморфного вещества из твердого состояния в жидкое происходит в некотором температурном интервале. Аморфные тела обладают изотропностью физико-химических свойств.
Аморфное вещество, которое образуется при охлаждении жидкости и переходе ее в твердое состояние без кристаллизации, называется стеклом.
В стеклообразное состояние переходят вещества с преимущественно ковалентным типом связи, например, некоторые оксиды (SiO2, P2O5, B2O3). Стеклами являются также и большинство органических полимеров.
Для описания строения стеклообразного состояния вещества существуют две основные модели.
Теория кристаллитов рассматривает стекло как совокупность мельчайших монокристаллических областей – кристаллитов.
Теория непрерывной неправильной сетки предполагает, что в стекле, как и в монокристалле, существует пространственная сетка из химически связанных атомов. Но, в отличие от монокристалла, отсутствует строгое периодическое повторение фрагментов сетки.
Пример. Диоксид кремния (SiO2) может существовать как в кристаллическом состоянии – кварц, так и в стеклообразном - кварцевое стекло (плавленый кварц). И в том и в другом состоянии структурной единицей является тетраэдр SiO2, в центре которого находится ион кремния, а в вершинах – ионы кислорода. Тетраэдры связаны между собой через ионы кислорода, которые одновременно принадлежат двум тетраэдрам. В кристаллическом состоянии структура периодически повторяется, а в стеклообразном состоянии она искажена и не повторяется в объеме (рис. 4.17).
Рис. 4‑17 Проекция структуры кристаллического и стеклообразного SiO2: ● - атом кремния, ○ - атом кислорода
К аморфным веществам относятся также и мелкодисперсные порошки, состоящие из частиц, размер которых составляет величину порядка 10÷100 длин химической связи (наночастицы), например сажа – мелкодисперсный углерод. Вещество в таком состоянии, в отличие от поликристаллов, не имеет фиксированной температуры плавления.
Полупроводник диэлектрик полупроводник металл
Одно из наиболее характерных свойств металлов — высокая электрическая проводимость, обусловленная направленным переносом их электронов в электрическом поле. С другом стороны, имеется большая группа твердых веществ с молекулярной, ионной или ковалентной решеткой, которые образуют класс диэлектриков. Их электрическая проводимость на 20—30 порядков ниже электрической проводимости металлов.
Известно большое число веществ, занимающих промежуточное положение между металлами и диэлектриками и относящихся к классу полупроводников. При очень низких температурах полупроводники не проводят электрический ток, т. е. являются типичными диэлектриками. Однако по мере роста температуры отмечается возрастание их электрической проводимости.
Любая теория твердого тела должна удовлетворительно объяснить наблюдающиеся огромные различия в электрической проводимости веществ, принадлежащих разным классам. К сожалению, ни теория ковалентной связи, рассматривающая электроны, принадлежащие лишь данной химической связи, как в ковалентных кристаллах, ни модель свободного электрона в металлах не в состоянии объяснить изменение электрической проводимости твердых тел больше чем на два порядка. С этой точки зрения применение в теории твердого тела квантово-механических представлений может быть весьма успешным.
Зонная теория кристаллов.
В модели свободного электрона волновое движение электрона может осуществляться по любому направлению и будет ограничиваться лишь размерами кристалла. Для простоты ограничимся одномерной задачей, рассматривая движение электрона лишь вдоль одной оси (одномерный
ящик). Решение уравнения Шредингера для такого свободного электрона дает следующее выражение для его энергии:
где — целое число; — постоянная Планка; — масса электрона; а — размеры кристалла в направлении характеристической оси (постоянная решетки).
Из формулы (III.4) видно, что с увеличением размеров кристалла разность энергий соседних уровней электрона будет уменьшаться. При большом числе энергетических уровней разность между ними будет настолько мала, что они образуют почти непрерывную зону энергий.
В процессе образования кристалла происходит перекрывание внешних электронных орбиталей атомов по аналогии с образованием химической связи в молекулах. В соответствии с методом при взаимодействии двух атомных орбиталей образуются две молекулярные орбитали: связывающая и разрыхляющая. При одновременном взаимодействии N микрочастиц образуется N молекулярных орбиталей. Величина N в кристаллах может достигать огромных значений (порядка 1023). Поэтому и число электронных орбиталей в твердом теле чрезвычайно велико. При этом разность между энергиями соседних орбиталей будет ничтожно мала. Так, в кристалле натрия разность энергетических уровней двух соседних орбиталей имеет порядок Дж. Таким образом, в кристалле металла образуется энергетическая зона с почти непрерывным распределением энергии, называемая зоной проводимости. Каждая орбиталь в этой зоне охватывает кристалл по всем его трем измерениям. Заполнение орбиталей зоны проводимости электронами происходит в соответствии с положениями квантовой механики. Так, из условий минимума энергии электроны будут последовательно заполнять все орбитали, начиная с наинизшей, причем на каждой орбитали в соответствии с запретом Паули может располагаться лишь два электрона с антипараллельными спинами. С повышением температуры за счет теплового возбуждения электроны будут последовательно перемещаться на более высокие энергетические уровни, передавая тепловую энергию с одного конца кристалла на другой и обеспечивая таким образом его теплопроводность.
Аналогично можно объяснить и действие приложенного к кристаллу электрического поля. Оно несколько изменяет относительные энергии орбиталей в зоне, понижая одни уровни и повышая другие (по отношению к силовым линиям поля). Это в свою очередь приводит к направленному переносу электронов на энергетически более выгодные орбитали, т. е. вызывает электронную проводимость кристалла.
С позиций квантовой механики орбиталь, занимаемая электроном, характеризует его полную энергию. Переходя с одного уровня на другой в зоне проводимости, электрон приобретает дополнительную энергию, за счет которой он ускоряется в силовом
поле. Какую же максимальную энергию способен приобрести электрон в твердом теле? Этот вопрос тесно связан с определением ширины энергетических зон в кристалле, т. е. разности энергий между самой высшей и самой низшей орбиталями в зоне.
Ширина энергетической зоны зависит от характера электронных орбиталей взаимодействующих атомов и -состояния), а также от глубины их перекрывания. Так, внутренние электронные орбитали атомов перекрываются довольно слабо. Поэтому образуемые ими зоны узки. Кроме того, такие зоны полностью или почти полностью заполнены электронами, так что их вклад в проводимость кристалла незначителен. Напротив, зоны, соответствующие валентным электронным состояниям, широки, хотя и в этом случае зоны, образованные d-орбнталямн, обычно значительно уже зон, сформированных р- и особенно -орбиталямн с тем же главным квантовым числом.
Количество взаимодействующих атомных орбиталей не влияет на ширину зоны, а определяет лишь плотность ее заполнения электронами. Ширина энергетических зон в твердых телах существенно зависит от внутренней структуры их кристаллов. Эта зависимость тесно связана с волновой природой движения электронов. Перемещаться по кристаллу способны лишь те электроны, длины волн которых не укладываются целое число раз между узлами кристаллической решетки. Электроны с длиной волны, равной где а — постоянная решетки, будут находиться в кристалле в условиях замкнутого отражения и не способны переносить энергию.
Таким образом, в кристаллах между энергетическими зонами, образованными взаимодействиями атомных орбиталей разного характера, могут возникать области запрещенных энергий, называемые запрещенными зонами. Теория, объясняющая свойства твердых тел на основании анализа строения и плотности заполнения электронами энергетических зон в их кристаллах, называется зонной теорией.
Металлы.
Рассмотрим в соответствии с положениями зонной теории энергетическую структуру металлов. На рис. II 1.5, а показано образование зон в кристалле натрия. Внутренние электронные орбитали атомов, в частности в кристалле натрия практически не перекрываются.
В зоне проводимости, образованной за счет взаимодействия З-орбиталей, N атомов натрия образуют такое же число энергетических уровней. Так как у каждого атома натрия имеется лишь по одному валентному электрону, при низких температурах в зоне проводимости будет заполнена только половина уровней. Большое число незанятых энергетических уровней в зоне приводит к высокой подвижности электронов и обеспечивает высокую электрическую проводимость металлического натрия. Аналогичное строение зоны проводимости имеют кристаллы и других элементов первой группы периодической системы элементов, причем ширина зоны проводимости максимальна у элементов побочной
Рис. III. 5. Возникновение энергетических зон кристалла из энергетических уровней атомов по мере их сближения: а натрий; б — алмаз
подгруппы: меди, серебра и золота, а у элементов главной подгруппы ширина зоны убывает с ростом их порядкового номера.
Итак, с точки зрения зонной теории металлические свойства проявляют те твердые тела, в кристаллах которых зона проводимости заполнена электронами лишь частично. При этом в переносе электричества будут участвовать не все электроны, находящиеся в зоне, а лишь те, для которых доступны незанятые орбитали с низкой энергией. Так, при нагревании металла тепловое возбуждение перемещает электроны с низкой энергией на более высокие энергетические уровни и тем самым ограничивает их возможность участвовать в переносе тока.
В кристаллическом натрии происходит перекрывание зон, образованных 3s- и 3р-орбиталями. Для металлов первой группы это перекрывание не играет существенной роли, так как число свободных орбиталей в -зоне у них велико. Однако такое перекрывание s- и р-зон, наблюдаемое и для металлов второй группы периодической системы элементов, играет важную роль. Атомы этих элементов имеют по два валентных -электрона, следовательно, все орбитали в -зоне их кристаллов будут полностью заполнены. Лишь глубокое перекрывание зон, образованных -орбиталями их атомов, сообщает металлические свойства кристаллам этих элементов. Образование зон проводимости в кристаллах d-элементов обычно сопровождается значительным перекрыванием -зон, причем последние значительно уже зон, образованных -орбиталями. Это значит, что перекрывание d-орбиталей в таких кристаллах невелико. Поэтому целый ряд свойств d-элементов можно трактовать на основании модели
локализованных d-электронов. Последние придают металлической связи в кристаллах d-элементов частично ковалентный характер. Так, малую химическую активность металлов, расположенных близко к концам периодов, качественно можно объяснить значительной ролью, которую играют в их кристаллах направленные ковалентные связи. Поэтому d-элементы иногда называют переходными металлами в отличие от типичных металлов главных подгрупп.
Электрическая проводимость кристаллов d-элементов обеспечивается главным образом электронами внешних -орбиталей. В связи с этим электрическая проводимость переходных металлов ниже, чем у типичных металлов. Исключением являются металлы подгрупп меди и цинка, у которых d-орбитали полностью заполнены электронами и не перекрываются с внешними -зонами.
Диэлектрики и полупроводники.
Рассмотрим применение зонной теории к кристаллам с ковалентными связями. При формировании подобных кристаллов наружные электронные орбитали их атомов, взаимодействуя, также образуют энергетические зоны. Однако направленный характер ковалентных связей приводит к тому, что симметрия кристалла полностью изменяет характер волновых функций электронов взаимодействующих атомов.
У атомов подавляющего большинства элементов, образующих ковалентные кристаллы (углерод, кремний, германий, серое олово), во внешнем квантовом слое имеются четыре орбитали: одна и три При образовании кристалла из N атомов эти орбитали расщепляются, образуя две энергетические зоны по орбиталей в каждой, как это показано на рис. III.5,б для кристалла алмаза.
Из условий минимума энергии все валентные электроны атомов углерода заполняют нижнюю зону, а так как их число составляет 4, то эта зона (ее называют валентной) оказывается заполненной полностью. Зона же проводимости кристалла пуста. Для перехода в эту зону электронам необходимо сообщить энергию порядка 7 эВ Требуемая энергия превышает энергию связи в кристалле алмаза и не может быть реализована. Поэтому подобные вещества не проводят электрический ток и являются диэлектриками.
Особенность собственных полупроводников состоит в том, что при переходе части электронов в зону проводимости в валентной зоне появляется эквивалентное им число так называемых дырок,
имеющих положительный заряд, которые также могут участвовать в переносе тока. Собственные полупроводники имеют электронно-дырочную проводимость.
Наряду с собственными большое распространение получили также полупроводники примесного типа. В них основное число переносчиков тока — электронов или дырок — поставляют введенные в собственный полупроводник специальные примеси, энергетические уровни которых располагаются между валентными зонами и зонами проводимости полупроводника. Так, при введении в кристалл германия так называемых донорных примесей, как, например, фосфора, мышьяка, сурьмы, электроны последних переходят в зону проводимости полупроводника, резко увеличивая в ней число электронов — переносчиков тока (п-про-водимость). При добавлении к германию акцепторных примесей типа бора, алюминия, индия электроны валентной зоны полупроводника переходят на свободные уровни зоны примесей, что увеличивает число дырок (р-проводимость) в валентной зоне.
При 0 К полупроводники представляют собой типичные диэлектрики, так как их зона проводимости пуста. При нагревании их проводимость растет, так как все большее число электронов перебрасывается в зону проводимости. Температурная зависимость электрической проводимости полупроводников обратна аналогичной зависимости для металлов.
Большая часть ионных кристаллов относится к классу диэлектриков. Изучение проводимости этих кристаллов позволило установить основные черты их зонной структуры. Особенность ионных кристаллов состоит в том, что они образованы при взаимодействии атомов разных элементов, внешние электронные орбитали которых имеют неодинаковую энергию. Так как зона образуется взаимодействием близких по энергии орбиталей, в ионных кристаллах всегда имеется две раздельные внешние зоны с большей и меньшей средней энергией.
Как и в ковалентных кристаллах, валентные электроны взаимодействующих атомов полностью заполняют зону с более низкой энергией (валентная зона). Зона же проводимости, образованная внешними орбиталями второго атома, пуста, и переброс в нее электронов требует затраты энергии. В кристалле например, все 3р-электроны атомов хлора и -электроны атомов натрия заполняют зону с более низкой энергией, образованную взаимодействием 3р-орбиталей атомов хлора. Зона же, соответствующая -орбиталям атомов натрия (зона проводимости), оказывается незаполненной, причем ширина запрещенной зоны достигает 7 эВ. Электронная проводимость большинства ионных кристаллов примерно на двадцать порядков ниже, чем у металлов. Известен ряд ионных кристаллов, ширина запрещенной зоны у которых не так велика и составляет порядка 2—3 эВ, как, например, у кристаллов Такие вещества при повышенных температурах проявляют полупроводниковые свойства.
Наконец, все твердые вещества типа молекулярных кристаллов
принадлежат к классу диэлектриков. Перекрывание электронных орбиталей взаимодействующих частиц в их кристаллах ничтожно мало. В связи с этим состояние электронов у частиц, занимающих узлы пространственных решеток в таких кристаллах, мало отличается от состояний в соответствующих свободных атомах и молекулах.
Особенности зонной структуры диэлектриков, полупроводников и металлов
Зонная теория - это квантовая механическая теория, которая рассматривает движение электронов в твердом теле.
Зонная теория твердого тела
Согласно теории, свободные электроны могут обладать любой энергией. Электроны в атомах твердого тела могут иметь только определенные дискретные значения энергии. Другими словами, спектр энергии электронов в атомах состоит из разрешенных и запрещенных энергетических зон.
Положения зонной теории
Итак, согласно постулатам Бора, электрон в отдельном атоме может находится на одной из нескольких энергетических орбиталей. Иначе говоря, иметь лишь определенные дискретные значения энергии. Когда атомы образуют молекулу, количество орбиталей расщепляется пропорционально числу атомов в молекуле.
При увеличении количества молекул до макроскопического тела количество орбиталей становится очень большим, а разница между соответствующими им энергиям - очень маленькой. Орбитали сливаются, образуя энергетические зоны.
Валентная зона - в диэлектриках и полупроводниках наивысшая энергетическая зона, которая заполнена полностью при температуре 0 К. Зона проводимости - следующая за валентной зона. В металлах зоной проводимости называется наивысшая разрешённая зона, в которой находятся электроны при температуре 0 К.
Зонная теория объясняет различие в электрических свойствах материалов: проводников, полупроводников, диэлектриков. Можно выделить следующие причины различий:
- Ширина запрещенных энергетических зон
- Разница в заполнении разрешенных энергетических зон электронами.
Зонная структура диэлектриков
Вещество является диэлектриком, когда валентная зона заполнена полностью, в высших зонах нет электронов, также отсутствует перекрытие зон. Такое вещество не проводит ток. Ширина между зонами у диэлектриков условно составляет более 2 электронвольт.
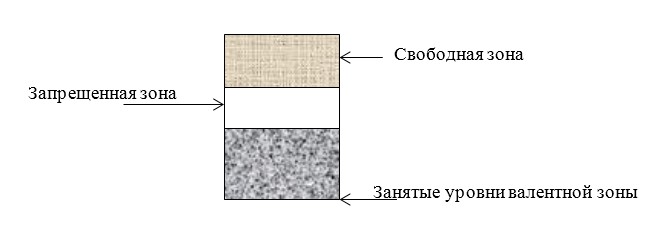
Зонная структура полупроводников
Вещество является полупроводником, если валентная зона разделена с соседними зонами узкой (менее 2 электронвольт) запрещающей зоной. Отметим, что такое вещество при температуре, близкой к абсолютному нулю, является диэлектриков. Однако при росте температуры электроны из верхней занятой зоны перескакивают в вакантную зону проводимости, и вещество становится электропроводным. Проводимость растет вместе с температурой и концентрацией электронов в зоне проводимости. Соответственно, в заполненной зоне, из которой электроны переходят в зону проводимости, растет концентрация дырок.
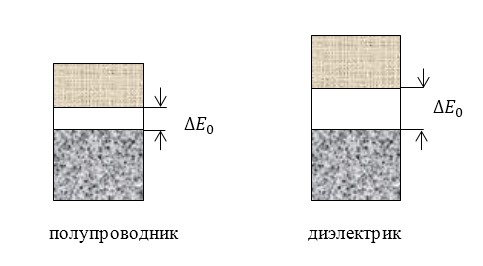
Разделение веществ на полупроводники и диэлектрики весьма условно. Вещества с шириной запрещённой зоны более 3—4 эВ и менее 4—5 эВ совмещают свойства диэлектриков и полупроводников.
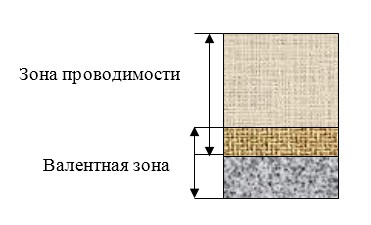
Зонная структура проводников (металлов)
В металлах валентная зона занята не полностью, и при воздействия на проводник разности потенциалов электроны могут свободно перемещаться из точек с меньшим потенциалом в точку с большим потенциалом.
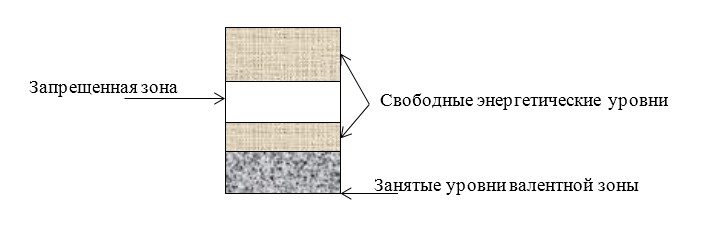
Также в проводниках зона проводимости пересекается с валентной зоной. Получившаяся зона пересечения заполнена не полностью.
Почему проводимость металлов не растет с увеличением валентности?
Валентность - это способность атома вещества образовать определенное число химических связей. Проще говоря, способность "прикрепить" к себе другой атом.
Однако электропроводность зависит не от количества валентных электронов на один атом, а от числа электронов в валентной зоне, для которых существуют свободные энергетические уровни. Так, у двухвалентных металлов число электронов, которые могут перейти под действием внешнего поля в свободное состояние меньше, чем у одновалентных. Таким образом, электропроводность двухвалентных металлов меньше, чем одновалентных.
Деление веществ на три класса: металлы, полупроводники, диэлектрики.
Металлы — группа элементов, обладающая характерными металлическими свойствами, такими как высокие тепло - и электропроводность, положительный температурный коэффициент сопротивления, высокая пластичность и металлический блеск.
Применение металлов
Конструкционные материалы
Металлы и их сплавы — одни из главных конструкционных материалов современной цивилизации. Это определяется прежде всего их высокой прочностью, однородностью и непроницаемостью для жидкостей и газов. Кроме того, меняя рецептуру сплавов, можно менять их свойства в очень широких пределах.
Электротехнические материалы
Металлы используются как в качестве хороших проводников электричества (медь, алюминий), так и в качестве материалов с повышенным сопротивлением для резисторов и электронагревательных элементов (нихром и т. п.).
Инструментальные материалы
Металлы и их сплавы широко применяются для изготовления инструментов (их рабочей части). В основном это инструментальные стали и твёрдые сплавы. В качестве инструментальных материалов применяются также алмаз, нитрид бора, керамика.
Полупроводник — материал, который по своей удельной проводимости занимает промежуточное место между проводниками и диэлектриками и отличается от проводников сильной зависимостью удельной проводимости от концентрации примесей, температуры и воздействия различных видов излучения. Основным свойством полупроводника является увеличение электрической проводимости с ростом температуры.
Полупроводниками являются вещества, ширина запрещённой зоны которых составляет порядка нескольких электрон-вольт (эВ). Например, алмаз можно отнести к широкозонным полупроводникам, а арсенид индия — к узкозонным. К числу полупроводников относятся многие химические элементы (германий, кремний, селен, теллур, мышьяк и другие), огромное количество сплавов и химических соединений (арсенид галлия и др.). Почти все неорганические вещества окружающего нас мира — полупроводники. Самым распространённым в природе полупроводником является кремний, составляющий почти 30 % земной коры.
В зависимости от того, отдаёт ли примесной атом электрон или захватывает его, примесные атомы называют донорными или акцепторными. Характер примеси может меняться в зависимости от того, какой атом кристаллической решётки она замещает, в какую кристаллографическую плоскость встраивается.
Проводимость полупроводников сильно зависит от температуры. Вблизи температуры абсолютного нуля полупроводники имеют свойства диэлектриков.
Полупроводники характеризуются как свойствами проводников, так и диэлектриков. В полупроводниковых кристаллах атомы устанавливают ковалентные связи (то есть, один электрон в кристалле кремния, как и алмаза, связан двумя атомами), электронам необходим уровень внутренней энергии для высвобождения из атома (1,76·10 −19 Дж против 11,2·10 −19 Дж, чем и характеризуется отличие между полупроводниками и диэлектриками). Эта энергия появляется в них при повышении температуры (например, при комнатной температуре уровень энергии теплового движения атомов равняется 0,4·10 −19 Дж), и отдельные атомы получают энергию для отрыва электрона от атома. С ростом температуры число свободных электронов и дырок увеличивается, поэтому в полупроводнике, не содержащем примесей, удельное сопротивление уменьшается. Условно принято считать полупроводниками элементы с энергией связи электронов меньшей чем 1,5—2 эВ. Электронно-дырочный механизм проводимости проявляется у собственных (то есть без примесей) полупроводников. Он называется собственной электрической проводимостью полупроводников.
По виду проводимости
Электронные полупроводники (n-типа)
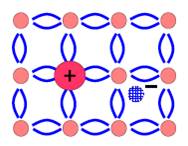
Термин «n-тип» происходит от слова «negative», обозначающего отрицательный заряд основных носителей. Этот вид полупроводников имеет примесную природу. В четырёхвалентный полупроводник (например, кремний) добавляют примесь пятивалентного полупроводника (например,мышьяка). В процессе взаимодействия каждый атом примеси вступает в ковалентную связь с атомами кремния. Однако для пятого электрона атома мышьяка нет места в насыщенных валентных связях, и он переходит на дальнюю электронную оболочку. Там для отрыва электрона от атома нужно меньшее количество энергии. Электрон отрывается и превращается в свободный. В данном случае перенос заряда осуществляется электроном, а не дыркой, то есть данный вид полупроводников проводит электрический ток подобно металлам. Примеси, которые добавляют в полупроводники, вследствие чего они превращаются в полупроводники n-типа, называются донорными.
Проводимость N-полупроводников приблизительно равна:
Дырочные полупроводники (р-типа)
Термин «p-тип» происходит от слова «positive», обозначающего положительный заряд основных носителей. Этот вид полупроводников, кроме примесной основы, характеризуется дырочной природой проводимости. В четырёхвалентный полупроводник (например, в кремний) добавляют небольшое количество атомов трехвалентного элемента (например, индия). Каждый атом примеси устанавливает ковалентную связь с тремя соседними атомами кремния. Для установки связи с четвёртым атомом кремния у атома индия нет валентного электрона, поэтому он захватывает валентный электрон из ковалентной связи между соседними атомами кремния и становится отрицательно заряженным ионом, вследствие чего образуется дырка. Примеси, которые добавляют в этом случае, называются акцепторными.
Диэлектрики – вещества, обладающие малой электропроводностью, т.к. у них очень мало свободных заряженных частиц – электронов и ионов. Эти частицы появляются в диэлектриках только при нагреве до высоких температур. Существуют диэлектрики газообразные (газы, воздух), жидкие (масла, жидкие органические вещества) и твердые (парафин, полиэтилен, слюда, керамика и т.п.).
При наложении электрического напряжения в диэлектрике, представляющем сложную электрическую систему, протекают разнообразные электрические процессы, связанные с его поляризацией, электрической проводимостью. В случае очень большого напряжения может произойти разрушение диэлектрика, называемое пробоем. Эти процессы определяют свойства диэлектриков, а, следовательно, надежность их работы в радиоустройствах.
Физическим параметром, который характеризует диэлектрик, является диэлектрическая проницаемость. Диэлектрическая проницаемость может иметь дисперсию.
Под дисперсией понимают частотную зависимость диэлектрической проницаемости. В широком диапазоне частот, обычно, наблюдается несколько областей дисперсии  , которые образуют диэлектрический спектр. Исследование дисперсии - один из важных физических методов изучения свойств диэлектриков, позволяющих получить данные о характерных частотах и диэлектрических вкладах разных механизмов поляризации.
Примеры
К диэлектрикам относятся воздух и другие газы, стёкла, различные смолы, пластмассы, многие виды резины.
Ряд диэлектриков проявляют интересные физические свойства. К ним относятся электреты, пьезоэлектрики, пироэлектрики, сегнетоэластики, сегнетоэлектрики, релаксоры исегнетомагнетики.
При применении диэлектриков — одного из наиболее обширных классов электротехнических материалов — довольно четко определилась необходимость использования как пассивных, так и активных свойств этих материалов.
Диэлектрики используются не только как изоляционные материалы.
Вопрос №13.
Конструкция, условное обозначение, параметры и область применения стабилитронов. Приведите примерымаркировки стабилитронов.
Стабилитроны работают только в цепях постоянного тока. При включении напряжения следует соблюдать полярность. Катод стабилитрона обозначается кружком. Для получения стабилизированного напряжения обязательно включать последовательно со стабилитроном ограничивающее сопротивление. Полезная нагрузка, на которой нужно получить стабильное напряжение, включается параллельно стабилитрону.
Для нормальной работы стабилитрона напряжение на нем в момент включения должно достигнуть величины так называемого напряжения зажигания.
При работе стабилитрона ток, проходящий через него, не должен выходить за пределы, указанные в справочнике, что является показателем правильного выбора режима стабилизации.
Необходимо помнить, что при отключении нагрузки ток, проходящий через стабилитрон, возрастает. Это иногда может вывести его из строя. Стабилитроны одного типа нельзя соединять параллельно с целью увеличения допустимых пределов изменения питающего напряжения, так как при этом невозможно обеспечить одновременность их зажигания и одинаковый режим работы.
Зажигание одного из двух параллельно соединенных стабилитронов делает невозможным зажигание второго, потому что при этом напряжение на нем становится равным номинальному рабочему напряжению зажегшегося стабилитрона, которое меньше напряжения зажигания.
Однотипные по току стабилитроны можно соединять последовательно для повышения стабилизируемого напряжения или образования делителя напряжений.
Некоторые стабилитроны в цоколе имеют перемычку, включая которую в цепь первичной, повышающей обмотки или в цепь высокого напряжения можно разорвать какую-либо из этих цепей при вынутом стабилитроне и, снимая этим с конденсатора фильтра выпрямленное напряжение, защитить конденсатор от возможного пробоя, т.к. при отсутствии стабилитрона напряжение на нем может достичь опасной величины.
Обозначения стабилитронов состоят из трех элементов: букв СГ (стабилитрон газовый), порядкового номера прибора и буквы, характеризующей конструкцию стабилитрона, С - стеклянный, П - пальчиковый.
Вопрос №30.
ПАРАМЕТРЫ ФОТОРЕЗИСТОРА
Если к неосвещенному ФР подключить источник питания, то в электрической цепи потечет небольшой ток, обусловленный наличием в полупроводнике малого количества свободных носителей заряда. Этот ток называют темновым током Iт.
Темновое сопротивление Rт — это сопротивление ФР при отсутствии освещения. Темновое сопротивление принято определять через 30 с после затемнения ФР.
Условное обозначение фоторезистора
Вопрос №35.
Вопрос № 45.
Вопрос № 59.
Литература
1. Иванов И. И., Соловьев Г. И., Фролов В. Я. Учебник.Электротехника и основы электроники: Учебник. 7-е изд., перераб. и доп. — СПб: Издательство «Лань», 2012. — 736 с.
2. Цыкни Г.С. Трансформаторы низкой частоты. М., Связьиздат, 1955.
3. Достанко А.П., Ланин В.П., Хмыль А.А., Ануфриев П.П. Под общей редакцией академика А. П. Достанко. Технология радиоэлектронных устройств и автоматизация производства. - Минск: Высшая школа 2002,
КОНТРОЛЬНАЯ РАБОТА
Гладченков Александр Сергеевич
Электрификация и автоматизация сельского хозяйства
Вопрос №4.
Деление веществ на три класса: металлы, полупроводники, диэлектрики.
Механическое удерживание земляных масс: Механическое удерживание земляных масс на склоне обеспечивают контрфорсными сооружениями различных конструкций.

Организация стока поверхностных вод: Наибольшее количество влаги на земном шаре испаряется с поверхности морей и океанов (88‰).


Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого.
© cyberpedia.su 2017-2020 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!
Читайте также:
