Проникновение одного металла в другой
Обновлено: 05.05.2024
Диффузия – это перенос вещества, обусловленный беспорядочным тепловым движением диффундирующих частиц. При диффузии газа его молекулы меняют направление движения при столкновении с другими молекулами Основными типами движения при диффузии в твердых телах являются случайные периодические скачки атомов из узла кристаллической решетки в соседний узел или вакансию.
Развитие процесса диффузии приводит к образованию диффузионного слоя, под которым понимают слой материала детали у поверхности насыщения, отличающийся от исходного по химическому составу, структуре и свойствам.
Диффузионное движение любого атома – это случайное блуждание из-за большой амплитуды колебаний, которое не зависит ни от движения других атомов, ни от предыдущего движения данного атома. Не зависящие от температуры колебания атомов вокруг положения равновесия обычно происходят с частотой ~10 13 с –1
Вопрос определения механизма диффузии является весьма сложным. Большую роль в решении этой проблемы сыграли работы Я.И. Френкеля, в которых показано огромное влияние дефектов кристаллической решетки, в особенности вакансий, на процесс диффузионного перемещения атомов. Наиболее затруднительным является простой обменный механизм диффузии, а наиболее вероятным – вакансионный. Каждому механизму диффузии соответствует определенная энергия активации Q, т. е. величина энергетического барьера, который необходимо преодолеть атому при переходе из одного положения в другое.
Перемещение при краудионном механизме диффузии подобно распространению волны: каждый атом смещается на малую величину, а возмущение распространяется быстро. Для диффузии большое значение имеют вакансии и их ассоциации (бивакансии, комплексы вакансия – атом примеси), а также дефекты, являющиеся их источниками (линейные и поверхностные).
Основным механизмом самодиффузии и диффузии в твердых растворах замещения является вакансионный. В твердых растворах внедрения основным механизмом перемещения примесных атомов небольшого размера является межузельный.
Если два хорошо соединенных между собой куска чистых металлов АиВ длительно отжигать, то будет наблюдаться взаимное проникновение металлов и смещение первоначальной границы раздела, отмеченной инертными метками (оксидными частицами или вольфрамовыми проволочками) на величину ?х, прямо пропорциональную квадратному корню из времени отжига. Если DА > DВ, то компонент А проникает в В с большей скоростью, чем В в А, вследствие этого часть В образца увеличивается в объеме.
Диффузионная металлизация – процесс диффузионного насыщения поверхности изделий металлами или металлоидами. Диффузионное насыщение проводят в порошкообразной смеси, газовой среде или расплавленном металле (если металл имеет низкую температуру плавления).
Борирование – диффузионное насыщение поверхности металлов и сплавов бором для повышения твердости, коррозионной стойкости, износостойкости проводят путем электролиза в расплавленной соли бора. Борирование обеспечивает особенно высокую твердость поверхности, сопротивление износу, повышает коррозионную стойкость и теплостойкость. Борированные стали обладают высокой коррозионной стойкостью в водных растворах соляной, серной и фосфорной кислот. Борирование применяют для чугунных и стальных деталей, работающих в условиях трения в агрессивной среде (в химическом машиностроении).
Хромирование – диффузионное насыщение хромом проводят в порошкообразных смесях хрома или феррохрома с добавками хромистого аммония (1 %) и окиси алюминия (49 %) при температуре 1000…1050 °C с выдержкой 6…12 ч. Хромирование применяют для деталей, которые работают на износ в пароводяных и агрессивных средах (арматура, вентили). При хромировании изделий из малоуглеродистых сталей твердость повышается и приобретается хорошая коррозионная стойкость.
Алитирование – это процесс диффузионного насыщения поверхностного слоя алюминием, проводят в порошкообразных смесях алюминия или в расплавленном алюминии. Цель – получение высокой жаростойкости поверхности стальных деталей. Алитирование проводят в твердых и жидких средах.
Силицирование – диффузионное насыщение кремнием проводят в газовой атмосфере. Насыщенный кремнием слой стальной детали имеет не очень высокую твердость, но высокую коррозионную стойкость и повышенную износостойкость в морской воде, азотной, соляной в серной кислотах. Силицированные детали применяют в химической, целлюлозно-бумажной и нефтяной промышленности. Для повышения жаростойкости силицирование применяют для изделий из сплавов на основе молибдена и вольфрама, обладающих высокой жаропрочностью.
В материаловедении разрабатываются макро– и микроскопические теории диффузии. В макроскопической теории делается акцент на формализме, т. е. на термодинамических силах и параметрах. В микроскопической теории используют механизмы, основанные на теории об атомных скачках.
Диффузия

Почему запахи летом распространяются быстро, а зимой — медленно? Почему вода способна изменить цвет? Можно ли соединить два твердых тела в одно? Мы получим ответы на все эти вопросы, изучив понятие «диффузия».
О чем эта статья:
Начнем с определения. Что такое диффузия?
Диффузия — это процесс взаимного проникновения молекул одного вещества между молекулами другого. При этом перенос вещества происходит из области с высокой концентрацией в область с низкой концентрацией.
Как и многие другие физические термины, это слово зародилось в языке древних римлян — латыни. Diffusio — распространение, растекание, рассеивание, взаимодействие.
«Но как это возможно? В каких веществах и телах происходит диффузия?» — спросите вы. Не беспокойтесь, сейчас во всем разберемся!
Строение вещества и агрегатные состояния
Наверняка вы слышали, что все вещества состоят из молекул. Золотой слиток, кактус на подоконнике и даже ваш любимый бургер 🍔 состоят из мельчайших частичек, которые являются носителями всех физических и химических свойств этого предмета или вещества.
В зависимости от агрегатного состояния, в газах, жидкостях и твердых телах меняются две вещи. Во-первых, расстояние между молекулами. Давайте вспомним (или догадаемся), каким должно быть расстояние между молекулами, чтобы предмет характеризовали слова «твердый», «крепкий», «держащий форму»? Правильно, расстояние должно быть очень маленьким, чтобы молекулы выстраивались в стройные рядочки и, держась друг за друга, не позволяли телу растечься и потерять форму.
А если нам все же нужна эта текучесть? Тогда расстояние между молекулами нужно немного увеличить, но так, чтобы силы взаимодействия еще держали молекулы рядом друг с другом и они не разлетались по всему объему сосуда. Представьте, как тяжело было бы пить сок, если бы его пришлось ловить по всей комнате!
С газами происходит именно такая история. Газы (кислород, водород, хлор и другие) также состоят из молекул, но расстояние между ними настолько большое, что они обладают свойствами, отличными от свойств жидкостей и твердых тел: газы занимают весь предоставленный объем, легко сжимаются, не имеют своей формы.
Кивните, если все понятно. Кивнули? Прекрасно, идем дальше.
В зависимости от того, в каком состоянии находится вещество, будет меняться и скорость движения молекул (скорость зависит также от температуры, но об этом позже). В твердых телах молекулы выстраиваются в так называемые кристаллические решетки, об этом мы говорили выше. Эта жесткая структура не позволяет молекулам летать где им вздумается и сталкиваться со своими братьями и сестрами. Все, что остается бедным молекулам, — вибрировать на своих местах и ждать тех времен, когда можно будет сменить агрегатное состояние на какое-нибудь другое.
Когда температура вещества поднимется и достигнет критического значения, тело начнет плавиться — становиться жидкостью. Молекулы при этом хоть и не обретают полную свободу, но начинают двигаться активнее. Они способны перепрыгивать со своих мест, сталкиваться с другими молекулами — вести активный образ жизни. И чем выше температура жидкости, тем быстрее двигаются молекулы.
А при переходе в газообразное состояние наступает полная свобода! Молекулы разрывают все связи друг с другом, двигаются очень быстро и хаотично, словно соревнуются по скорости полета, красоте кувырков и количеству столкновений.
В разрезе этой темы стоит упомянуть и броуновское движение. Похоже ли оно на диффузию?
Броуновское движение — беспорядочное движение микроскопических видимых взвешенных частиц твердого вещества в жидкости или газе, вызываемое тепловым движением частиц жидкости или газа.
Как мы видим, броуновское движение отвечает за хаотичное перемещение микрочастичек в жидкостях или газах, в то время как благодаря явлению диффузии вещества проникают друг в друга.
«Это все, конечно, увлекательно, — можете возразить вы, — но когда возникает диффузия?»
Она происходит прямо сейчас! 😱
Диффузия газов
Давайте проведем небольшой эксперимент — вам он точно понравится. Посадим родителей в зале и попросим проследить за окружающей обстановкой, понять, что изменилось. А сами уйдем в соседнюю комнату и начнем чистить апельсин. Как скоро родители почувствуют аромат цитрусов? Вероятно, очень скоро. Скорее, чем вам удастся съесть апельсин в одиночку.
А если вы забыли вынести мусор, хотя обещали? Неприятный запах выдаст вас достаточно скоро.
Каким образом происходит распространение запахов по воздуху? Правильный ответ — диффузия! Расстояния между молекулами в газах (а воздух — это газ) достаточно большие, поэтому между ними легко проскакивают другие частицы. Молекулы вещества маневрируют между частицами воздуха и перемешиваются в одну большую компанию.
Представьте футбольное поле с двумя командами. В начале игры каждая стоит на своей части, но как только звучит свисток арбитра, футболисты начинают матч, каждую секунду занимая новое положение. В конечном итоге мы увидим, как команды перемешались между собой. То же самое происходит и в процессе диффузии.
Интересно, что чем выше температура, тем быстрее этот процесс протекает. Именно поэтому запах свежеиспеченного хлеба можно почувствовать за несколько кварталов от булочной, а запах мороженого — нет.
Диффузия жидкостей
Если вы немного устали, можно сделать короткий перерыв и выпить горячего чая. А может, кофе или какао? Какой напиток вы предпочитаете? С молоком или без?
Важно ли это в свете изучаемой нами темы? Очень, ведь даже в таком обычном деле, как приготовление чая или кофе, можно наблюдать диффузию.
Записываем рецепт: берем стакан горячей воды, наливаем туда заварки, а потом молока. Добавляем сахар по вкусу. Но не спешите перемешивать! Обратите внимание, как жидкости сами перемешиваются между собой — и в итоге мы получаем ароматный бодрящий напиток.
Теперь вы можете объяснить это явление с помощью физики. Попробуем?
Дело в том, что молекулы заварки проникают в промежутки между молекулами воды и перемешиваются друг с другом до тех пор, пока мы не получим однородную смесь. Тот же процесс происходит и при добавлении молока, сиропов и других ингредиентов подобно тому, как этот процесс происходит в газах.
Единственное отличие — скорость протекания диффузии. В жидкостях расстояние между молекулами меньше, а значит, другим молекулам сложнее протиснуться — это занимает больше времени.
Диффузия жидкостей также зависит и от температуры. Именно поэтому есть смысл заваривать чай в горячей воде, а не в холодной или солить горячий суп.
Диффузия твердых тел
А как вы думаете, возможна ли диффузия твердых тел? Как быстро она будет протекать?
Да, диффузия возможна, и да, протекать она будет очень медленно. Чтобы молекулы одного твердого вещества проникли в другое всего на несколько миллиметров, понадобятся не дни и не месяцы, а годы! И причиной этому является очень маленькое расстояние между молекулами и их расположение в узлах кристаллической решетки.
Как ускорить этот процесс? Правильно, на помощь снова приходит температура. В огромных доменных печах слить несколько металлов в один можно достаточно быстро — для этого потребуется несколько часов.
Самые распространенные примеры диффузии твердых тел зачастую связаны именно с металлами. В обычной жизни мы используем большое количество предметов, в состав которых входят одновременно алюминий и железо, золото и серебро. Чтобы изготовить самокат без использования технологии сварки и наплавления, пришлось бы ждать десятки лет — и катались бы вы на нем уже со своими внуками. А развитие космической отрасли и компьютерных технологий с их чипами, микросхемами и платами вообще было бы невозможным.
Диффузия в окружающем мире
Затронем еще один вопрос: происходит ли диффузия в окружающем мире?
Думаем, вы уже знаете ответ: да, конечно! Можно сказать, что этот процесс происходит постоянно и является причиной многих явлений, о которых мы даже не задумывались. Давайте рассмотрим некоторые интересные примеры:
кровообращение: благодаря диффузии молекулы кислорода проникают в кровь, которая доставляет их ко всем органам;
питание: витамины и минералы, которые содержатся в пище, проникают в клетки организма;
растворение веществ в жидкости;
неоднородность воздуха (воздух — сложное вещество, которое состоит из кислорода, углекислого газа, азота и других газов);
К сожалению, диффузия отвечает не только за положительные явления. Она также является причиной загрязнения нашей планеты: воздуха, воды, почвы. Молекулы канцерогенных, ядовитых веществ попадают в атмосферу и гидросферу, вызывая необратимые изменения.
И последнее: для решения задач про диффузию формула не нужна! Достаточно материала, который мы обсудили в этой статье. Приятная новость, правда?
На уроках физики в онлайн-школе Skysmart вы познакомитесь и с другими интересными явлениями, которые не раз заставят вас удивиться, а может, даже вдохновят разобраться в устройстве нашего мира еще лучше. Ждем вас на наших уроках!
Коррозия металлов

Всякое явление или процесс вокруг нас связан с химией. Скажем, ржавление железа. Хоть раз в жизни вы наверняка задумывались, почему одни металлы ржавеют и разрушаются, а другие — нет. И что такого особенного в нержавеющей стали, что этот процесс ей нипочем? Обо всем это мы и поговорим в сегодняшней статье.
Коротко о главном
Коррозия металлов или ржавление в химии — это явление, которое возникает из-за взаимодействия металлической пластинки с веществами окружающей среды (кислородом воздуха или кислотами, с которыми может реагировать металлическое изделие).
Обычно окисляются металлы, включая железо, которые находятся левее водорода в ряду напряжений.

Чаще всего встречаются химическая и электрохимическая коррозии. Чтобы понять, чем они отличаются друг от друга, давайте сравним их по нескольким критериям в таблице ниже.
Таблица 1. Сравнение химической и электрохимической коррозии металлов
Признаки сравнения
Химическая коррозия
Электрохимическая коррозия
Разрушение металлов в из-за взаимодействия с газами или растворами, которые не проводят электрический ток
Разрушение металла, при котором возникает электрический ток в воде или среде другого электролита
При контакте железа с цинком коррозии подвергается цинк:
Zn 0 - 2e - = Zn 2+ .
Защитить металл от коррозии можно по-разному: покрытием защитными материалами, электрохимическими методами, шлифованием и т. д. Далее — подробно обо всем этом.
Что такое коррозия
Коррозия — это самопроизвольное разрушение элементов, чаще всего металлов, под действием химического или физико-химического влияния окружающей среды.
Иными словами, из-за химического воздействия железо начинает ржаветь. Это весьма сложный процесс, который состоит из несколько этапов. Но суммарное уравнение коррозии выглядит так:
Часто под коррозией понимают химическую реакцию между материалом и средой либо между их компонентами, которая протекает на границе раздела фаз. Обычно это окисление металла. Например:
Некоторые металлы, даже активные, покрываются плотной оксидной пленкой при коррозии. Это одна из их характерных черт. Оксидная пленка не дает окислителям проникнуть в более глубокий слой и поэтому защищает металл от коррозии. Алюминий обычно устойчив при контакте с воздухом и водой, даже горячей. Тем не менее, если поверхность алюминия покрыть ртутью, то образуется амальгама. Она разрушает оксидную пленку, и алюминий начинает быстро превращаться в белые хлопья метагидроксида алюминия:
Коррозии подвергаются и многие малоактивные металлы. Например, поверхность медного изделия покрывается патиной — зеленоватым налетом. Это происходит потому, что на ней образуются смеси основных солей.
Виды коррозии металлов
Химическая коррозия
Химическая коррозия — это процесс разрушения металла, который связан с реакцией между металлом и коррозионной средой.
Химическая коррозия протекает без воздействия электрического тока, и в результате этой реакции металлы окисляются. Этот вид коррозии можно разделить на два подвида:
газовая коррозия — металл корродирует под воздействием различных газов при высоких температурах;
коррозия в жидкостях — неэлектролитах.
Их них более распространенной считают газовую коррозию. Она протекает во время прямого контакта твердого тела с активным газом воздуха. Чаще всего это кислород. В результате на поверхности тела образуется пленка продуктов химической реакции между веществом и газом. Дальше эта пленка мешает контакту корродирующего материала с газом. При высоких температурах газовая коррозия развивается интенсивно. Возникшая при этом пленка называется окалиной, которая со временем становится толще.
Важную роль в процессе коррозии играет состав газовой среды. Но для каждого металла он индивидуален и изменяется с переменой температур.
Электрохимическая коррозия
Электрохимическая коррозия — это разрушение металла, которое протекает при его взаимодействии с окружающей средой электролита.
Этот вид коррозии считают наиболее распространенным. Самым важным происхождением электрохимической коррозии является то, что металл неустойчив в окружающей среде с точки зрения термодинамики. Вот несколько ярких примеров этой реакции: ржавчина в трубопроводе, на обшивке днища морского судна и на различных металлоконструкциях в атмосфере.
В механизме электрохимической коррозии обычно выделяют два направления: гомогенное и гетерогенное. Разберем их подробнее в таблице ниже.
Гомогенный механизм электрохимической коррозии
Гетерогенный механизм электрохимической коррозии
Поверхность металла рассматривается как однородный слой.
У твердых металлов поверхность неоднородна из-за структуры сплава, в котором атомы по-разному расположены в кристаллической решетке.
Растворение металла происходит из-за термодинамической возможности для катодного или анодного процессов.
Неоднородность можно наблюдать при наличии в сплаве каких-либо включений.
Скорость, с которой протекает электрохимическая коррозия, зависит от времени протекания процесса.
В электрохимической коррозии протекает одновременно два процесса на аноде и на катоде, которые зависят друг от друга. Растворение основного металла происходит только на анодах. Анодный процесс заключается в том, что ионы металла отрываются и переходят в раствор:
В результате происходит реакция окисления металла. В данном случае анод заряжается отрицательно.
При катодном процессе избыточные электроны переходят в молекулы или атомы электролита, которые, в свою очередь, восстанавливаются. На катоде идет реакция восстановления. Он носит заряд положительного электрода.
Торможение одного процесса приводит к торможению и другого процесса. Окисление металла может происходить только в анодном процессе.
Как защитить металлы от коррозии
От коррозии можно и нужно защищаться. Чтобы уберечь металлы от этой реакции, их покрывают защитными материалами, обрабатывают электрохимическими методами, шлифованием и т. д. Рассмотрим все эти способы подробнее.
Способ № 1. Защитные покрытия.
Для защиты от коррозии металлические изделия покрывают другим металлом, т. е. производят никелирование, хромирование, цинкование, лужение и т. д. Еще один вариант защиты — покрыть поверхность металла специальными лаками, красками, эмалями.
Способ № 2. Легирование.
Легирование — это введение добавок, которые образуют защитный слой на поверхности металла. Например, при легировании железа хромом и никелем получают нержавеющую сталь.
Способ № 3. Протекторная защита.
Протекторная защита — это способ уберечь металл от коррозии, при котором металлическое изделие соединяют с более активным металлом. Этот второй металл в итоге и разрушается в первую очередь.
Способ № 4. Электрохимическая защита.
Чтобы защитить металлы от электрохимической коррозии, нейтрализуют ток, который возникает при ней. Это делают с помощью постоянного тока, который пропускают в обратном направлении.
Способ № 5. Изменение состава среды путем добавления ингибиторов.
Для защиты от коррозии используют специальные средства, которые ее замедляют — ингибиторы. Они изменяют состояние поверхности металла — образуют труднорастворимые соединения с катионами металла. Защитные слои, образованные ингибиторами, всегда тоньше наносимых покрытий.
Способ № 6. Замена корродирующего металла на другие материалы: керамику и пластмассу.
Способ № 7. Шлифование поверхностей изделия.
Проверьте себя
Что такое коррозия?
Где в повседневной жизни можно встретить ржавление железа и других металлов? Приведите примеры.
Гидроксид железа Fe(OH)3 называют:
Что является причиной возникновения коррозии?
Чем отличаются химический и электрохимический типы коррозии?
Что такое коррозионная среда?
Узнайте все о коррозии металлов и разберитесь в других темах за 9 класс на онлайн-курсах по химии в Skysmart! Наши преподаватели помогут выяснить, где скрываются пробелы в знаниях, и восполнить их. Никаких скучных задач и сухих лекций — только интерактивные упражнения, опыты и теория простым языком. Все это поможет разобраться даже в тех темах, которые не давались в школе. Ждем на бесплатном вводном уроке!
Диффузия в металлах

Доклад по физике 7 класс на тему Диффузия
Кроме броуновского движения, опытным доказательством того, что тела состоят из молекул, которые находятся в непрерывном беспорядочном движении, является диффузия.
Запах духов, как известно, ощущается на довольно большом расстоянии. Объясняется это тем, что пары духов легко диффундируют в воздухе. Капли жидкого красителя в воде легко диффундируют по всему сосуду. Намного труднее наблюдать диффузию в твердом теле. По этой причине изучение диффузии в твердых телах стало одним из наиболее интересных исследований в физике наших дней.
Как и во многих других областях человеческой деятельности, в данном случае умение предшествовало знанию. Столетиями рабочие сваривали металлы и получали сталь нагреванием твердого железа в атмосфере углерода, не имея ни малейшего представления о происходящих при этом диффузионных процессах. Лишь в 1896 г. началось научное изучение проблемы.
Английский металлург Вильям Робертс-Аустин в простом эксперименте измерил диффузию золота в свинце. Он наплавил тонкий диск золота на конец цилиндра из чистого свинца длиной в 1 дюйм (2,45 см), поместил этот цилиндр в печь, где поддерживалась температура около 200 о С, и держал его в печи 10 дней. Затем он разрезал цилиндр на тонкие диски и измерил количество золота, которое продиффундировало в каждый срез свинца.
Оказалось, что к «чистому» концу через весь цилиндр прошло вполне измеримое количество золота; в противоположном направлении в глубь золотого диска продиффундировал свинец.
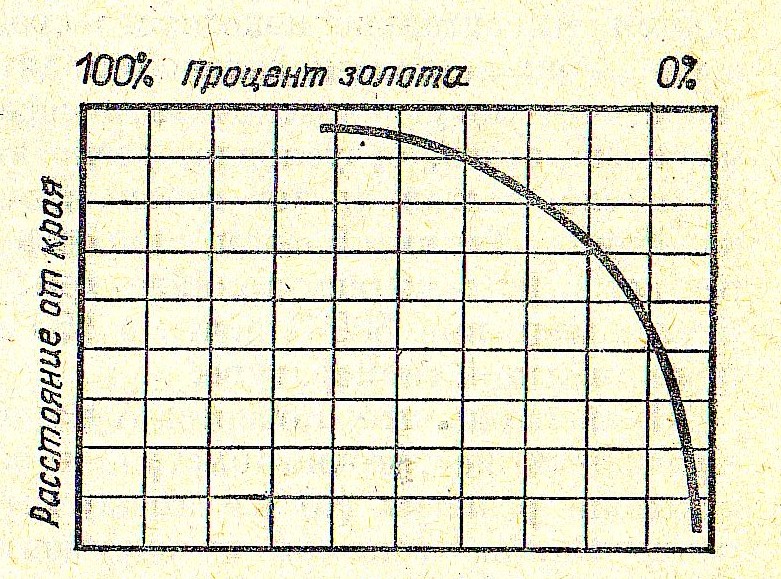
Рис.1. График, показывающий изменение концентрации золота в цилиндре в зависимости от расстояния до края.
Робертс-Аустин обнаружил, что нагретый металл диффундирует в другой, когда они тесно прижаты друг к другу. С точки зрения атомного строения вещества проницаемость твердых тел не является странной. В настоящее время мы хорошо представляем себе, что даже наиболее твердое тело — всего довольно слабо связанный набор атомов. В кристаллах, образующих металл, атомы располагаются в определенных положениях, из которых их довольно трудно сместить. Такое расположение атомов в кристаллах называют кристаллической решеткой. Однако идеальных и полностью застроенных решеток не существует. В них всегда имеется некоторое количество пустых мест — вакансий, или дырок, в которые могут перепрыгнуть диффундирующие атомы. Перепрыгнув в некую вакансию, атом оставляет после себя новую вакансию. В нее может перейти соседний атом; итак, путем непрерывных перемещений атомов в решетке атом может пройти через кристалл.
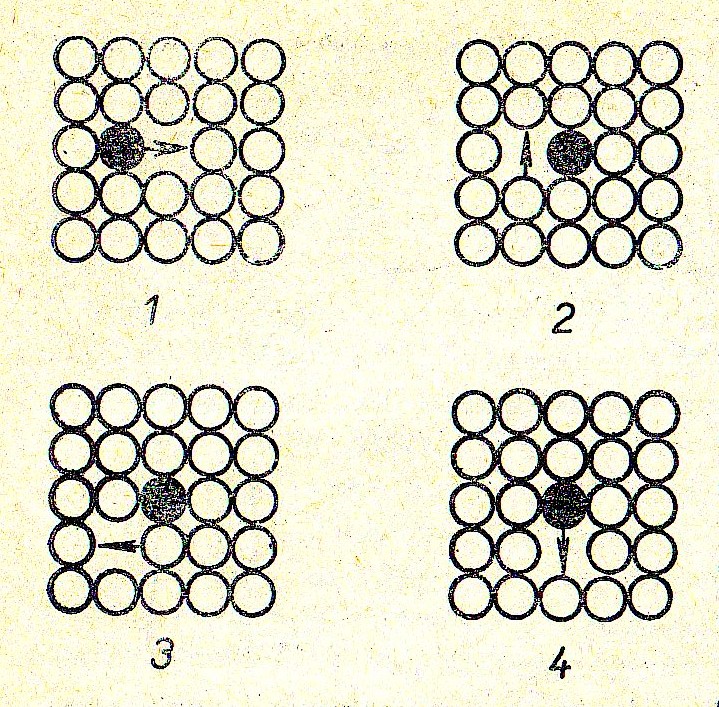
Рис. 2. Иллюстрация диффузии золота в кристалле свинца.
Что же заставляет атом покидать свое место в решетке и «перескакивать» в вакансию? Дело в том, что атомы непрерывно колеблются относительно некоторого среднего положения. Время от времени они настолько далеко отходят от своего положения равновесия, что могут перескочить в соседнее вакантное место. Возможность этого, безусловно, резко возрастает, если тело подогревают, заставляя тем самым атомы совершать более сильные колебания.
В эксперименте Робертса-Аустина атомы золота при 200 о С колебались достаточно быстро. чтобы начать перескакивать в вакансии решетки (то же имело место и для атомов свинца). В конце концов, если бы эксперимент продолжался очень долго, атомы золота равномерно распределились бы по всему свинцовому цилиндру.
Рис. 3. Атомы золота ищут вакансию в кристаллической решетке свинца.
Металл может диффундировать в другой металл лишь при наличии вакансий в кристаллических решетках, поскольку атомы даже двух разных металлов имеют размеры примерно одного и того же порядка. Однако атомы неметаллического элемента, размеры которых много меньше, чем размеры атомов металла, могут «втиснуться» между атомами в металлическом кристалле. При этом диффузия не зависит от вакансий, и, следовательно, происходит намного быстрее. Одним из наиболее важных примеров такого случая может служить диффузия углерода в железе.

Рис. 4. Диффузия углерода в железе
В своей наипростейшей форме сталь является сплавом углерода и железа. Свойства стали меняются в зависимости от содержания в сплаве углерода.
Рис.5. Атомы углерода удобно размещаются между атомами железа.
Сталь с небольшим содержанием углерода (например, около 0,25%) не очень прочна и хорошо куется. Повышение содержания углерода делает сталь более прочной, но более хрупкой. Такая деталь машины, как передаточный механизм, должна обладать твердой поверхностью, чтобы сопротивляться износу, и быть достаточно упругой в своих внутренних частях, чтобы не сломаться при внезапных ударах. Эти свойства приобретаются в следующем процессе. Кусок металла разогревается и выдерживается в газе, богатом углеродом, например в метане. Атомы углерода из газа немедленно диффундируют в сталь. Через несколько часов они проникают на глубину около одной двенадцатой дюйма (примерно на 2 мм). Поверхность или «оболочка» этого куска стали после такой обработки содержит около 1,2% углерода, тогда как внутренняя его часть содержит всего лишь 0,25% углерода.
Читайте также:
