Разрушение металлов под воздействием окружающей среды
Обновлено: 11.05.2024
Почти все металлы и сплавы постепенно разрушаются под воздействием факторов окружающей среды. При взаимодействии металлов с веществами воздуха и атмосферными осадками на их поверхности образуется плёнка, состоящая из оксидов, сульфидов, карбонатов и других соединений.
Свойства образовавшихся на поверхности металла веществ отличаются от свойств самого металла. Так, на железе образуется ржавчина — рыхлая коричнево-красная масса. Коррозию железа обычно называют ржавлением.
Коррозия — это процесс самопроизвольного разрушения металлов и их сплавов под влиянием внешней среды (от лат. corrosio — «разъедание»).
Предметы из меди и её сплавов (предметы искусства, памятники, крыши зданий) со временем подвергаются коррозии. Патина — налёт зелёного цвета — состоит в основном из гидроксокарбоната меди(\(II\))
 |  |  |
Из-за коррозии поверхность металлических изделий покрывается налётом из продуктов окисления и теряет блеск. Изменяется электропроводность металла, уменьшается его пластичность и прочность.
- приходится постоянно восполнять потери из-за ржавления нефтепроводов, газопроводов, водопроводов, сельскохозяйственной техники, автомобилей, кораблей, мостов, станков;
- металлические конструкции теряют прочность;
- простаивает производство из-за необходимости замены разрушенного коррозией оборудования;
- при разрушении нефте- и газопроводов теряется часть сырья;
- при утечке нефтепродуктов и других веществ загрязняется окружающая среда;
- загрязняется продукция, а следовательно, ухудшается её качество.
- Металлическое изделие покрывают другими металлами (никелирование, хромирование, цинкование, лужение — покрытие оловом).
- Металлические изделия покрывают лаками, красками, эмалями, маслами, полимерами.
 |  |  |
| Рис. \(6\). Нанесение защитного покрытия на поверхность металла | Рис. \(7\). Эмалированная стальная кастрюля | Рис. \(8\). Металлочерепица из жести, покрытой полимером |
Детали машин, аппаратов, инструменты и предметы быта изготовляют из нержавеющей стали, содержащей специальные легирующие (замедляющие коррозию) добавки: хром, никель и другие металлы.
К металлу прикрепляют кусок более активного металла. Под действием среды происходит его разрушение, а защищаемый металл сохраняется. Так защищают от коррозии трубопроводы, корпуса кораблей. В качестве протектора применяют такие металлы, как цинк, магний.
Для предотвращения потерь из-за коррозии особым образом обрабатывают электролит или среду, в которой находится металл. Используют также ингибиторы — вещества, которые замедляют процесс коррозии.
Например, при подготовке воды, поступающей в котельные установки, проводят удаление растворённого в воде кислорода (деаэрацию).
Коррозия металлов

Всякое явление или процесс вокруг нас связан с химией. Скажем, ржавление железа. Хоть раз в жизни вы наверняка задумывались, почему одни металлы ржавеют и разрушаются, а другие — нет. И что такого особенного в нержавеющей стали, что этот процесс ей нипочем? Обо всем это мы и поговорим в сегодняшней статье.
О чем эта статья:
Коротко о главном
Коррозия металлов или ржавление в химии — это явление, которое возникает из-за взаимодействия металлической пластинки с веществами окружающей среды (кислородом воздуха или кислотами, с которыми может реагировать металлическое изделие).
Обычно окисляются металлы, включая железо, которые находятся левее водорода в ряду напряжений.

Чаще всего встречаются химическая и электрохимическая коррозии. Чтобы понять, чем они отличаются друг от друга, давайте сравним их по нескольким критериям в таблице ниже.
Таблица 1. Сравнение химической и электрохимической коррозии металлов
Признаки сравнения
Химическая коррозия
Электрохимическая коррозия
Разрушение металлов в из-за взаимодействия с газами или растворами, которые не проводят электрический ток
Разрушение металла, при котором возникает электрический ток в воде или среде другого электролита
При контакте железа с цинком коррозии подвергается цинк:
Zn 0 - 2e - = Zn 2+ .
Защитить металл от коррозии можно по-разному: покрытием защитными материалами, электрохимическими методами, шлифованием и т. д. Далее — подробно обо всем этом.
Что такое коррозия
Коррозия — это самопроизвольное разрушение элементов, чаще всего металлов, под действием химического или физико-химического влияния окружающей среды.
Иными словами, из-за химического воздействия железо начинает ржаветь. Это весьма сложный процесс, который состоит из несколько этапов. Но суммарное уравнение коррозии выглядит так:
Часто под коррозией понимают химическую реакцию между материалом и средой либо между их компонентами, которая протекает на границе раздела фаз. Обычно это окисление металла. Например:
Некоторые металлы, даже активные, покрываются плотной оксидной пленкой при коррозии. Это одна из их характерных черт. Оксидная пленка не дает окислителям проникнуть в более глубокий слой и поэтому защищает металл от коррозии. Алюминий обычно устойчив при контакте с воздухом и водой, даже горячей. Тем не менее, если поверхность алюминия покрыть ртутью, то образуется амальгама. Она разрушает оксидную пленку, и алюминий начинает быстро превращаться в белые хлопья метагидроксида алюминия:
Коррозии подвергаются и многие малоактивные металлы. Например, поверхность медного изделия покрывается патиной — зеленоватым налетом. Это происходит потому, что на ней образуются смеси основных солей.
Виды коррозии металлов
Химическая коррозия
Химическая коррозия — это процесс разрушения металла, который связан с реакцией между металлом и коррозионной средой.
Химическая коррозия протекает без воздействия электрического тока, и в результате этой реакции металлы окисляются. Этот вид коррозии можно разделить на два подвида:
газовая коррозия — металл корродирует под воздействием различных газов при высоких температурах;
коррозия в жидкостях — неэлектролитах.
Их них более распространенной считают газовую коррозию. Она протекает во время прямого контакта твердого тела с активным газом воздуха. Чаще всего это кислород. В результате на поверхности тела образуется пленка продуктов химической реакции между веществом и газом. Дальше эта пленка мешает контакту корродирующего материала с газом. При высоких температурах газовая коррозия развивается интенсивно. Возникшая при этом пленка называется окалиной, которая со временем становится толще.
Важную роль в процессе коррозии играет состав газовой среды. Но для каждого металла он индивидуален и изменяется с переменой температур.
Электрохимическая коррозия
Электрохимическая коррозия — это разрушение металла, которое протекает при его взаимодействии с окружающей средой электролита.
Этот вид коррозии считают наиболее распространенным. Самым важным происхождением электрохимической коррозии является то, что металл неустойчив в окружающей среде с точки зрения термодинамики. Вот несколько ярких примеров этой реакции: ржавчина в трубопроводе, на обшивке днища морского судна и на различных металлоконструкциях в атмосфере.
В механизме электрохимической коррозии обычно выделяют два направления: гомогенное и гетерогенное. Разберем их подробнее в таблице ниже.
Гомогенный механизм электрохимической коррозии
Гетерогенный механизм электрохимической коррозии
Поверхность металла рассматривается как однородный слой.
У твердых металлов поверхность неоднородна из-за структуры сплава, в котором атомы по-разному расположены в кристаллической решетке.
Растворение металла происходит из-за термодинамической возможности для катодного или анодного процессов.
Неоднородность можно наблюдать при наличии в сплаве каких-либо включений.
Скорость, с которой протекает электрохимическая коррозия, зависит от времени протекания процесса.
В электрохимической коррозии протекает одновременно два процесса на аноде и на катоде, которые зависят друг от друга. Растворение основного металла происходит только на анодах. Анодный процесс заключается в том, что ионы металла отрываются и переходят в раствор:
В результате происходит реакция окисления металла. В данном случае анод заряжается отрицательно.
При катодном процессе избыточные электроны переходят в молекулы или атомы электролита, которые, в свою очередь, восстанавливаются. На катоде идет реакция восстановления. Он носит заряд положительного электрода.
Торможение одного процесса приводит к торможению и другого процесса. Окисление металла может происходить только в анодном процессе.
Как защитить металлы от коррозии
От коррозии можно и нужно защищаться. Чтобы уберечь металлы от этой реакции, их покрывают защитными материалами, обрабатывают электрохимическими методами, шлифованием и т. д. Рассмотрим все эти способы подробнее.
Способ № 1. Защитные покрытия.
Для защиты от коррозии металлические изделия покрывают другим металлом, т. е. производят никелирование, хромирование, цинкование, лужение и т. д. Еще один вариант защиты — покрыть поверхность металла специальными лаками, красками, эмалями.
Способ № 2. Легирование.
Легирование — это введение добавок, которые образуют защитный слой на поверхности металла. Например, при легировании железа хромом и никелем получают нержавеющую сталь.
Способ № 3. Протекторная защита.
Протекторная защита — это способ уберечь металл от коррозии, при котором металлическое изделие соединяют с более активным металлом. Этот второй металл в итоге и разрушается в первую очередь.
Способ № 4. Электрохимическая защита.
Чтобы защитить металлы от электрохимической коррозии, нейтрализуют ток, который возникает при ней. Это делают с помощью постоянного тока, который пропускают в обратном направлении.
Способ № 5. Изменение состава среды путем добавления ингибиторов.
Для защиты от коррозии используют специальные средства, которые ее замедляют — ингибиторы. Они изменяют состояние поверхности металла — образуют труднорастворимые соединения с катионами металла. Защитные слои, образованные ингибиторами, всегда тоньше наносимых покрытий.
Способ № 6. Замена корродирующего металла на другие материалы: керамику и пластмассу.
Способ № 7. Шлифование поверхностей изделия.
Проверьте себя
Что такое коррозия?
Где в повседневной жизни можно встретить ржавление железа и других металлов? Приведите примеры.
Гидроксид железа Fe(OH)3 называют:
Что является причиной возникновения коррозии?
Чем отличаются химический и электрохимический типы коррозии?
Что такое коррозионная среда?
Узнайте все о коррозии металлов и разберитесь в других темах за 9 класс на онлайн-курсах по химии в Skysmart! Наши преподаватели помогут выяснить, где скрываются пробелы в знаниях, и восполнить их. Никаких скучных задач и сухих лекций — только интерактивные упражнения, опыты и теория простым языком. Все это поможет разобраться даже в тех темах, которые не давались в школе. Ждем на бесплатном вводном уроке!
Коррозия металлов и способы защиты от нее
Коррозионная стойкость металла зависит от его природы, характера среды и температуры.
- Благородные металлы не подвергаются коррозии из-за химической инертности.
- Металлы Al, Ti, Zn, Cr, Ni имеют плотные газонепроницаемые оксидные плёнки, которые препятствуют коррозии.
- Металлы с рыхлой оксидной плёнкой – Fe, Cu и другие – коррозионно неустойчивы. Особенно сильно ржавеет железо.
Различают химическую и электрохимическую коррозию.
| Химическая коррозия сопровождается химическими реакциями. Как правило, химическая коррозия металлов происходит при действии на металл сухих газов, её также называют газовой. |
При химической коррозии также возможны процессы:
Fe + 2HCl → FeCl2 + H2
2Fe + 3Cl2 → 2FeCl3
Как правило, такие процессы протекают в аппаратах химических производств.
| Электрохимическая коррозия – это процесс разрушения металла, который сопровождается электрохимическими процессами. Как правило, электрохимическая коррозия протекает в присутствии воды и кислорода, либо в растворах электролитов. |
В таких растворах на поверхности металла возникают процессы переноса электронов от металла к окислителю, которым является либо кислород, либо кислота, содержащаяся в растворе.
При этом электродами являются сам металл (например, железо) и содержащиеся в нем примеси (обычно менее активные металлы, например, олово).
В таком загрязнённом металле идёт перенос электронов от железа к олову, при этом железо (анод) растворяется, т.е. подвергается коррозии:
Fe –2e = Fe 2+
На поверхности олова (катод) идёт процесс восстановления водорода из воды или растворённого кислорода:
2H + + 2e → H2
O2 + 2H2O + 4e → 4OH –
| Например, при контакте железа с оловом в растворе соляной кислоты происходят процессы: |
Анод: Fe –2e → Fe 2+
Катод: 2H + + 2e → H2
Суммарная реакция: Fe + 2H + → H2 + Fe 2+
Если реакция проходит в атмосферных условиях в воде, в ней участвует кислород и происходят процессы:
Анод: Fe –2e → Fe 2+
Катод: O2 + 2H2O + 4e → 4OH –
Суммарная реакция:
Fe 2+ + 2OH – → Fe(OH)2
4Fe(OH)2 + O2+ 2H2O → 4Fe(OH)3
При этом образуется ржавчина.
Методы защиты от коррозии
Защитные покрытия
Защитные покрытия предотвращают контакт поверхности металла с окислителями.
- Катодное покрытие – покрытие менее активным металлом (защищает металл только неповреждённое покрытие).
- Покрытие краской, лаками, смазками.
- Создание на поверхности некоторых металлов прочной оксидной плёнки химическим путём (анодирование алюминия, кипячение железа в фосфорной кислоте).
Создание сплавов, стойких к коррозии
Физические свойства сплавов могут существенно отличаться от свойств чистых металлов. Добавление некоторых металлов может приводить к повышению коррозионной стойкости сплава. Например, нержавеющая сталь, новые сплавы с большой коррозионной устойчивостью.
Изменение состава среды
Коррозия замедляется при добавлении в среду, окружающую металлическую конструкцию, ингибиторов коррозии. Ингибиторы коррозии — это вещества, подавляющие процессы коррозии.
Электрохимические методы защиты
Протекторная защита: при присоединении к металлической конструкции пластинок из более активного металла – протектора. В результате идёт разрушение протектора, а металлическая конструкция при этом не разрушается.
КОРРОЗИЯ МЕТАЛЛОВ И ЗАЩИТА МЕТАЛЛОВ ОТ КОРРОЗИИ
Металлы вследствие своей высокой прочности, пластичности, износоустойчивости, тепло- и электропроводности являются наиболее важными конструкционными материалами.
В процессе эксплуатации в результате воздействия окружающей среды происходит их разрушение, так называемая коррозия.
Потери от коррозии в ведущих индустриальных странах составляют около 3-5% валового национального продукта, а затраты на возмещениекоррозионных потерь во всем мире исчисляются сотнями миллиардов долларов, поэтому раздел «Коррозия металлов и методы защиты их от коррозии» является одним из важнейших в курсе химии для инженерных специальностей.
Обычно корродируют металлы, которые встречаются в природе не в самородном состоянии, как Au, Pt, а в виде различных руд. На извлечение этих металлов из природных соединений расходуется значительное количество энергии (Ме +n + n? → Me 0 ; ΔG>0), которая накапливается в металлах, делая их термодинамически неустойчивыми, химически активными веществами (Ме 0 - n? → Me + n ; ΔG<0). В результате такого самопроизвольно протекающего коррозионного процесса металлы переходят в оксиды, гидроксиды, карбонаты, сульфиды и другие соединения и теряются безвозвратно.
Итак, коррозию можно определить как самопроизвольно протекающий окислительно-восстановительный процесс (ΔG<0) разрушения металла под воздействием окружающей среды, происходящий с выделением энергии (ΔН<0) и рассеиванием вещества (ΔS>0).
Механическое разрушение металлов, происходящее по физическим причинам, не называют коррозией, а называют эрозией, истиранием, износом.
По характеру разрушения поверхности коррозию подразделяют на сплошную и местную. Сплошная коррозия подразделяется на равномерную, если процесс окисления происходит по всей поверхности металла с одинаковой скоростью, и неравномерную – процесс окисления происходит по всей поверхности с различной скоростью на различных участках металла.
Местная коррозия подразделяется на коррозию пятнами, точечную, питтинг (углубленно-точечную), межкристаллитную (наиболее опасна, т.к. ослабляет связи между зернами структуры сплавов), растрескивающуюся, селективную (избирательную).
По механизму протекания различают следующие виды коррозии:
- электрохимическая (концентрационная, контактная, электрокоррозия);
- особые виды (биологическая, радиационная, ультразвуковая).
По характеру дополнительных воздействий различают:
- коррозию под влиянием механических напряжений;
- коррозию при трении;
- кавитационную коррозию (возникает при одновременном коррозионном и ударном воздействии агрессивной среды, когда лопаются пузырьки воздуха при работе лопастей гребного винта, роторов насосов).
Рассмотрим более подробно виды коррозии по механизму протекания.
Под химической коррозией понимают разрушение металлов окислением в окружающей среде без возникновения электрического тока в системе.
Газовая коррозия протекает при обычных условиях, но чаще при высоких температурах. Наблюдается при разливе расплавленных металлов, их термической обработке, ковке, прокатке, сварке и т.д.
Самый распространенный случай газовой коррозии – взаимодействие металла с кислородом:
Образующаяся при такой коррозии оксидная пленка в ряде случаев играет защитную функцию. Для этого она должна быть сплошной, беспористой, иметь хорошее сцепление с металлом, обладать твердостью, износостойкостью и иметь коэффициент термического расширения, близкий к этой величине для металла. Все эти качества оксидной пленки можно оценить по фактору Пиллинга-Бэдвордса (a). Металлы (щелочные, щелочноземельные), у которых a2O3, ZnO, NiO и т.д.).
При значениях a значительно больше единицы пленки получаются неслошные, лекго отделяющиеся от поверхности металла (железная окалина). Коррозионно-активными газами, кроме кислорода, являются: угарный газ, углекислый газ, сернистый ангидрид, азот, его оксиды и галогены. Например, при разливе расплавленного алюминия, происходит его взаимодействие не только с кислородом, но и с азотом воздуха.
Жидкостная коррозия протекает, как правило, в жидких неэлектролитах: спиртах, хлороформе, бензоле, бензине, керосине и других нефтепродуктах. Ускоряет процесс жидкостной коррозии сера,кислород, галогены, влага, атакже повышенная температура (коррозия поршней в двигателях внутреннего сгорания),что можно описать уравнениями : Me(II) + R1 – S – R2 → MeS + R1 – R2
Me(I) + nR – Cl → MeCl + 1/2nR – R ,
где R1 – S – R2и nR – Cl углеводороды, содержащие серу и хлор.
Электрохимическая коррозия наиболее распространенный вид коррозии. Это разрушение деталей, машин, конструкций в грунтовых, речных, морских водах, под влиянием воды (росы), под воздействием смазочно-охлаждающих жидкостей, используемых при механической обработке металлов, атмосферная коррозия и т.д.
Электрохимическая коррозия – это пространственно разделенный окислительно-восстановительный процесс разрушения металла, протекающий в среде электролита, с возникновением внутри системы электрического тока, называемого коррозионным током.
Рассмотрим химизм атмосферной коррозии стального изделия. Сталь – это сплав железа с углеродом, в котором углерода менее 2%, например, цементит (Fe3C4). При электрохимической коррозии во влажном воздухе (О2 + 2Н2О) железо и цементит образуют микрогальванопару, в которой роль анода выполняет железо, а цементит – роль катода.
Схема процесса:
Анодный процесс: Fe 0 - 2? → Fe 2+ 2 поляризация
Катодный процесс: 2H2O + O2 + 4? → 4OH - 1 деполяризация
Суммарное уравнение коррозионного процесса разрушения стального изделия, находящегося во влажном воздухе:
Для железа более характерна степень окисления (3+), поэтому процесс окисления идет дальше:
4Fe(OH)2+2H2O+O2→4Fe(OH)3, образующийся Fe(OH)3 при нагревании может терять воду.
То есть продуктами коррозии железа (ржавчина) является смесь различных соединений. Если учесть, что в воздухе присутствуют углекислый газ, сернистый газ, следовательно, могут образовываться и соли железа.
Часто из-за различной рельефности металлических конструкций, в том числе и стальных, на некоторых участках скапливается вода, при этом происходит так называемая концентрационная коррозия, обусловленная различной концентрацией деполяризатора кислорода (в случае атмосферной коррозии), водорода (в кислой среде) на различных участках металла. Там, где концентрация деполяризатора больше (края капли воды), формируется катодный участок, где концентрация деполяризатора меньше (центр капли воды) – анодный участок (рис.15).
После высыхания капли в её центре обнаруживается углубление, а иногда даже и отверстие (для пластин толщиной 0,1-0,2 мм). Такие процессы часто наблюдаются при атмосферной и почвенной коррозии железных и стальных изделий (троса, стопки листов и т.д.) – точечная коррозия, переходящая в питтинг. Следует отметить, что хотя конечный продукт коррозии (ржавчина) нерастворим, однако он не препятствует процессу растворения металла, поскольку формируется за пределами анодного участка (на границе соприкосновения его с катодами) в виде кольца внутри капли.
На практике часто встречаются случаи, когда металлы различной активности находятся в контакте друг с другом, образуя гальванопары. Кроме того, технические металлы содержат примеси других металлов, сплавы содержат различные металлы. Такой металл или сплав, находясь в среде электролита, дает множество микро - и макрогальванопар, в которых анодом является более активный металл, т.е. металл с меньшим значением электродного потенциала, именно он и подвергается коррозии.
Рассмотрим случай контактной коррозии с водородной деполяризациейцинка и меди, в сернокислой среде. Цинк и медь, имеют различные значения электродных потенциалов. Более активным в этой гальвано паре является цинк (Е 0 Zn2+/Zn = -0,76 В), он имеет меньшее значение электродного потенциала и будет анодом, т. е именно цинк будет подвергаться коррозионным процессам, менее активным металлом является медь (Е 0 Cu2+/Cu = +0,34 В), она будет катодом.
Запишем схему: (А) Zn | H2SO4 | Cu (K)
Анодный процесс: Zn 0 - 2? → Zn 2+
Катодный процесс: 2Н + + 2? → Н2 деполяризатор
Суммарное ионное уравнение: Zn + 2H + → Zn 2+ + H2
Факторы, влияющие на скорость коррозии:
а) напряжение и деформация при механической обработке металлов;
б) перемешивание агрессивной среды;
в) дифференциальная аэрация;
д) кислотность среды (рН).
Рассматривая фактор (д) обратите внимание, что электродные потенциалы металлов существенно зависят от состава электролита и рН среды. Так, в случае контактной (Al-Zn) коррозии в 1М растворе HCl
возникает гальвано пара, в которой роль анода выполняет Al, а катода- Zn, схема такого процесса: (А) Al | HCl | Zn (K)
В 0,1 М растворе HCl в этом случае большую активность имеет цинк, он будет в гальвано паре анодом, алюминий – катодом, а схему запишем так: (А) Zn | HCl | Al (K)
Электрокоррозия – протекает под действием блуждающих токов, возникает от постоянных источников тока (электротранспорт, трансформаторы, линии электропередач). Рассматривая коррозию под действием блуждающих токов, надо помнить, что место выхода тока – будет анодным участком, входа тока – катодным, участок протекания тока – нейтральной зоной. Радиус действия блуждающих токов может достигать нескольких десятков километров. Ток силой 1А за год разрушает до 3 кг алюминия, 9 кг железа, 11 кг цинка или меди, 34 кг свинца.
ЗАЩИТА МЕТАЛЛОВ ОТ КОРРОЗИИ
Потери от коррозии в мировой экономике огромны. Около 1/3 вводимого в эксплуатацию металла подвергается коррозии, при этом примерно 10% теряется безвозвратно.
Борьба с коррозией осуществляется различными методами. Наиболее рациональный и надежный путь – изготовление аппаратов и машин изкоррозионно-стойких металлических или неметаллических материалов,но из-за дороговизны таких материалов, чаще используют дешевые и доступные металлы с последующей защитой их от коррозии. Полностью избежать коррозии невозможно, но, применив определенные методы защиты, можно снизить ее воздействие.
Можно условно выделить следующие группы методов защиты металлов от коррозии:
1. Создание рациональных конструкций, т.е. таких, которые не имеют застойных зон и других мест скопления влаги, грязи и других коррозионно-агрессивных сред, допускают быструю очистку и аэрацию.
2. Легирование металлов. Это эффективный, хотя обычно дорогой метод повышения коррозионной стойкости металлов. При легировании в состав сплава вводят компоненты (Cr, Ni, W, Si, V, Mo, Re и другие), вызывающие пассивирование металла. Механизм защиты (например, в нержавеющих сталях) состоит в образовании на поверхности плотных оксидных слоев, типа шпинелей состава NiO . Cr2O, FeO . Cr2O3, которые оказываются более устойчивыми, чем просто оксиды хрома или никеля.
3. Создание аморфных структур металлов. Путь к этому способу защиты открыла сверхбыстрая закалка. Расплавленный металл из тигля подают в тончайший зазор между двумя массивными валками и подвергают формированию и резкому охлаждению. В этих условиях атомы не успевают выстраиваться в присущие металлам кристаллические решетки, фиксируется «хаос атомов», свойственный расплавленному металлу. В результате получается аморфная структура, подобная стеклу, резко возрастает коррозионная устойчивость металлов.
4. Защитные покрытия – самый распространенный метод защиты металлов от коррозии. Смысл их нанесения – изоляция от агрессивной среды. Различают неметаллические и металлические покрытия.
а) неметаллические покрытия получают нанесением на поверхность металла лака, краски, смолы, олифы, эмали или стеклоэмали. Поверхность металла покрывают также резиной, эбонитом, полимерными материалами, цементом, бетоном, оксидными пленками: ZnO, Al2O3 (оксидирование) и нитридными пленками: Fe4N, Fe2N (азотирование). Покрыть поверхность металла можно осаждением нерастворимых фосфатов этого металла: Fe(H2PO4)2 + 2 Fe 2+ ® Fe3(PO4)2¯ + 4H ( фосфатирование) или насыщением поверхности металла углеродом (цементация).
б) защитные покрытия металлами. Для этого используют коррозионно-устойчивые металлы (Sn, Zn, Al, Au, Ag, Ni, Cr и др.) Различают анодные и катодные металлические покрытия. Если защищаемый металл покрывают более активным металлом, то такое покрытие называют анодным. При нарушении покрытия разрушается металл покрытия. Рассмотрим это на примере оцинкованного железа. Составим схему коррозионного разрушения.
A: Zn 0 - 2? → Zn 2+ 2
Если защищаемый металл покрыт менее активным металлом, например, железо покрыто оловом, то такой вид покрытия называется катодным. При нарушении покрытия разрушается основной металл. Рассмотрим этот случай коррозии.
(А) Fe | 2H + | Sn (K)
A: Fe 0 - 2? → Fe 2+ 1
Fe + 2H + → Fe 2+ + H2
5. Электрохимические методы защиты:
а) защита внешним потенциалом);
б) анодная (протекторная).
Защита внешним потенциалом (чаще катодная) осуществляется подключением защищаемой конструкции к отрицательному полюсу (катоду) внешнего источника тока с очень малым напряжением (0,1 В). К положительному полюсу подсоединяется лом, который и разрушается. Этот вид защиты используют для металлических сооружений: трубопроводов, резервуаров и т.д.
Протекторная защита заключается в том, что к изделию, подвергающемуся электрохимической коррозии, подключают деталь – протектор из более активного металла, чем металл изделия. Протектор будет разрушаться, а изделие останется неизменным. Применяют в паровых котлах, для защиты корпусов морских и речных судов, трубопроводов, рельсов и т.д.
Задача. Приведите пример протекторной защиты в электролите, содержащем растворенный кислород. Составьте уравнения анодного и катодного процессов и вычислите ЭДС реакции.
Решение. Протекторная защита осуществляется путем присоединения к железу более активного металла, обычно цинка, магния и их сплавов. Таким образом, создается искусственный микрогальванический элемент. Чаще всего используют протекторную защиту в растворах электролитов (паровые котлы, химические аппараты), в морской воде и в почве (защита трубопроводов). Рассмотрим протекторную защиту от почвенной коррозии:
Среда нейтральная или слабощелочная, так как концентрация солей невелика. В этом, созданном нами, коррозионном элементе анодом служит протектор (цинк), он растворяется.
Анод: Zn 0 – 2 ® Zn 2+ .
Электроны передаются на железо. Деполяризатором в этом случае является кислород.
Катод: O2 + 2H2O + 4® 4OH - ; E 0 = 0,40 B.
ЭДС реакции определяем: DЕ = Екатода – Еанода = 0,40 – (-0,75) = 1,16 В.
Ответ: протектор Zn, он окисляется и защищает железо; DЕ = 1,16 В.
6. Воздействие на агрессивную среду. Для замедления коррозии в агрессивную среду вводят вещества, называемые ингибиторами (замедлителями). Это чаще всего органические вещества, пассивирующие поверхность металла: тиомочевина C(NH2)2S, диэтиламин C2H5 — NH — C2H5, уротропин (CH2)6N4, неорганические вещества SiO3 2- , NO2 - , Cr2O7 2- , а также освобождение воды от растворенного в ней кислорода (воду фильтруют через слой железных опилок). Либо удаляют активаторы коррозии, например, ионы Cl - , Br - , F - , SO4 2- , NO3 - .
Литература:
1. Фролов В.В. Химия. Гл.V, §51-56.
3. Общая химия под ред. Соколовской Е.М. и др. Гл.6, §1-11.
4. Абраменко В.Л. Методические указания к самостоятельному изучению темы “Коррозия и защита металлов от нее”. Луганск, 1991 г.
Конспекты лекций. Коррозия – разрушение метала под воздействием окружающей среды
Коррозия – разрушение метала под воздействием окружающей среды. В зависимости от характера физико-химического воздействия среды различают:
- химическую коррозию, обусловленную воздействием сухих газов и жидкостей, не являющихся электролитами;
- электролитическую коррозию, обусловленную воздействием электролитов.
Химическая коррозия – это чаще всего окисление металлов в газовой среде, усиливающееся при повышении температуры. Защита от окисления металлов основана на образовании защитной окисной плёнки на поверхности. Плёнка должна быть прочной, хорошо сцепляться с поверхностью металла, а главное быть сплошной. Материал будет стоек к химической коррозии, если объём образующегося окисла больше объёма металла его образовавшего. Это и есть условие сплошности плёнки окисла. Этим требованием удовлетворяет плёнка оксида хрома Cr2O3, образующая на поверхности сталей с высоким (более 12%) содержанием хрома.
Электрохимическая коррозия – наиболее распостранённый вид коррозии. Разнородные металлы (или участки различных фаз в сплавах), контактируя с электролитом, образуют гальванический элемент. Металл, имеющий более низкий потенциал (анод) отдаёт ионы в электролит и растворяется (корродирует). Чем ниже электродный потенциал металла по отношению к стандартному водородному потенциалу, тем ниже его коррозионная стойкость. Электрохимическая неоднородность поверхности сплава является причиной коррозии. Чем больше различия электродных потенциалов отдельных структурных состовляющих, тем более сплав склонен к коррозии. Более коррозионно-стойкими являются сплавы со структурой однородного твёрдого раствора.
Различные виды электрохимической коррозии представлены на рис.1.
Равномерная коррозия (а) развивается на поверхности чистых металлов или однородных твердых растворов.
В гетерофазных сплавах развивается местная коррозия (б), охватывающая отдельные участки поверхности с низким электродным потенциалом. К местной коррозии относятся питтинг или точечная коррозия , пятнистая, язвенная. Очаги такий коррозии являются концентраторами напряжения.
В некоторых сплавах границы зерен, обогощенные примесями, имеют низкий электродный потенциал. В них развивается наиболее опасная межкристаллитная коррозия.
Устойчивость против коррозии повышается при введении в состав стали хрома, алюминия, кремния. Алюминий и кремний повышают хрупкость стали, их применяют редко.
Сталь, содержащая более 12% хрома устойчива в атмосфере, морской воде, ряде кислот, щелочей и солей. Примерами таких коррозионностойких сталей являются хромистые стали: 08Х13, 20Х13, 40Х13, 65Х13, 95Х18.
Низкоуглеродистые хромистые стали применяют для изготовления деталей конструкций, высокоуглеродистые (40Х13, 65Х13, 95Х18) для различных инструментов (ножи, скальпели). Помимо хрома коррозиостойкие стали могут содержать никель, эти стали называют хромоникелиевые и они весьма распростронены в качестве конструкционных (12Х18Н10Т, 12Х18Н9, 04Х18Н10, 10Х17Н13М2Т). Эти стали более коррозионностойки чем хромистые и сохроняют эту стойкость при нагреве в отличие от хромистых. Послезакалки хромоникелевые стали имеют структуру однородного аустенита, обеспечивающую их повышенную стойкость.
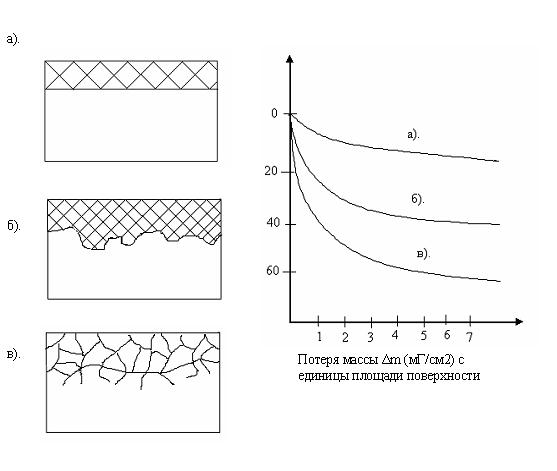
Рис. 1 Основные разновидности электрохимической коррозии (схемы) и их относительное влияние на прочность листового дуралюминия (графики):
а). равномерная коррозия; б). местная коррозия; в). межкристаллитная коррозия
Способность материала сопротивляться химической коррозии при высоких температурах называется жаростойкостью.
Способность материала сопротивляться деформации и разрушению при высоких температурах называется жаропрочностью. Жаропрочность в сталях достигается легированием тугоплавкими элементами (хром, ванадий, вольфрам, молибден). Эти элементы затрудняют диффузионные процессы и повышают температуру рекристаллизации. Жаропрочностью обладают также хромоникелевые стали аустенитного класса (диффузия в плотноупакованной решетке ГЦК существенно затруднена). Примеры жаропрочных сталей: 12ХМФ. 08Х12ВНМФ, 12Х18Н10Т, 08Х18Н9.
Общим для всех инструментальных сталей является повышенное содержание углерода, обеспечивающее их прочность, твердость, износостойкость. По назначению они делятся на стали для режущего инструмента, штамповочного и измерительного.
Стали для режущего инструмента различают по теплостойкости – способности сохранять твердость при нагреве: низкой теплостойкости (углеродистые и инструментальные стали У7 … У13) для инструмента, не испытывающего нагрева (Т
Стали для штампового инструмента делят на стали для холодного деформирования (отличаются повышенным содержанием углерода Х6ВФ, Х12, Х12М, ХВГ) и стали для горячего деформирования (5ХНМ, 4ХМФС, 3Х2В2Ф, 4Х2В5МФ как правило среднеуглеродистые, легированные хромом, молибденом, вольфрамом, ванадием).
Стали для измерительного инструмента должны обладать высокой твердостью, износостойкостью, стабильностью формы и размеров (У8 … У12, Х, ХГС, ХГВ, 9ХС).
Медь – металл с ГЦК решеткой, высоким удельным весом (8,95 г/см3), температурой плавления 10830С. Это пластичный материал с высокой электро- и теплопроводностью, низкой твердостью и прочностью. Обладает высокой коррозийной стойкостью. Из-за низкого предела текучести не применяется в чистом виде как конструкционный материал. В чистом виде медь применяют для изготовления электропроводов (высокая электропроводимость) и теплообменников (высокая теплопроводность). Медь широко применяют как основу конструкционных сплавов: латуней и бронз.
Латунь – двойной или многокомпонентный сплав меди, где основным легирующим элементом является цинк. Латуни подразделят на деформируемые и литейные по способу получения заготовок и изделий. Деформируемые отличаются меньшим количеством легирующих элементов и обладают высокой прочностью на ряду с достаточной прочностью. Из них изготавливают трубы, проволоку, профили, листы. Литейные латуни применяются для получения отливок сложной формы литьем в землю, кокиль, под давлением. Для усиления тех или иных свойств латуни помимо цинка легируют железом, оловом, марганцем, кремнием, алюминием, свинцом.
Деформируемые латуни от литейных легко отличить по маркировке: деформируемая ЛАЖ 60-1-1 (после буквы Л подряд начальные буквы русского названия легирующего элемента (кроме цинка), затем подряд идут группы цифр, указывающие процентное содержание меди и по порядку легирующих элементов (кроме цинка); литейная ЛЦ4ОМ\цЗЖ (после буквы Л идут начальные буквы русского названия легирующего элемента (начиная с цинка) и за буквой цифры, отражающие содержание этого элемента в процентах).
Бронзы – многокомпонентные сплавы меди с другими элементами, где цинк не является основным. Подразделяют бронзы аналогично латуням на деформируемые (БрОЦС 4-4-2,5) и литейные (БрО6Ц6С2). Отличия маркировки деформируемых и литейных бронз такие же как у латуней.
Алюминий – металл с ГЦК решеткой, низким удельным весом (2,7 г/м3) и температурой плавления 6600С. Обладает высокой электро- и теплопроводимостью, коррозийной стойкостью, пластичностью. Из-за низкого предела текучести алюминий в чистом виде как конструкционный материал не используют, а используют для изготовления электропроводов. Широкое применение нашли алюминиевые сплавы.
Деформируемые алюминиевые сплавы, не упрочняемые термической обработкой.
В этих сплавах содержание легирующих элементов меньше предела растворимости при комнатной температуре (зона I рис. 2). Сплавы эти обладают высокой пластичностью, наибольшей коррозийной стойкостью, но невысокой прочностью. Примерами сплавов этой группы являются сплавы систем Al – Mn и Al – Mg (АМц3, АМг6).
Деформируемые алюминиевые сплавы, упрочняемые термической обработкой.
В этих сплавах содержание легирующих элементов больше предела растворимости при комнатной температуре (зона II рис. 2). Примерами сплавов этой группы являются сплавы систем Al – Сu - дуралюмины (Д1, д16). Эти сплавы достаточно пластичны в состоянии перенасыщенного твердого раствора, а при последующей старении (естественном или искусственном) приобретают высокую прочность. Наибольшей прочностью обладают высокопрочные алюминиевые сплавы системы Al – Zn – Mg – Cu (В95, В96). Самыми легкими являются сплавы системы Al – Mg – Li (1420).
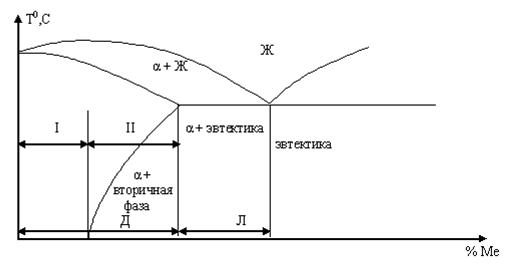
Рис. 2 Типовая диаграмма (схема) состояния системы Al – легирующий элемент (Ме).
Д – деформируемые сплавы, Л – литейные.
I – деформируемые сплавы, не упрочняемые термической обработкой; II - деформируемые сплавы, упрочняемые термической обработкой.
Читайте также:
