Сколько процентов всех элементов являются металлами
Обновлено: 21.09.2024
МЕТАЛЛЫ — это вещества, обладающие высокой электропроводностью и теплопроводностью, ковкостью, пластичностью и металлическим блеском. Эти характерные свойства металла обусловлены наличием свободно перемещающихся электронов в его кристаллической решетке. Из известных в настоящее время 107 химических элементов 85 относятся к металлам.
Деление всех химических элементов периодической системы Д. И. Менделеева на металлы и неметаллы является условным. Если в периодической таблице провести диагональ через бор и астат, то в главных подгруппах, расположенных справа от диагонали, будут неметаллы, а в главных подгруппах слева от диагонали, побочных подгруппах и в восьмой группе (кроме инертных газов) — металлы. Причем элементы рядом с разделительной линией являются так называемыми металлоидами, т. е. веществами с промежуточными свойствами (металлов и неметаллов) . К ним относятся: бор В, кремний Si, германий Gе, мышьяк Аs, сурьма Sb, теллур Те, полоний Ро.
В соответствии с местом, занимаемым в периодической системе, различают переходные (элементы побочных подгрупп) и непереходные металлы (элементы главных подгрупп) . Металлы главных подгрупп характеризуются тем, что в их атомах происходит последовательное заполнение электронных s- и р-подуровней. В атомах металлов побочных подгрупп происходит достраивание d- и f-подуровней.
Неметаллы - Это химические элементы, которые образуют в свободном виде простые вещества, не обладающие физическими свойствами металлов.
Из известных химических элементов только 22 являются неметаллами. Если провести условную диагональ в переодической системе от берилия к астату, неметаллы окажутся над ней т. е. они находятся в правом верхнем углу.
Атомы неметаллов ( по сравнению с атомами металлов) содержат большее число электронов на внешнем энергетическом уровне, по этому простые вещества - неметаллы обладают, как правило, окислительно - восстановительной деятельностью (кроме фтора и кислорода, которые являются окислителями)
Неметаллы различны по своему агрегатному состоянию. Многие из них газы (кислород, азот, гелий, водород, неон, ксенон, криптон и т. д.). Твердые вещества (фосфор, фтор, йод, бор и т. д.). Бром является жидкостью.
Для неметаллов характерно явление аллотропии. многие из них существуют в виде аллотропных видоизменений, например - фосфор, углерод, кислород, сера и т. д.
Неметаллы имеют различные типы кристаллической решетки - атомную (бор, кремний, углерод в виде алмаза) и молекулярную (йод, белый фосфор, сера кристаллическая)
Физические свойства неметаллов зависят от типа решетки. Вещества с молекулярной решеткой - летучие, легкоплавкие, непрочные, с незначительной растворимостью в воде.
Кароче, там есть такая таблица металлов (такая полосочка, начинаеться Литем (кажись) а заканчиваеться чем-то тяжёлым) .
Основным признаком что эллемент - металл, являеться слабая связь электронов последнего уровня с ядром, они (металлы) могут эти электроны отдавать.
С этим связна причина их электропроводности.
проще говоря, металлы, это те элементы, которые на внешнем электронном уровне имеют 1-3 электрона, т. е. при взаимодействии с другими элементами, , они легко отдают эти электроны. Это 1, 2, 3 группа (гл. подг) перидической системы
А неметаллы, это те элементы, которые имеют почти завершенный электронный уровень, которым не хватает до завершения 1-3 электрона. Это 5,6,7 группа
А вы знали, что 69,5% элементов таблицы Менделеева - это металлы ?
Скорее всего, русский ученый Дмитрий Иванович Менделеев, отец и создатель таблицы химических элементов, и не подозревал, к чему приведут его двадцатилетние труды, и как упорядоченная им таблица - увековечит его имя на века. Да, да, именно - упорядоченная.
Элементы химической таблицы Менделеева
Мало кто знает об этом, но Дмитрий Иванович не единственный ученый-химик, пытавшийся упорядочить (уже известные на тот момент) химические элементы в единую таблицу. В тот период развития человеческого мышления, были и другие ученые, ставившие перед собой аналогичные задачи. Из таких господ можно перечислить итальянского химика Станислав Канниццаро, предложившего теорию составления таблицы - используя атомный вес каждого элемента. Или французского химика-геолога Александра Эмиль Шанкуртуа, создавшего на размеченном цилиндре - свой винтовой график химических элементов. Таковых было много и много, но выдающегося результата добился только Менделеев, с его таблицей на основе зависимости различных свойств элементов от их заряда атомного ядра. Хоть наша страница не совсем об этом - но и не-упомянуть об этом факте было бы недопустимо.
Как известно, в таблице Дмитрий Ивановича содержится 118 химических элементов. Из этих 118 элементов - 85 элемента являются (в том или ином виде) металлами.
Давайте перечислим их:
- Литий (Li) третий химический элемент в таблице, входит в группу щелочных металлов. Открыт в 1817 году шведским химиком Иоганном Арфведсоном;
- Берилий (Be) четвертый элемент таблицы, один из относительно твердых металлов. Открыт в 1798 году французским химиком Луи Никола Вокленом;
- Натрий (Na) одиннадцатый элемент таблицы, входит в группу мягких щелочных металлов;
- Магний (Mg) двенадцатый элемент был открыт в 1695 году в Англии, и назван аптекарями Англии «горькой солью»;
- Алюминий (Al) тринадцатый элемент, открыт датским физиком Гансом Эрстедом в 1825 году. Благодаря стойкости к коррозии, и легко поддающейся формовке - является одним из часто применяемых металлов в промышленности;
- Калий (K) девятнадцатый элемент, ;
- Кальцый (Ca) двадцатый элемент
- Скандий (Sc) двадцать первый элемент
- Титан (Ti) двадцать второй элемент
- Ванадий (V) двадцать третий элемент
- Хром (Cr) двадцать четвертый элемент
- Марганец (Mn) двадцать пятый элемент
- Железо (Fe) двадцать шестой элемент
- Кобальт (Co) двадцать седьмой элемент
- Никель (Ni) двадцать восьмой элемент
- Медь (Cu) двадцать девятый элемент
- Цинк (Zn) тридцатый элемент
- Галлий (Ga) тридцать первый элемент
- Рубидий (Rb) тридцать седьмой элемент
- Стронций (Sr) тридцать восьмой элемент
- Иттрий (Y) тридцать девятый элемент
- Цирконий (Zr) сороковой элемент
- Ниобий (Nb) сорок первый элемент
- Молибден (Mo) сорок второй элемент
- Технеций (Tc) сорок третий элемент
- Рутений (Ru) сорок четвертый элемент
- Родий (Rh) сорок пятый элемент
- Палладий (Pd) сорок шестой элемент
- Серебро (Ag) сорок седьмой элемент
- Кадмий (Cd) сорок восьмой элемент
- Индий (In) сорок девятый элемент
- Олово (Sn) пятидесятый элемент
- Цезий (Cs) пятьдесят пятый элемент
- Барий (Ba) пятьдесят шестой элемент
- Лантан (La) пятьдесят седьмой элемент
- Церий (Ce) 58
- Празеодим (Pr) 59
- Неодим (Nd) 60
- Прометий (Pm) 61
- Самарий (Sm) 62
- Европий (Eu) 63
- Гадолиний (Gb) 64
- Тербий (Tb) 65
- Диспрозий (Dy) 66
- Гольмий (Ho) 67
- Эрбий (68) Er
- Тулий (Tm) 69
- Иттербий (Yb) 70
- Лютеций (Lu) 71
- Графний (Hf) семьдесят второй элемент
- Тантал (Ta) семьдесят третий
- Вольфрам (W) семьдесят четвертый
- Рений (Re) семьдесят пятый элемент
- Осмий (Os) семьдесят шестой элемент
- Иридий (Ir) семьдесят седьмой элемент
- Платина (Pt) семьдесят восьмой элемент
- Золото (Au) семьдесят девятый элемент
- Ртуть (Hg) восьмидесятый элемент
- Таллий (Tl) восемьдесят первый элемент
- Свинец (Pb) восемьдесят второй элемент
- Висмут (Bi) восемьдесят третий элемент
- Полоний (Po) восемьдесят четвертый элемент
- Франций (Fr) восемьдесят седьмой элемент
- Радий (Ra) восемьдесят восьмой элемент
- Актиний (Ac) восемьдесят девятый элемент
- Торий (Th) 90
- Протактиний (Pa) 91
- Уран (U) 92
- Нептуний (Np) 93
- Плутоний (Pu) 94
- Америций (Am) 95
- Кюрий (Cm) 96
- Берклий (Bk) 97
- Калифорний (Cf) 98
- Эйнштений (Es) 99
- Фермий (Fm) 100
- Менделевий (Md) 101
- Нобелий (No) 102
- Лоуренсий (Lr) 103
- Резенфордий (Rf) сто четвертый элемент
- Дубний (Db) сто пятый элемент
- Сиборгий (Sg) сто шестой элемент
- Борий (Bh) сто седьмой элемент
- Хассий (Hs) сто восьмой элемент
- Мейтнерий (Mt) сто девятый элемент
Мы перечислили все 85 химических элементов, входящих в группу металлов. Остальные 33 элемента, не являющиеся металлами, входят в газы (к примеру: фтор, хлор, кислород, азот, водород и т.д.), и другую группу, называющуюся «неметаллы.
Сколько процентов всех элементов являются металлами

Металлы (от лат. metallum — шахта, рудник) — группа элементов, в виде простых веществ обладающих характерными металлическими свойствами, такими как высокие тепло- и электропроводность, положительный температурный коэффициент сопротивления, высокая пластичность и металлический блеск.
Из 118 химических элементов, открытых на данный момент (из них не все официально признаны), к металлам относят:
- 6 элементов в группе щелочных металлов,
- 6 в группе щёлочноземельных металлов,
- 38 в группе переходных металлов,
- 11 в группе лёгких металлов,
- 7 в группе полуметаллов,
- 14 в группе лантаноиды + лантан,
- 14 в группе актиноиды (физические свойства изучены не у всех элементов) + актиний,
- вне определённых групп бериллий и магний.
В астрофизике термин «металл» может иметь другое значение и обозначать все химические элементы тяжелее гелия
- Металлический блеск (характерен не только для металлов: его имеют и неметаллы иод и углерод в виде графита)
- Хорошая электропроводность
- Возможность лёгкой механической обработки
- Высокая плотность (обычно металлы тяжелее неметаллов)
- Высокая температура плавления (исключения: ртуть, галлий и щелочные металлы)
- Большая теплопроводность
- В реакциях чаще всего являются восстановителями.
Все металлы (кроме ртути и, условно, франция) при нормальных условиях находятся в твёрдом состоянии, однако обладают различной твёрдостью. Ниже приводится твёрдость некоторых металлов по шкале Мооса.
Температуры плавления чистых металлов лежат в диапазоне от −39 °C (ртуть) до 3410 °C (вольфрам). Температура плавления большинства металлов (за исключением щелочных) высока, однако некоторые «нормальные» металлы, например олово и свинец, можно расплавить на обычной электрической или газовой плите.
В зависимости от плотности, металлы делят на лёгкие (плотность 0,53 ÷ 5 г/см³) и тяжёлые (5 ÷ 22,5 г/см³). Самым лёгким металлом является литий (плотность 0.53 г/см³). Самый тяжёлый металл в настоящее время назвать невозможно, так как плотности осмия и иридия — двух самых тяжёлых металлов — почти равны (около 22.6 г/см³ — ровно в два раза выше плотности свинца), а вычислить их точную плотность крайне сложно: для этого нужно полностью очистить металлы, ведь любые примеси снижают их плотность.
Большинство металлов пластичны, то есть металлическую проволоку можно согнуть, и она не сломается. Это происходит из-за смещения слоёв атомов металлов без разрыва связи между ними. Самыми пластичными являются золото, серебро и медь. Из золота можно изготовить фольгу толщиной 0.003 мм, которую используют для золочения изделий. Однако не все металлы пластичны. Проволока из цинка или олова хрустит при сгибании; марганец и висмут при деформации вообще почти не сгибаются, а сразу ломаются. Пластичность зависит и от чистоты металла; так, очень чистый хром весьма пластичен, но, загрязнённый даже незначительными примесями, становится хрупким и более твёрдым. Некоторые металлы такие как золото, серебро, свинец, алюминий, осмий могут срастаться между собой, но на это может уйти десятки лет.
Все металлы хорошо проводят электрический ток; это обусловлено наличием в их кристаллических решётках подвижных электронов, перемещающихся под действием электрического поля. Серебро, медь и алюминий имеют наибольшую электропроводность; по этой причине последние два металла чаще всего используют в качестве материала для проводов. Очень высокую электропроводность имеет также натрий, в экспериментальной аппаратуре известны попытки применения натриевых токопроводов в форме тонкостенных труб из нержавеющей стали, заполненных натрием. Благодаря малому удельному весу натрия, при равном сопротивлении натриевые «провода» получаются значительно легче медных и даже несколько легче алюминиевых.
Высокая теплопроводность металлов также зависит от подвижности свободных электронов. Поэтому ряд теплопроводностей похож на ряд электропроводностей и лучшим проводником тепла, как и электричества, является серебро. Натрий также находит применение как хороший проводник тепла; широко известно, например, применение натрия в клапанах автомобильных двигателей для улучшения их охлаждения.
Цвет у большинства металлов примерно одинаковый — светло-серый с голубоватым оттенком. Золото, медь и цезий соответственно жёлтого, красного и светло-жёлтого цвета.
На внешнем электронном уровне у большинства металлов небольшое количество электронов (1-3), поэтому они в большинстве реакций выступают как восстановители (то есть «отдают» свои электроны)
- С кислородом реагируют все металлы, кроме золота, платины. Реакция с серебром происходит при высоких температурах, но оксид серебра(II) практически не образуется, так как он термически неустойчив. В зависимости от металла на выходе могут оказаться оксиды, пероксиды, надпероксиды:
оксид лития
пероксид натрия
надпероксид калия
- С азотом реагируют только самые активные металлы, при комнатной температуре взаимодействует только литий, образуя нитриды:
- С серой реагируют все металлы, кроме золота и платины:
- С водородом реагируют только самые активные металлы, то есть металлы IA и IIA групп кроме Be. Реакции осуществляются при нагревании, при этом образуются гидриды. В реакциях металл выступает как восстановитель, степень окисления водорода −1:
- С углеродом реагируют только наиболее активные металлы. При этом образуются ацетилениды или метаниды. Ацетилениды при взаимодействии с водой дают ацетилен, метаниды — метан.
Взаимодействие неокисляющих кислот с металлами, стоящими в электрическом ряду активности металлов до водорода
Металлы

К металлам относится большая часть элементов периодической системы – 82 химических элементов. Какими свойствами они обладают, и чем отличаются от неметаллов?
Общая характеристика
Металлами называют группу элементов, в виде простых веществ, которые обладают металлическими свойствами (пластичность, ковкость, блеск, электронная проводимость и т. д.)
Основное отличие элементов-металлов – они обладают только восстановительными свойствами, а в реакциях могут только окисляться. В соединениях они могут иметь только положительные степени окисления как в элементарных положительно заряженных ионах, так и в сложных ионах, где они образуют положительные центры.
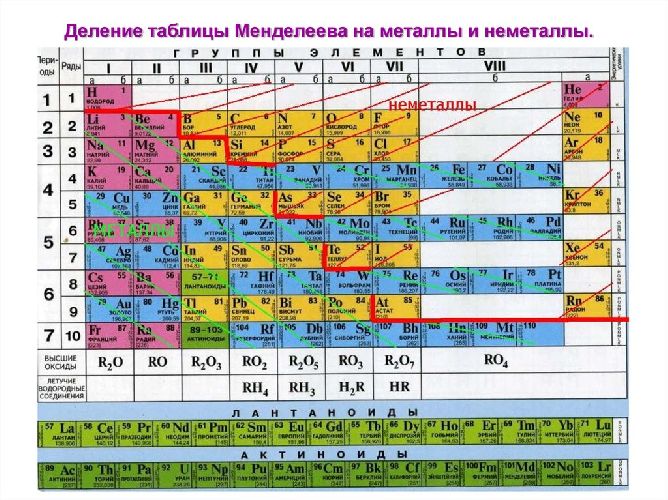
Рис. 1. Список металлов.
Как правило, на внешнем уровне элементов металлов находится небольшое число электронов (1-3), значения электроотрицательности невысокие. К металлам относятся все s-элементы (кроме водорода и гелия), d- и f-элементы, а также p-элементы под чертой бор-астат. Для типичных металлов характерен большой размер атомов, что способствует легкости отдачи валентных электронов. Образующиеся положительные ионы устойчивы, так как имеют завершенную внешнюю электронную оболочку.
Физические и химические свойства
Все металлы, кроме ртути, при нормальных условиях в виде простых веществ находятся в твердом агрегатном состоянии и образуют металлическую кристаллическую решетку.

Рис. 2. Металлы в таблице Д.И. Менделеева.
Таблица «Металлы»
В следующей таблицы представлены группы основных металлов:
| Группа металлов | Металл |
| Щелочные | литий, натрий, калий и т.д. |
| Щелочноземельные | кальций, стронций, барий и т.д. |
| Переходные | уран, титан, железо, платина и т.д. |
| постпереходные | алюминий, свинец, олово и т.д. |
| Тугоплавкие | молибден, вольфрам |
| Цветные | медь, титан, магний и т.д. |
| Благородные | золото, серебро и т.д. |
Металлы пластичны и ковки, особенно если на внешнем электронном уровне атомов по одному электрону: слои атомов перемещаются относительно друг друга без разрушения кристаллической решетки (щелочные металлы, медь, серебро, золото). В атомах непластичных хрупких металлов хрома и марганца – большое число валентных электронов.
Плотность, твердость, температура плавления металлов изменяются в широком диапазоне и зависят от атомной массы, строения атома и геометрии кристаллической решетки. Самый легкий металл – литий (плотность 0,53 г/см 3 ), самый тяжелый – осмий (плотность 22,5 г/см 3 ). Металлы с плотностью больше 5 г/см 3 относят к тяжелым, меньше 5 г/см 3 – к легким металлам.
Самая низкая температура плавления у ртути (-39 градусов по Цельсию), самый тугоплавкий металл – вольфрам (температура плавления 3410 градусов по Цельсию.) Энергия атомизации вольфрама составляет 836 кДж/моль, а температура кипения его 5930 градусов.
Металлы вступают в реакцию как с простыми, так и со сложными веществами. Как типичные восстановители металлы реагируют почти со всеми неметаллами-окислителями (кислород, сера, азот и т. д.):
Также металлы реагируют с такими сложными веществами, как оксиды и гидроксиды, разбавленные растворы кислот, с растворенными в воде щелочами.
В пределах одного и того же периода металлические свойства ослабевают, а неметаллические усиливаются; в пределах одной и той же группы (в главной подгруппе) металлические свойства усиливаются, а неметаллические ослабевают

Рис. 3. Металлы главных подгрупп.
Нахождение металлов и способы их получения
Самый распространенный на земле элемент-металл – алюминий. За ним следуют железо, кальций, натрий.
Некоторые металлы встречаются в природе в самородном состоянии (золото, ртуть, платина), но в основном они находятся в природе в виде оксидов и солей.
Получение металлов происходит с помощью металлургии (получение из руд), пирометаллургии (получение с помощью реакции восстановления при высокой температуре), гидрометаллургии (извлечение из руд в виде растворимых соединений), электрометаллургии (получение металлов электролизом расплавов и растворов их соединений).
Что мы узнали?
Металлы – вещества, которые обладают высокой электро- и теплопроводностью, ковкостью, пластичностью и металлическим блеском. В данной статье по химии 9 класса рассматриваются их физические и химические свойства, формулы класса металлов, а также способы получения.
Активные металлы

Металлы, легко вступающие в реакции, называются активными металлами. К ним относятся щелочные, щелочноземельные металлы и алюминий.
Положение в таблице Менделеева
Металлические свойства элементов ослабевают слева направо в периодической таблице Менделеева. Поэтому наиболее активными считаются элементы I и II групп.
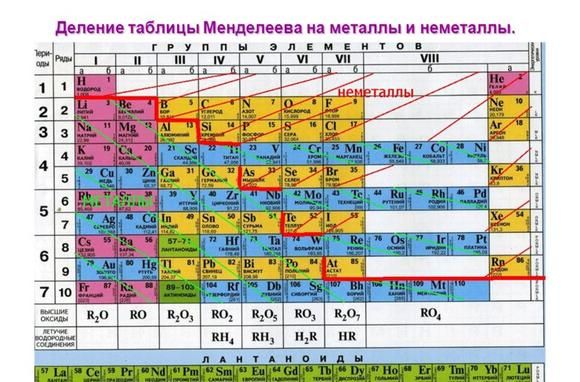
Рис. 1. Активные металлы в таблице Менделеева.
Все металлы являются восстановителями и легко расстаются с электронами на внешнем энергетическом уровне. У активных металлов всего один-два валентных электрона. При этом металлические свойства усиливаются сверху вниз с возрастанием количества энергетических уровней, т.к. чем дальше электрон находится от ядра атома, тем легче ему отделиться.
Наиболее активными считаются щелочные металлы:
- литий;
- натрий;
- калий;
- рубидий;
- цезий;
- франций.
К щелочноземельным металлам относятся:
- бериллий;
- магний;
- кальций;
- стронций;
- барий;
- радий.
Узнать степень активности металла можно по электрохимическому ряду напряжений металлов. Чем левее от водорода расположен элемент, тем более он активен. Металлы, стоящие справа от водорода, малоактивны и могут взаимодействовать только с концентрированными кислотами.

Рис. 2. Электрохимический ряд напряжений металлов.
К списку активных металлов в химии также относят алюминий, расположенный в III группе и стоящий левее водорода. Однако алюминий находится на границе активных и среднеактивных металлов и не реагирует с некоторыми веществами при обычных условиях.
Свойства
Активные металлы отличаются мягкостью (можно разрезать ножом), лёгкостью, невысокой температурой плавления.
Основные химические свойства металлов представлены в таблице.
Реакция
Уравнение
Исключение
Щелочные металлы самовозгораются на воздухе, взаимодействуя с кислородом
Литий реагирует с кислородом только при высокой температуре
Щелочноземельные металлы и алюминий на воздухе образуют оксидные плёнки, а при нагревании самовозгораются
Реагируют с простыми веществами, образуя соли
Алюминий не вступает в реакцию с водородом
Бурно реагируют с водой, образуя щёлочи и водород
Реакция с литием протекает медленно. Алюминий реагирует с водой только после удаления оксидной плёнки
Реагируют с кислотами, образуя соли
Взаимодействуют с растворами солей, сначала реагируя с водой, а затем с солью
Активные металлы легко вступают в реакции, поэтому в природе находятся только в составе смесей – минералов, горных пород.

Рис. 3. Минералы и чистые металлы.
К активным металлам относятся элементы I и II групп – щелочные и щелочноземельные металлы, а также алюминий. Их активность обусловлена строением атома – немногочисленные электроны легко отделяются от внешнего энергетического уровня. Это мягкие лёгкие металлы, быстро вступающие в реакцию с простыми и сложными веществами, образуя оксиды, гидроксиды, соли. Алюминий находится ближе к водороду и для его реакции с веществами требуются дополнительные условия – высокие температуры, разрушение оксидной плёнки.
Читайте также:
