Способы защиты металлов от коррозии материаловедение
Обновлено: 11.05.2024
Металлы вследствие своей высокой прочности, пластичности, износоустойчивости, тепло- и электропроводности являются наиболее важными конструкционными материалами.
В процессе эксплуатации в результате воздействия окружающей среды происходит их разрушение, так называемая коррозия.
Потери от коррозии в ведущих индустриальных странах составляют около 3-5% валового национального продукта, а затраты на возмещениекоррозионных потерь во всем мире исчисляются сотнями миллиардов долларов, поэтому раздел «Коррозия металлов и методы защиты их от коррозии» является одним из важнейших в курсе химии для инженерных специальностей.
Обычно корродируют металлы, которые встречаются в природе не в самородном состоянии, как Au, Pt, а в виде различных руд. На извлечение этих металлов из природных соединений расходуется значительное количество энергии (Ме +n + n? → Me 0 ; ΔG>0), которая накапливается в металлах, делая их термодинамически неустойчивыми, химически активными веществами (Ме 0 - n? → Me + n ; ΔG<0). В результате такого самопроизвольно протекающего коррозионного процесса металлы переходят в оксиды, гидроксиды, карбонаты, сульфиды и другие соединения и теряются безвозвратно.
Итак, коррозию можно определить как самопроизвольно протекающий окислительно-восстановительный процесс (ΔG<0) разрушения металла под воздействием окружающей среды, происходящий с выделением энергии (ΔН<0) и рассеиванием вещества (ΔS>0).
Механическое разрушение металлов, происходящее по физическим причинам, не называют коррозией, а называют эрозией, истиранием, износом.
По характеру разрушения поверхности коррозию подразделяют на сплошную и местную. Сплошная коррозия подразделяется на равномерную, если процесс окисления происходит по всей поверхности металла с одинаковой скоростью, и неравномерную – процесс окисления происходит по всей поверхности с различной скоростью на различных участках металла.
Местная коррозия подразделяется на коррозию пятнами, точечную, питтинг (углубленно-точечную), межкристаллитную (наиболее опасна, т.к. ослабляет связи между зернами структуры сплавов), растрескивающуюся, селективную (избирательную).
По механизму протекания различают следующие виды коррозии:
- электрохимическая (концентрационная, контактная, электрокоррозия);
- особые виды (биологическая, радиационная, ультразвуковая).
По характеру дополнительных воздействий различают:
- коррозию под влиянием механических напряжений;
- коррозию при трении;
- кавитационную коррозию (возникает при одновременном коррозионном и ударном воздействии агрессивной среды, когда лопаются пузырьки воздуха при работе лопастей гребного винта, роторов насосов).
Рассмотрим более подробно виды коррозии по механизму протекания.
Под химической коррозией понимают разрушение металлов окислением в окружающей среде без возникновения электрического тока в системе.
Газовая коррозия протекает при обычных условиях, но чаще при высоких температурах. Наблюдается при разливе расплавленных металлов, их термической обработке, ковке, прокатке, сварке и т.д.
Самый распространенный случай газовой коррозии – взаимодействие металла с кислородом:
Образующаяся при такой коррозии оксидная пленка в ряде случаев играет защитную функцию. Для этого она должна быть сплошной, беспористой, иметь хорошее сцепление с металлом, обладать твердостью, износостойкостью и иметь коэффициент термического расширения, близкий к этой величине для металла. Все эти качества оксидной пленки можно оценить по фактору Пиллинга-Бэдвордса (a). Металлы (щелочные, щелочноземельные), у которых a2O3, ZnO, NiO и т.д.).
При значениях a значительно больше единицы пленки получаются неслошные, лекго отделяющиеся от поверхности металла (железная окалина). Коррозионно-активными газами, кроме кислорода, являются: угарный газ, углекислый газ, сернистый ангидрид, азот, его оксиды и галогены. Например, при разливе расплавленного алюминия, происходит его взаимодействие не только с кислородом, но и с азотом воздуха.
Жидкостная коррозия протекает, как правило, в жидких неэлектролитах: спиртах, хлороформе, бензоле, бензине, керосине и других нефтепродуктах. Ускоряет процесс жидкостной коррозии сера,кислород, галогены, влага, атакже повышенная температура (коррозия поршней в двигателях внутреннего сгорания),что можно описать уравнениями : Me(II) + R1 – S – R2 → MeS + R1 – R2
Me(I) + nR – Cl → MeCl + 1/2nR – R ,
где R1 – S – R2и nR – Cl углеводороды, содержащие серу и хлор.
Электрохимическая коррозия наиболее распространенный вид коррозии. Это разрушение деталей, машин, конструкций в грунтовых, речных, морских водах, под влиянием воды (росы), под воздействием смазочно-охлаждающих жидкостей, используемых при механической обработке металлов, атмосферная коррозия и т.д.
Электрохимическая коррозия – это пространственно разделенный окислительно-восстановительный процесс разрушения металла, протекающий в среде электролита, с возникновением внутри системы электрического тока, называемого коррозионным током.
Рассмотрим химизм атмосферной коррозии стального изделия. Сталь – это сплав железа с углеродом, в котором углерода менее 2%, например, цементит (Fe3C4). При электрохимической коррозии во влажном воздухе (О2 + 2Н2О) железо и цементит образуют микрогальванопару, в которой роль анода выполняет железо, а цементит – роль катода.
Схема процесса:
Анодный процесс: Fe 0 - 2? → Fe 2+ 2 поляризация
Катодный процесс: 2H2O + O2 + 4? → 4OH - 1 деполяризация
Суммарное уравнение коррозионного процесса разрушения стального изделия, находящегося во влажном воздухе:
Для железа более характерна степень окисления (3+), поэтому процесс окисления идет дальше:
4Fe(OH)2+2H2O+O2→4Fe(OH)3, образующийся Fe(OH)3 при нагревании может терять воду.
То есть продуктами коррозии железа (ржавчина) является смесь различных соединений. Если учесть, что в воздухе присутствуют углекислый газ, сернистый газ, следовательно, могут образовываться и соли железа.
Часто из-за различной рельефности металлических конструкций, в том числе и стальных, на некоторых участках скапливается вода, при этом происходит так называемая концентрационная коррозия, обусловленная различной концентрацией деполяризатора кислорода (в случае атмосферной коррозии), водорода (в кислой среде) на различных участках металла. Там, где концентрация деполяризатора больше (края капли воды), формируется катодный участок, где концентрация деполяризатора меньше (центр капли воды) – анодный участок (рис.15).
После высыхания капли в её центре обнаруживается углубление, а иногда даже и отверстие (для пластин толщиной 0,1-0,2 мм). Такие процессы часто наблюдаются при атмосферной и почвенной коррозии железных и стальных изделий (троса, стопки листов и т.д.) – точечная коррозия, переходящая в питтинг. Следует отметить, что хотя конечный продукт коррозии (ржавчина) нерастворим, однако он не препятствует процессу растворения металла, поскольку формируется за пределами анодного участка (на границе соприкосновения его с катодами) в виде кольца внутри капли.
На практике часто встречаются случаи, когда металлы различной активности находятся в контакте друг с другом, образуя гальванопары. Кроме того, технические металлы содержат примеси других металлов, сплавы содержат различные металлы. Такой металл или сплав, находясь в среде электролита, дает множество микро - и макрогальванопар, в которых анодом является более активный металл, т.е. металл с меньшим значением электродного потенциала, именно он и подвергается коррозии.
Рассмотрим случай контактной коррозии с водородной деполяризациейцинка и меди, в сернокислой среде. Цинк и медь, имеют различные значения электродных потенциалов. Более активным в этой гальвано паре является цинк (Е 0 Zn2+/Zn = -0,76 В), он имеет меньшее значение электродного потенциала и будет анодом, т. е именно цинк будет подвергаться коррозионным процессам, менее активным металлом является медь (Е 0 Cu2+/Cu = +0,34 В), она будет катодом.
Запишем схему: (А) Zn | H2SO4 | Cu (K)
Анодный процесс: Zn 0 - 2? → Zn 2+
Катодный процесс: 2Н + + 2? → Н2 деполяризатор
Суммарное ионное уравнение: Zn + 2H + → Zn 2+ + H2
Факторы, влияющие на скорость коррозии:
а) напряжение и деформация при механической обработке металлов;
б) перемешивание агрессивной среды;
в) дифференциальная аэрация;
д) кислотность среды (рН).
Рассматривая фактор (д) обратите внимание, что электродные потенциалы металлов существенно зависят от состава электролита и рН среды. Так, в случае контактной (Al-Zn) коррозии в 1М растворе HCl
возникает гальвано пара, в которой роль анода выполняет Al, а катода- Zn, схема такого процесса: (А) Al | HCl | Zn (K)
В 0,1 М растворе HCl в этом случае большую активность имеет цинк, он будет в гальвано паре анодом, алюминий – катодом, а схему запишем так: (А) Zn | HCl | Al (K)
Электрокоррозия – протекает под действием блуждающих токов, возникает от постоянных источников тока (электротранспорт, трансформаторы, линии электропередач). Рассматривая коррозию под действием блуждающих токов, надо помнить, что место выхода тока – будет анодным участком, входа тока – катодным, участок протекания тока – нейтральной зоной. Радиус действия блуждающих токов может достигать нескольких десятков километров. Ток силой 1А за год разрушает до 3 кг алюминия, 9 кг железа, 11 кг цинка или меди, 34 кг свинца.
ЗАЩИТА МЕТАЛЛОВ ОТ КОРРОЗИИ
Потери от коррозии в мировой экономике огромны. Около 1/3 вводимого в эксплуатацию металла подвергается коррозии, при этом примерно 10% теряется безвозвратно.
Борьба с коррозией осуществляется различными методами. Наиболее рациональный и надежный путь – изготовление аппаратов и машин изкоррозионно-стойких металлических или неметаллических материалов,но из-за дороговизны таких материалов, чаще используют дешевые и доступные металлы с последующей защитой их от коррозии. Полностью избежать коррозии невозможно, но, применив определенные методы защиты, можно снизить ее воздействие.
Можно условно выделить следующие группы методов защиты металлов от коррозии:
1. Создание рациональных конструкций, т.е. таких, которые не имеют застойных зон и других мест скопления влаги, грязи и других коррозионно-агрессивных сред, допускают быструю очистку и аэрацию.
2. Легирование металлов. Это эффективный, хотя обычно дорогой метод повышения коррозионной стойкости металлов. При легировании в состав сплава вводят компоненты (Cr, Ni, W, Si, V, Mo, Re и другие), вызывающие пассивирование металла. Механизм защиты (например, в нержавеющих сталях) состоит в образовании на поверхности плотных оксидных слоев, типа шпинелей состава NiO . Cr2O, FeO . Cr2O3, которые оказываются более устойчивыми, чем просто оксиды хрома или никеля.
3. Создание аморфных структур металлов. Путь к этому способу защиты открыла сверхбыстрая закалка. Расплавленный металл из тигля подают в тончайший зазор между двумя массивными валками и подвергают формированию и резкому охлаждению. В этих условиях атомы не успевают выстраиваться в присущие металлам кристаллические решетки, фиксируется «хаос атомов», свойственный расплавленному металлу. В результате получается аморфная структура, подобная стеклу, резко возрастает коррозионная устойчивость металлов.
4. Защитные покрытия – самый распространенный метод защиты металлов от коррозии. Смысл их нанесения – изоляция от агрессивной среды. Различают неметаллические и металлические покрытия.
а) неметаллические покрытия получают нанесением на поверхность металла лака, краски, смолы, олифы, эмали или стеклоэмали. Поверхность металла покрывают также резиной, эбонитом, полимерными материалами, цементом, бетоном, оксидными пленками: ZnO, Al2O3 (оксидирование) и нитридными пленками: Fe4N, Fe2N (азотирование). Покрыть поверхность металла можно осаждением нерастворимых фосфатов этого металла: Fe(H2PO4)2 + 2 Fe 2+ ® Fe3(PO4)2¯ + 4H ( фосфатирование) или насыщением поверхности металла углеродом (цементация).
б) защитные покрытия металлами. Для этого используют коррозионно-устойчивые металлы (Sn, Zn, Al, Au, Ag, Ni, Cr и др.) Различают анодные и катодные металлические покрытия. Если защищаемый металл покрывают более активным металлом, то такое покрытие называют анодным. При нарушении покрытия разрушается металл покрытия. Рассмотрим это на примере оцинкованного железа. Составим схему коррозионного разрушения.
A: Zn 0 - 2? → Zn 2+ 2
Если защищаемый металл покрыт менее активным металлом, например, железо покрыто оловом, то такой вид покрытия называется катодным. При нарушении покрытия разрушается основной металл. Рассмотрим этот случай коррозии.
(А) Fe | 2H + | Sn (K)
A: Fe 0 - 2? → Fe 2+ 1
Fe + 2H + → Fe 2+ + H2
5. Электрохимические методы защиты:
а) защита внешним потенциалом);
б) анодная (протекторная).
Защита внешним потенциалом (чаще катодная) осуществляется подключением защищаемой конструкции к отрицательному полюсу (катоду) внешнего источника тока с очень малым напряжением (0,1 В). К положительному полюсу подсоединяется лом, который и разрушается. Этот вид защиты используют для металлических сооружений: трубопроводов, резервуаров и т.д.
Протекторная защита заключается в том, что к изделию, подвергающемуся электрохимической коррозии, подключают деталь – протектор из более активного металла, чем металл изделия. Протектор будет разрушаться, а изделие останется неизменным. Применяют в паровых котлах, для защиты корпусов морских и речных судов, трубопроводов, рельсов и т.д.
Задача. Приведите пример протекторной защиты в электролите, содержащем растворенный кислород. Составьте уравнения анодного и катодного процессов и вычислите ЭДС реакции.
Решение. Протекторная защита осуществляется путем присоединения к железу более активного металла, обычно цинка, магния и их сплавов. Таким образом, создается искусственный микрогальванический элемент. Чаще всего используют протекторную защиту в растворах электролитов (паровые котлы, химические аппараты), в морской воде и в почве (защита трубопроводов). Рассмотрим протекторную защиту от почвенной коррозии:
Среда нейтральная или слабощелочная, так как концентрация солей невелика. В этом, созданном нами, коррозионном элементе анодом служит протектор (цинк), он растворяется.
Анод: Zn 0 – 2 ® Zn 2+ .
Электроны передаются на железо. Деполяризатором в этом случае является кислород.
Катод: O2 + 2H2O + 4® 4OH - ; E 0 = 0,40 B.
ЭДС реакции определяем: DЕ = Екатода – Еанода = 0,40 – (-0,75) = 1,16 В.
Ответ: протектор Zn, он окисляется и защищает железо; DЕ = 1,16 В.
6. Воздействие на агрессивную среду. Для замедления коррозии в агрессивную среду вводят вещества, называемые ингибиторами (замедлителями). Это чаще всего органические вещества, пассивирующие поверхность металла: тиомочевина C(NH2)2S, диэтиламин C2H5 — NH — C2H5, уротропин (CH2)6N4, неорганические вещества SiO3 2- , NO2 - , Cr2O7 2- , а также освобождение воды от растворенного в ней кислорода (воду фильтруют через слой железных опилок). Либо удаляют активаторы коррозии, например, ионы Cl - , Br - , F - , SO4 2- , NO3 - .
Литература:
1. Фролов В.В. Химия. Гл.V, §51-56.
3. Общая химия под ред. Соколовской Е.М. и др. Гл.6, §1-11.
4. Абраменко В.Л. Методические указания к самостоятельному изучению темы “Коррозия и защита металлов от нее”. Луганск, 1991 г.
4.1 Основные способы защиты металлов от коррозии …………. 8
Коррозия — это самопроизвольный процесс разрушения материалов и изделий из них под химическим воздействием окружающей среды.
Коррозия металлов — разрушение металлов вследствие физико-химического воздействия внешней среды, при котором металл переходит в окисленное (ионное) состояние и теряет присущие ему свойства.
В тех случаях, когда окисление металла необходимо для осуществления какого-либо технологического процесса, термин “коррозия” употреблять не следует. Например, нельзя говорить о коррозии растворимого анода в гальванической ванне, поскольку анод должен окислятся, посылая свои ионы в раствор, чтобы протекал нужный процесс. Нельзя также говорить о коррозии алюминия при осуществлении аллюмотермического процесса. Но физико-химическая сущность изменений, происходящих с металлом во всех подобных случаях, одинакова: металл окисляется.
Типы коррозии
Различают 4 основных вида коррозии, например: электрохимическая коррозия, водородная, кислородная коррозия и химическая.
· Электрохимическая коррозии
Разрушение металла под воздействием возникающих в коррозионной среде гальванических элементов-называют электрохимической коррозией. Не следует путать с электрохимической коррозией коррозию однородного материала, например, ржавление железа или т. п. При электрохимической коррозии всегда требуется наличие электролита, с которым соприкасаются электроды — либо различные элементы структуры материала, либо два различных соприкасающихся материала с различающимися окислительно-восстановительными потенциалами. Если в воде растворены ионы солей, кислот, или т. п., электропроводность её повышается, и скорость процесса увеличивается.
Водородная коррозия - повреждение стали и ее страновление более хрупкой под влиянием длительного воздействия водородной среды при повышенных (gt; 200 °С) температурах эксплуатации в результате физико-химического взаимодействия водорода с отдельными компонентами и/или фазами сплава.
Водородное повреждение при повышенных температурах связано с образованием продуктов реакции между водородом и углеродом по типу: В углеродистой стали суммарная химическая реакция между углеродом, связанным в карбидах железа, и водородом может быть представлена в виде
образующийся в результате реакции метан покидает металл и/или образует внутренние полости и трещины, наполненные газообразным метаном под высоким давлением. В поверхностных слоях металла формируются обезуглероженные зоны. Водородная коррозия может протекать во всех сталях, если они содержат углерод в доступной для реакции форме и он достаточно подвижен, чтобы вступать в реакцию с водородом.
Восприимчивость стали к водородной коррозии зависит от легирующих элементов, которые воздействуют на активность углерода. Скорость водородной коррозии зависит от давления водорода и температуры, а также от размера зерен, состава их границ, степени наклепа стали и других факторов.
Кислородная коррозия возникает при питании парогенератора водой, содержащей кислород. Проявляется эта коррозия в виде язвин и питтингов на трубах. Причиной питтинговой коррозии является двойственное влияние кислорода на коррозионный процесс. С одной стороны, кислород является активным деполяризатором и ускоряет катодный процесс и коррозию в целом. С другой стороны, окисляя металл и образуя окислы, кислород играет роль пассиватора, снижающего скорость коррозии. В результате в присутствии кислорода уменьшается число анодных участков и возрастает площадь катодных участков. Коррозия становится местной, интенсивность её возрастает, разрушения идут, вглубь образуя язвы. Язвенный характер кислородной коррозии делает её особенно опасной.Наблюдается кислородная коррозия главным образом в экономайзерах. При значительном содержании кислорода в питательной воде (более 0,3 мг/кг) кислородная коррозия может протекать в пароводяном коллекторе и отпускных трубах парогенераторов с естественной циркуляцией.
Величина кислородной коррозии пропорциональна содержанию кислорода в питательной воде.
Подъёмные парообразующие трубы также могут разрушаться вследствие кислородной коррозии. Однако коррозионный процесс в них протекает менее интенсивно и практически мало зависит от содержания кислорода. Это обстоятельство связано с деаэрирующией способностью пара при кипении воды в подъёмных трубах.
Повышение давления и температуры при неизменном содержании кислорода приводит к усилению коррозии. Это связано с возрастанием скорости диффузии кислорода к катодным участкам.
Скорость кислородной коррозии зависит от плотности теплового потока, скорости циркуляции, наличия в воде солей. Если в питательной воде наряду с О2 содержаться хлориды, то коррозия усиливается Химическая коррозия
Химическая коррозия — самопроизвольное взаимодействие металла с коррозионной средой, при котором окисление металла и восстановление окислительного компонента коррозионной среды протекают в одном акте. Как и любая химическая реакция, этот вид коррозии носит временной характер. Окислителями (корродирующими агентами) могут быть сухие газы (О2, СО2, SО2, HC1, оксиды азота и др.), перегретый водяной пар, жидкости, не являющиеся электролитами, а также расплавы органических и неорганических веществ, в том числе металлов. Наиболее часто химической коррозии подвергается металлургическое оборудование, сопла реактивных двигателей, детали газовых турбин и двигателей внутреннего сгорания, оболочки ракет и космических кораблей, т. е. изделия, работающие при высоких температурах.
Скорость коррозии
Скорость коррозии металлов и металлических покрытий в атмосферных условиях определяется комплексным воздействием ряда факторов: наличием на поверхности фазовых и адсорбционных пленок влаги, загрязненностью воздуха коррозионно-агрессивными веществами, изменением температуры воздуха и металла, образованием продуктов коррозии и так далее.
Оценка и расчет скорости коррозии должны основываться на учете продолжительности и материальном коррозионном эффекте действия на металл наиболее агрессивных факторов.
В зависимости от факторов, влияющих на скорость коррозии, целесообразно следующее подразделение условий эксплуатации металлов, подвергаемых атмосферной коррозии:
Закрытые помещения с внутренними источниками тепла и влаги (отапливаемые помещения);
Закрытые помещения без внутренних источников тепла и влаги (неотапливаемые помещения);
Открытая атмосфера.
Классификация коррозионных процессов по типу разрушений
Наиболее часто встречаются следующие виды коррозии металлов:
1. Равномерная – охватывает всю поверхность равномерно
4. Местная пятнами – корродируют отдельные участки поверхности
5. Язвенная (или питтинг)
7. Межкристаллитная – распространяется вдоль границ кристалла металла
Защита от коррозии
Основные способы защиты металлов от коррозии
Для защиты металлов от коррозии применяются различные способы, которые условно можно разделить на следующие основные направления: легирование металлов; защитные покрытия; электрохимическая защита; изменение свойств коррозионной среды; рациональное конструирование изделий.
Легирование металлов. Это эффективный метод повышения коррозионной стойкости металлов. При легировании в состав сплава или металла вводят легирующие элементы (хром, никель, молибден и др.), вызывающие пассивность металла. Пассивацией называют процесс перехода металла или сплава в состояние его повышенной коррозионной устойчивости, вызванное торможением анодного процесса. Пассивное состояние металла объясняется образованием на его поверхности совершенной по структуре оксидной пленки (оксидная пленка обладает защитными свойствами при условии максимального сходства кристаллических решеток металла и образующегося оксида).
Широкое применение нашло легирование для защиты от газовой коррозии. Легированию подвергаются железо, алюминий, медь, магний, цинк, а также сплавы на их основе. В результате чего получаются сплавы с более высокой коррозионной стойкостью, чем сами металлы. Эти сплавы обладают одновременно жаростойкостью и жаропрочностью.
Жаростойкость – стойкость по отношению к газовой коррозии при высоких температурах. Жаропрочность – свойства конструкционного материала сохранять высокую механическую прочность при значительном повышении температуры. Жаростойкость обычно обеспечивается легированием металлов и сплавов, например, стали хромом, алюминием и кремнием. Эти элементы при высоких температурах окисляются энергичнее, чем железо, и образуют при этом плотные защитные пленки оксидов.
Легирование также используется с целью снижения скорости электрохимической коррозии, особенно коррозии с выделением водорода. К коррозионностойким сплавам, например, относятся нержавеющие стали, в которых легирующими компонентами служат хром, никель и другие металлы.
Защитные покрытия. Слои, искусственно создаваемые на поверхности металлических изделий для защиты их коррозии, называются защитными покрытиями. Нанесение защитных покрытий – самый распространенный метод борьбы с коррозией. Защитные покрытия не только предохраняют изделия от коррозии, но и придают поверхностям ряд ценных физико-химических свойств. Они подразделяются на металлические и неметаллические. Общими требованиями для всех видов защитных покрытий являются высокая адгезионная способность, сплошность и стойкость в агрессивной среде.
Металлические покрытия. Металлические покрытия занимают особое положение, так как их действие имеет двойственный характер. До тех пор, пока целостность слоя покрытия не нарушена, его защитное действие сводится к изоляции поверхности защищаемого металла от окружающей среды. Это не отличается от действия любого механического защитного слоя (окраска, оксидная пленка и т.д.). Металлические покрытия должны быть непроницаемы для коррозионных агентов.
При повреждении покрытия образуется гальванический элемент. Характер коррозионного разрушения основного металла определяется электрохимическими характеристиками обоих металлов. Защитные антикоррозионные покрытия могут быть катодными и анодными. К катодным покрытиям относятся покрытия, потенциалы которых в данной среде имеют более положительное значение, чем потенциал основного металла. Анодные покрытия имеют наиболее отрицательный потенциал, чем потенциал основного металла.
При повреждении никелевого покрытия на анодных участках происходит процесс окисления железа вследствие возникновения микрокоррозионных гальванических элементов. На катодных участках - восстановление водорода. Следовательно, катодные покрытия могут защищать металл от коррозии лишь при отсутствии пор и повреждения покрытия.
Местное повреждение защитного цинкового слоя ведет к дальнейшему его разрушению, при этом поверхность железа защищена от коррозии. На анодных участках происходит процесс окисления цинка. На катодных участках - восстановление водорода.
Электродные потенциалы металлов зависят от состава растворов, поэтому при изменении состава раствора может меняться и характер покрытия.
Для получения металлических защитных покрытий применяются различные способы:электрохимический(гальванические покрытия);погружение в расплавленный металл(горячее цинкование, лужение);металлизация(нанесение расплавленного металла на защищаемую поверхность с помощью струи сжатого воздуха);химический(получение металлических покрытий с помощью восстановителей, например гидразина).
Методы защита от коррозии
На скорость коррозии влияют как внутренние факторы (наличие дефектов кристаллической решетки металла, механические напряжения и др.), так и внешние: температура, природа и состав электролита. С повышением температуры скорость коррозии, как и большинства химических реакций, возрастает. Усиливают коррозию содержащаяся в атмосфере промышленных городов пыль, SO2, СO2 и другие газы. Поэтому в городах коррозия протекает в 5-10 раз быстрее, чем в сельской местности. Ионы присутствующие в морской воде, являются катализаторами коррозии железа и его сплавов, так как адсорбируясь на поверхности металла, разрушают или препятствуют образованию на нем защитных слоев. Кроме того, скорость коррозии двух контактирующих металлов будет тем больше, чем больше разность потенциалов этих металлов. Полностью предотвратить процессы коррозии металлов практически не удается, однако существуют способы защиты металлов от коррозии.
1. Изменение коррозионной среды - этот метод пригоден для тех случаев, когда защищаемые изделия эксплуатируются в небольшом объеме. Суть метода состоит в удалении из электролита растворенного кислорода или добавлении к этому раствору веществ, замедляющих коррозию - ингибиторов.
2. Легирование металлов. Это введение в состав сплавов компонентов, повышающих химическую стойкость. Наибольшее применение находят нержавеющие стали, в состав которых входит хром , до 15 % и никель, до 10 %. Кроме того, в качестве легирующих компонентов используют марганец, кремний, вольфрам, молибден, титан и другие металлы.
3. Неметаллические покрытия . Механически защищают металлы от коррозии, изолируя их от влияния внешней среды. Неметаллические покрытия делятся на неорганические и органические. Из неорганических покрытий наиболее распространены оксидные и фосфатные пленки. Так, при кипячении железа в растворе солей фосфорной кислоты получают фосфатные пленки, хорошо защищающие от коррозии в атмосфере. Среди органических, покрытий наиболее распространенными являются масляные краски, лаки, полимерные пленки. Лакокрасочные покрытия - самый дешевый метод защиты от коррозии.
4. Металлические покрытия. По характеру защитного действия различают анодные и катодные покрытия. Аноднымявляется покрытие металлом, электродный потенциал которого меньше, чем у защищаемого металла. Покрытие из металла менее активного (с большим электродным потенциалом), чем защищаемый металл, называется катодным.Если покрытие не нарушено и полностью изолирует основной металл от воздействия окружающей среды, принципиального различия между анодными и катодными покрытиями нет. При нарушении слоя защищающего металла возникают коррозионные гальванические элементы, в которых защищаемый металл может играть роль или инертного катода, или активного анода.
5. Электрохимическая защита:
а) катодная защита. Защищаемую конструкцию присоединяют к катоду внешнего источника тока, в результате она становится катодом, не окисляется, на ней идет восстановление компонентов среды. В качестве анода применяют любой металлический лом, который присоединяют к аноду внешнего источника тока. Таким способом защищают, например, подземные трубопроводы;
б) протекторная защита. Защищаемый металл соединяют с более активным металлом, имеющим меньший электродный потенциал. Последний служит анодом, растворяется и защищает основной металл.
Для более активной защиты металлических конструкций можно совмещать несколько способов защиты от коррозии, например, покрытие и катодную электрозащиту.
Заключение
Металлы составляют одну из основ цивилизации на планете Земля. Их широкое внедрение в промышленное строительство и транспорт произошло на рубеже XVIII-XIX. В это время появился первый чугунный мост, спущено на воду первое судно, корпус которого был изготовлен из стали, созданы первые железные дороги. Начало практического использования человеком железа относят к IX веку до нашей эры. Именно в этот период человечество перешло из бронзового века в век железный.
В XXI веке высокие темпы развития промышленности, интенсификация производственных процессов, повышение основных технологических параметров (температура, давление, концентрация реагирующих средств и др.) предъявляют высокие требования к надежной эксплуатации технологического оборудования и строительных конструкций. Особое место в комплексе мероприятий по обеспечению бесперебойной эксплуатации оборудования отводится надежной защите его от коррозии и применению в связи с этим высококачественных химически стойких материалов.
Необходимость осуществления мероприятий по защите от коррозии диктуется тем обстоятельством, что потери от коррозии приносят чрезвычайно большой ущерб. По имеющимся данным, около 10% ежегодной добычи металла расходуется на покрытие безвозвратных потерь вследствие коррозии и последующего распыления. Основной ущерб от коррозии металла связан не только с потерей больших количеств металла, но и с порчей или выходом из строя самих металлических конструкций, т.к. вследствие коррозии они теряют необходимую прочность, пластичность, герметичность, тепло- и электропроводность, отражательную способность и другие необходимые качества. К потерям, которые терпит народное хозяйство от коррозии, должны быть отнесены также громадные затраты на всякого рода защитные антикоррозионные мероприятия, ущерб от ухудшения качества выпускаемой продукции, выход из строя оборудования, аварий в производстве и так далее.
Защита от коррозии является одной из важнейших проблем, имеющей большое значение для народного хозяйства.
Коррозия является физико-химическим процессом, защита же от коррозии металлов – проблема химии в чистом виде.
Коррозия и защита металлов
1. Общие сведения. Классификация коррозии. Современные коррозионностойкие конструкционные сплавы
Коррозией металлов называют самопроизвольное разрушение металлических конструкций вследствие их химического или электрохимического взаимодействия с окружающей средой.
Коррозионный процесс протекает на границе двух фаз: металл– окружающая среда, т. е. является гетерогенным процессом.
Коррозия металлов наносит огромный ущерб практически любой отрасли промышленности. Потери от коррозии можно разделить на две группы: прямые и косвенные.
Прямые потери складываются в основном из потерь непосредственно самого металла вследствие коррозии.
Косвенные потери огромны и обусловлены расходами, связанными с отказом в работе оборудования, его простоем, со стоимостью ремонта и заменами деталей оборудования, с утечками нефти, газа через повреждения в трубопроводах и т. п.
С химической точки зрения металлы являются восстановителями. Они легко отдают валентные электроны и образуют положительно заряженные ионы. Во всех соединениях они проявляют только положительные степени окисления. Многие металлы, например, железо, хром, марганец, имеют переменные степени окисления. Восстановительные свойства металлов различны и определяются их стандартным электродным потенциалом. В табл. 1 приведены электродные потенциалы для металлов.
По своей химической активности и положению в ряду стандартных потенциалов металлы делятся на три группы:
- активные – от Li до Al включительно – вытесняют водород из воды и растворов кислот;
- средней активности – от Mn до Pb включительно – вытесняют водород из растворов кислот;
- неактивные – стоящие в ряду после водорода – не вытесняют водород из растворов кислот.
Все эти металлы могут самопроизвольно окисляться. Следовательно, основной причиной коррозии металлов в атмосфере или других средах является их термодинамическая нестабильность. Степень
термодинамической нестабильности металла зависит от его природы, характера коррозионной среды и конкретных условий.
Таблица 1. Ряд стандартных электродных потенциалов металлов
способности (М n+ )
способности (М о )
Основной причиной, вызывающей коррозионное разрушение металлов и сплавов, является протекание на их поверхности электрохимических или химических реакций.
В зависимости от характера этих реакций и механизма протекания, все коррозионные процессы делят на два вида:
- химической коррозией называют процессы, протекающие при непосредственном химическом взаимодействии между металлом и агрессивной средой и не сопровождающиеся возникновением электрического тока;
- электрохимической коррозией называют процессы взаимодействия металлов с водными растворами электролитов, сопровождающиеся возникновением в системе электрического тока, то есть упорядоченным передвижением электронов и ионов от одного участка металла к другому.
По условиям протекания коррозии, различают несколько видов коррозии:
- газовую – коррозию в газах при высоких температурах;
- атмосферную – коррозию в воздухе или влажном газе;
- жидкостную – коррозию в жидкой среде (в растворах неэлектролитов и электролитов);
- подземную – коррозию в почвах и грунтах;
- биокоррозию – коррозию под влиянием жизнедеятельности микроорганизмов;
- структурную – коррозию, связанную со структурной неоднородностью металла;
- коррозию блуждающими токами;
- контактную – электрохимическую коррозию, вызванную контактом металлов, имеющих разные электродные потенциалы в данном электролите;
- щелевую – коррозию в щелях и зазорах между металлами;
- под напряжением – коррозию при одновременном воздействии коррозионной среды и механических напряжений;
- коррозионную кавитацию – разрушение металла, вызванное одновременным коррозионным и ударным воздействием внешней среды.
По характеру коррозионных разрушений различают следующие виды коррозии:
- сплошную, или общую, коррозию, охватывающую всю поверхность металла, находящуюся под воздействием коррозионной среды. Она бывает: равномерной, неравномерной, избирательной;
- местную коррозию, охватывающую отдельные участки металла. Она бывает: точечной (питтинг), сквозной, язвенной и др.
2. Методы защиты металлов от коррозии
Для защиты металлов от коррозии применяются различные методы: легирование металлов, обработка коррозионной среды, электрохимическая защита, нанесение металлических и неметаллических покрытий.
Легирование металлов позволяет получать коррозионностойкие сплавы, превосходящие по стойкости основной металл. Примерами могут служить сплавы меди (латунь и бронза), ее легирование алюминием для повышения коррозионной стойкости в атмосферных условиях; легирование стали хромом и никелем с целью создания хромоникелевых сплавов.
Обработку коррозионной среды выполняют с целью уменьшения ее агрессивного воздействия на металл. Однако такая обработка целесообразна при небольших объемах электролитов. Обработка среды заключается во введении в среду ингибиторов коррозии или в уменьшении содержания деполяризатора в электролитах.
Ингибиторы коррозии, введенные в коррозионную среду в малых количествах, полностью предотвращают коррозию металлов или значительно снижают ее скорость. В зависимости от характера среды ингибиторы выступают как замедлители кислотной или щелочной коррозии, коррозии в нейтральных растворах, в неводных средах. В основном, ингибиторы являются органическими соединениями.
Электрохимическая защита подразделяется на катодную и анодную защиту. Катодная защита подразделяется на защиту внешним током и протекторную защиту.
Механизм защиты внешним током (рис. 1) сводится к тому, что за счет внешней катодной поляризации защищаемому металлу навязывают потенциал, при котором его коррозия замедляется. Суть этого способа заключается в том, что защищаемую конструкцию подсоединяют к отрицательному полюсу внешнего источника постоянного тока, а к положительному полюсу подсоединяют электрод, которым может являться металлолом, а именно отрезок стальной трубы, рельсы и т. п. (рис. 1).
Протекторная защита (рис. 2) состоит в том, что к защищаемой конструкции подсоединяют металл или сплав, электродный потенциал которого более электроотрицателен, чем потенциал металла защищаемой конструкции. В качестве протекторов обычно используют цинк или сплавы цинка с алюминием. Иногда применяют сплавы на основе магния. Протекторы применяют для защиты металлических конструкций от коррозии в морской воде, других нейтральных коррозионных средах, а также в почве.
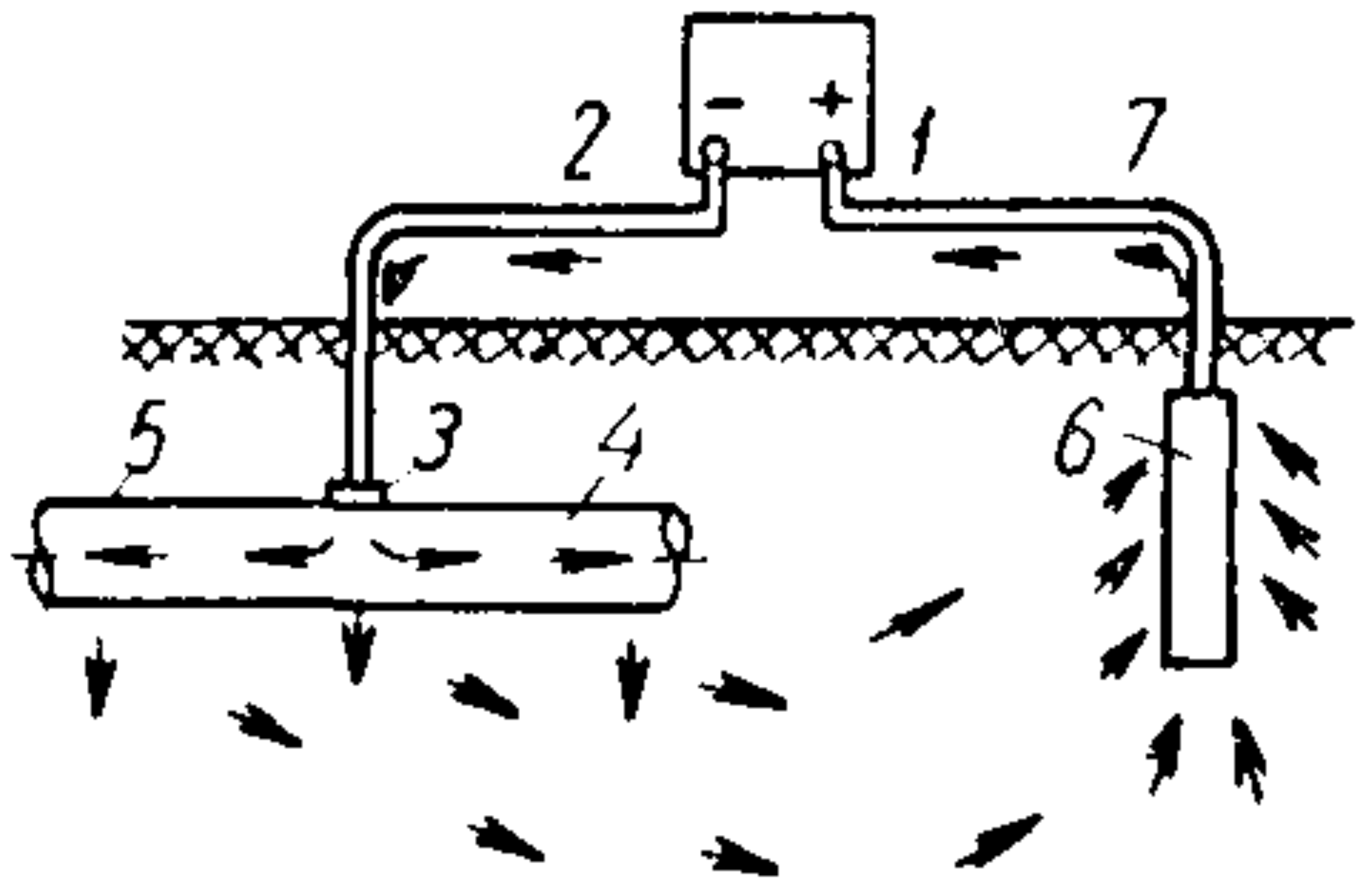
Рис. 1. Схема катодной защиты внешним током: 1 – источник постоянного тока; 2 – соединительный провод; 3 – пункт дренажа; 4 – защищаемая труба; 5 – изолирующее покрытие; 6 – анодное заземление; 7 – соединительный провод
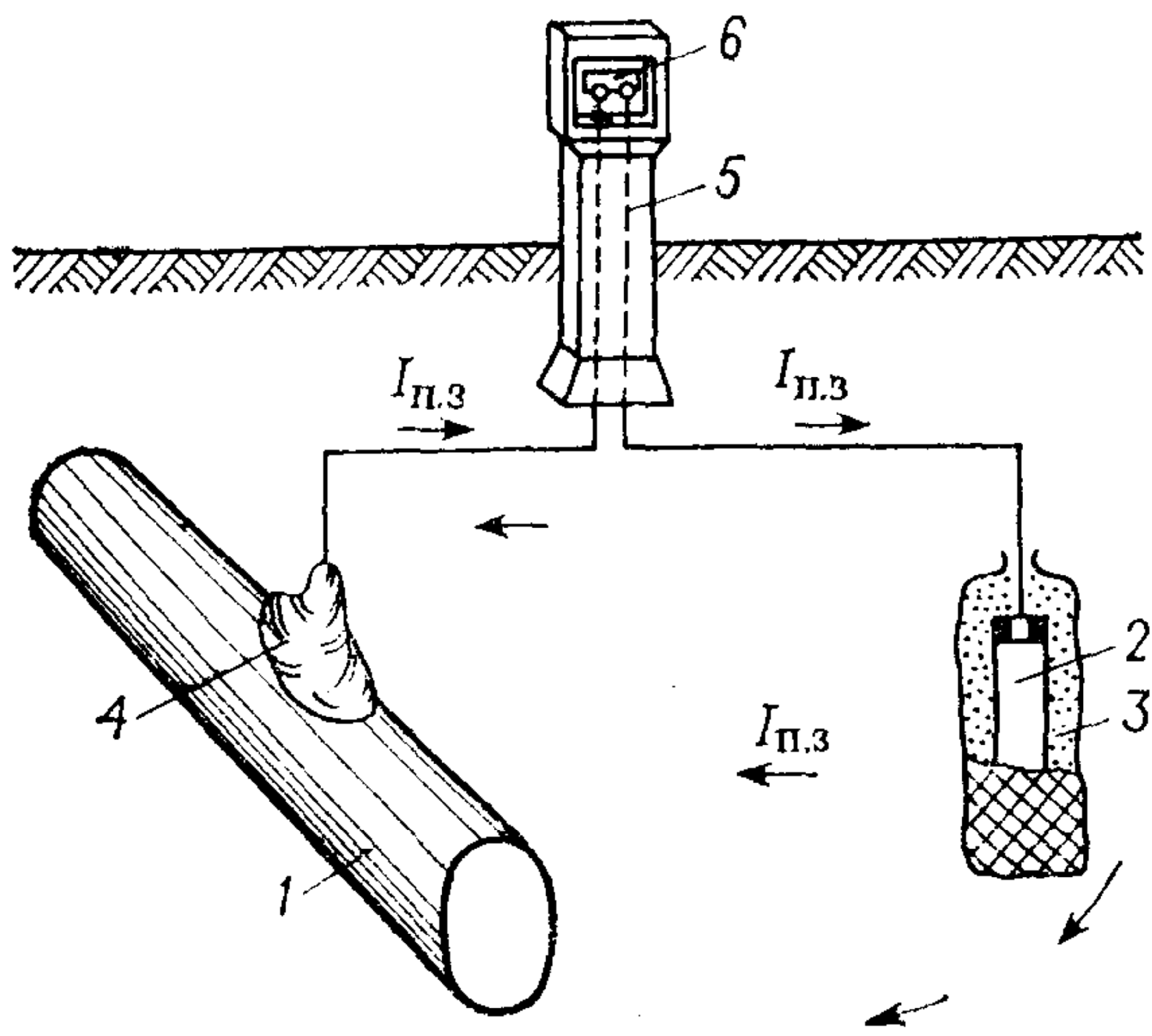
Рис. 2. Схема протекторной защиты: 1 – подземная стальная конструкция; 2 – протектор–магниевый сплав; 3 – заполнитель; 4 – электрический контакт; 5 – контрольно-измерительный вывод; 6 – закороченные клеммы; Iп.з – сила тока протекторной защиты
Защита металлическими и неметаллическими покрытиями. Для защиты металлов от коррозии используют различные виды покрытий: металлические, лакокрасочные и полимерные покрытия и покрытия, образованные в результате химической или электрохимической обработки поверхности металла. Роль любого покрытия сводится в основном к изоляции металла от внешней среды.
Выбор типа покрытия зависит от условий, в которых следует использовать металл. Для защиты изделий, не подвергающихся механическим воздействиям и применяющимся в сухих жилых помещениях, обычно бывает достаточно однослойного лакокрасочного покрытия или соответствующей химической обработки поверхности металла: оксидирования или фосфатирования. Для защиты металлических конструкций (железнодорожные мосты, подъемные краны и т. п.), а также железнодорожных вагонов, наружных деталей автомобилей, велосипедов и др., подвергающихся воздействию влажной атмосферы, применяют сложные по составу и способу нанесения лакокрасочные покрытия.
3. Коррозионностойкие металлы и сплавы
Под понятием коррозионностойкие металлы и сплавы понимают конструкционные материалы, которые в агрессивных коррозионных средах обладают достаточной коррозионной стойкостью и жаростойкостью и могут быть использованы без специальных средств противокоррозионной защиты.
При этом коррозионная стойкость конструкционного материала заключается не только в сохранении его основной массы, но и выполнении функциональных нагрузок самой металлической конструкцией.
Характеристика степени термодинамической стабильности различных металлов приближенно может быть сделана по величине стандартных электродных потенциалов: чем более электроотрицателен потенциал металла, тем он активнее (табл. 2).
Таблица 2. Стандартные электродные потенциалы
Величины электродных потенциалов –0,414 В и +0,815 В представляют собой значения равновесных потенциалов водородного и кислородного электродов в нейтральной среде.
Некоторые металлы, например, железо, алюминий, титан, хром, никель, относительно устойчивы благодаря наступлению пассивного состояния. Пассивное состояние поверхности металла нарушается при наличии в растворе некоторых активных ионов (ионы хлора, брома, фтора) и, наоборот, усиливается при наличии окислителей. Часть металлов устойчива вследствие возникновения малорастворимых и достаточно плотных пленок на поверхности из продуктов коррозии. Некоторые металлы коррозионностойки из-за отсутствия примесей, образующих эффективные катоды, так как наличие загрязнений может привести к образованию коррозионных микрогальванических элементов.
Теория коррозионностойкого легирования металлов, устойчивых к электрохимической коррозии, основывается на учении о контролирующих факторах коррозии – омическом, катодном и анодном торможении процесса коррозии.
На основе этих факторов разработаны три направления повышения коррозионной устойчивости сплавов:
- Создание сплавов, образующих более совершенный защитный слой продуктов коррозии на своей поверхности. В металл вводят компоненты, способствующие образованию плотной защитной пленки на поверхности металла. Торможение коррозии достигается как за счет увеличения омического сопротивления, так и за счет экранирующего слоя, тормозящего доставку к металлической поверхности веществ, необходимых для протекания катодного процесса или удаление продуктов электродной реакции. Например, при легировании железа медью наступает пассивное состояние железа, но этот метод имеет ограниченное применение, так как при электрохимической коррозии трудно достичь полного экранирования поверхности.
- Уменьшение катодной активности металлов. Защитные свойства металлов повышаются вследствие уменьшения площади микрокатодов или увеличения на них перенапряжения выделения водорода, т. е. происходит торможение катодного процесса. При легировании железа сурьмой, висмутом, мышьяком увеличивается перенапряжение выделения водорода.
- Снижение анодной активности металлов. Защитные свойства металлов повышаются в результате уменьшения активности анодной фазы путем введения компонентов, повышающих или термодинамическую устойчивость сплава, или его пассивность. Повышение коррозионной стойкости, например, стали, достигается легированием ее хромом; хромом и никелем; хромом, никелем и небольшими добавками палладия.
Какой из приведенных методов повышения коррозионной устойчивости сплавов надежнее и перспективнее, можно определить, исходя из конкретных условий.
При кислотной коррозии в восстановительных средах с выделением водорода и в отсутствии возможности повышения склонности к пассивированию весьма полезными могут оказаться методы уменьшения катодной активности сплавов или повышения термодинамической устойчивости анодной фазы. В условиях возможности установления пассивного состояния, наоборот, совершенно неэффективны методы снижения катодной активности, а окажутся полезными все методы, снижающие анодную активность сплавов.
При возможности установления пассивного состояния сплава эффективен метод введения активных катодов. Однако этот метод окажется вредным, если по условиям коррозии (восстановительная среда, наличие ионов хлора) установление стойкого пассивного состояния невозможно.
Повышение коррозионной стойкости металлов в кислотах достигается кислотостойким легированием. Коррозия металлов в кислотах с неокисляющимся анионом (разбавленная серная кислота, соляная кислота) протекает, в основном, с водородной деполяризацией. При коррозии в окисляющих кислотах (азотная кислота, концентрированная серная кислота) основным катодным процессом является восстановление аниона кислоты.
Коррозионную стойкость сплавов в окисляющих кислотах можно повысить, вводя легкопассивирующиеся металлы, например, хром. Сталь, легированная хромом, имеет повышенную стойкость в азотной кислоте. Стойкость металлов в кислотах, в которых возможно наступление пассивного состояния, повышается также в результате легирования металлами, являющимися эффективными катодами. Так, легирование стали типа Х18Н10 палладием повышает стойкость сплава в серной кислоте.
Для повышения коррозионной стойкости в неокисляющих кислотах сплавы легируют молибденом и медью. Кислотостойкость молибдена объясняется его склонностью к пассивированию и образованию защитных пленок.
Кислотостойкость меди связана с ее термодинамической устойчивостью в условиях коррозии с водородной деполяризацией. При коррозии легированных медью сплавов их поверхность обогащается медью вследствие ее более высокой коррозионной стойкости.
Коррозия. Виды и способы защиты от коррозии
Коррозия – это процесс самопроизвольного разрушения металлов, сплавов и других материалов – бетонов, цементов в результате физико-химического взаимодействия с окружающей средой.
Среда, в которой происходит разрушение металлов, называется коррозионной. Химические соединения, образующиеся в результате коррозии, называются продуктами коррозии. Способность металлов сопротивляться коррозии воздушной среды называется коррозионной стойкостью.
Коррозия материалов является одной из важных мировых проблем. Практика показывает, что только прямые безвозвратные потери металла от коррозии составляют 10…12% всей производимой стали, при этом суммарный ущерб в промышленных странах достигает 4-5% от национального дохода. Ведь корродирует не только черный металл ( сталь, чугун, железо и некоторые его сплавы ), но и бетон, дерево, камень, даже полимеры.
Наиболее интенсивная коррозия наблюдается в зданиях и сооружениях химических производств, что объясняется действием различных газов, жидкостей и мелкодисперсных частиц непосредственно на строительные конструкции, оборудование и сооружения, а также проникновением этих агентов в грунты и действием их на фундаменты. Агрессивному воздействию подвержено до 75% строительного фонда. Коррозия металла приводит к ослаблению конструктива и, как следствие, снижению безопасности эксплуатации сооружений.

По характеру самого процесса коррозию разделяют на две основные группы: химическую и электрохимическую.
Химическая коррозия протекает в не электролитах – жидкостях, не проводящих электрического тока и в сухих газах при высокой температуре.
Электрохимическая коррозия происходит в электролитах и во влажных газах и характеризуется наличием двух параллельно идущих процессов: окислительного (растворение металлов) и восстановительного (выделение металла из раствора).
По внешнему виду коррозию различают: пятнами, язвами, точками, внутрикристаллитную, подповерхностную.
По характеру коррозионной среды различают следующие основные виды коррозии: газовую, атмосферную, жидкостную и почвенную.
Газовая коррозия происходит при отсутствии конденсации влаги на поверхности. На практике такой вид коррозии встречается при эксплуатации металлов при повышенных температурах.
Атмосферная коррозия относится к наиболее распространенному виду электрохимической коррозии, так как большинство металлических конструкций эксплуатируются в атмосферных условиях. Коррозия, протекающая в условиях любого влажного газа, также может быть отнесена к атмосферной коррозии.
Жидкостная коррозия в зависимости от жидкой среды бывает кислотная, щелочная, солевая, морская и речная. По условиям воздействия жидкости на поверхность металла эти виды коррозии получают добавочные характеристики : с полным и переменным погружением, капельная, струйная. Кроме того, по характеру разрушения различают коррозию равномерную и неравномерную.
По степени воздействия на металлы коррозионные среды делятся на неагрессивные, слабоагрессивные, среднеагрессивные и сильноагрессивные.
В атмосферных условиях железо и сталь подвергаются общей равномерной коррозии.
- коррозия в растворах электролитов – жидкостях, проводящих электрический ток;
- почвенная или подземная коррозия металлических сооружений, находящихся под землей;
- биологическая коррозия – это коррозия, протекающая под влиянием жизнедеятельности микроорганизмов.
По видам дополнительных воздействий различают следующие случаи коррозии:
- электрокоррозия под действием внешнего источника тока, т.е. коррозия изделий, находящихся под землей, вызванная блуждающими токами;
- контактная коррозия металлов – разрушение металла в растворе электролита вследствие контакта с другим металлом, имеющим более положительный электродный потенциал, чем потенциал основного металла.
- радиационная коррозия – это процессы коррозии в условиях радиоактивного облучения;
- коррозия в условиях механического воздействия .
Наиболее типичными видами подобного разрушения являются коррозионные растрескивание, усталость, кавитация, эрозия и фреттинг-коррозия
Бетон и железобетон находят широкое применение в качестве конструкционного материала при строительстве зданий и сооружений химических производств. Но они не обладают достаточной химической стойкостью против действия кислых сред. Свойства бетона и его стойкость в первую очередь зависит от химического состава цемента из которого он изготовлен.
Наибольшее применение в конструкциях и оборудовании находят бетоны на портландцементе. Причиной пониженной химической стойкости бетона к действию минеральных и органических кислот является наличие свободной гидроокиси кальция (до 20%), трехкальциевого алюмината (3CaO×Al2O3) и других гидратированных соединений кальция.
Коррозия бетона происходит тем интенсивнее, чем выше концентрация водных растворов кислот. При повышенных температурах агрессивной среды коррозия бетонов ускоряется. Несколько более высокой кислотостойкостью обладает бетон, изготовленный на глиноземистом цементе, из-за пониженного содержания оксида кальция.
Кислотостойкость бетонов на цементах с повышенным содержанием оксида кальция в некоторой степени зависит от плотности бетона. При большей плотности бетона кислоты оказывают на него несколько меньшее воздействие из-за трудности проникновения агрессивной среды внутрь материала.
Щелочестойкость бетонов определяется главным образом химическим составом вяжущих, на которых они изготовлены, а также щелочестойкостью мелких и крупных заполнителей.
Увеличение срока службы строительных конструкций и оборудования достигается путем правильного выбора материала с учетом его стойкости к агрессивным средам, действующим в производственных условиях. Кроме того, необходимо принимать меры профилактического характера.
К таким мерам относятся:
- герметизация производственной аппаратуры и трубопроводов, хорошая вентиляция помещения, улавливание газообразных и пылевидных продуктов, выделяющихся в процессе производства;
- правильная эксплуатация различных сливных устройств, исключающая возможность проникновения в почву агрессивных веществ;
- применение гидроизолирующих устройств и др.
Непосредственная защита металлов от коррозии осуществляется нанесением на их поверхность неметаллических и металлических покрытий либо изменением химического состава металлов в поверхностных слоях:
- оксидированием,
- азотированием,
- фосфатированием.
Для защиты поверхностей от коррозии существуют разнообразные покрытия:
- лакокрасочные (антистатичные и армированные, полиуретановые, акриловые, порошковые эпоксидно – полиэфирные, органосиликатные и кремнийорганические),
- металлизационные с цинком, алюминием, медью и комбинациями этих металлов.
Это краски, лаки, эмали, тонкодисперсные порошки, пленки.
Лакокрасочные покрытия вследствие экономичности, удобства и простоты нанесения, хорошей стойкости к действию промышленных агрессивных газов нашли широкое применение для защиты металлических и железобетонных конструкций от коррозии.
Защитные свойства лакокрасочного покрытия в значительной степени обуславливаются механическими и химическими свойствами, сцеплением пленки с защищаемой поверхностью.
Лакокрасочные материалы в зависимости от назначения и условий эксплуатации делятся на десять групп:
- А – покрытия стойкие на открытом воздухе;
- АН – то же, под навесом;
- П – то же, в помещении;
- Х – химически стойкие;
- Т – термостойкие;
- М – маслостойкие;
- В – водостойкие;
- ХК – кислотостойкие;
- ХЩ – щелочестойкие;
- Б – бензостойкие.
Наиболее распространены в промышленности покрытия металлические, неметаллические (органического и неорганического происхождения), а также покрытия, образованные в результате химической и электрохимической обработки металла.
Выбор вида покрытия зависит от условий, в которых используется защищаемое изделие (перепад температур, повышенная влажность, морская или пресная вода, щелочь, кислота, соли металлов, радиация, электроток и огонь), и технологичность возможностей формирования покрытия.
Наиболее часто применяемые способы защиты металлов:
- легирование;
- электрохимическая защита;
- покрытие металлами;
- защитные пленки.
Легирование – это введение в металл на стадии его производства определенного количества специальных добавок, например – хрома или марганца. Это придает сталям особые свойства, необходимые для использования в сложных условиях. Для возведения современных зданий, особенно повышенной этажности, необходима высококачественная атмосферостойкая легированная сталь, например, погодоустойчивая марка COR-TEN. Такой материал позволяет решить проблемы эксплуатации сооружений даже в экстремальных климатических условиях.
Одними из самых популярных и относительно недорогих мер защиты от коррозии сегодня являются методы, изменяющие химический состав металла в поверхностных слоях. Как правило, это электрохимические способы нанесения покрытий на металл. Наиболее известный процесс называется оцинковкой, которая в зависимости от способа обработки металла делится на горячую и холодную.
В первом случае обрабатываемый материал погружается в специальную ванну. Затем под воздействием переменного тока осуществляется его обработка в растворе фосфата цинка при плотности тока 4 А/дм², напряжении 20 В и температуре 600-700ºС. В результате электрохимической реакции образуется ферроцинковый сплав. При применении второго способа на подготовленную поверхность стального листа наносится защитный слой из цинка. Оцинковка толщиной 0,3 мм позволяет обеспечить защиту обработанной поверхности металла более чем на 30 лет.
Итальянская фирма «Metalnastri» разработала метод, сочетающий в себе качество горячего и технологичность холодного цинкования. Это простая идея наклейки цинковой фольги на стальную поверхность. Высокую антикоррозийность создает сплошной цинковый слой, а токопроводящие клеевые композиции обеспечивают и электрохимическую защиту поверхности.
ЦНИИПСК им. А.П. Мельникова предложил метод термодиффузионного цинкования (ТДЦ) метизных и малогабаритных изделий из стали и чугуна. Метод заключается в нагреве металлоизделий в среде, содержащей порошок цинка. В результате на поверхности изделия образуется цинковое покрытие с хорошими защитными и декоративными свойствами.
Технологический процесс такого цинкования экологически чист и практически безотходен. В качестве сырья используются отечественные материалы, не требующие специальной обработки. ТДЦпокрытие обладает высокой адгезией и износостойкостью, обеспечиваемой в результате взаимной диффузии железа и цинка. Срок службы покрытия в 1,5-4 раза больше по сравнению с традиционными цинковыми покрытия.
Широкое распространение цинковых покрытий обусловлено их хорошими химическими свойствами. Для стали (катод) цинк является анодом, за счет этого образуется гальваническая пара, имеющая высокие защитные свойства, хорошо сохраняемые даже при малой толщине слоя. Скорость разрушения цинкового покрытия составляет примерно 1-10 мкм в год в зависимости от различных факторов. Оцинковка может осуществляться совместно с другими металлами – с добавлением алюминия (Al) или железа (Fe). В настоящее время в России широко используется сталь Galfan c цинкоалюминиевым покрытием и сталь Galvannealed с цинкожелезным покрытием.
При покрытии другими металлами в зависимости от вида коррозии покрывающий слой наносят различными способами. В качестве покрывающего материала часто используется хром или никель. Хромирование – электролитическое нанесение покрытия из хрома на поверхность металлического изделия. Никелирование, также нанесение на поверхность изделий никеля толщиной от 2 до 50 мкм.
На практике обычно применяются следующие методы:
- Погружение изделий в расплавленный металл (горячий способ). Заключается в том, что изделия погружают в ванну с расплавленным металлом или же нагретую поверхность деталей обволакивают расплавленным металлом.
- Метод термической диффузии. Основан на диффузии (проникновении) в поверхностные слои деталей присадок при высокой температуре. Диффузионные покрытия наносятся при нагреве деталей в твердой (порошкообразной), жидкой или газообразной фазе металла.
- Металлизация. Заключается в нанесении (распылении) на поверхность деталей слоя присадок расплавленного металла с помощью пульверизаторов.
- Контактный метод осаждения металла. Осуществляется без применения внешнего источника тока за счет вытеснения менее благородными металлами более благородных из растворов их солей. Толщина таких покрытий невелика и защитные свойства их невысоки.
Следует отметить, что металлические покрытия достаточно хорошо защищают металл от коррозии. Однако при нарушении защитного слоя она может протекать даже более интенсивно, чем без покрытия. Поэтому в промышленности для улучшения свойств металлических поверхностей, обработанных электротехническим методом, используется способ нанесения защитных покрытий из полимерных материалов. Такие продукты получили широкое распространение в строительной индустрии.
Использование полимерных материалов для антикоррозионной защиты обусловлено их уникальными физико-химическими показателями. Полимеры имеют небольшой удельный вес, высокую стойкость к не механическим воздействиям (соприкосновение с водой, солями, щелочами или кислотами). Обладают пластичностью и светостойкостью. В настоящее время наибольшее распространение получили « трехслойные» продукты с двойным уровнем защиты.
Первый уровень – непосредственно оцинковка, второй – полимер. Благодаря такой структуре сталь становится стойкой к воздействию агрессивных сред, механическим повреждениям и ультрафиолетовому изучению. Срок их службы составляет порядка 50 лет, в зависимости от качества и толщины покрытия. Необходимо также учесть, что высокие эксплуатационные характеристики таких материалов напрямую зависят от качества оцинковки исходного металла, а потребительские качества – от применяемого в составе полимера.
Альтернативой полимерным материалам являются конструкционные пластмассы и стеклопластики, получаемые на основе различных синтетических смол и стекловолокнистых наполнителей. В настоящее время выпускается значительный ассортимент материалов, особое место среди них занимает полиэтилен. Он инертен во многих кислотах, щелочах и растворителях, а также имеет высокую теплостойкость.
Другим направлением использования полиэтилена в качестве химически стойкого материала является порошковое напыление. Применение полиэтиленовых покрытий объясняется их дешевизной и хорошими защитными свойствами. Покрытия легко наносятся на поверхность различными способами, в том числе пневматическим и электростатическим распылением.
Защитные пленки. Способ заключается в нанесении на металл защитной оболочки из различных компонентов в следующей последовательности: шпатлевка, грунтовка, краска, лак или эмаль.
Для противокоррозионной защиты конструкций зданий и сооружений (ферм, ригелей, балок, колонн, стеновых панелей), а также наружных и внутренних поверхностей емкостного технологического оборудования, трубопроводов, газоводов, воздуховодов вентиляционных систем, которые в процессе эксплуатации не подвергаются механическим воздействиям абразивных частиц, применяют лакокрасочные покрытия. Такие покрытия наиболее эффективны для защиты от атмосферной коррозии. Однако срок службы лакокрасочных покрытий невелик и составляет 4-5 лет. Для повышения коррозионной стойкости лакокрасочных покрытий используют различные противокоррозионные пигменты.
Следует назвать антикоррозионные пигменты фирмы SNCZ (Франция): фосфаты цинка; модифицированные фосфаты цинка; фосфаты, не содержащие цинк; полифосфаты; феррит кальция, а также тетраоксихромат цинка; хроматы стронция, цинка, бария.
Наиболее часто используются фосфаты цинка PZ 20 и PZ W2 в большинстве лакокрасочных систем: органоразбавляемых, водоразбавляемых, воздушной и горячей сушки.
Там, где нельзя использовать противокоррозионные пигменты, содержащие цинк (контакт с пищевыми продуктами), используются пигменты на основе щелочеземельных фосфатов Новинокс РАТ 30, Новинокс РАТ 15 и Новинокс РС01.
Металлоконструкции, подвергающиеся воздействию соляного тумана, могут быть защищены лакокрасочными материалами, содержащими фосфат щелочеземельных металлов. Фосфат щелочеземельных металлов – нетоксичный пигмент, что повышает экологичность лакокрасочного покрытия и увеличивает сферу его применения.
Тетраоксихромат цинка ТС 20, хромат стронция L203E и хромат цинка CZ20 – применяются в лакокрасочных материалах, использующихся в авиационных, судовых покрытиях, а также в составе адгезивов для легких сплавов.
Для защитных покрытий, эксплуатирующихся в условиях высоких температур (до 600ºС), используются хромат бария М 20 и феррит кальция FC 71. Применение феррита кальция для защитных покрытий – новое направление в лакокрасочных материалах. В табл. 1 представлена стойкость различных лакокрасочных материалов (ЛКМ) к агрессивным средам.
Таблица 1. Стойкость лакокрасочных материалов
Примечания: ++ отлично, + хорошо, ± удовлетворитльно
Наиболее распространенным способом защиты от коррозии строительных конструкций, сооружений и оборудования является использование неметаллических химически стойких материалов: кислотоупорной керамики, жидких резиновых смесей, листовых и пленочных полимерных материалов (винипласта, поливинилхлорида, полиэтилена, резины), лакокрасочных материалов, синтетических смол и др.
Для правильного использования неметаллических химически стойких материалов необходимо знать не только их химическую стойкость, но и физико-химические свойства, обеспечивающие условия совместной работы покрытия и защищаемой поверхности. При использовании комбинированных защитных покрытий, состоящих из органического подслоя и футеровочного покрытия, важным является обеспечение на подслое температуры, не превышающей максимальной для данного вида подслоя.
Для листовых и пленочных полимерных материалов необходимо знать величину их адгезии с защищаемой поверхностью. Ряд неметаллических химически стойких материалов, широко используемых в противокоррозионной технике, содержит в своем составе агрессивные соединения, которые при непосредственном контакте с поверхностью металла или бетона могут вызвать образование побочных продуктов коррозии, что, в свою очередь, снизит величину их адгезии с защищаемой поверхностью. Эти особенности необходимо учитывать при использовании того или иного материала для создания надежного противокоррозионного покрытия.
Читайте также:
