Стали чугуны и цветные металлы
Обновлено: 21.09.2024
1. Сварка углеродистых и легированных сталей
Низкоуглеродистые и низколегированные стали обладают хорошей свариваемостью и соединяются большинством способов сварки без особых трудностей.
Углеродистые и легированные стали, с содержанием углерода более 0,3% при типовых режимах сварки, претерпевают закалку в з. т. в. (вероятность образования трещин).
Для обеспечения хорошей свариваемости при дуговой сварке этих сталей рекомендуются следующие технологические мероприятия:
- предварительный и последующий подогрев заготовок до температуры 100 – 300 о С в целях замедленного охлаждения и исключения закалки з. т. в.
- прокалка электродов, флюсов при температуре 400 – 450 о С в течение 3 часов и осушение защитных для предупреждения попадания водорода в металл сварного соединения;
- низкий или высокий отпуск сварных соединений сразу после окончания сварки в целях повышения пластичности закалочных структур и выделения водорода.
2. Сварка высоколегированных коррозионностойких сталей
Коррозионная стойкость стали обеспечивается содержанием более 12% Сr, а содержание 8% Ni стабилизирует аустенитную структуру и сохраняет её при нормальных температурах (сталь 10Х18Н9Т и др.). при сварке этих сталей на режимах, обуславливающих продолжительное пребывание металла в области температур 500 – 800 о С, возможна потеря коррозионной стойкости металлом и з. т. в. Причиной этого является образования карбидов хрома на границах зёрен и обеднение приграничных участков зёрен хромом. В результате металл сварного соединения становится склонным к так называемой межкристаллитной коррозии рис. 1.

Рис. 1. Межкристаллитная коррозия стали
При дуговой сварке для предупреждения межкристаллитной коррозии сварных соединений рекомендуется:
- сварка на малых погонных энергиях (q/v, Дж/см) с применением теплоотводящих медных подкладок;
- термическая обработка после сварки – нагрев до Т = 1100 о С и закалка в воде.
При нагреве происходит растворение карбидов, а закалка фиксирует чисто аустенитную структуру.
При дуговой сварке аустенитных сталей возможно образование в сварных швах горячих трещин. Для предупреждения их рекомендуется вводить в сварочные материалы (электроды, проволоку) легирующие элементы Si, Al, Mo, Mn и другие способствующие измельчению зерна, и снижать содержание вредных примесей. Аустенитные стали, хорошо, свариваются контактной сваркой.
Для обеспечения герметичности тройников, которые ранее производились из двух труб с фасонными вырезами и сваркой встык, была внедрена в производство новая технология – холодная вытяжка кромки фасонного отверстия основной трубы тройника. К образующейся после вытяжки цилиндрической отбортовки приваривается боковая труба на станке контактной сварки. Таким образом, было получено изделие по принципиально новой технологии с герметичным сварным швом (рис. 2).


Рис. 2. Контактная сварка нержавеющей стали
3. Сварка чугуна
Чугун относится к категории плохо сваривающихся сплавов. Его сваривают при исправлении дефектов в отливках и ремонте деталей. Дуговая сварка чугуна чугунными электродами и с покрытиями не обеспечивает хорошего качества сварных соединений. Металл шва получает структуру белого чугуна, а зона термического влияния закаливается.
Горячую сварку чугуна выполняют с предварительным подогревом свариваемых деталей до температуры 400 – 700 о С. Сваривают чугунными электродами (диаметром 8 – 25 мм) со стабилизирующей или специальной обмазкой. Сваренные детали охлаждают вместе с печью. Однако горячая сварка – дорогой и трудоёмкий процесс. Её применяют для ремонта уникальных деталей. Горячую сварку также выполняют науглероживающим газовым пламенем с флюсом на основе буры (Na2B4О7).
При холодной сварке чугун сваривают без подогрева стальными, медножелезными, медноникелевыми электродами и электродами из аустенитного чугуна. Стальные электроды применяют со стабилизирующей или качественной обмазкой. Стальные электроды не исключают отбел и закалочных структур, но они просты и обеспечивают мягкий хорошо обрабатываемый шов. Наибольшее применение имеют медно-железные электроды, как более дешёвые и обеспечивающие достаточную прочность металла шва. На рис. 3.изображён рабочий момент сварки чугуна.

Рис. 3. Холодная сварка чугуна медно-железным электродом
Сварка медно-железными электродами обеспечивает достаточные пластичность и плотность шва; ее широко применяют для заварки трещин в блоках цилиндров. Наиболее широко используемые электроды — ОЗЧ-1 и МНЧ-1. Электрод состоит из медного стержня и основного покрытия, в состав которого входит 50 % железного порошка. При сварке используют постоянный ток обратной полярности. Сварку ведут участками длиной 30…50 мм с тщательной проковкой каждого слоя.
4. Сварка меди и её сплавов
На свариваемость меди большое влияние оказывает содержащиеся в ней вредные примеси (О2, Н2, Вi, Рb и др.). Кислород, находящийся в меди в виде оксида Сu2О, является одной из причин образования горячих трещин в сварных швах. Выделение водорода при затвердевании сварочной ванны
может привести к образованию газовой пористости (водородная хрупкость). Она может привести к образованию трещин в твёрдом металле в процессе охлаждения.
Для предотвращения указанных дефектов при дуговой сварке меди рекомендуются:
- сварка в атмосфере защитных газов;
- применение сварочной и присадочной проволок, содержащих сильные раскислители (титан, цирконий, бор, фосфор, кремний и др.).
Поскольку медь обладает, высокой теплопроводностью сварку её, выполняют на повышенной погонной энергии, с предварительным подогревом до 300 о С. Сварку выполняют с флюсом на основе буры.
Основная трудность при сварке латуней – испарения цинка. В результате снижается прочность и коррозионная стойкость латунных швов. Пары цинка ядовиты. При сварке в защитных газах преимущественно применяют сварку неплавящимся вольфрамовым электродом (рис. 4, рис. 5, рис. 6), так как при этом меньше испаряется цинк. Латунь обладает меньшей теплопроводностью, чем медь, поэтому для металла толщиной свыше 12 мм необходим подогрев до Т = 150 о С.
Для сварки бронзы применяют те же способы и технологию, что и для сварки меди, за исключением оловянных бронз. Их сваривают с большой скоростью и без подогрева, так как в противном случае возможно вплавление легкоплавкой составляющей – олова.
Латуни и бронзы имеют высокое удельное электросопротивление, чем медь, и они достаточно хорошо свариваются контактной сваркой.
Медь контактной сваркой не сваривается.

Рис. 4. Сварка медных труб

Рис. 5. Сварка вольфрамовым электродом
Сварку меди неплавящимся вольфрамовым электродом осуществляют на постоянном токе прямой полярности; используют электрод из лантанированного вольфрама, который обладает удовлетворительной устойчивостью в защитных газах, в том числе, и в азоте особой чистоты. При сварке электрод располагают строго в плоскости стыка, наклон электрода 60—80 о «углом назад». При сварке меди толщиной более 4—5 мм рекомендуется, подогрев до 300—400 0 С.

Рис. 6. Сварка в защитном газе (аргон)
5. Сварка алюминия и его сплавов
(рис. 7, рис. 8). Трудности при сварке алюминия и его сплавов обусловлены образованием тонкой прочной и тугоплавкой поверхностной плёнки оксида Al2O3, плавящегося при температуре 2050 о С; склонностью к образованию газовой пористости; склонностью к образованию горячих трещин.
Плёнка оксида. Для разрушения и удаления плёнки и защиты металла от повторного окисления при сварке используют специальные флюсы или ведут сварку в атмосфере инертных газов. Сварку ведут плавящимся электродом на постоянном токе обратной полярности или сваривают неплавящимся электродом на переменном токе с использованием специальных источников тока.
Причиной газовой пористости в сварных швах алюминия является водород. Для предупреждения пористости необходима тщательная механическая очистка свариваемой поверхности заготовок и сварочной проволоки или химическая очистка (например, раствором NaОН).
Образования горячих трещин в алюминии и некоторых его сплавов связано с крупнокристаллитной макроструктурой в сварных швах. Склонность к трещинам увеличивается при наличии небольшого количества Si (до 0,5%). Борьба с горячими трещинами ведётся металлургическим путём. В шов через проволоку вводят железо, нейтрализующий вредное влияние кремния, и модификаторы Zr, Ti, и В, способствующие измельчению кристаллов в шве.
Наиболее трудно свариваются термически упрочняемые сплавы системы – дуралюмины. Относительно хорошо свариваются термически не упрочняемые сплавы системы АМц, АМг.
Алюминий и его сплавы также сваривают плазменной и электрошлаковой сваркой; они достаточно хорошо свариваются контактной сваркой. Учитывая высокую теплопроводность и электропроводность алюминия, для его сварки необходимо применять большие силы тока.


Рис. 7. Аргонная сварка алюминиевых сплавов


Рис. 8. Установка для автоматической аргонодуговой сварки продольных и кольцевых швов обечаек из алюминиевых сплавов
Материалы и сварочная проволока. Спектр алюминиевых сплавов сегодня весьма широк. Что касается алюминиевой проволоки, общим требованием является ее своевременное использование. Хранение при вскрытой упаковке должно быть сведено к минимуму: быстрое окисление поверхности ведет к ухудшению качества проволоки. Особенно сильно вредит проволоке высокая влажность воздуха. Место будущего сварного шва должно быть тщательно очищено от жирных, масляных и других загрязнений. Это должно быть сделано непосредственно перед сваркой. За очень короткое время алюминий покрывается слоем оксида алюминия (Al2O3). Этот оксидный слой удаляется посредством очищающего эффекта сварки (при положительной поляризации).
Защитные газы для сварки. Алюминиевые материалы должны свариваться в среде защитных инертных газов. В основном для этого применяется аргон. Но предпочтительнее использовать газовую смесь аргона и гелия. Более высокий показатель теплопроводности гелия определяет соответственно и более высокую температуру сварочной ванны, что оказывается преимуществом при сварке толстых металлических листов. Применение смеси защитных газов способствует более полному газовыделению – образование пор уменьшается.
6. Сварка тугоплавких металлов и сплавов
Трудности при сварке тугоплавких металлов Ti, Zr, Mo, Ni других связаны с тем, что они при нагреве интенсивно поглощают газы – кислород, водород и азот. При этом даже незначительное содержание газов приводит к резкому снижению пластических свойств этих металлов.
Титан и его сплавы сваривают в защитной атмосфере аргона высшего сорта. При этом дополнительно защищают струями 1 и 2 аргона корень шва и ещё не остывший до температуры 350 о С участок 3 (рис. 9, рис. 10). Перед сваркой проволоку, и основной металл дегазируют путём отжига в вакууме. Ответственные узлы сваривают в камерах с контролируемой аргонной атмосферой, в том числе и обитаемых, в которых сварщики работают в скафандрах (рис. 11).
Для сварки титана и его сплавов также применяют плазменную и электронно-лучевую сварку.
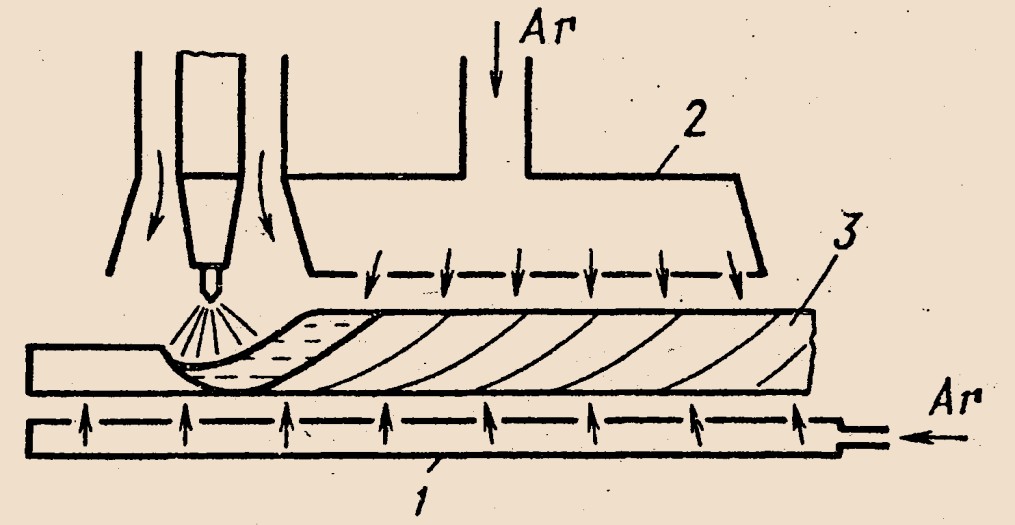
Рис. 9. Горелка с удлинённой насадкой для аргонодуговой сварки
Технологические особенности сварки сталей, чугунов и цветных металлов
14 различных типов металлов

Термин "металл" происходит от греческого слова "metalléuō", что означает выкапываю или добываю из земли. Наша планета содержит много металла. На самом деле из 118 элементов периодической системы порядка 95 являются металлами.
Это число не является точным, потому что граница между металлами и неметаллами довольно расплывчата: нет стандартного определения металлоида, как нет и полного согласия относительно элементов, соответствующим образом классифицированных как таковые.
Сегодня мы используем различные виды металлов, даже не замечая их. Начиная с зажимов в сантехнике и заканчивая устройством, которое вы используете для чтения этой статьи, все они сделаны из определенных металлов. Фактически, некоторые металлические элементы необходимы для биологических функций, таких как приток кислорода и передача нервных импульсов. Некоторые из них также широко используются в медицине в виде антацидов.
Все металлы в периодической таблице можно классифицировать по их химическим или физическим свойствам. Ниже мы перечислили некоторые различные типы металлов вместе с их реальным применением.
Классификация по физическим свойствам
14. Легкие металлы

Сплав титана 6AL-4V
Примеры: Алюминий, титан, магний
Легкие металлы имеют относительно низкую плотность. Формального определения или критериев для идентификации этих металлов нет, но твердые элементы с плотностью ниже 5 г/см³ обычно считаются легкими металлами.
Металлургия легких металлов была впервые развита в середине 19 века. Хотя большинство из них происходит естественным путем, значительная их часть образуется при электротермии и электролизе плавленых солей.
Их сплавы широко используются в авиационной промышленности благодаря их низкой плотности и достаточным механическим свойствам. Например, сплав титана 6AL-4V составляет почти 50 процентов всех сплавов, используемых в авиастроении. Он используется для изготовления роторов, лопастей компрессоров, мотогондол, компонентов гидравлических систем.
13. Тяжелые металлы

Окисленные свинцовые конкреции и кубик размером 1 см3
Примеры: железо, медь, кобальт, галлий, олово, золото, платина.
Тяжелые металлы - это элементы с относительно высокой плотностью (обычно более 5 г/см³) и атомным весом. Они, как правило, менее реактивны и содержат гораздо меньше растворимых сульфидов и гидроксидов, чем более легкие металлы.
Эти металлы редки в земной коре, но они присутствуют в различных аспектах современной жизни. Они используются в солнечных батареях, сотовых телефонах, транспортных средствах, антисептиках и ускорителях частиц.
Тяжелые металлы часто смешиваются в окружающей среде из-за промышленной деятельности, ухудшая качество почвы, воды и воздуха, а затем вызывая проблемы со здоровьем у животных и растений. Выбросы транспортных средств, горнодобывающие и промышленные отходы, удобрения, свинцово-кислотные батареи и микропластики, плавающие в океанах, являются одними из наиболее распространенных источников тяжелых металлов в этом контексте.
12. Белый металл

Подшипники из белого металла
Примеры: Обычно изготавливается из олова, свинца, висмута, сурьмы, кадмия, цинка.
Белые металлы - это различные светлые сплавы, используемые в качестве основы для украшений или изделий из серебра. Например, многие сплавы на основе олова или свинца используются в ювелирных изделиях и подшипниках.
Белый металлический сплав изготавливается путем объединения определенных металлов в фиксированных пропорциях в соответствии с требованиями конечного продукта. Основной металл для ювелирных изделий, например, формуется, охлаждается, экстрагируется, а затем полируется, чтобы придать ему точную форму и блестящий вид.
Они также используются для изготовления тяжелых подшипников общего назначения, подшипников внутреннего сгорания среднего размера и электрических машин.
11. Хрупкий металл

Хрупкое разрушение чугуна
Примеры: сплавы углеродистой стали, чугуна и инструментальной стали.
Металл считается хрупким, если он твердый, но не может противостоять ударам или вибрации под нагрузкой. Такие металлы под воздействием напряжения ломаются без заметной пластической деформации. Они имеют низкую прочность на разрыв и часто издают щелкающий звук при поломке.
Многие стальные сплавы становятся хрупкими при низких температурах, в зависимости от их обработки и состава. Чугун, например, твердый, но хрупкий из-за высокого содержания углерода. Напротив, керамика и стекло гораздо более хрупки, чем металлы, из-за их ионных связей.
Галлий, висмут, хром, марганец и бериллий также хрупки. Они часто используются в различных гражданских и военных целях, связанных с высокими деформационными нагрузками. Чугун, устойчивый к повреждениям в результате окисления, используется в машинах, трубах и деталях автомобильной промышленности, таких как корпуса коробок передач и головки цилиндров.
10. Тугоплавкий металл
Микроскопическое изображение вольфрамовой нити в лампе накаливания
Примеры: молибден, вольфрам, тантал, рений, ниобий.
Тугоплавкие металлы имеют чрезвычайно высокие температуры плавления (более 2000 °С) и устойчивы к износу, деформации и коррозии. Они являются хорошими проводниками тепла и электричества и имеют высокую плотность.
Другой ключевой характеристикой является их термостойкость: они не расширяются и не растрескиваются при многократном нагревании и охлаждении. Однако они могут деформироваться при высоких нагрузках и окисляться при высоких температурах.
Благодаря своей прочности и твердости они идеально подходят для сверления и резки. Карбиды и сплавы тугоплавких металлов используются почти во всех отраслях промышленности, включая горнодобывающую, автомобильную, аэрокосмическую, химическую и ядерную.
Металлический вольфрам, например, используется в ламповых нитях. Сплавы рения используются в гироскопах и ядерных реакторах. А ниобиевые сплавы используются для форсунок жидкостных ракетных двигателей.
9. Черные и цветные металлы

Валы-шестерни из (черной) нержавеющей стали
Черные металлы: Сталь, чугун, сплавы железа.
Цветные металлы: Медь, алюминий, свинец, цинк, серебро, золото.
Термин "железо" происходит от латинского слова "Ferrum", что переводится как "железо". Таким образом, термин "черный металл" обычно означает "содержащий железо", тогда как "цветной металл" означает металлы и сплавы, которые не содержат достаточного количества железа.
Поскольку черные металлы могут иметь широкий спектр легирующих элементов, которые значительно изменяют их характеристики, очень трудно поместить свойства всех черных металлов под один зонт. Тем не менее некоторые обобщения могут быть сделаны, например, большинство черных металлов являются твердыми и магнитными.
Черные металлы используются для применения с высокой нагрузкой и низкой скоростью, в то время как цветные металлы предпочтительны для применения с высокой скоростью и нулевой нагрузкой для применения с низкой нагрузкой.
Сталь является наиболее распространенным черным металлом. Она составляет около 80% всего металлического материала благодаря своей доступности, высокой прочности, низкой стоимости, простоте изготовления и широкому спектру свойств. Она широко используется в строительстве и обрабатывающей промышленности. Фактически, рост производства стали показывает общее развитие промышленного мира.
8. Цветные и благородные металлы

Ассортимент благородных металлов
Цветные металлы: медь, алюминий, олово, никель, цинк
Благородные металлы: родий, ртуть, серебро, рутений, осмий, иридий
Цветные металлы - это обычные и недорогие металлы, которые корродируют, окисляются или тускнеют быстрее, чем другие металлы, когда подвергаются воздействию воздуха или влаги. Они в изобилии встречаются в природе и легко добываются.
Они широко используются в промышленных и коммерческих целях и имеют неоценимое значение для мировой экономики благодаря своей полезности и повсеместности. Некоторые цветные металлы обладают отличительными характеристиками, которые не могут быть продублированы другими металлами. Например, цинк используется для гальванизации стали, чтобы защитить ее от коррозии, а никель - для изготовления нержавеющей стали.
Благородные металлы, с другой стороны, устойчивы к окислению и коррозии во влажном воздухе. Согласно атомной физике, благородные металлы имеют заполненный электрон d-диапазона. В соответствии с этим строгим определением, медь, серебро и золото являются благородными металлами.
Они находят применение в таких областях, как орнамент, металлургия и высокие технологии. Их точное использование варьируется от одного элемента к другому. Некоторые благородные металлы, такие как родий, используются в качестве катализаторов в химической и автомобильной промышленности.
7. Драгоценные металлы

Родий: 1 грамм порошка, 1 грамм прессованного цилиндра и 1 г аргонодуговой переплавленной гранулы
Примеры: палладий, золото, платина, серебро, родий.
Драгоценные металлы считаются редкими и имеют высокую экономическую ценность. Химически они менее реакционноспособны, чем большинство элементов (включая благородные металлы). Они также пластичны и имеют высокий блеск.
Несколько веков назад эти металлы использовались в качестве валюты. Но сейчас они в основном рассматриваются как промышленные товары и инвестиции. Многие инвесторы покупают драгоценные металлы (в основном золото), чтобы диверсифицировать свои портфели или победить инфляцию.
Серебро - второй по популярности драгоценный металл для ювелирных изделий (после золота). Однако его значение выходит далеко за рамки красоты. Оно обладает исключительно высокой тепло- и электропроводностью и чрезвычайно низким контактным сопротивлением. Именно поэтому серебро широко используется в электронике, батареях и противомикробных препаратах.
Классификация по химическим свойствам
6. Щелочные металлы

Твердый металлический натрий
Примеры: натрий, калий, рубидий, литий, цезий и франций.
Щелочь относится к основной природе гидроксидов металлов. Когда эти металлы реагируют с водой, они образуют сильные основания, которые легко нейтрализуют кислоты.
Они настолько реактивны, что обычно встречаются в природе в слиянии с другими веществами. Карналлит (хлорид калия-магния) и сильвин (хлорид калия), например, растворимы в воде и, таким образом, легко извлекаются и очищаются. Нерастворимые в воде щелочи, такие, как фторид лития, также существуют в земной коре.
Одно из самых популярных применений щелочных металлов - использование цезия и рубидия в атомных часах, наиболее точных из известных эталонов времени и частоты. Литий используется в качестве анода в литиевых батареях, композиты калия используются в качестве удобрений, а ионы рубидия используются в фиолетовых фейерверках. Чистый металлический натрий широко используется в натриевых лампах, которые очень эффективно излучают свет.
5. Щелочноземельные металлы

Изумрудный кристалл, основной минерал бериллия.
Примеры: бериллий, кальций, магний, барий, стронций и радий.
Щелочноземельные металлы в стандартных условиях мягкие и серебристо-белые. Они имеют низкую плотность, температуру кипения и температуру плавления. Хотя они не так реакционноспособны, как щелочные металлы, они очень легко образуют связи с элементами. Как правило, они вступают в реакцию с галогенами, образуя галогениды щелочноземельных металлов.
Все они встречаются в земной коре, кроме радия, который является радиоактивным элементом. Радий уже распадался в ранней истории Земли из-за относительно короткого периода полураспада (1600 лет). Современные образцы поступают из цепочки распада урана и тория.
Щелочноземельные металлы имеют широкий спектр применения. Бериллий, например, используется в полупроводниках, теплопроводниках, электрических изоляторах и в военных целях. Магний часто сплавляют с цинком или алюминием для получения материалов со специфическими свойствами. Кальций в основном используется в качестве восстановителя, а барий используется в вакуумных трубках для удаления газов.
4. Переходные металлы
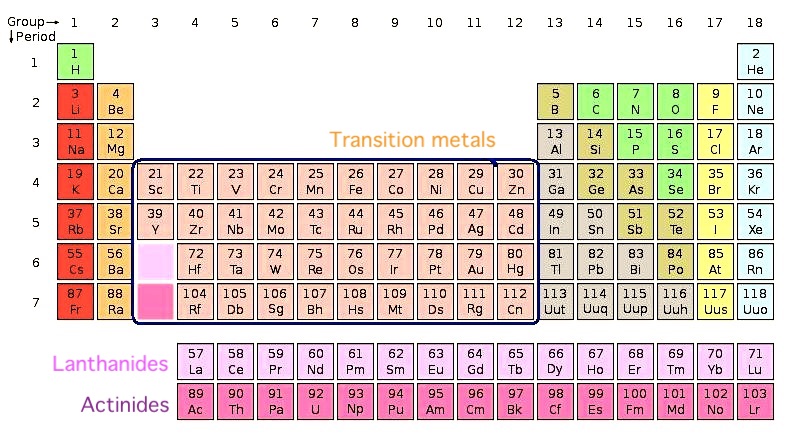
Примеры: титан, ванадий, хром, никель, серебро, вольфрам, платина, кобальт.
Большинство элементов используют электроны из своей внешней оболочки для связи с другими элементами. Переходные металлы, однако, могут использовать две крайние оболочки для соединения с другими элементами. Это химическая особенность, которая позволяет им связываться со многими различными элементами в различных формах.
Они занимают среднюю часть таблицы Менделеева, служа мостом между (или переходом) между двумя сторонами таблицы. Более конкретно, есть 38 переходных металлов в группах с 3 по 12 периодической таблицы. Все они являются пластичными, податливыми и хорошими проводниками тепла и электричества.
Многие из этих металлов, такие как медь, никель, железо и титан, используются в конструкциях и в электронике. Большинство из них образуют полезные сплавы друг с другом и с другими металлическими веществами. Некоторые из них, включая золото, серебро и платину, называются благородными металлами, потому что они крайне инертны и устойчивы к кислотам.
3. Постпереходные металлы

Висмут в виде синтетических кристаллов
Примеры: алюминий, галлий, олово, свинец, таллий, индий, висмут.
Постпереходные металлы в периодической таблице - это элементы, расположенные справа от переходных металлов и слева от металлоидов. Из-за своих свойств они также называются "бедными" или "другими" металлами.
Физически они хрупки (или мягки) и имеют более низкую температуру плавления и механическую прочность, чем переходные металлы. Их кристаллическая структура довольно сложна: они проявляют ковалентные или направленные эффекты связи.
Различные металлы этого семейства имеют различное применение. Алюминий, например, используется для изготовления оконных рам, кухонной посуды, банок, фольги, деталей автомобилей. Оловянные сплавы используются в мягких припоях, оловянных и сверхпроводящих магнитах.
Индиевые сплавы используются для изготовления плоских дисплеев и сенсорных экранов, а галлий - в топливных элементах и полупроводниках.
2. Лантаноиды

1-сантиметровый кусок чистого лантана
Примеры: лантан, церий, прометий, гадолиний, тербий, иттербий, лютеций.
Лантаноиды - это редкоземельные металлы с атомными номерами от 57 до 71. Впервые они были обнаружены в 1787 году в необычном черном минерале (гадолините), обнаруженном в Иттербю, Швеция. Позже минерал был разделен на различные элементы лантаноидов.
Лантаноиды - это металлы с высокой плотностью, плотность которых колеблется от 6,1 до 9,8 г/см³, и они, как правило, имеют очень высокие температуры кипения (1200-3500 °C) и очень высокие температуры плавления (800-1600 °C).
Сплавы лантаноидов используются в металлургии из-за их сильных восстановительных способностей. Около 15 000 тонн лантаноидов ежегодно расходуется в качестве катализаторов и при производстве стекол. Они также широко используются в лазерах и оптических усилителях.
Некоторые исследования показывают, что лантаноиды могут быть использованы в качестве противораковых средств. Лантан и церий, в частности, могут подавлять пролиферацию раковых клеток и способствовать цитотоксичности.
1. Актиниды

Металлический уран, высокообогащенный ураном-235
Примеры: актиний, уран, торий, плутоний, фермий, нобелий, лоренций
Подобно лантаноидам, актиниды образуют семейство редкоземельных элементов с аналогичными свойствами. Они представляют собой серию из 15 последовательных химических элементов в периодической системе от атомных номеров 89 до 103.
Все они радиоактивны по своей природе. Синтетически произведенный плутоний, а также природные уран и торий являются наиболее распространенными актинидами на Земле. Первым актинидом, который был открыт в 1789 году, был уран. И большая часть существующих продуктов актинидов была произведена в 20 веке.
Их свойства, такие как излучение радиоактивности, пирофорность, токсичность и ядерная критичность, делают их опасными для обращения. Сегодня значительная часть (кратковременных) актинидов производится ускорителями частиц в исследовательских целях.
Некоторые актиниды нашли применение в повседневной жизни, например, газовые баллоны (торий) и детекторы дыма (америций), большинство из них используются в качестве топлива в ядерных реакторах и для изготовления ядерного оружия. Уран-235 является наиболее важным изотопом для применения в ядерной энергетике, который широко используется в тепловых реакторах.
Стали, чугуны и цветные металлы. Классификация и маркировка
Классификация и разновидности, а также правила и принципы маркировки сталей, чугунов и цветных металлов. Особенности химического состава, а также функциональные особенности и свойства каждого из исследуемых металлов, их использование в промышленности.
| Рубрика | Производство и технологии |
| Вид | реферат |
| Язык | русский |
| Дата добавления | 19.07.2017 |
| Размер файла | 25,6 K |
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Стали, чугуны и цветные металлы. Классификация и маркировка
Используемые в технике металлы принято подразделять на две основные группы - черные и цветные. К черным металлам относят железо и его сплавы (чугун, сталь, ферросплавы). Остальные металлы и их сплавы составляют группу цветных.
Из металлов особое значение имеют железо и его сплавы, являющиеся до настоящего времени основным машиностроительным материалом. В общемировом производстве металлов свыше 90% приходится на железо и его сплавы. Это связано с тем, что железные руды широко распространены в природе, а производство чугуна и стали сравнительно дешево и просто.
Наряду с черными металлами важное значение в технике имеют и цветные металлы. Это объясняется рядом важных физико - химических свойств, которыми не обладают черные металлы. Наиболее широко используют в самолетостроении, радиотехнике, электронике и в других отраслях промышленности медь, алюминий, магний, никель, титан, вольфрам и другие цветные металлы.
1. Классификация и маркировка сталей
сталь чугун металл
Сталями принято называть сплавы железа с углеродом, содержание до 2,14% углерода. Кроме того, в состав сплава обычно входят марганец, кремний, сера и фосфор; некоторые элементы могут быть введены для улучшения физико-химических свойств специально (легирующие элементы).
Стали, классифицируют по самым различным признакам. Мы рассмотрим следующие:
Химический состав.
В зависимости от химического состава различают стали углеродистые (ГОСТ 380-71, ГОСТ 1050-75) и легированные (ГОСТ 4543-71, ГОСТ 5632-72, ГОСТ 14959-79). В свою очередь углеродистые стали могут быть:
A) малоуглеродистыми, т.е. содержащими углерода менее 0,25%;
Б) среднеуглеродистыми, содержание углерода составляет 0,25-0,60%
B) высокоуглеродистыми, в которых концентрация углерода превышает 0,60%
Легированные стали подразделяют на:
а) низколегированные содержание легирующих элементов до 2,5%
б) среднелегированные, в их состав входят от 2,5 до 10% легирующих элементов;
в) высоколегированные, которые содержат свыше 10% легирующих элементов.
По назначению стали бывают:
конструкционные, предназначенные для изготовления строительных и машиностроительных изделий.
Инструментальные, из которых изготовляют режущий, мерительный, штамповый и прочие инструменты. Эти стали содержат более 0,65% углерода.
С особыми физическими свойствами, например, с определенными магнитными характеристиками или малым коэффициентом линейного расширения: электротехническая сталь, суперинвар.
С особыми химическими свойствами, например, нержавеющие, жаростойкие или жаропрочные стали.
В зависимости от содержания вредных примесей: серы и фосфора-стали подразделяют на:
Стали обыкновенного качества, содержание до 0.06% серы и до 0,07% фосфора.
Качественные - до 0,035% серы и фосфора каждого отдельно.
Высококачественные - до 0.025% серы и фосфора.
Особовысококачественные, до 0,025% фосфора и до 0,015% серы.
4. Степень раскисления.
По степени удаления кислорода из стали, т.е. По степени её раскисления, существуют:
спокойные стали, т.е., полностью раскисленные; такие стали обозначаются буквами «сп» в конце марки (иногда буквы опускаются);
кипящие стали - слабо раскисленные; маркируются буквами «кп»;
полу спокойные стали, занимающие промежуточное положение между двумя предыдущими; обозначаются буквами «пс».
Сталь обыкновенного качества подразделяется еще и по поставкам на 3 группы:
сталь группы А поставляется потребителям по механическим свойствам (такая сталь может иметь повышенное содержание серы или фосфора);
сталь группы Б - по химическому составу;
сталь группы В-с гарантированными механическими свойствами и химическим составом.
В зависимости от нормируемых показателей (предел прочности у, относительное удлинение д%, предел текучести дт, изгиб в холодном состоянии) сталь каждой группы делится на категории, которые обозначаются арабскими цифрами.
Стали обыкновенного качества обозначают буквами «Ст» и условным номером марки (от 0 до 6) в зависимости от химического состава и механических свойств. Чем выше содержание углерода и прочностные свойства стали, тем больше её номер. Буква «Г» после номера марки указывает на повышенное содержание марганца в стали. Перед маркой указывают группу стали, причем группа «А» в обозначении марки стали не ставится. Для указания категории стали к обозначению марки добавляют номер в конце соответствующий категории, первую категорию обычно не указывают.
Ст1кп2 - углеродистая сталь обыкновенного качества, кипящая, № марки 1, второй категории, поставляется потребителям по механическим свойствам (группа А);
ВСт5Г - углеродистая сталь обыкновенного качества с повышенным содержанием марганца, спокойная, № марки 5, первой категории с гарантированными механическими свойствами и химическим составом (группа В);
Вст0 - углеродистая сталь обыкновенного качества, номер марки 0, группы Б, первой категории (стали марок Ст0 и Бст0 по степени раскисления не разделяют).
Качественные стали маркируют следующим образом:
в начале марки указывают содержание углерода цифрой, соответствующей его средней концентрации;
а) в сотых долях процента для сталей, содержащих до 0,65% углерода;
05 кп - сталь углеродистая качественная, кипящая, содержит 0,05% С;
60 - сталь углеродистая качественная, спокойная, содержит 0,60% С;
б) в десятых долях процента для индустриальных сталей, которые дополнительно снабжаются буквой «У»:
У7 - углеродистая инструментальная, качественная сталь, содержащая 0,7% С, спокойная (все инструментальные стали хорошо раскислены);
У12 - углеродистая инструментальная, качественная сталь, спокойная содержит 1,2% С;
2) легирующие элементы, входящие в состав стали, обозначают русскими буквами:
А - азот К - кобальт Т - титан Б - ниобий М - молибден Ф - ванадий
В-вольфрам Н - никель Х - хром Г - марганец
П - фосфор Ц - цирконий Д - медь Р - бор Ю - алюминий
Е - селен С - кремний Ч - редкоземельные металлы
14Г2 - низко легированная качественная сталь, спокойная, содержит приблизительно 14% углерода и до 2,0% марганца.
03Х16Н15М3Б - высоко легированная качественная сталь, спокойная содержит 0,03% C, 16,0% Cr, 15,0% Ni, до З, 0% Мо, до 1,0% Nb.
Высококачественные и особовысококачественные стали.
Маркируют, так же как и качественные, но в конце марки высококачественной стали ставят букву А, (эта буква в середине марочного обозначения указывает на наличие азота, специально введённого в сталь), а после марки особовысококачественной - через тире букву «Ш».
У8А - углеродистая инструментальная высоко качественная сталь, содержащая 0,8% углерода;
30ХГС-III - особовысококачественная среднелегированная сталь, содержащая 0,30% углерода и от 0,8 до 1,5% хрома, марганца и кремния каждого.
Отдельные группы сталей обозначают несколько иначе.
Шарикоподшипниковые стали маркируют буквами «ШХ», после которых указывают содержание хрома в десятых долях процента:
ШХ6 - шарикоподшипниковая сталь, содержащая 0,6% хрома;
ШХ15ГС - шарикоподшипниковая сталь, содержащая 1,5% хрома и от 0,8 до 1,5% марганца и кремния.
Быстрорежущие стали (сложнолегированные) обозначают буквой «Р», следующая за ней цифра указывает на процентное содержание в ней вольфрама:
Р6М5К5-быстрорежущая сталь, содержащая 6,0% вольфрама 5,0% молибдена 5,0% кобальта.
Автоматные стали обозначают буквой «А» и цифрой, указывающей среднее содержание углерода в сотых долях процента:
А12 - автоматная сталь, содержащая 0,12% углерода (все автоматные стали имеют повышенное содержание серы и фосфора);
А40Г - автоматная сталь с 0,40% углерода и повышенным до 1,5% содержанием
2. Классификация и маркировка чугунов
Чугун отличается от стали по составу - более высоким содержанием углерода, по технологическим свойствам - лучшими литейными качествами, малой способностью к пластической деформации (в обычных условиях не поддается ковке). Чугун дешевле стали.
Чугунами называют железоуглеродистые сплавы с содержанием углерода от 2 до 6,67%.однако применяемые чугуны содержат углерода не более 4,3%, редко _ до 5%.
Изделия из чугуна получают главным образом путем литья (чугунные отливки), хотя имеются данные о том, что чугуны можно при определенных условиях подвергать горячей обработке давлением, после которой механические свойства чугунов повышаются, приближаясь к свойствам высококачественной углеродистой конструкционной стали.
Высокие литейные свойства, хорошая обрабатываемость резанием и небольшая стоимость обеспечивают широкое применение серых, высокопрочных и ковких чугунов.
Структура белых чугунов образуется у железоуглеродистых сплавов, содержащих углерода более 2%, при их относительно быстром охлаждении. Важнейшей структурной составляющей белых чугунов, определяющей их свойства, является ледебурит. При комнатной температуре ледебурит представляет эвтектическую смесь перлита и цементита. Наибольшее влияние на свойства белых чугунов оказывает цементит. Чем больше цементита в структуре белого чугуна, тем выше его твердость и хрупкость.
Применение белых чугунов для деталей машин ограничено из-за их невысоких литейных свойств и плохой обрабатываемости резанием. Поэтому белые чугуны используют в основном как предельные (для производства стали), а также для производства ковких чугунов.
Серые чугуны. Их получают при медленном охлаждении железоулеродистых сплавов, содержащих углерода более 2%.
Основной структурной составляющей серых чугунов, определяющей их свойства, является графит. Процесс кристаллизации графита называют графитизацией. Графит может выделяться как непосредственно из жидкого раствора, так и из аустенита и цементита.
На процесс графитизации, кроме скорости охлаждения, температуры нагрева и других технологических факторов, оказывает влияние содержание различных элементов. Одни элементы, как кремний, углерод, алюминий, титан, способствуют графитизации, другие, например, марганец, сера, хром, затрудняют ее и способствуют отбеливанию, т.е. производству белого чугуна.
Основными элементами, влияющими на графитизацию, помимо углерода, являются кремний и марганец. Кремний способствует графитизации и улучшает литейные свойства; его содержание в серых чугунах составляет от 0,5 до 4,5%. Марганец, наоборот, способствует отбеливанию и ухудшает литейные свойства; поэтому его содержание в серых чугунах допускается от 0,5 до 1%.Сера является вредной примесью в чугуне: она затрудняет графитизацию и ухудшает литейные свойства; в серых чугунах ее содержание ограничивают 0,07%.Фосфор в небольших количествах улучшает литейные свойства чугуна: содержание его составляет от 0,5 до 1%.В небольших количествах присутствуют также газы.
Структура серых чугунов состоит их стальной основы и выделений графита. По структуре стальной основы серые чугуны розделяют на четыре группы:
1) ферритные; структура феррит и графит;
2) ферритно-перлитные; структура феррит, перлит и графит;
3) перлитные; структура перлит и графит;
4) перлитно-цементитные; структура перлит, цементит и графит.
Наибольшее влияние на механические свойства серых чугунов оказывают выделения графита.
Имея малую прочность, графит ослабляет стальную основу; его влияние на чугун подобно действию надрезов. Поэтому чем больше графита в структуре, тем ниже прочность серого чугуна. Однако механические свойства серого чугуна зависят и не только от количества, но и от формы, величины и расположения графитных выделений. В серых чугунах выделения графита имеют форму пластинок. Чем крупнее пластинки графита, тем ниже механические свойства серого чугуна.
По физико-механическим характеристикам серые чугуны условно можно разделить на четыре группы: малой прочности, повышенной прочности, высокой прочности и со специальными свойствами.
Серый чугун малой прочности имеет в основе микроструктуру феррита или феррита и перлита с пластинчатым графитом. Такой чугун обладает прочностью на растяжение 300Мпа и соответствует маркам до СЧ-30.В марке буквы сокращенно обозначают наименование чугуна, а следующая за ними двухзначная цифра - предел прочности на растяжение.
Серый чугун повышенной прочности имеет перлитную основу и более мелкое, завихренное строение графита. Он соответствует маркам от СЧ 35 до СЧ 40. Прочность этих чугунов обеспечивается легированием модифицированием чугуна.
Легированный серый чугун имеет мелкозернистую структуру небольших количеств никеля и хрома, молибдена, а иногда титана или меди.
Модифицированный серый чугун имеет однородное строение по сечению отливки и более мелкую завихренную форму графита. В структуре отливок из модифицированного серого чугуна не содержится ледебуритного цементита. Вследствие малого количества вводимого в чугун модификатора его химический состав практически остается неизменным.
Серые чугуны имеют низкий предел прочности на растяжение и высокие предел прочности на сжатие и твердость; поэтому их в основном используют для изготовления деталей, работающих на сжатие и подвергающихся износу (станины и суппорты станков, стойки и р.) Пластические свойства серого чугуна низкие. По литейным качествам серые чугуны превосходят стали. Серые чугуны хорошо обрабатываются резанием.
Ковкий чугун. Ковкий чугун - условное название более пластичного чугуна по сравнению с серым. Ковкий чугун никогда не куют. Отливки их ковкого чугуна получают длительным отжигом отливок из белого чугуна с перлитно - цементитной структурой. При отжиге цементит белого чугуна распадается с образованием графита хлопьевидной формы.
В зависисимости от структуры металлической основы различают ковкий ферритный чугун и ковкий перлитный чугун.
В зависимости от предела прочности ковкий чугун (ГОСТ 1215 -79) разделяют на следующие марки: КЧ 30 -6 (163), КЧ 33 - 8 (163), КЧ 35-10 (163), КЧ 37 - 12
(163) - ферритные черносердечные и КЧ 45 - 6 (241),
КЧ 50 - 4 (241), КЧ 56 - 4 (269), КЧ 60 - 3 (269), КЧ 63 -2 (269) - перлитные светлосердечные.
Ковкий чугун широко применяют в автомобильном, сельскохозяйственном и текстильном машиностроении. Из него изготовляют детали высокой прочности, способные воспринимать повторно-переменные и ударные нагрузки и работающие в условиях повышенного износа. Широкое распространение ковкого чугуна, занимающего по механическим свойствам промежуточное положение между серым чугуном и сталью, обусловлено лучшими по сравнению со сталью литейными свойствами исходного белого чугуна, что позволяет получать отливки сложной формы. Ковкий чугун характеризуется достаточно высокими антикоррозионными свойствами и хорошо работает в среде влажного воздуха, топочных газов и воды.
3. Классификация и маркировка цветных сплавов
1. Медь и её сплавы.
Технически чистая медь обладает высокими пластичностью и коррозийной стойкостью, малым удельным электросопротивлением и высокой теплопроводностью. По чистоте медь подразделяют на марки (ГОСТ 859-78):
Читайте также:
