Строение металлов и кристаллизация
Обновлено: 06.05.2024
Определение металлов можно дать с позиций химии, физики и техники.
В химии металлы — это химические элементы, находящиеся в левой части периодической системы элементов Д. И. Менделеева, которые обладают особым механизмом взаимодействия валентных электронов (ионов) с ядром как в самих металлах, так и при вступлении в химические реакции с другими элементами, в том числе с металлами.
Физика характеризует металлы как твердые тела, обладающие цветом, блеском, способностью к плавкости (расплавлению) и затвердеванию (кристаллизации), тепло- и электропроводностью, магнитными и другими свойствами.
В технике металлы — это конструкционные материалы, обладающие высокой обрабатываемостью (ковкостью, штампуемостью, обрабатываемостью резанием, паяемостью, свариваемостью и др.), прочностью, твердостью, ударной вязкостью и рядом других ценных свойств, благодаря которым они находят широкое применение.
Русский ученый М. В. Ломоносов (1711 — 1765), исследуя металлы и неметаллы в своем труде «Первые основания металлургии или рудных дел», дал металлам определение: «Металлом называется светлое тело, которое ковать можно. Таких тел находим только шесть: золото, серебро, медь, олово, железо и свинец». Это определение М. В. Ломоносов дал в 1773 г., когда известны были только шесть металлов.
Из металлов, добываемых из недр земли, получают большую группу конструкционных материалов, применяемых в различных отраслях промышленности. В природе одни металлы встречаются в чистом, самородном виде, другие — в виде оксидов (соединений металла с кислородом), нитридов и сульфидов, из которых состоят различные руды этих металлов.
Самыми распространенными металлами, применяемыми в качестве конструкционных материалов, являются железо, алюминий, медь и сплавы на основе этих металлов.
К металлам относятся более 80 элементов периодической системы Менделеева. Все эти металлы подразделяются на две большие группы: черные металлы и цветные металлы.
Характерными признаками черных металлов являются темно-серый цвет, блеск, высокие плотность и температура плавления, твердость, прочность, вязкость и полиморфизм (аллотропия). По физикохимическим свойствам черные металлы подразделяют на пять групп:
- железистые (железо, кобальт, никель, марганец);
- тугоплавкие (вольфрам, рений, тантал, молибден, ниобий, ванадий, хром, титан и др.);
- урановые — актиниды (уран, торий, плутоний и др.);
- редкоземельные — лантаниды (лантан, церий, иттрий, скандий и др.);
- щелочно-земельные (литий, натрий, калий, кальций и др.).
Из этих пяти групп черных металлов особенно широкое применение в промышленном производстве находят железистые и тугоплавкие металлы.
Железистые металлы, кроме марганца, называют еще ферромагнетиками. Ферромагнетики способны намагничиваться и притягивать металлы своей группы.
К тугоплавким относятся металлы, которые имеют температуру плавления выше температуры плавления железа (1 539 °С): титан — 1 667 °С, ванадий — 1 902 °С, хром — 1 903 °С, молибден — 2 615 °С, ниобий — 2 460 °С, тантал — 2 980 °С, вольфрам — 3 410 °С. Тугоплавкие металлы в основном применяются как легирующие элементы в производстве жаропрочных, жаростойких, теплостойких и специальных сплавов, в том числе твердых сплавов и высоколегированных сталей.
2. Строение металлов
Атомно-кристаллическая структура металлов. Как известно, все вещества состоят из атомов, в том числе и металлы. Каждый металл (химический элемент) может находиться в газообразном, жидком или твердом агрегатных состояниях. Каждое агрегатное состояние будет иметь свои особенности, отличные друг от друга. В газообразном металле расстояние между атомами велико, силы взаимодействия малы и атомы хаотично перемещаются в пространстве; газ стремится к расширению в сторону большего объема. При понижении температуры и давления вещество переходит в жидкое состояние. Свойства жидкого вещества резко отличаются от свойств газообразного. В жидком металле атомы сохраняют лишь так называемый ближний порядок атомов, т. е. в объеме расположено небольшое количество атомов, а не атомы всего объема. При понижении температуры жидкий металл переходит в твердое состояние, которое имеет строгую закономерность расположения атомов.
Если условно провести вертикальные и горизонтальные линии связи через центры атомов, можно увидеть, что у металлов в твердом состоянии атомы расположены в строго определенном порядке и представляют собой множество раз повторяющиеся элементарные геометрические фигуры — параллелепипеды (рис. 1). Наименьшую геометрическую фигуру называют элементарной ячейкой. Элементарные ячейки, расположенные на горизонтальных и вертикальных кристаллографических плоскостях (рис. 2), образуют пространственную кристаллическую решетку.
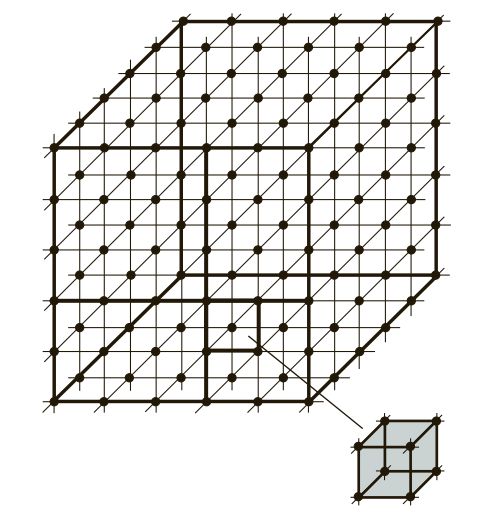
Рис. 1. Схема расположения элементарных геометрических ячеек в атомных решетках металлов и сплавов
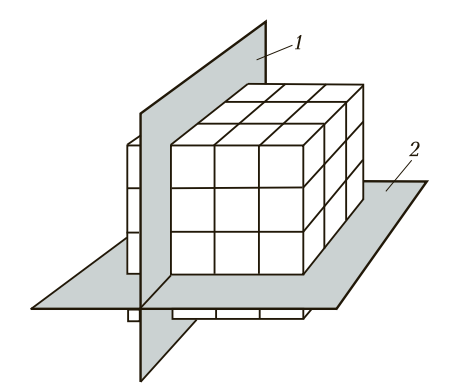
Рис. 2. Расположение кристаллографических плоскостей: 1 и 2 — соответственно горизонтальная и вертикальная кристаллографические плоскости
Элементарные кристаллические решетки характеризуют следующие основные параметры: расстояние между атомами по осям координат (по линиям связи), углы между линиями связи, координационное число — число атомов, находящихся на наиболее близком и равном расстоянии от любого атома в решетке. Форму элементарной ячейки рассматривают по кристаллографическим плоскостям в трех измерениях.
Таким образом, любой металл можно представить не как однородную цельную массу, а как массу, сложенную из множества элементарных ячеек. Блок элементарных атомных кристаллических ячеек образует атомно-кристаллическую ячейку (решетку). Если выделить эту элементарную ячейку, то в зависимости от металла получим следующие типы кристаллических ячеек (рис. 3): куб (К), объемно-центрированный куб (ОЦК), гранецентрированный куб (ГЦК), гексагональная плотноупакованная ячейка (ГПУ), гексагональная простая ячейка (Г) и др.
Простая кубическая ячейка (рис. 3, а) характерна для неметаллов, которые обладают наибольшими плотностью и удельным весом, и имеет восемь атомов, которые расположены в каждой вершине куба.
Объемно-центрированная кубическая ячейка (рис. 3, б ) состоит из восьми атомов, которые расположены по одному атому в каждой вершине куба, и одного, находящегося в центре куба на равных расстояниях от его граней. Эту форму атомной кристаллической ячейки имеют железо модификации Fe-α, ванадий, вольфрам, молибден, тантал и хром, т. е. в основном черные металлы.
Гранецентрированная кубическая ячейка (рис. 3, в) имеет 14 атомов — по одному атому в каждой вершине куба (восемь атомов) и по одному атому в центре каждой грани (шесть атомов). Гранецентрированную кубическую ячейку имеют алюминий, железо модификации Fe-γ, золото, кобальт, медь, никель, платина и серебро, в основном это цветные металлы и часть черных металлов.
Гексагональная плотноупакованная ячейка (рис. 3, г) состоит из 17 атомов. Форма геометрического тела, которую образуют эти атомы, является шестигранной призмой. При этом по шесть атомов расположены в каждой вершине верхнего и нижнего оснований, по одному атому в центре этих оснований и три атома в центре одной их трех граней (через грань). Гексагональную плотноупакованную ячейку имеют бериллий, кадмий, магний, ванадий, тантал.
Простая гексагональная ячейка (рис. 3, д) состоит из 12 атомов, которые расположены в вершинах верхнего и нижнего оснований шестигранной призмы. Такую кристаллическую ячейку имеют ртуть и цинк.
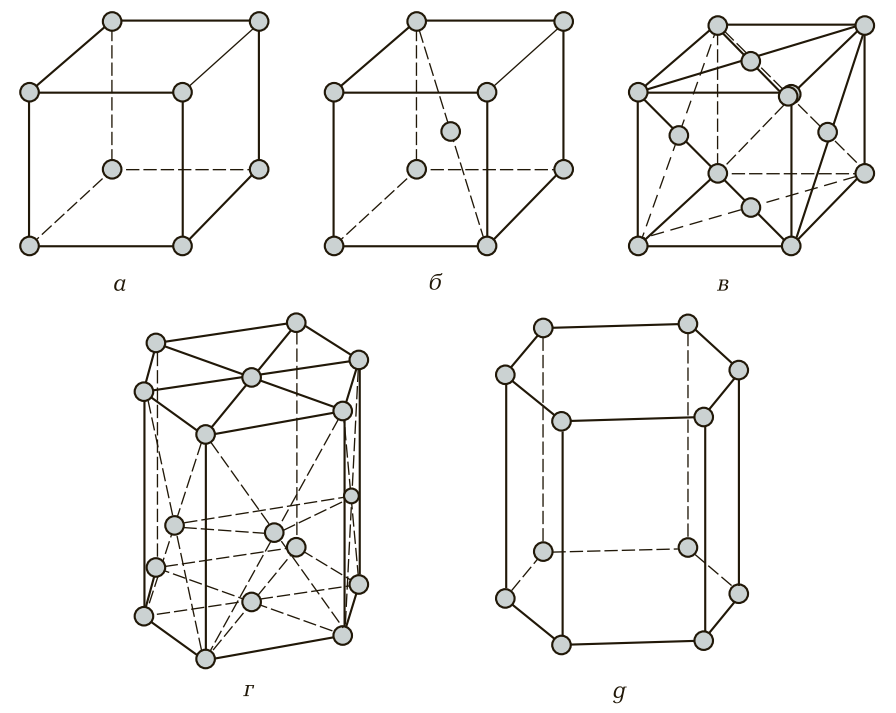
Рис. 3. Геометрические формы элементарных кристаллических ячеек: а — куб; б — объемно-центрированный куб; в — гранецентрированный куб; г — гексагональная плотноупакованная ячейка; д — гексагональная простая ячейка
Связь между атомами в кристаллической решетке и между решетками осуществляется за счет так называемой металлической связи. От прочности этой связи зависят прочность и твердость металлов. Чем выше эта связь, тем бо´льшую прочность и твердость имеют металлы. Механизм связи между атомами в решетке и между решетками имеет сложную физико-химическую природу.
В практике идеальное расположение кристаллических решеток обычно не наблюдается. Кристаллы, образуемые кристаллическими решетками, имеют искаженную геометрическую форму и различную величину.
Анизотропия металлов. Анизотропия (от гр. anisos — неравный и tropos — направление) — неодинаковость физических свойств среды (тела) в различных направлениях. Анизотропия предполагает зависимость свойств металлов от направления по плоскостям атомно-кристаллических решеток. Чем больше в плоскости атомов, тем выше свойства металлов. В горизонтальных плоскостях в любой форме атомно-кристаллических решеток больше, чем в вертикальных плоскостях. Следовательно, прочность металлов, испытанная в горизонтальном направлении, выше, чем в вертикальном. Анизотропия проявляется в процессе обработки конструкционных материалов давлением (проката, волочения, штамповки и других технологических способов получения заготовок и изделий).
На рис. 2 кристаллографические плоскости совпадают с линиями связи, проходящими через атомы металла. Форма элементарной кристаллической ячейки, расстояние между атомами и прочность металлической связи определяют физические, механические и технологические свойства металлов. Если исследуемый металл рассматривать по трем кристаллографическими плоскостям, по линиям связи между атомами, то можно заметить, что свойства по этим трем измерениям будут различны. Число атомов в этих плоскостях неодинаково. Металлическая связь между горизонтально и вертикально расположенными атомами также неодинакова. Это, в свою очередь, приводит к различной прочности металлов в продольном и поперечном направлениях. Например, предел прочности меди в продольном направлении будет в 2 раза больше, чем в поперечном.
Все металлы анизотропны, так как они состоят из кристаллов. Кристаллическое строение металлов обусловливает пластическую деформацию, т. е. изменение внешней формы и размеров под действием нагрузок без разрушения. Способность металлов и сплавов пластически деформироваться положена в основу их обработки давлением (прокатка, волочение, ковка, штамповка и прессование). При обработке давлением, например прокатке (рис. 4, а), происходит перемещение одного слоя атомных решеток по другому по кристаллографическим плоскостям (рис. 4, б).
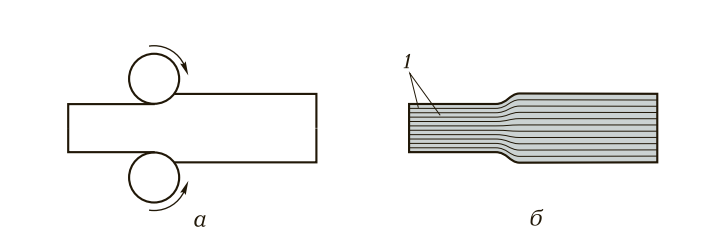
Рис. 4. Схема деформации металлов и сплавов (прокатка): а — деформация; б — скольжение металлов по кристаллографическим плоскостям в процессе деформации; 1 — кристаллографические плоскости
В процессе деформации металла при прокатке происходит не только изменение поперечных и продольных размеров заготовок, но и изменение микроструктуры металла.
Зерна под действием давления прокатных валков искажаются, приобретая продолговатую или пластинчатую форму, а затем преобразуются в волокна. Изменение микроструктуры металла в процессе деформации условно показано на рис. 5.
Процесс кристаллизации. Рассмотрим, как происходит образование кристаллов у чистых металлов. Установлено, что процесс кристаллизации металлов из жидкого состояния в твердое идет в две стадии:
- образование центров кристаллизации;
- рост кристаллов вокруг этих центров (рис. 6).
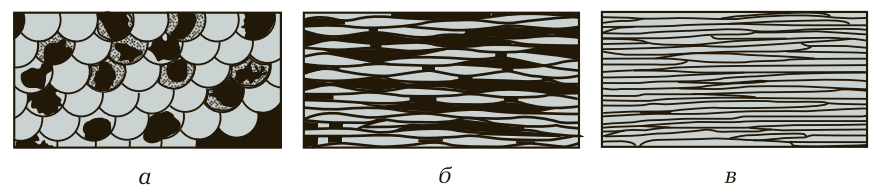
Рис. 5. Изменение микроструктуры металла в процессе деформации: а — микроструктура металла до деформации; б — микроструктура металла после первой операции деформации; в — микроструктура металла после окончательной деформации
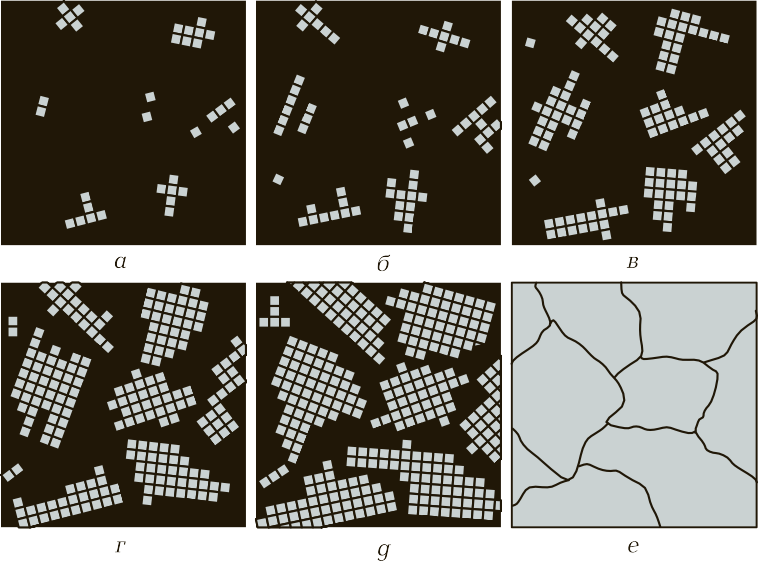
Рис. 6. Процесс кристаллизации металлов и сплавов: а — е — последовательные этапы процесса
Далее вновь появляются новые центры, и происходит рост твердой фазы вокруг первичных и вторичных центров. Процесс происходит до того момента, пока образованные таким образом кристаллы не будут соприкасаться друг с другом и не будет наличия жидкой фазы металла (см. рис. 6, г — е). Когда образование кристалла идет в жидкой фазе (в расплавленном металле), он будет иметь правильную форму, т. е. состоять из определенных геометрических фигур правильной формы. Когда кристаллы начинают соприкасаться друг с другом, а процесс затвердевания еще не закончен, тогда происходят искажения формы зерен. В практике замечено, что когда идет быстрое охлаждение, образуются мелкие зерна — мелкозернистая структура. При медленном охлаждении появление новых центров кристаллизации замедляется, но происходит рост зерна вокруг первичных центров кристаллизации. В этом случае металл будет иметь крупнозернистую структуру.
Процесс образования кристаллов в жидком состоянии и перехода металла в твердое состояние называется первичной кристаллизацией. Величина и форма зерна влияет на механические свойства металлов. Чем зерна мельче и чем правильнее их форма, тем большую твердость и прочность будет иметь металл. Чем зерна больше и чем искаженнее их форма, тем ниже твердость и прочность металла.
Аллотропия металлов. Такие металлы, как железо, кобальт, никель и др., обладают способностью изменять кристаллическую решетку при нагревании в твердом состоянии. Процесс изменения кристаллических решеток в твердом состоянии называется вторичной кристаллизацией, или аллотропией, а состояние вещества (металла) при наличии нескольких кристаллических решеток при изменении параметров (давления, температуры) — аллотропическими модификациями, или полиморфизмом. Такие металлы, как железо, молибден, вольфрам, литий в твердом состоянии при нормальной температуре имеют объемно-центрированную кубическую ячейку; алюминий, медь, серебро в твердом состоянии при нормальной температуре имеют форму гранецентрированной кубической ячейки.
На рис. 7 представлены кривые нагрева и охлаждения металла (на примере марганца). Аллотропные состояния (модификации), имеющие те или иные кубические ячейки, обозначаются греческими буквами. Первоначальное аллотропное состояние при нормальной температуре обозначается буквой α, при дальнейших повышении температуры и перекристаллизации металла — буквами β, γ, δ и т. д. При охлаждении металлов и сплавов процесс аллотропного превращения происходит в обратном порядке, как правило при тех же температурах.
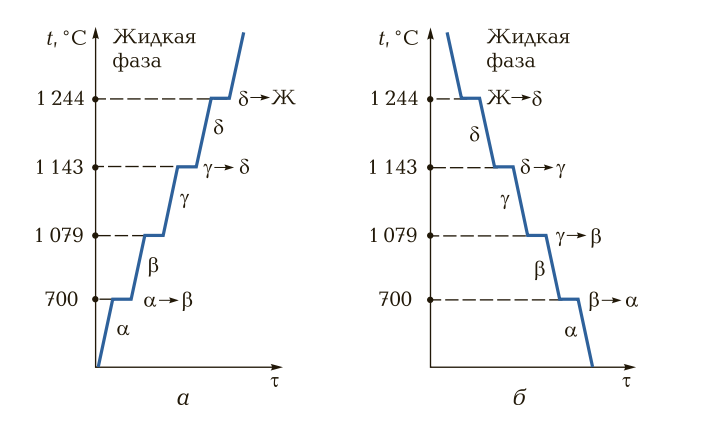
Рис. 7. Кривые нагрева (а) и охлаждения (б) марганца: t — температура; τ — время
2. Кристаллизация и структура металлов и сплавов
Порядок расположения атомов – тип кристаллической решетки – природное свойство металла, форма кристаллов и их размеры зависят от процесса перехода металла из жидкого состояния в твердое. Процесс образования кристаллов при затвердевании металлов называется кристаллизацией. При кристаллизации металлов выделяется тепло, а при переходе металлов из твердого состояния в жидкое происходит поглощение тепла. Наблюдения с помощью измеряющих температуру проборов за процессом понижения температуры
при переходе металла из жидкого состояния в твердое позволили установить определенную закономерность. Сначала температура понижается равномерно. В начальный период образования кристаллов вследствие выделения скрытой теплоты при формировании кристаллической решетки падение температуры прекращается, и она остается неизменной до полного затвердения металла. После того как весь металл затвердеет, температура снова начинает понижаться. Температура, соответствующая горизонтальной площадке, называется критической. Кристаллизация металлов подобна кристаллизации солей, и этот процесс состоит из двух элементарных процессов, протекающих одновременно. Первый заключается в образовании центров кристаллизации, или зародышей кристаллов, второй – в росте кристаллов из этих центров.
Первый этап – появление зародышей кристаллов металла. Второй этап – по мере остывания металла к зародышам присоединяются все новые и новые атомы жидкого металла, которые группируются в определенном порядке один возле другого, образуя элементарные ячейки кристаллической решетки. Этот процесс продолжается до тех пор, пока не закончится кристаллизация. Причем кристаллы затвердевшего металла имеют неправильную и весьма разнообразную форму, что объясняется условиями кристаллизации.
В процессе кристаллизации увеличивается количество кристаллов – в 1 мм 3 может образоваться свыше 1000 кристаллов. Кристаллы, имеющие неправильную внешнюю форму, называются кристаллитами, или зернами. Чистые металлы относительно редко применяются в машиностроении и других отраслях хозяйственного комплекса. Более широко используются сплавы, состоящие из двух и более элементов (из двух металлов, например меди и цинка, или из металла и неметалла, например железа и углерода). Элементы, входящие в сплав, называются компонентами. В зависимости от расположения атомов в кристаллической решетке различают твердые растворы замещения и твердые растворы внедрения. В твердом растворе замещения атомы растворимого компонента замещаются атомами растворителя, а в твердом растворе внедрения атомы растворителя размещаются между атомами растворимого компонента в наиболее слабых местах элементов кристаллической решетки.
Сплавы, представляющие собой твердые растворы, отличаются ценными свойствами. Они тверже и прочнее, чем входящие в него компоненты.
Компоненты некоторых сплавов при кристаллизации могут входить в химическую связь, образуя химическое соединение. Химические соединения обладают очень высокой твердостью и хорошим электросопротивлением.
Данный текст является ознакомительным фрагментом.
Продолжение на ЛитРес
Свойства металлов и сплавов
Свойства металлов и сплавов В этой главе будет рассказано о металлах, сплавах и их свойствах, что полезно не только для мастеров слесарного дела, но для всех, кто занимается чеканкой, ковкой, художественным литьем (этому посвящены последующие главы).Металл относится к
3. Способы упрочнения металлов и сплавов
3. Способы упрочнения металлов и сплавов Поверхностное упрочнение металлов и сплавов широко применяется во многих отраслях промышленности, в частности в современном машиностроении. Оно позволяет получить высокую твердость и износостойкость поверхностного слоя при
9. Кристаллизация металлов; зарождение кристаллов, критический зародыш; гомогенное и гетерогенное зарождение кристаллов; рост кристаллов. Кривые Таммана
9. Кристаллизация металлов; зарождение кристаллов, критический зародыш; гомогенное и гетерогенное зарождение кристаллов; рост кристаллов. Кривые Таммана Кристаллизация – это процесс перехода металла из жидкого состояния в твердое с образованием кристаллической
17. Теплоемкость и теплопроводность металлов и сплавов
17. Теплоемкость и теплопроводность металлов и сплавов Теплоемкость – это способность вещества поглощать теплоту при нагреве. Ее характеристикой является удельная теплоемкость – количество энергии, поглощаемой единицей массы при нагреве на один градус. От величины
18. Дилатометрия. Магнитные свойства металлов и сплавов. Методы определения
18. Дилатометрия. Магнитные свойства металлов и сплавов. Методы определения Дилатометрия – раздел физики; основная задача: изучение влияния внешних условий (температуры, давления, электрического, магнитного полей, ионизирующих излучений) на размеры тел. Главный предмет
32. Отжиг 1-го рода. Неравновесная кристаллизация
32. Отжиг 1-го рода. Неравновесная кристаллизация Этот вид термической обработки возможен для любых металлов и сплавов. Его проведение не обусловлено фазовыми превращениями в твердом состоянии. Нагрев при отжиге 1 рода, повышая подвижность атомов, частично или полностью
43. Маркировка, структура, свойства и области применения цветных металлов и их сплавов
43. Маркировка, структура, свойства и области применения цветных металлов и их сплавов К цветным металлам относятся медь, алюминий, магний, титан, свинец, цинк и олово, которые обладают ценными свойствами и применяются в промышленности, несмотря на относительно высокую
8. Плавление металлов и строение расплавов
Плавление – это физический процесс перехода металла из твердого состояния в жидкое расплавленное. Плавление – процесс, обратный кристаллизации, происходит при температуре выше равновесной, т. е. при перегреве. Поскольку жидкий металл обладает большей внутренней энергией, чем твердый, при кристаллизации выделяется теплота. Между теплотой Q и температурой кристаллизации Тк существует определенная связь. Степень перегрева при плавлении металлов не превышает нескольких градусов.
В жидком состоянии атомы вещества из-за теплового движения перемещаются беспорядочно, в жидкости имеются группировки атомов небольшого объема, в их пределах расположение атомов аналогично расположению в решетке кристалла. Эти группировки неустойчивы, они рассасываются и снова появляются в жидкости. При переохлаждении жидкости некоторые крупные группировки становятся устойчивыми и способными к росту. Эти устойчивые группировки атомов называют центрами кристаллизации (зародышами). Для осуществления процесса плавления необходимо наличие некоторого перегрева над равновесной температурой, т. е. термодинамического потенциала. Выше равновесной температуры более устойчив жидкий металл, он имеет меньший запас свободной энергии. Ниже этой температуры более устойчив твердый металл. При равновесной температуре свободные энергии жидкого и твердого состояния одинаковы, поэтому при этой температуре обе фазы (жидкая и твердая) могут сосуществовать одновременно и притом бесконечно долго. Равновесная температура очень близка к температуре плавления Тпл, с которой ее часто сравнивают. При охлаждении переход из жидкого состояния в твердое сопровождается образованием кристаллической решетки, т. е. кристаллизацией. Чтобы вызвать кристаллизацию, жидкий металл нужно переохладить до температуры ниже температуры плавления.
Жидкости, находящиеся при температуре, близкой к температуре плавления называются расплавами. Расплавы бывают металлическими, ионными, полупроводниковыми, органическими и высокополимерными. В зависимости от того, какие химические соединения образуют расплавы, выделяют солевые, оксидные, оксидно-силикатные и другие расплавы.
Большинство расплавов имеют в составе искосаэдрические частицы.
В процессе плавления химические связи в расплавах подвергаются видоизменению. В полупроводниках наблюдается образование металлической проводимости, у некоторых галогенидов вместо ионной проводимости происходит снижение электрической проводимости из-за образования расплава с молекулярным составом. Уровень температуры также влияет на тип связи в расплавах.
Среднее координационное число и межатомные расстояния также являются характеристиками расплавов. В процессе плавления металлов происходит уменьшение координационного числа примерно на 10–15 %. В тоже время межатомные расстояния остаются прежними. При плавлении полупроводников происходит увеличение их координационного числа в 1,5 раза, расстояние между атомами также увеличивается. Многокомпонентные расплавы характеризуются неравновесными, метастабильными состояниями, которые имеют взаимосвязь со структурой первоначальных твердых фаз.
Во многих случаях встречается отставание (гистерезис) свойств расплавов в процессе изменения температуры. На свойства и строения расплавов оказывают влияние следующие факторы: температура, время выдержки, скорость колебания температуры, тот материал, из которого создан контейнер, а также наличие примесей.
Состав расплавов отличается своей сложностью. В ионных расплавах могут содержаться простые или комплексные ионы, недиссоциированные и полимерные молекулы, а также свободные объемы. Силикатные расплавы могут содержать изолированные кремнекислородные тетраэдры и образуемые ими цепи, кольца, сетки и каркасы.
Однозначная модель структуры расплавов формируется достаточно сложно, т. к. расплавы содержат разные виды частиц и связи. Основная функция моделей: определение и интерпретация свойств расплавов, а также расчет свойств.
Расплавы в металлургической области подразделяются на промежуточные, побочные и конечные продукты. Используя расплавы в качестве электролитов, в металлургии производят и рафинируют металлы, а также осуществляют нанесение покрытий. Многие сплавы образуются в виде расплавов. Монокристаллы и эпитаксиальные пленки выращиваются из расплавов. В качестве катализаторов принято использовать металлические, солевые и оксидные расплавы. Солевые расплавы применяют в отжиговых и закалочных ваннах, высокотемпературных топливных элементах, в качестве теплоносителей, флюсов в процессе пайки и сварки металлов, реакционных сред в неорганическом и органическом синтезе, а также как поглотители, экстрагенты и т. д. Некоторые расплавы используются для получения силикатных, фторидных и иных специальных стеков и аморфных металлов.
Строение древесины
Строение древесины Сделав только поперечный срез, можно четко рассмотреть строение древесины. Каждый брусок необтесанного дерева имеет кору – это кожа дерева, которая не используется в работе, ее обязательно снимают. Под корой располагается зона роста дерева, которая
ЛЕКЦИЯ № 1. Строение древесины
ЛЕКЦИЯ № 1. Строение древесины 1. Виды древесных пород и части дерева Растущие деревья имеют следующие составные части: корни, ствол, ветви, листья. Корневая система деревьев выполняет функции поставщика влаги и питательных веществ из почвы по стволу и ветвям к листьям.
2. Макроскопическое строение древесины
2. Макроскопическое строение древесины При поперечном разрезе ствола дерева можно установить главные макроскопические признаки: заболонь, ядро, годичные слои, сердцевинные лучи, сосуды, смоляные ходы и сердцевинные повторения.У молодых деревьев всех пород древесина
1. Строение металлов
1. Строение металлов Металлы и их сплавы – основной материал в машиностроении. Они обладают многими ценными свойствами, обусловленными в основном их внутренним строением. Мягкий и пластичный металл или сплав можно сделать твердым, хрупким, и наоборот. Для того чтобы
Свойства расплавов стекол
Свойства расплавов стекол К свойствам расплавов стекломассы относятся вязкость, связанная с ней скорость твердения, поверхностное натяжение и кристаллизация, а также теплоемкость, теплопроводность, электрическая проводимость. Значение этих свойств при производстве
§ 3.3 Строение атомов и периодический закон Менделеева
§ 3.3 Строение атомов и периодический закон Менделеева Свойства простых тел, а также формы и свойства соединений элементов, находятся в периодической зависимости (или, выражаясь алгебраически, образуют периодическую функцию) от их атомных весов. Д.И. Менделеев Считается,
§ 3.6 Строение ядер
§ 3.6 Строение ядер Чем больше в ядре должно поместиться нуклонов, тем больше должна быть площадь поверхности ядра, где происходят присоединения то протонов, то нейтронов… Этим особенностям лучше всего отвечает форма ядра в виде двух пирамид Хеопса, соединённых
§ 4.14 Строение вещества и химическая связь
§ 4.14 Строение вещества и химическая связь Что, наконец, представляется нам затверделым и плотным, То состоять из начал крючковатых должно несомненно, Сцепленных между собой наподобие веток сплетённых. В этом разряде вещей, занимая в нём первое место, Будут алмазы
Глава 32 Строение Пространства – Времени
Глава 32 Строение Пространства – Времени «Действие есть кривизна Мира» Павел Дмитриевич Успенский, 1911 год Мы уже предполагали аналогии квантового строения микромира и макромира, при определенных условиях. Далее, будет показаны законы резонансного строения нашего
2. Зеренное строение металлов. Границы зерен и субзерен
2. Зеренное строение металлов. Границы зерен и субзерен Металлы – это поликристаллические тела, они состоят из мелких кристаллов. Характеризуются металлическими свойствами и составляют 50 % всех химических элементов. Строение металлов и их сплавов кристаллическое.В
10. Строение слитка и аморфные сплавы
10. Строение слитка и аморфные сплавы Строение стального слитка впервые дано в 1878 г. Д.К. Черновым. Структура литого слитка состоит из трех основных зон. Первая зона – наружная мелкозернистая корка, которая состоит из дезориентированных мелких кристаллов –
Кристаллическое строение и кристаллизация сплавов
Строение сплавов более сложное, чем строение чистого металла, и зависит от взаимодействия компонентов при кристаллизации.
Компоненты сплава при кристаллизации могут образовывать:
• твердые растворы, когда элементы сплава взаимно растворяются один в другом;
• механическую смесь – при полной взаимной нерастворимости, когда сплав состоит из смеси кристаллов составляющих ее компонентов;
• химическое соединение, при котором компоненты сплава вступают в химическое взаимодействие, образуя новую кристаллическую решетку.
Процесс перехода сплава из жидкого состояния в твердое с образованием кристаллических решеток (кристаллов) называется первичной кристаллизацией. Свойства металлических сплавов зависят от образующейся в процессе кристаллизации структуры. Под структурой понимают наблюдаемое кристаллическое строение сплава. Процесс кристаллизации начинается с образования кристаллических зародышей – центров кристаллизации.
Скорость кристаллизации зависит от скорости зарождения центров кристаллизации и скорости роста кристаллов в прямой зависимости, т. е. чем выше скорость роста кристаллов и больше число образующихся зародышей, тем быстрее протекает процесс кристаллизации сплава. Внутренняя структура сплава зависит от формы ориентировки кристаллических решеток в пространстве и скорости кристаллизации.
Центрами кристаллизации могут быть группы элементарных кристаллических решеток, неметаллические включения, тугоплавкие примеси. Процесс кристаллизации обычно начинается в направлении, противоположном отводу тепла.
Если процесс роста кристаллов не ограничивается, то образуются кристаллы неограниченной длины, в форме дерева или елочек-дендриты (рис. 38).
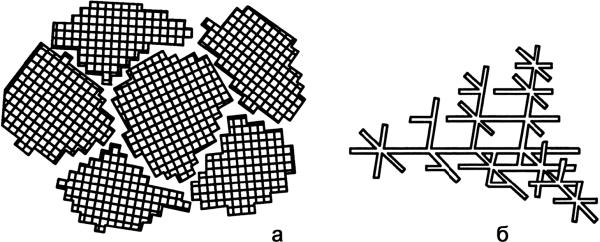
Рис. 38.
Схема строения поликристалла (а), и дендритный кристалл (б)
Так как процесс кристаллизации происходит в различных направлениях из многих центров кристаллизации, то ветви дендритов обычно искажаются, ограничивая при этом рост других кристаллов. Кристаллы неправильной формы называются зернами, или кристаллитами. В месте соприкосновения кристаллов рост их граней прекращается, и развиваются только отдельные грани. Число центров кристаллизации и скорость роста кристаллов влияют на величину зерна и, следовательно, на свойства металлов. При этом особую роль играет скорость охлаждения и переохлаждения расплавленного металла.
Зерна отличаются размером и ориентацией в кристалле. Они обычно повернуты относительно друг друга на десятки градусов. На границах зерен находится поврежденный переходный слой, порядка нескольких атомных слоев. Свойства и химический состав этого слоя могут сильно отличаться от свойств и состава зерен основного металла или сплава.
Кристаллические решетки могут иметь структурные дефекты: точечные, линейные, поверхностные, возникающие в результате вакансий (перемещения на свободные места) атомов.
При наличии таких дефектов зерно (кристаллит) разделяется на блоки в виде микромозаичной структуры (рис. 38).
При переходе сплава из жидкого состояния в твердое происходит усадка, т. е. уменьшение удельного объема зерен кристаллов. В результате усадки между зернами кристаллов в местах соприкосновения растущих дендритов в междуосных пространствах возникают микропустоты. Пустоты могут заполняться неметаллическими включениями (фосфидами, сульфидами и т. п.) или оставаться в виде раковин, микротрещин, пустот. Такие включения становятся центрами развития трещин, надрывов при приложении нагрузки или нагреве.
Кристаллическое строение металлов
Кристаллическое строение металлов Все металлы в твердом состоянии имеют кристаллическое строение. Атомы в твердом металле расположены упорядоченно и образуют кристаллические решетки. Расстояние между атомами называют параметрами кристаллической решетки и измеряют в
Механические свойства металлов и сплавов
Механические свойства металлов и сплавов Основные механические свойства:• прочность;• пластичность;• твердость;• ударная вязкость.Приложение внешней нагрузки вызывает в твердом теле напряжение и деформацию.Напряжение – это нагрузка (сила), отнесенная к площади
Физические свойства металлов и сплавов
Физические свойства металлов и сплавов К физическим свойствам металлов и сплавов относятся:• температура плавления;• плотность;• температурный коэффициент;• электросопротивление;• теплопроводность.Физические свойства металлов и сплавов обусловлены их составом
Химические свойства металлов и сплавов
Химические свойства металлов и сплавов К химическим свойствам относится способность к химическому взаимодействию с агрессивными
Технологические свойства металлов и сплавов
Технологические свойства металлов и сплавов Технологические свойства – это способность материала подвергаться различным методам горячей и холодной обработки.У металлов и сплавов такими свойствами являются:• литейные свойства определяются жидкотекучестью, усадкой
Эксплуатационные свойства металлов и сплавов
Эксплуатационные свойства металлов и сплавов Эксплуатационные, или служебные, свойства металлов и сплавов определяются условиями работы машин или конструкций, изготовленных из этих материалов.В зависимости от условий работы выделяют:• коррозионную стойкость –
Кристаллизация металла сварочной ванны
Кристаллизация металла сварочной ванны Формирование сварного шва при дуговой сварке происходит путем кристаллизации расплавленного металла сварочной ванны.Кристаллизацией называют процесс образования кристаллов металла из расплава при переходе его из жидкого в
Сварка меди и ее сплавов
Сварка меди и ее сплавов Медь относится к тяжелым цветным металлам. Ее плотность составляет 8,9 г/см3, что выше, чем у железа. Благодаря высокой электропроводности, теплопроводности и коррозионной стойкости медь заняла прочное место в электропромышленности, приборной
Сварка алюминия и его сплавов
Сварка алюминия и его сплавов Алюминий – очень легкий металл, имеющий плотность 2,7 г/см3. Отличаясь малой массой, сравнительно высокой прочностью, хорошей обрабатываемостью, алюминиевые сплавы широко применяются во всех отраслях народного хозяйства. Высокая
Сварка титана и его сплавов
Сварка титана и его сплавов Титановые сплавы являются сравнительно новыми конструкционными материалами. Они обладают рядом ценных свойств, обусловливающих их широкое применение в авиационной промышленности, ракетостроении, судостроении, химическом машиностроении и
Кристаллизация
Кристаллизация Кристаллизация – процесс перехода тела из жидкого (иногда и газообразного) состояния в твердое, причем оно принимает более или менее правильную геометрическую форму
Машиностроение и механика
Металлы и сплавы - Строение и кристаллизация металлов
Строение и кристаллизация металлов
Металлы и сплавы в твердом состоянии имеют поликристаллическую структуру, состоящую из отдельных зерен – монокристаллических областей, ориентированных относительно друг друга под различными углами. На границе между зернами атомы имеют менее правильное расположение, чем в объеме зерна. Линейный размер зерен составляет 1–10 4 мкм.
С помощью рентгеноструктурного анализа установлено, что кристаллическое строение твердых тел, состоящих из различных атомов, описывается 14 различными типами пространственных элементарных ячеек.
Наиболее широко применяются металлы и сплавы, образованные одним из 3-х типов пространственных решеток, определяемых отдельно взятой элементарной ячейкой: кубической объемно центрированной ОЦК (a–Fe, b–Fe, d–Fe, Cr, W, Mo, V и др.); кубической гранецентрированной ГЦК (g–Fe, Cu, Al, Ni, Pb и др.); гексагональной плотноупакованной ГПУ (Ti, Mg, Zn, Be и др.) (рис. 3.1).
Переход металла из жидкого состояния в твердое (кристаллическое) называется кристаллизацией. Подвижность атомов при снижении температуры уменьшается, устанавливается определенный порядок в их расположении с образованием отдельных групп атомов, близких к элементарным ячейкам, имеющимся в твердом металле. Возникают центры кристаллизации – зародыши, вокруг которых постепенно образуется твердая фаза. Кристаллизация происходит вследствие перехода к более устойчивому состоянию с меньшей свободной энергией [7].
Рис. 3.1. Атомно-кристаллическое строение металлов с кубической объемно центрированной (а); гранецентрированной (б) и гексагональной плотноупакованной (в) элементарными ячейками
Процесс кристаллизации характеризуют кривыми охлаждения или нагревания, изображенными в координатах температура – время. На рис. 3.2 изображены кривые охлаждения металла и двухкомпонентного сплава. При охлаждении расплавленного чистого металла вначале (участок 1 – 2 рис. 3.2,а) понижение температуры идет плавно. При достижении температуры кристаллизации на кривой охлаждения (рис. 3.2,а) появляется горизонтальный участок 2 – 3, так как отвод тепла в окружающую среду компенсируется выделяющейся скрытой теплотой кристаллизации. После окончания кристаллизации температура вновь понижается равномерно (участок 3 – 4 рис. 3.2, а).
При охлаждении из жидкого состояния сплава двух металлов процесс кристаллизации протекает несколько иначе (рис. 3.2, б).
Точка 2 соответствует началу выделения из жидкой фазы кристаллов одного из компонентов сплава. Выделяющаяся при кристаллизации теплота замедляет ход кривой охлаждения, и в точке 2 кривая изменяет наклон (участок 2 – 3). Выпадение кристаллов избыточного компонента и равномерное понижение температуры происходят, пока сплав не достигнет определенного состава. В дальнейшем наблюдается одновременная кристаллизация компонентов, происходящая при постоянной температуре (участок 3 – 4 рис. 3.2,б). После полного затвердевания сплава в точке 4 его температура снова начинает снижаться по плавной кривой 4 – 5.
Рис. 3.2. Кривые охлаждения металла (а) и двухкомпонентного сплава (б)
Температура, соответствующая каким-либо фазовым превращениям в металле или сплаве, называется критической точкой. При нагревании твердых металлов или сплавов процесс их расплавления сопровождается поглощением теплоты.
Читайте также:
