Вопросы по теме металлы 9 класс с ответами
Обновлено: 21.09.2024
Проведение игр является одной из форм внеурочной работы по химии. Участие студентов в подготовке к мероприятию и в самой игре повышает мотивацию, способствует всестороннему развитию учащихся, вырабатывает самостоятельность и ответственность.
Актуализация знаний по дисциплине и развитие учебных умений
Формирование компетенций в соответствии с требованиями ФГОС:
· Организовывать собственную деятельность, выбирать типовые методы и способы выполнения поставленных задач, оценивать их эффективность и качество.
· Принимать решения в стандартных и нестандартных ситуациях и нести за них ответственность.
· Осуществлять поиск и использование информации, необходимой для эффективного выполнения поставленных задач, профессионального и личностного развития
· Использовать информационно-коммуникационные технологии.
· Работать в коллективе и команде, эффективно общаться с коллегами, руководством, потребителями.
· Брать на себя ответственность за результат выполнения заданий, за работу членов команды.
Во время подготовки и проведения игры происходит применение предметных знаний для объяснения явлений, наблюдаемых в жизни,
- применение химических знаний в нестандартных условиях, для разрешения вопросов из истории, биологии, литературы и т. д.
- работа по обеспечению внутри- и межпредметной интеграции знаний,
Внеурочные мероприятия создают благоприятные условия для развития творческих способностей учащихся во всем их многообразии, дают возможность существенно расширить и конкретизировать знания студентов, помогают решать воспитательные задачи.
Являясь важной составной частью работы преподавателя, внеурочная работа по химии помогает успешно решать педагогические задачи обучения и воспитания при органичном сочетании учебно-воспитательной работы в ходе уроков с целенаправленным воздействием на учащегося во внеурочное время. Внеурочная работа должна вызывать интерес у студентов, увлекать их различными видами деятельности. Во внеурочную работу необходимо вовлекать как учащихся, интересующихся химией, так и тех, кто не имеет к ней еще устойчивого интереса. В соответствии со склонностями студента подбираются различные виды работ. Начало внеурочной работе должно быть положено на уроках химии. Принцип единства урочной и внеурочной работы – важнейший принцип учебно-воспитательного процесса.
Металлы отверзают недро земное к плодородию;
металлы служат нам для пропитания нашего;
металлы облегчают купечество удобною к сему монетою.
И кратко сказать, ни едино художество,
ни едино ремесло простое
употребление металлов миновать не может.
Игра проходит в два этапа
1. Подготовительный этап.
2. Соревнование команд (два тура).
На подготовительном этапе преподаватель в учебных группах объявляет план мероприятий.
К запланированной дате игры каждая учебная группа должна подготовить: команду участников, выбрать металл для представления, разработать сценарий представления, включая компьютерную презентацию-характеристику выбранного металла по плану: строение, свойства, получение, применение. Задачи преподавателя – вызвать у учащихся стремление проявить свои способности, разбудить любознательность, дать первые импульсы к поиску дополнительной информации, желание реализовать свои возможности. А так же контролировать и направлять процесс подготовки
Для проведения соревнования необходимо подготовить помещение: подготовить места для команд, жюри и ведущих, установить аппаратуру для демонстрации презентаций.
Жюри оценивает:
- Уровень выступления группы, учитывая содержание, изобразительное и художественное исполнение;
- Качество электронной презентации, учитывая соответствие плану характеристики
- Правильность и находчивость при ответах на вопросы.
Членами жюри могут быть как преподаватели, так и студенты старших курсов. Система оценки продумывается заранее с учетом особенностей параллели студентов первого курса.
Для того, чтобы игра была интересной, форма проведения каждого из туров викторины различна. Желательно музыкальное(звуковое) сопровождение, применение различного реквизита. Максимум творчества!
I тур
В первом туре команды представляют выбранный металл. К этому туру участники готовились заранее.
II тур
Вопросы второго тура демонстрируются в форме презентации и сопровождаются комментарием ведущих. На ответ отводится по одной минуте.
Пока жюри подводит итоги, ведущие задают вопросы зрителям из области химических курьезов. (Верите ли Вы?)
Вопросы викторины МЕТАЛЛЫ
1. Некоторые металлы называются "благородными".Почему они носят такое название?
2. Оксиды и гидроксиды алюминия и некоторых других металлов могут взаимодействовать и с кислотами и со щелочами. Каким красивым словом называется такое двуликое поведение?
3. Химический состав человеческого организма сложен и разнообразен. В его состав входят и химические элементы – металлы.Атомов какого металла в человеческом организме больше всего?
4. Вы видите изображение под микроскопом одного хорошо известного вам вещества. Различимы микроскопические раковины. Назовите это вещество и напишите химическую формулу
5. Вы видите архитектурные шедевры. Каркас купола Казанского собора и Эйфелева башня созданы из одного металла.О каком металле идет речь?
6. Вы видите символическое изображение “лев, пожирающий солнце”. Так алхимики изображали одно из химических взаимодействий. Солнце здесь – символ золота. Какое вещество символизирует лев?
7. Вы видите чайник, который неоднократно использовался, но в нем, как и в другом в нашей местности нет накипи, но есть рыжий налёт. А) почему в наших чайниках нет накипи? Б)что это за рыжий налёт?
8. Ионы какого металла придают красный цвет и этому раствору и настоящей крови?
9. Вы видите прекрасное произведение архитектуры – решётку Летнего сада. Какая связь между решёткой и “свинским” железом?
10. Вы видите красивое природное образование. Это скелет морских организмов – кораллов. Какой “живой” металл содержат живые организмы?
Вопросы и ответы викторины МЕТАЛЛЫ
Ответ: Потому что не вступают в химические реакции с большинством веществ (не окисляются)
Ответ: амфотерность
Ответ: Кальция( Ca ) в организме взрослого человека более 2 кг. В основном кальций входит в состав костной ткани.
Ответ: Вещество – мел, основной его компонент – карбонат кальция СаСО3
Ответ: О железе.
Ответ: “ Царскую водку” – смесь концентрированных соляной и азотной кислот, растворяющую золото.
Ответ: А) потому что вода в Неве мягкая. Б) это соединения железа.
Ответ: Ионы железа
Ответ: Она сделана из чугуна, который в Англии называют “свинским” железом. Считалось, что чугун – непригодный продукт.
Вопросы по теме металлы 9 класс с ответами
Тесты по химии 9 класс. Тема: "Металлы"
Правильный вариант ответа отмечен знаком +
1. В какой группе находится металл полоний:
2. К четвертой группе относится элемент:
3. Как проходит условная граница между металлическими и неметаллическими элементами:
4. Металлургический процесс включает в себя:
+ восстановление ионов металла
- окисление ионов неметалла
- восстановление ионов неметалла
5. Пирометаллургией является:
+ процесс получения металлов из их соединений при высокой температуре
- процесс получения неметаллов из их соединений при низкой температуре
- процесс получения неметаллов из их соединений при высокой температуре
6. В пирометаллургии используются:
- как восстановители, так и окислители
7. При алюмотермии используют металл:
8. В гидрометаллургии получают:
+ металлы из растворов их соединений
- неметаллы из растворов их соединений
- воду из растворов их соединений
9. В электрометаллургии используется процесс:
- обработка при предельно высокой температуре
- реакция замещения и соединения
тест 10. При электролизе восстановителем является:
11. Чем определяются физические свойства металлов:
+ типом кристаллической решетки
- количеством протонов, электронов, нейтронов
- расположением в определенной группе или подгруппе
12. Отличием атомов металлов от неметаллов можно назвать:
+ содержат небольшое количество электронов на внешнем уровне, большой радиус и низкая электроотрицательность
- содержат большое количество электронов на внешнем энергетическом уровне, маленький радиус и высокая электроотрицательность
- содержат большое количество электронов на внешнем энергетическом уровне, большой радиус и высокая электроотрицательность
13. Металлической является связь:
+ между ионами металлов
- между ионами неметаллов
- между ионами металла и неметалла
14. Для какого агрегатного состояния не характерна металлическая связь:
- для жидкого состояния
- для твердого состояния
15. Чем обусловлена электропроводность металлов?
+ наличием свободных электронов
- наличием свободных нейтронов
- наличием свободных протонов
16. С повышением температуры электропроводность:
- может как повышаться, так и понижаться
17. Электропроводность увеличивается от:
+ ртути к серебру
- алюминия к цинку
18. Максимальной теплопроводностью обладает:
19. Наиболее пластичным металлом называют:
тест-20. Твердым веществом при нормальных условиях не является:
21. Самым твердым металлом является:
- щелочно – земельные металлы
22. Самым тяжелым металлом является:
23. Самым тугоплавким металлом является:
24. К черным металлам можно отнести:
25. Какие степени окисления имеют металлы:
- как положительные, так и отрицательные
26. Металлы в соединениях проявляют свойства:
- окислительно – восстановительные свойства
27. Какая закономерность уменьшения восстановительных свойств металлов:
+ слева направо, снизу вверх
- справа налево, сверху вниз
28. Легкому окислению поддаются:
29. Чем левее находится металл в ряду, тем:
+ больше его восстановительная способность
- меньше его восстановительная способность
- больше его окислительная способность
тест_30. Лантаноиды на внешнем энергетическом уровне содержат по:
31. Сколько примерно имеются металлов в периодической системе Менделеева:
+ более девяти ста
- менее восьми ста
- менее двадцати ста
32. Во сколько раз литий легче осмия:
+ в сорок пять раз
- в шестьдесят раз
- в семьдесят раз
33. Провода высоковольтных изготавливают из:
34. Бронза является сплавом:
- железа и алюминия
- вольфрама и серебра
35. Кто изображен на данной фотографии:

36. При взаимодействии с кислородом металлы образуют:
37. При взаимодействии щелочноземельных металлов с водой образуются:
- альдегиды и кетоны
38. Оксидом железа можно назвать:
39. В алюминотермии используется:
тест*40. Взаимодействие металлов с оксидами является реакцией:
Тесты по химии 11 класс. Тема: "Металлы"
3. Как проходит условная граница между между металлическими и неметаллическими элементами:
+ слева направо, снизу-вверх
28. На данном изображении представлена:
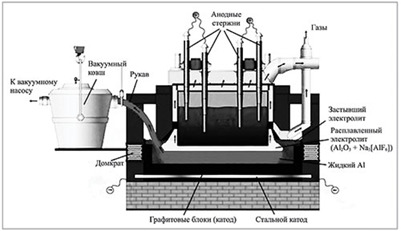
+ схема получения алюминия электролизом
- схема получения железа электролизом
- схема получения гидроксида алюминия электролизом
35. На данном рисунке представлена:
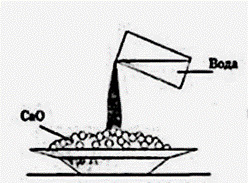
+ реакция гашения извести водой
- реакция соединения калия с хлором
- окисление перманганата калия
Викторина по теме "Металлы" (9 класс)
Какой из металлов в глубокой древности называли «небесная медь» и почему?
Железо. Первое железо, с которым познакомился человек, было метеоритным, т.е. «небесного» происхождения, обрабатывали его так же, как и медь. Древнегреческое название железа «сидерос» означает «звездный», а древнегреческое название железа «еркат» переводится как «капнувший с неба».
В каких географических названиях встречается слово «медь»?
Медногорск (город на Южном Урале), остров Медный (один из Командорских островов), Кипр (от латинского названия меди «купрум»).
Если бы существовал приз за активность, то атомам, какого металла его присудили бы?
Цезию, если не считать франций, которого практически нет в природе.
Почему во время похода Александра Македонского в Индию офицеры его армии реже болели желудочно-кишечными заболеваниями, чем солдаты?
Потому что посуда офицеров была изготовлена из серебра, обладающего бактерицидными свойствами.
На каком свойстве ртути был основан древний способ золочения?
Какой из металлов может быть «чумой»? Что вы об этом знаете?
Олово. «Оловянная чума» - это своеобразное явление, при котором белое олово при температуре ниже 1-3,5 градусов превращается в серое. Поскольку плотность и кристаллическая структура модификаций разные, оловянные изделия разрушаются. Этот процесс на слабом морозе идет медленно. Он быстро нарастает при температуре ниже -25 градусов и достигает максимальной скорости при -48 градусах.
Вторая и последняя экспедиция английского путешественника Роберта Фолкона Скотта в 1912г. К Южному полюсу закончилась трагически. В январе 1912г. Скотт и четверо его друзей пешком достигли Южного полюса и обнаружили по оставленной палатке и записке, что всего за четыре недели до них Южный полюс был открыт экспедицией Р. Амундсена. С огорчением они двинулись в обратный путь при очень сильном морозе. На промежуточной базе, где должно было храниться горючее, они его не нашли. Железные канистры с керосином оказались пустыми, так как имели «кем-то вскрытые швы», которые раньше были запаяны оловом.
Так при трагических обстоятельствах было обнаружено, что белое олово, которым были запаяны канистры, превратились в пылевидное олово. Скотт и его спутники замерзли около распаянных канистр.
Гуси спасли Рим, а погубил Рим, по мнению токсикологов, металл. Какой это металл, что вам известно об этом?
Рим спасли гуси – это известно всем. А в падении Рима, по мнению некоторых ученых-токсикологов, повинно отравление свинцом. Есть версия, что использование отравленной в свинце посуды и свинцовых косметических красок было причиной быстрого вымирания римской аристократии. Из-за систематического отравления малыми дозами свинца средняя продолжительность жизни римских патрициев не превышала 25 лет. Люди низших сословий, согласно этой теории, в меньшей степени подвергались отравлению, поскольку не имели дорогой посуды и не употребляли косметических средств.
«Семь металлов создал свет
По числу семи планет…»
Назовите эту великолепную семерку.
Солнце-золото, Луна_серебро, Марс-железо, Меркурий-ртуть, Юпитер-олово, Венера-медь, Сатурн-свинец. Известный русский революционер, ученый-химик академик Н. А. Морозов написал:
Читайте также:
