Впитывает ли воду металл
Обновлено: 19.05.2024
То, что грязную и мутную воду пить не стоит, знают даже дети. Однако земля, пыль и даже бактерии в жидкости — это далеко не все опасные элементы, которые в ней встречаются.
В воде могут быть и куда более страшные враги человеческого здоровья — тяжелые металлы.
Что это такое?
Под термином «тяжелые металлы» принято понимать элементы, чья относительная атомная масса превышает 50 единиц, или чья плотность составляет более 8 г/см3. К ним относят около 40 единиц.
С учетом токсичности, стойкости, способности накапливаться во внешней среде и масштабов распространения, особого контроля требует только ¼. Сам термин получил широкое распространение больше не как химический, а как медицинский или природоохранный.
Все химические элементы в малых количествах нужны человеческому организму для нормального роста и функционирования. Но избыток некоторых металлов приводит к развитию патологий, болезням, нервным расстройствам.
Источником опасных веществ сегодня часто становится вода, не прошедшая надлежащую очистку, либо вода из родников, расположенных в местах загрязнения. Даже жидкость из водопровода в жилых домах иногда опасна для питья.
Что такое тяжелые металлы, расскажет видео:
Какие элементы относят к этой группе:
Некоторые химики относят сюда еще алюминий, бериллий, кремний и мышьяк. Железо относят в группу условно, поскольку оно в больших количествах ухудшает цвет и вкус воды, что уже выступает явной преградой для ее употребления.
Все вещества в воду попадают не в чистом виде, а в виде ионов и солей, которые порой еще более токсичны.
Абсолютно чистой воды в природе не существует. В ней в любом случае будут какие-то минимальные остатки минералов, металлов и микроэлементов.
Разработаны предельно допустимые концентрации тяжелых металлов в воде бытового и хозяйственного назначения, при которых она считается пригодной для питья и использования.
| Элемент | Предельный показатель вредности | ПКД мл/л |
| Cu Медь | Привкус, органолептический | 1,0 |
| Fe Железо | Цвет | 0,3 |
| Zn²⁺ Цинк | Общий | 1,0 |
| Cd Кадмий | — | 0,001 |
| Si Кремний | Санитарно-токсикологический | 0,05 |
| Hg Ртуть | Санитарно-токсикологический | 0,0005 |
| Mo Молибден | Санитарно-токсикологический | 0,25 |
| Pb Свинец | Санитарно-токсикологический | 0,03 |
| Mn Марганец | Органолептический | 0,1 |
| Со Кобальт | Санитарно-токсикологический | 0,1 |
| As Мышьяк | Санитарно-токсикологический | 0,05 |
| Ве2+ Бериллий | Санитарно-токсикологический | 0,0002 |
Каков вред и опасность для человека?
В воде ионы тяжелых металлов обладают большей биологической активностью, а значит им легче внедриться в организм и влиять на него:
Ионы тяжелых металлов в совокупном воздействии провоцируют рак, подавляют выработку гормонов и даже повреждают структуру ДНК.
Источники
Их делят на естественные и искусственные (вызванные деятельностью человека). К естественным причисляют грунтовые воды, вымывание полиметаллической руды, извержения вулканов, кислотные дожди.
К искусственным или антропогенным относят:
Постепенное увеличение примесей тяжелых металлов в воде происходит при ее испарении. Аналогично при кипячении не все элементы удаляются, поэтому кипячение, как метод очистки воды, в данном случае не актуален.
Методы проверки и выявления содержания примесей
Современные лабораторные исследования водяных проб позволяют выяснить наличие тяжелых металлов в жидкости тремя способами:
- Фотометрический анализ. Основан на избирательном поглощении электромагнитного излучения.
- Атомно-эмиссионная спектрометрия. Это исследование спектров испускания свободных атомов и ионов вещества.
- Флуориметрический или люминесцентный анализ. Предполагает исследование интенсивности излучения, возникающего при выделении избыточной энергии молекулами тестируемого вещества.
Определение тяжелых металлов в воде в домашних условиях, видео-инструкция:
Технологии и способы очистки сточных вод
На водоочистных сооружениях используют несколько способов. На их выбор влияет степень загрязнения и концентрация тех или иных элементов в жидкости:
- Ионный обмен. Это обмен между ионами в растворе и ионами на поверхности твердой фазы — ионита (смолы). Плюс — очистка от Zn, Cu, Cr, Ni, Pb, Hg, Cd и цианидов. Недостаток способа — вторичное загрязнение воды после восстановления.
- Нанофильтрация. Прогонка воды через и вдоль микрофильтров из полиамида, керамики, целлюлозы. Подходит для заключительного этапа очистки либо для умеренных загрязнений.
- Реагентный. Предполагает химическое превращение высокотоксичных растворов в нетоксичные соединения путем добавления в воду различных концентратов. Концентраты формируются исходя из первичных проб воды. Недостатки метода: часто требуется доочистка, дороговизна реагентов.
Заключение
Тяжелые металлы в воде опасны для человека. Эта проблема — результат многолетнего прогресса. Решить ее можно только путем улучшения экологической обстановки, поскольку даже современные методы очистки воды не позволяют досконально удалить все вредные примеси.
Взаимодействие воды с металлами
Вода обладает разнообразными свойствами. Она может замерзать. Превращаться в пар. С водой человек дружит с рождения. Помимо всего этого она так же может вступать во взаимодействие с металлом. Как? Читайте нашу статью, и Вы узнаете об этом! Вступая в контакт с жидкостью, металлы способны давать самые удивительные реакции! Например: чтобы насытить воду железом её настаивают несколько часов на железе, после чего употребляют во внутрь, а если бросить в стакан с водой щелочной металл то произойдет взрыв. Существует множество разнообразных металлов и каждый случай взаимодействия уникален! Проводите опыты, делайте собственные открытия, а посвятить Вас в основы взаимодействия воды с металлами поможет наша статья!
Как они взаимодействуют?
Взаимодействие металла с водой может происходить по разному, в зависимости от металла и воды. Каждый металл обладает своими неповторимыми особенностями. Так же, может показаться, что формулы очень сложные, однако со временем Вы легко научитесь их читать. Если алюминий, железо вступает в активные реакции с водой, то это значит что в нем присутствуют образующиеся соли. Он окисляется ионами водорода. Проследить это можно по формуле и записать в виде сокращенной формулировки Me + nH + → Me n+ + H2↑
Вступая в реакцию с водой, в исключительных ситуациях образуются гидроксиды. Очень активно в спокойных условиях вступают в реакцию с влагой щелочные металлы, например Литий (Li), натрий (Na) , Калий (К), Рубидий (Rb) , Цезий (Cs), Франций (FR).
Щелочные металлы вступают в очень бурную реакцию с водой. Отследить процесс взаимодействия металлов с водой можно по формулам:
NaH + HCl ® NaCl + H2

Разные активные реакции металлы выдают так же при различных условиях. Например, в состоянии покоя и при комнатной температуре реакция может быть одна, а в других условиях взаимодействие проявляться по разному: Тихо, спокойно, бурно.
Активные металлы способны вступать во взаимодействие с водой при обычных условиях согласно схеме: 2Me + 2nH2O → 2Me(OH)n + nH2 .Итогом окисления как правило становится гидроксид Me(OH)n (где n-степень окисления металла).
Приведем пример: Ca + 2H2O → Ca(OH)2 + H2↑
Металлы же со средней степенью активности вступают во взаимодействие с водой при нагревании по схеме: 2Me + nH2O Me2On + nH2 . Итогом такой реакции становится появление оксида металла. Его формула — Me2On (где n-степень окисления металла) .
Пример взаимодействие активных металлов с водой
Металлы так же используют при изготовлении кухонной утвари. К примеру алюминиевая сковородка, металлический корпус чайника, лопасти блендера. Тут важна стойкость металла. Самой известной реакцией металла на воду является окисление самой обыкновенной стали на воздухе и в воде. Железо в таком случае разрушается, ржавеет. Происходящие при этом процессы являются весьма сложными и удивительным природным процессом. Если же окисление происходит в морской воде, то процесс ускоряется, этому способствует определенная концентрация соли находящаяся в составе воды.
Противостоять образованию ржавчины можно при использовании разнообразных лаков, призванных защитить от коррозии металла и перехитрить химические законы! Так же, вода вступая в реакцию с нагретым металлом способна образовывать накипь.
Это явление можно наблюдать на частях чайника сделанных из алюминия или стали, который давно не чистили. Такой чайник достаточно прокипятить с лимонной кислотой и он снова будет как новый!
Иногда образование накипи не связано с активными металлами, а имеет немного другую природу. В частности, накипь может появляться из-за солей жесткости в воде. В таком случае нужно купить качественный фильтр для жесткой воды.
Страшно опасные: тяжелые металлы в воде
На Земле впервые создана металлическая вода. Она оказалась золотой

Примерно через пять секунд вокруг капли образовалась тонкая металлическая пленка воды, которую можно было распознать по золотистому мерцанию.
Фото HZB.

Последовательность образования металлической воды на капле натрий-калиевого сплава. Она окрашивается в золотой цвет по мере того, как электроны и катионы металлов перемещаются в слой воды.
Фото HZB.

Установка для получения металлической воды.
Фото HZB.



Большинству людей, хоть что-то понимающих в физике и технике, может показаться удивительным, что вода, которая может ударить током, на самом деле является изолятором.
Все дело в примесях. Вода из-под крана проводит электрический ток благодаря содержащимся в ней солям. Дистиллированная же вода имеет свойства диэлектрика, потому что молекулы воды сами по себе электрически нейтральны.
Соответственно, чтобы сделать дистиллированную воду проводником, нужно изменить ее структуру таким образом, чтобы в ней появились свободные электроны.
Этого можно добиться, сжимая воду под давлением около 48 мегабар. По сути, таким образом можно "выдавить" электроны из молекул воды. Однако такое давление ни в лабораторных, ни в производственных условиях недостижимо. Оно, к сожалению, может существовать только в ядрах очень больших планет или звезд.
Другой способ наделить воду свободными электронами – отдать ей чужие. Этим и занялась команда исследователей, работающая на установке BESSY II в Берлине.

Необычный эксперимент объединил 11 научных институтов разных стран мира. Ученые решили подарить воде электроны щелочных металлов, которые легко отдают их со внешних оболочек своих атомов.
Проблема состояла в том, как соединить воду со щелочным металлом, чтобы он поделился с ней своими электронами. Ведь в обычных условиях щелочные металлы, попадая в воду, шипят, воспламеняются и даже взрываются. Поэтому исследователи не стали погружать металл в воду, а нанесли тонкий слой воды на щелочной металл.
Внутри вакуумной камеры из сопла капал сплав натрия и калия. Поясним, что оба эти металла при комнатной температуре находятся в жидком состоянии. Затем в камеру по трубам подавался водяной пар. Он осаждался чрезвычайно тонким слоем на металлические капле.

Последовательность образования металлической воды на капле натрий-калиевого сплава. Она окрашивается в золотой цвет по мере того, как электроны и катионы металлов перемещаются в слой воды.
Электроны и катионы (атомы, лишенные электронов) металлов перетекали из капель в наружный слой воды. В итоге получалась проводящая электричество вода. То есть вода из диэлектрика (плохо проводящего ток) превратилась в металл.
"И вы можете увидеть фазовый переход воды в металл невооруженным глазом! – говорит Роберт Зайдель (Robert Seidel), автор исследования. – Серебристая натриево-калиевая капля становится отчетливо золотистой, что очень впечатляет".
Полученный образец короткоживущей металлической воды ученые изучили с помощью оптической и синхротронной рентгеновской фотоэлектронной спектроскопии. Анализ подтвердил, что вода стала металлом.
"Наше исследование не только показывает, что металлическая вода может быть получена на Земле, но и обладает спектроскопическими свойствами, связанными с ее прекрасным золотистым металлическим блеском", – говорит Зайдель.
Результаты любопытного исследования были опубликованы в журнале Nature.
Ранее мы писали о том, как физики согнули в дугу волокно изо льда, как ученые ННГУ создали девятислойный кремний, который в 100 раз лучше излучает свет. А еще мы рассказывали, как физики вырастили гибкие, как резина, алмазы. О, наука, спасибо тебе за всю эту "магию"!
Больше новостей из мира науки вы найдёте в разделе "Наука" на медиаплатформе "Смотрим".
Процессы, происходящие при погружении металла в воду
2.Измерение электродных потенциалов. Электродный электрод.
3.Факторы, влияющие на величину электродного потенциала. Уравнение Нернста. Стандартный потенциал.
4. Ряд напряжений.
5. Гальванический элемент.
Литература:
1. Коровин Н.В. Общая химия. Учебник. – М.: Высшая школа, 1998. – с. 264 - 275.
Учебно – материальное обеспечение:
1. Мультимедийный проектор.
2. Гальванический элемент Даниэля-Якоби.
Цель занятия:
Знать: 1.Скачки потенциалов на границе фаз.
2.Электродные потенциалы и ЭДС гальванической цепи.
Ознакомиться:с диффузионным потенциалом и концентрационными цепями.
Организационно-методические указания:
1.Проверить наличие обучаемых и их готовность к занятиям, устранить недостатки.
2.Объявить тему и цель занятия, учебные вопросы, литературу.
3.Обосновать необходимость изучения данной темы на примерах применения гальванических элементов в приборостроении.
4.Рассмотреть учебные вопросы с применением кадров презентации и гальванического элемента Даниэля-Якоби.
5.По каждому учебному вопросу и в конце занятия подвести итоги.
6.В конце занятия выдать задание на самоподготовку.
В приборах различного типа широко применяются химические источники энергии. Поэтому будущему специалисту в области приборостроения необходимо знать механизм возникновения электрического тока при протекании химических реакций, который лежит в основе работы химических источников тока.
Твердый металл представляет собой систему правильно расположенных (в виде решетки) катионов металла, среди которых двигаются полусвободные (то есть не закрепленные около определенных катионов) валентные электроны.
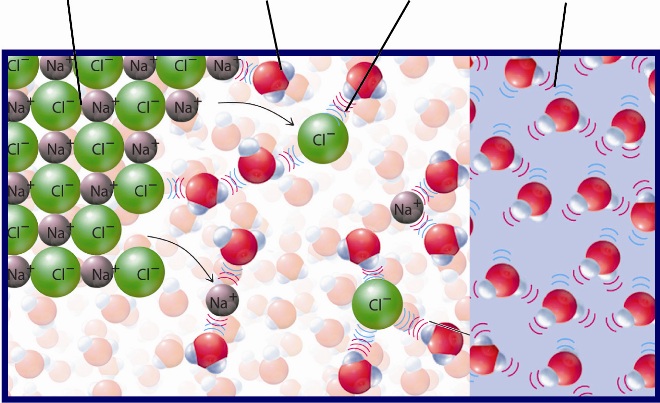
Если металлическую пластинку опустить в воду, то катионы металла на поверхности гидратируются полярными молекулами воды и переходят в жидкость.
При этом электроны, в избытке остающиеся в металле, заряжают его поверхностный слой отрицательно. Возникает электростатическое притяжение между перешедшими в жидкость гидратированными катионами и поверхностью металла. В результате этого в системе устанавливается подвижное равновесие:
При этом поверхность металла заряжается положительно, а раствор у поверхности – отрицательно.
В результате установления электрохимического равновесия образуется двойной электрический слой.
Рис. 1. Схема процессов, протекающих при погружении в воду цинковой (а) и медной (б) пластинок.
| + |
| + |
| + |
Отметим, что растворение металла – всегда процесс окисления, при этом атомы металла переходят в раствор в виде катионов, оставляя избыточные электроны на поверхности металла.
Способность посылать катионы в раствор у разных металлов выражена неодинаково (например, цинк растворяется легче, чем медь). Эта способность зависит от соотношения между энергией кристаллической решетки металла и энергией гидратации катиона металла.
Энергия кристаллической решетки металла – это энергия, необходимая для удаления катиона металла из кристаллической решетки.
В растворе ионы металла окружены полярными молекулами воды, то есть находятся в гидратированном состоянии. Чтобы вывести катион металла из раствора, необходимо совершить работу, равную энергии гидратации.
Стремление катионов металла переходить в раствор будет тем больше, чем меньше прочность (энергия) кристаллической решетки и чем сильнее удерживаются катионы в растворе водой (то есть чем больше энергия гидратации катиона).
Читайте также:
