Все металлы таблицы менделеева список
Обновлено: 19.05.2024
Периодическая система элементов Д. И. Менделеева
Таблица Менделеева - это, вероятно, одна из наиболее часто используемых таблиц. Вряд ли найдется хотя бы один человек старше 14 лет, который ни разу не слышал о ней. Это неудивительно, ибо эта таблица - кладезь полезной информации для любого химика. Напомню основное.
- В каждой ячейке данной таблицы указаны название химического элемента, его символ, порядковый номер и приближенное значение атомной массы.
- Порядковый номер элемента совпадает с количеством протонов в ядре атома данного элемента и с количеством электронов в атоме.
- Элементы, расположенные в таблице Менделеева в одной группе (в одном вертикальном ряду) и в одной подгруппе, имеют похожие свойства.
- Свойства элементов в периодах (горизонтальных рядах) изменяются похожим образом. Например, 2-й и 3-й периоды включают 8 элементов, начинаются со щелочного металла, заканчиваются благородным газом.
Последние два пункта - следствия периодического закона , который в современной формулировке звучит так:
Свойства элементов и образуемых ими соединений находятся в периодической зависимости от заряда ядра атома.
Периодический закон Менделеева - один из основных законов химии, а таблица, которую мы обсуждаем, является лишь средством, позволяющим наглядно выразить этот закон.
Я предлагаю вам несколько вариантов таблицы Менделеева:
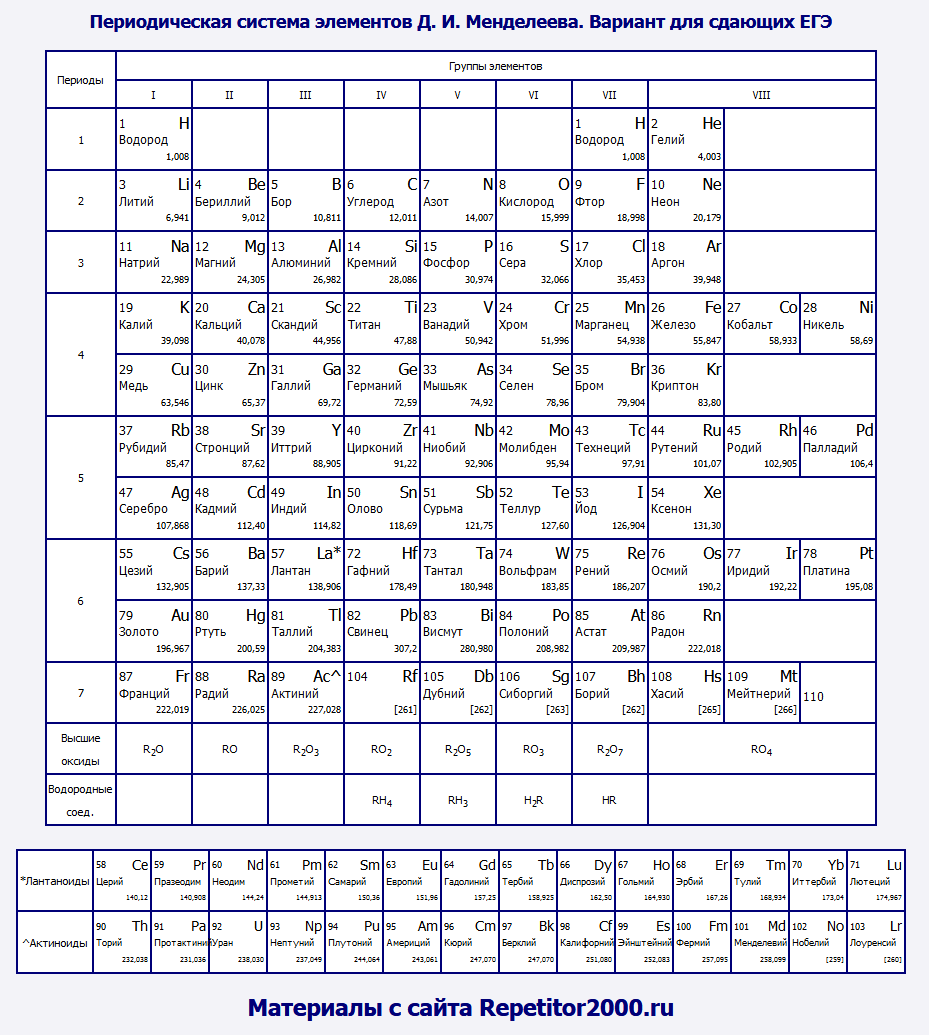
Классический вариант таблицы Менделеева
Вероятно, именно такой вариант периодической таблицы является для вас наиболее привычным. Нечто подобное мы видим в любом школьном учебнике химии. К сожалению, данный вариант (т. н. короткопериодный) не очень наглядно отражает периодический закон. Возьмите, например, элементы седьмой группы: ярко выраженные неметаллы (F, Cl, Br, I) соседствуют здесь с типичными металлами (Mn, Tc, Re). А ведь мы ожидаем видеть в одной группе элементы с похожими свойствами.
Приходится выделять т. н. главные и побочные подгруппы, прибегать к другим ухищрениям (например, "вырезать" из таблицы лантаноиды и актиноиды). В действительности, правильный вариант таблицы Менделеева выглядит так, а короткопериодная форма - это некоторый компромиссный вариант, который используется в целях экономии места.
| *Лантаноиды |
Длиннопериодная форма таблицы МенделееваИменно нечто подобное и было создано Дмитрием Ивановичем Менделеевым. Именно такой вариант таблицы наиболее наглядно иллюстрирует периодический закон. К сожалению, у длиннопериодной формы есть один недостаток: таблица занимает слишком много места. Именно поэтому многие отдают предпочтение короткопериодной форме.
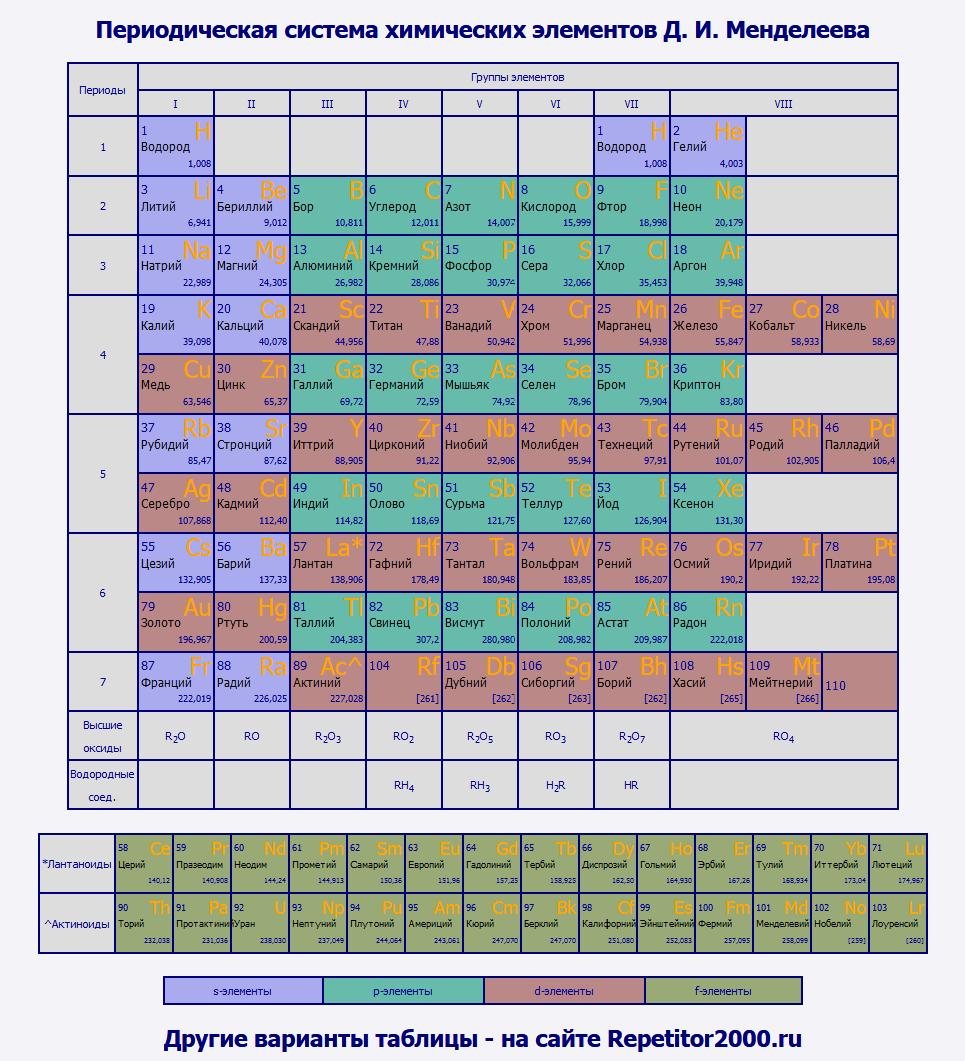
Таблица Менделеева с выделением s-, p-, d-, f- элементовРазными цветами в данном варианте таблицы Менделеева отмечены s-, p-, d- и f- элементы. Напоминаю, что элемент относится к одному из этих типов, если внешние электроны в атоме данного элемента находятся соответственно на s-, p-, d- или f- подуровне. Например, электронная формула натрия имеет вид: 1s 2 s2s 2 2p 6 3s 1 . Внешний электронный уровень - 3s, следовательно, натрий относится к s-элементам. Электронная формула кислорода: 1s 2 s2s 2 2p 4 . Внешний электронный подуровень - 2p, значит кислород - это р-элемент. Свойства элементов из этих 4 групп отличаются достаточно сильно. Например, среди d-элементов присутствуют только металлы, а большинство неметаллов относятся к p-элементам. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Высшие оксиды | R 2 O | RO | R 2 O 3 | RO 2 | R 2 O 5 | RO 3 | R 2 O 7 | RO 4 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Водородные соед. | RH 4 | RH 3 | H 2 R | HR | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| *Лантаноиды |
Таблица Менделеева, в которой отмечены металлы и неметаллыНеметаллы отмечены в этой таблице красным цветом. Обратите внимание: неметаллы сосредоточены в правой верхней части таблицы Менделеева. Все они, кроме водорода и гелия, относятся к p-элементам. Вы не найдете ни одного неметалла среди d-элементов и f-элементов. Именно по этой причине я счел возможным не приводить в данном варианте список лантаноидов и актиноидов - все они относятся к металлам. Иногда особым образом выделяют группу элементов, сочетающих в себе свойства металлов и неметаллов (например, к ним можно отнести германий). Данные элементы называют полуметаллами или металлоидами. | |||||||||
| Высшие оксиды | R 2 O | RO | R 2 O 3 | RO 2 | R 2 O 5 | RO 3 | R 2 O 7 | RO 4 | ||
| Водородные соед. | RH 4 | RH 3 | H 2 R | HR | ||||||
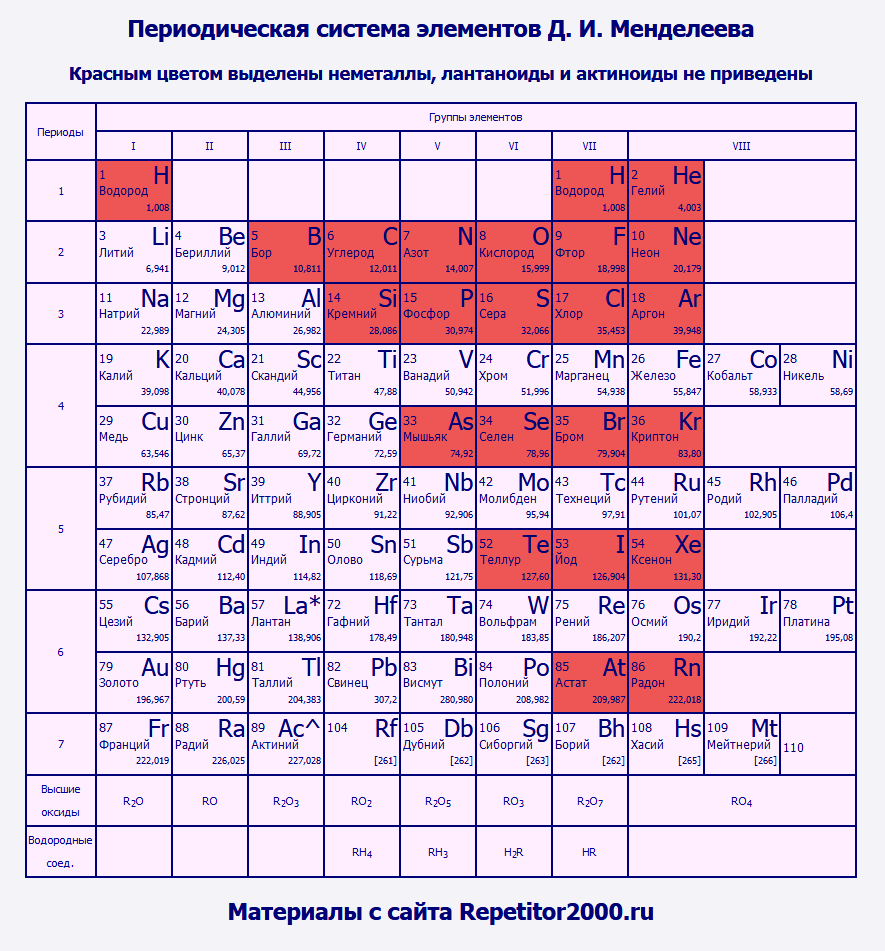
Таблица Менделеева с выделением главных и побочных подгрупп
Элементы главных подгрупп обозначены фиолетовым цветом, побочных - серым. Я напоминаю, что свойства элементов, находящихся в одной группе, но в разных подгруппах, отличаются достаточно сильно.
Например, натрий, калий, медь и серебро находятся в I группе: Na и K - в главной подгруппе, Cu и Ag - в побочной. Свойства натрия и калия весьма похожи - активные металлы, бурно реагирующие с водой, легко окисляющиеся на воздухе, имеют низкие температуры плавления и кипения. Все это сильно отличается от свойств меди и серебра: инертные металлы, которые не реагируют не только с водой, но и с большинством кислот, на воздухе устойчивы, температуры плавления и кипения достаточно высоки.
Еще ярче отличия заметны, например, в VI группе. Кислород, сера, селен (главная подгруппа) - типичные неметаллы, а хром, молибден и вольфрам, находящиеся в побочной подгруппе, относятся к металлам.
Все проблемы исчезают, если вы используете длиннопериодную форму таблицы Менделеева: "мешанина" из элементов главных и побочных подгрупп исчезает, и мы начинаем отчетливо видеть логику периодического закона.
Полный список металлов, известных науке
Посмотрите вокруг на секунду. Сколько металлических вещей вы можете увидеть? Обычно, когда мы думаем о металлах, мы вспоминаем о веществах, которые являются блестящими и прочными. Однако они также находятся в нашей пище и в наших телах. Давайте познакомимся с полным списком металлов, известных науке, узнаем их основные свойства и выясним, почему они такие особенные.

Элементы, легко теряющие электроны, которые являются блестящими (отражающими), податливыми (могут быть отлиты в другие формы) и считаются хорошими проводниками тепла и электричества, называют металлами. Они имеют решающее значение для нашего образа жизни, так как не только являются частью структур и технологий, но и важны для производства почти всех предметов. Металл есть даже в человеческом теле. Взглянув на этикетку состава мультивитаминов, вы увидите десятки перечисленных соединений.
Возможно, вы не знали, что такие элементы, как натрий, кальций, магний и цинк, необходимы для жизни, и, если они отсутствуют в наших телах, наше здоровье может быть в серьезной опасности. Например, кальций необходим для здоровых костей, магний - для метаболизма. Цинк усиливает функцию иммунной системы, а железо помогает клеткам крови переносить кислород по всему телу. Однако металлы в наших телах отличаются от металла в ложке или стальном мосте тем, что они потеряли электроны. Они называются катионами.
Металлы также обладают антибиотическими свойствами, поэтому перила и ручки в общественных местах часто изготавливаются из этих элементов. Известно, что многие инструменты делаются из серебра для предотвращения размножения бактерий. Искусственные суставы изготавливаются из титановых сплавов, которые одновременно предотвращают заражение и делают реципиентов сильнее.
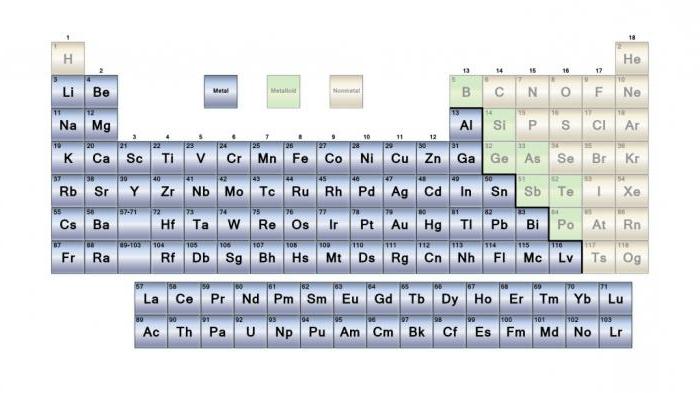
Металлы в периодической таблице
Все элементы в периодической системе Дмитрия Менделеева делятся на две большие группы: металлы и неметаллы. Первая является самой многочисленной. Большинство элементов - металлы (синий). Неметаллы в таблице изображены на желтом фоне. Есть также группа элементов, которые относят к металлоидам (красный). Все металлы сгруппированы в левой части таблицы. Обратите внимание, что водород сгруппирован с металлами в верхнем левом углу. Несмотря на это, он считается неметаллическим. Однако некоторые ученые теоретизируют, что в ядре планеты Юпитер может быть металлический водород.

Металлическое связывание
Многие из замечательных и полезных качеств элемента связаны с тем, как его атомы соединяются друг с другом. При этом возникают определенные связи. Металлическое взаимодействие атомов приводит к созданию металлических структур. Любой образец этого элемента в повседневной жизни, от автомобиля до монет в кармане, включает в себя металлическое соединение.

Во время этого процесса атомы металла разделяют свои внешние электроны равномерно друг с другом. Электроны, протекающие между положительно заряженными ионами, легко передают тепло и электроэнергию, делая эти элементы такими хорошими проводниками тепла и электричества. Медные провода используются для электроснабжения.

Реакции металлов
Реакционная способность относится к тенденции элемента реагировать с химическими веществами в его окружении. Она бывает разная. Некоторые металлы, например, калий и натрий (в колонках 1 и 2 в периодической таблице), легко реагируют со многими различными химическими веществами и редко встречаются в своей чистой, элементарной форме. Оба обычно существуют только в соединениях (связанных с одним или несколькими другими элементами) или как ионы (заряженная версия их элементарной формы).

С другой стороны, существуют и другие металлы, их еще называют ювелирными. Золото, серебро и платина являются не очень реактивными и обычно встречаются в чистом виде. Эти металлы легче теряют электроны, чем неметаллы, но не так легко, как реактивные металлы, например, натрий. Платина относительно нереакционноспособна и очень устойчива к реакциям с кислородом.
Свойства элементов
Когда вы изучали алфавит в начальной школе, вы обнаружили, что все буквы имеют свой собственный уникальный набор свойств. Например, у некоторых были прямые линии, у некоторых - кривые, а у других были линии обоих типов. То же самое можно сказать и об элементах. Каждый из них имеет уникальный набор физических и химических свойств. Физические свойства - это качества, присущие определенным веществам. Блестящий или нет, насколько он хорошо проводит тепло и электричество, при какой температуре тает, насколько большую имеет плотность.

Химические свойства включают те качества, которые наблюдаются при реагировании на воздействие кислородом, если они будут гореть (то, насколько сложно им будет удерживать их электроны во время химической реакции). Различные элементы могут иметь общие свойства. Например, железо и медь являются одновременно элементами, которые проводят электричество. Однако они не имеют одинаковых свойств. Например, когда железо подвергается воздействию влажного воздуха, оно покрывается ржавчиной, но когда медь оказывается под действием тех же условий, она приобретает специфический зеленый налет. Вот почему статуя Свободы зеленая, а не ржавая. Она сделана из меди, а не железа).

Организация элементов: металлы и неметаллы
Тот факт, что элементы имеют некоторые общие и уникальные свойства, позволяет сортировать их в красивую, аккуратную диаграмму, которая называется периодической таблицей. Она организует элементы на основе их атомного числа и свойств. Итак, в периодической таблице мы находим элементы, сгруппированные вместе, которые имеют общие свойства. Железо и медь находятся близко друг к другу, оба являются металлами. Железо обозначено символом «Fe», а медь обозначается символом «Cu».

Большинство элементов периодической таблицы - это металлы, и они, как правило, находятся в левой части таблицы. Они группируются вместе, потому что обладают определенными физическими и химическими свойствами. Например, металлы плотные, блестящие, они хорошие проводники тепла и электричества, и они легко теряют электроны в химических реакциях. Напротив, неметаллы имеют противоположные свойства. Они не плотные, не проводят тепло и электричество, и стремятся получить электроны, а не отдать их. Когда мы смотрим в периодическую таблицу, мы видим, что большинство неметаллов сгруппированы справа. Это такие элементы, как гелий, углерод, азот и кислород.

Что такое тяжелые металлы?
Список металлов достаточно многочисленный. Некоторые из них могут накапливаться в организме и не наносить ему при этом вреда, как например, природный стронций (формула Sr), который является аналогом кальция, так как продуктивно откладывается в костной ткани. Какие из них называются тяжелыми и почему? Рассмотрим четыре примера: свинец, медь, ртуть и мышьяк.
Где находятся эти элементы и как они влияют на окружающую среду и здоровье человека? Тяжелые металлы представляют собой металлические, встречающиеся в природе соединения, которые имеют очень высокую плотность по сравнению с другими металлами - по меньшей мере, они в пять раз больше плотности воды. Они токсичны для людей. Даже небольшие дозы могут привести к серьезным последствиям.

- Свинец. Это тяжелый металл, являющийся токсичным для людей, особенно для детей. Отравление этим веществом может привести к проблемам неврологического характера. Несмотря на то что когда-то он был весьма привлекательным из-за его гибкости, высокой плотности и способности поглощать вредное излучение, свинец был выведен из употребления по многим направлениям. Этот мягкий серебристый металл, который встречается на Земле, является опасным для людей и накапливается в организме в течение долгого времени. Самое страшное, что от него нельзя избавиться. Он сидит там, накапливается и постепенно отравляет тело. Свинец токсичен для нервной системы и может вызвать серьезное повреждение головного мозга у детей. Он широко использовался в 1800-х годах для создания макияжа и вплоть до 1978 года использовался в качестве одного из ингридиентов в краске для волос. Сегодня свинец используется в основном в больших батареях, в качестве экранов для рентгеновских лучей или изоляции для радиоактивного материала.
- Медь. Это красновато-коричневый тяжелый металл, у которого есть множество применений. Медь по-прежнему является одним из лучших проводников электричества и тепла, и многие электрические провода сделаны из этого металла и покрыты пластиком. Монеты, в основном мелочь, также делают из этого элемента периодической системы. Острые отравления медью встречаются редко, но, как и свинец, она может накапливаться в тканях, что в конечном итоге приводит к токсичности. Люди, которые подвергаются воздействию большим количеством меди или медной пыли, также находятся в зоне риска.
- Ртуть. Этот металл токсичен в любой форме и может даже поглощаться кожей. Его уникальность состоит в том, что он является жидким при комнатной температуре, его иногда называют «быстрым серебром». Его можно увидеть в термометре, потому что в качестве жидкости он поглощает тепло, изменяя объем даже с малейшей разницей в температуре. Это позволяет ртути подниматься или падать в стеклянной трубке. Поскольку это вещество является мощным нейротоксином, многие компании переходят на спиртовые термометры, окрашенные в красный цвет.
- Мышьяк. Со времен Римской империи вплоть до викторианской эпохи мышьяк считался «королем ядов», а также «ядом царей». История пронизана бесчисленными примерами как королевских лиц, так и простых людей, совершающих убийства для личной выгоды, используя соединения мышьяка, у которых не было ни запаха, ни цвета, ни вкуса. Несмотря на все отрицательные влияния, этот металлоид также имеет свои области применения, даже в медицине. Например, триоксид мышьяка является очень эффективным препаратом, используемым для лечения людей с острым промиелоцитарным лейкозом.

Что такое драгоценный металл?
Драгоценный металл представляет собой металл, который может быть редким или трудно добываемым, а также экономически очень ценным. Каков список металлов, являющихся драгоценными? Всего их три:
- Платина. Несмотря на свою тугоплавкость, она используется в ювелирных изделиях, электронике, автомобилях, в химических процессах и даже в медицине.
- Золото. Этот драгоценный металл используется для изготовления ювелирных изделий и золотых монет. Однако он имеет много других применений. Он используется в медицине, производстве и лабораторном оборудовании.
- Серебро. Этот благородный металл серебристо-белого цвета является очень ковким. в чистом виде является достаточно тяжелым, оно легче свинца, но тяжелее меди.

Металлы: виды и свойства
Большинство элементов можно рассматривать как металлы. Они сгруппированы в середине в левой стороне таблицы. Металлы бывают щелочные, щелочноземельные, переходные, лантаноиды и актиниды.

- твердое вещество при комнатной температуре (за исключением ртути);
- обычно блестящее;
- с высокой температурой плавления;
- хороший проводник тепла и электричества;
- с низкой способностью к ионизации;
- с низкой электроотрицательностью;
- податливый (способный принимать заданную форму);
- пластичный (можно вытянуть в проволоку);
- с высокой плотностью;
- вещество, которое теряет электроны в реакциях.

Список металлов, известных науке
- литий;
- бериллий;
- натрий;
- магний;
- алюминий;
- калий;
- кальций;
- скандий;
- титан;
- ванадий;
- хром;
- марганец;
- железо;
- кобальт;
- никель;
- медь;
- цинк;
- галлий;
- рубидий;
- стронций;
- иттрий;
- цирконий;
- ниобий;
- молибден;
- технеций;
- рутений;
- родий;
- палладий;
- серебро;
- кадмий;
- индий;
- коперниций;
- цезий;
- барий;
- олово;
- железо;
- висмут;
- свинец;
- ртуть;
- вольфрам;
- золото;
- платина;
- осмий;
- гафний;
- германий;
- иридий;
- ниобий;
- рений;
- сурьма;
- таллий;
- тантал;
- франций;
- ливерморий.

Всего известно около 105 химических элементов, большая часть из которых - металлы. Последние являются очень распространенным элементом в природе, который встречается как в чистом виде, так и в составе всевозможных соединений.

Металлы залегают в недрах земли, их можно найти в различных водоемах, в составе тел животных и человека, в растениях и даже в атмосфере. В периодической системе они располагаются начиная с лития (металл с формулой Li) и заканчивая ливерморием (Lv). Таблица она продолжает пополняться новыми элементами, и в основном это металлы.
ПЕРИОДИЧЕСКАЯ ТАБЛИЦА МЕНДЕЛЕЕВА
Еще в школе, сидя на уроках химии, все мы помним таблицу на стене класса или химической лаборатории. Эта таблица содержала классификацию всех известных человечеству химических элементов, тех фундаментальных компонентов, из которых состоит Земля и вся Вселенная. Тогда мы и подумать не могли, что таблица Менделеева бесспорно является одним из величайших научных открытий, который является фундаментом нашего современного знания о химии.
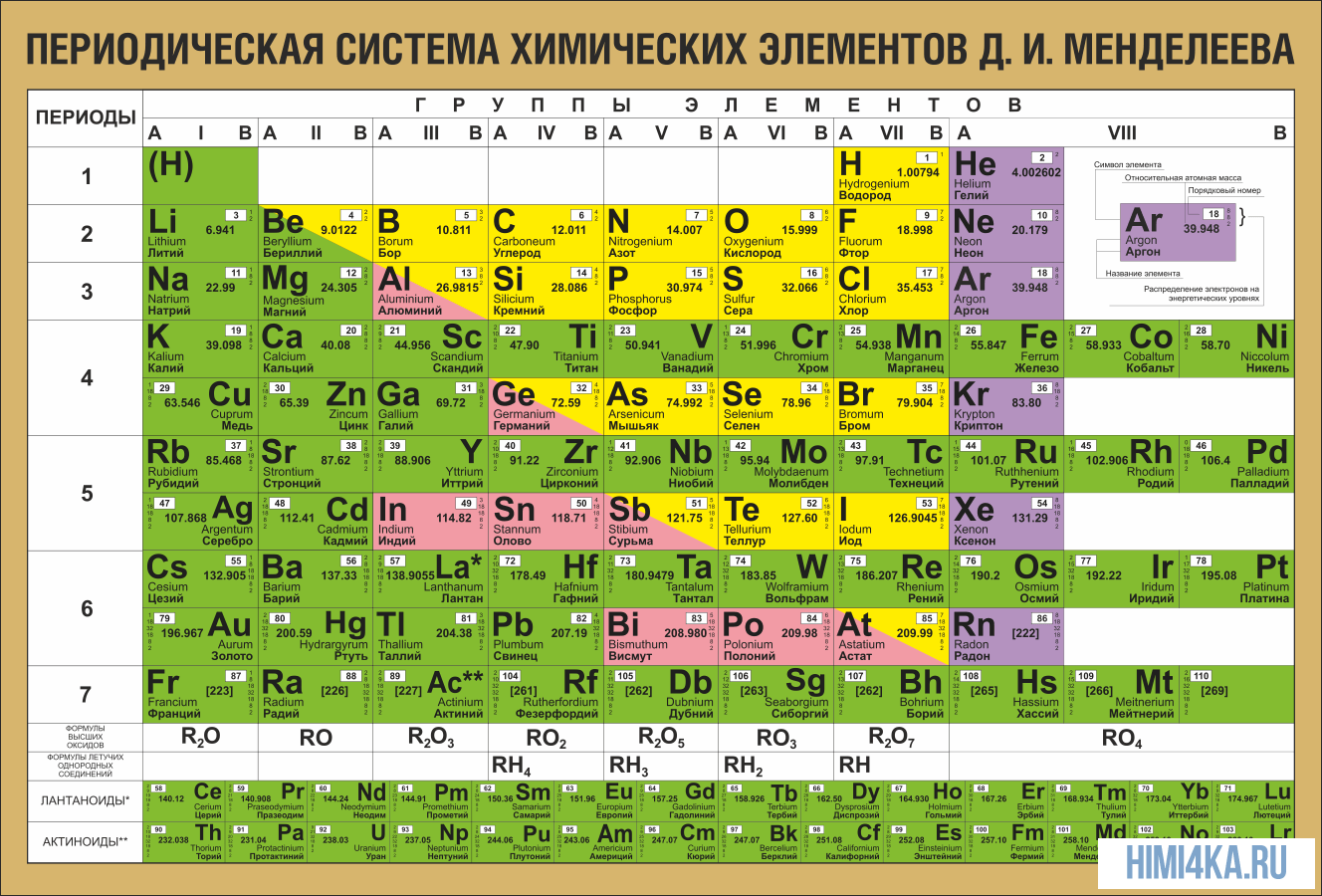
На первый взгляд, ее идея выглядит обманчиво просто: организовать химические элементы в порядке возрастания веса их атомов. Причем в большинстве случаев оказывается, что химические и физические свойства каждого элемента сходны с предыдущим ему в таблице элементом. Эта закономерность проявляется для всех элементов, кроме нескольких самых первых, просто потому что они не имеют перед собой элементов, сходных с ними по атомному весу. Именно благодаря открытию такого свойства мы можем поместить линейную последовательность элементов в таблицу, очень напоминающую настенный календарь, и таким образом объединить огромное количество видов химических элементов в четкой и связной форме. Разумеется, сегодня мы пользуемся понятием атомного числа (количества протонов) для того, чтобы упорядочить систему элементов. Это помогло решить так называемую техническую проблему «пары перестановок», однако не привело к кардинальному изменению вида периодической таблицы.
В периодической таблице Менделеева все элементы упорядочены с учетом их атомного числа, электронной конфигурации и повторяющихся химических свойств. Ряды в таблице называются периодами, а столбцы группами. В первой таблице, датируемой 1869 годом, содержалось всего 60 элементов, теперь же таблицу пришлось увеличить, чтобы поместить 118 элементов, известных нам сегодня.
Периодическая система Менделеева систематизирует не только элементы, но и самые разнообразные их свойства. Химику часто бывает достаточно иметь перед глазами Периодическую таблицу для того, чтобы правильно ответить на множество вопросов (не только экзаменационных, но и научных).
The YouTube ID of 1M7iKKVnPJE is invalid.
Периодический закон
Существуют две формулировки периодического закона химических элементов: классическая и современная.
Классическая, в изложении его первооткрывателя Д.И. Менделеева: свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величин атомных весов элементов.
Современная: свойства простых веществ, а также свойства и формы соединений элементов находятся в периодической зависимости от заряда ядра атомов элементов (порядкового номера).
Графическим изображением периодического закона является периодическая система элементов, которая представляет собой естественную классификацию химических элементов, основанную на закономерных изменениях свойств элементов от зарядов их атомов. Наиболее распространёнными изображениями периодической системы элементов Д.И. Менделеева являются короткая и длинная формы.

Группы и периоды Периодической системы
Группами называют вертикальные ряды в периодической системе. В группах элементы объединены по признаку высшей степени окисления в оксидах. Каждая группа состоит из главной и побочной подгрупп. Главные подгруппы включают в себя элементы малых периодов и одинаковые с ним по свойствам элементы больших периодов. Побочные подгруппы состоят только из элементов больших периодов. Химические свойства элементов главных и побочных подгрупп значительно различаются.
Периодом называют горизонтальный ряд элементов, расположенных в порядке возрастания порядковых (атомных) номеров. В периодической системе имеются семь периодов: первый, второй и третий периоды называют малыми, в них содержится соответственно 2, 8 и 8 элементов; остальные периоды называют большими: в четвёртом и пятом периодах расположены по 18 элементов, в шестом — 32, а в седьмом (пока незавершенном) — 31 элемент. Каждый период, кроме первого, начинается щелочным металлом, а заканчивается благородным газом.
Физический смысл порядкового номера химического элемента: число протонов в атомном ядре и число электронов, вращающихся вокруг атомного ядра, равны порядковому номеру элемента.

Свойства таблицы Менделеева
Напомним, что группами называют вертикальные ряды в периодической системе и химические свойства элементов главных и побочных подгрупп значительно различаются.
Свойства элементов в подгруппах закономерно изменяются сверху вниз:
- усиливаются металлические свойства и ослабевают неметаллические;
- возрастает атомный радиус;
- возрастает сила образованных элементом оснований и бескислородных кислот;
- электроотрицательность падает.
Все элементы, кроме гелия, неона и аргона, образуют кислородные соединения, существует всего восемь форм кислородных соединений. В периодической системе их часто изображают общими формулами, расположенными под каждой группой в порядке возрастания степени окисления элементов: R2O, RO, R2O3, RO2, R2O5, RO3, R2O7, RO4, где символом R обозначают элемент данной группы. Формулы высших оксидов относятся ко всем элементам группы, кроме исключительных случаев, когда элементы не проявляют степени окисления, равной номеру группы (например, фтор).
Оксиды состава R2O проявляют сильные основные свойства, причём их основность возрастает с увеличением порядкового номера, оксиды состава RO (за исключением BeO) проявляют основные свойства. Оксиды состава RO2, R2O5, RO3, R2O7 проявляют кислотные свойства, причём их кислотность возрастает с увеличением порядкового номера.
Элементы главных подгрупп, начиная с IV группы, образуют газообразные водородные соединения. Существуют четыре формы таких соединений. Их располагают под элементами главных подгрупп и изображают общими формулами в последовательности RH4, RH3, RH2, RH.
Соединения RH4 имеют нейтральный характер; RH3 — слабоосновный; RH2 — слабокислый; RH — сильнокислый характер.
Напомним, что периодом называют горизонтальный ряд элементов, расположенных в порядке возрастания порядковых (атомных) номеров.
В пределах периода с увеличением порядкового номера элемента:
- электроотрицательность возрастает;
- металлические свойства убывают, неметаллические возрастают;
- атомный радиус падает.
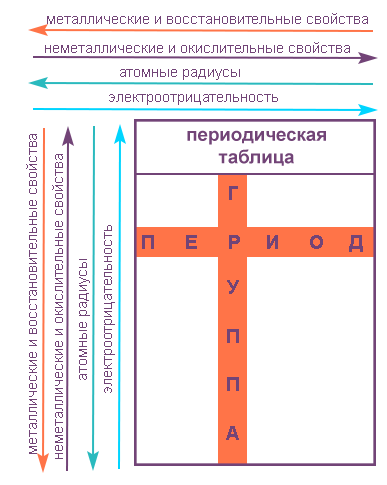
Элементы таблицы Менделеева
Щелочные и щелочноземельные элементы
К ним относятся элементы из первой и второй группы периодической таблицы. Щелочные металлы из первой группы — мягкие металлы, серебристого цвета, хорошо режутся ножом. Все они обладают одним-единственным электроном на внешней оболочке и прекрасно вступают в реакцию. Щелочноземельные металлы из второй группы также имеют серебристый оттенок. На внешнем уровне помещено по два электрона, и, соответственно, эти металлы менее охотно взаимодействуют с другими элементами. По сравнению со щелочными металлами, щелочноземельные металлы плавятся и кипят при более высоких температурах.
| Щелочные металлы | Щелочноземельные металлы |
| Литий Li 3 | Бериллий Be 4 |
| Натрий Na 11 | Магний Mg 12 |
| Калий K 19 | Кальций Ca 20 |
| Рубидий Rb 37 | Стронций Sr 38 |
| Цезий Cs 55 | Барий Ba 56 |
| Франций Fr 87 | Радий Ra 88 |
Лантаниды (редкоземельные элементы) и актиниды
Лантаниды — это группа элементов, изначально обнаруженных в редко встречающихся минералах; отсюда их название «редкоземельные» элементы. Впоследствии выяснилось, что данные элементы не столь редки, как думали вначале, и поэтому редкоземельным элементам было присвоено название лантаниды. Лантаниды и актиниды занимают два блока, которые расположены под основной таблицей элементов. Обе группы включают в себя металлы; все лантаниды (за исключением прометия) нерадиоактивны; актиниды, напротив, радиоактивны.
| Лантаниды | Актиниды |
| Лантан La 57 | Актиний Ac 89 |
| Церий Ce 58 | Торий Th 90 |
| Празеодимий Pr 59 | Протактиний Pa 91 |
| Неодимий Nd 60 | Уран U 92 |
| Прометий Pm 61 | Нептуний Np 93 |
| Самарий Sm 62 | Плутоний Pu 94 |
| Европий Eu 63 | Америций Am 95 |
| Гадолиний Gd 64 | Кюрий Cm 96 |
| Тербий Tb 65 | Берклий Bk 97 |
| Диспрозий Dy 66 | Калифорний Cf 98 |
| Гольмий Ho 67 | Эйнштейний Es 99 |
| Эрбий Er 68 | Фермий Fm 100 |
| Тулий Tm 69 | Менделевий Md 101 |
| Иттербий Yb 70 | Нобелий No 102 |
Галогены и благородные газы
Галогены и благородные газы объединены в группы 17 и 18 периодической таблицы. Галогены представляют собой неметаллические элементы, все они имеют семь электронов во внешней оболочке. В благородных газахвсе электроны находятся во внешней оболочке, таким образом с трудом участвуют в образовании соединений. Эти газы называют «благородными, потому что они редко вступают в реакцию с прочими элементами; т. е. ссылаются на представителей благородной касты, которые традиционно сторонились других людей в обществе.
| Галогены | Благородные газы |
| Фтор F 9 | Гелий He 2 |
| Хлор Cl 17 | Неон Ne 10 |
| Бром Br 35 | Аргон Ar 18 |
| Йод I 53 | Криптон Kr 36 |
| Астат At 85 | Ксенон Xe 54 |
| — | Радон Rn 86 |
Переходные металлы
Переходные металлы занимают группы 3—12 в периодической таблице. Большинство из них плотные, твердые, с хорошей электро- и теплопроводностью. Их валентные электроны (при помощи которых они соединяются с другими элементами) находятся в нескольких электронных оболочках.
| Переходные металлы |
| Скандий Sc 21 |
| Титан Ti 22 |
| Ванадий V 23 |
| Хром Cr 24 |
| Марганец Mn 25 |
| Железо Fe 26 |
| Кобальт Co 27 |
| Никель Ni 28 |
| Медь Cu 29 |
| Цинк Zn 30 |
| Иттрий Y 39 |
| Цирконий Zr 40 |
| Ниобий Nb 41 |
| Молибден Mo 42 |
| Технеций Tc 43 |
| Рутений Ru 44 |
| Родий Rh 45 |
| Палладий Pd 46 |
| Серебро Ag 47 |
| Кадмий Cd 48 |
| Лютеций Lu 71 |
| Гафний Hf 72 |
| Тантал Ta 73 |
| Вольфрам W 74 |
| Рений Re 75 |
| Осмий Os 76 |
| Иридий Ir 77 |
| Платина Pt 78 |
| Золото Au 79 |
| Ртуть Hg 80 |
| Лоуренсий Lr 103 |
| Резерфордий Rf 104 |
| Дубний Db 105 |
| Сиборгий Sg 106 |
| Борий Bh 107 |
| Хассий Hs 108 |
| Мейтнерий Mt 109 |
| Дармштадтий Ds 110 |
| Рентгений Rg 111 |
| Коперниций Cn 112 |
Металлоиды
Металлоиды занимают группы 13—16 периодической таблицы. Такие металлоиды, как бор, германий и кремний, являются полупроводниками и используются для изготовления компьютерных чипов и плат.
| Металлоиды |
| Бор B 5 |
| Кремний Si 14 |
| Германий Ge 32 |
| Мышьяк As 33 |
| Сурьма Sb 51 |
| Теллур Te 52 |
| Полоний Po 84 |
Постпереходными металлами
Элементы, называемые постпереходными металлами, относятся к группам 13—15 периодической таблицы. В отличие от металлов, они не имеют блеска, а имеют матовую окраску. В сравнении с переходными металлами постпереходные металлы более мягкие, имеют более низкую температуру плавления и кипения, более высокую электроотрицательность. Их валентные электроны, с помощью которых они присоединяют другие элементы, располагаются только на внешней электронной оболочке. Элементы группы постпереходных металлов имеют гораздо более высокую температуру кипения, чем металлоиды.
| Постпереходные металлы |
| Алюминий Al 13 |
| Галлий Ga 31 |
| Индий In 49 |
| Олово Sn 50 |
| Таллий Tl 81 |
| Свинец Pb 82 |
| Висмут Bi 83 |
Неметаллы
Из всех элементов, классифицируемых как неметаллы, водород относится к 1-й группе периодической таблицы, а остальные — к группам 13—18. Неметаллы не являются хорошими проводниками тепла и электричества. Обычно при комнатной температуре они пребывают в газообразном (водород или кислород) или твердом состоянии (углерод).
| Неметаллы |
| Водород H 1 |
| Углерод C 6 |
| Азот N 7 |
| Кислород O 8 |
| Фосфор P 15 |
| Сера S 16 |
| Селен Se 34 |
| Флеровий Fl 114 |
| Унунсептий Uus 117 |
А теперь закрепите полученные знания, посмотрев видео про таблицу Менделеева и не только.
Отлично, первый шаг на пути к знаниям сделан. Теперь вы более-менее ориентируетесь в таблице Менделеева и это вам очень даже пригодится, ведь Периодическая система Менделеева является фундаментом, на котором стоит эта удивительная наука.
ТАБЛИЦА МЕНДЕЛЕЕВА - периодическая система химических элементов
Таблица Менделеева (периодическая система химических элементов) - это такая таблица, в которой классифицируются химические элементы по различным свойствам в зависимости от заряда их атомного ядра. Таблица является графическим изображением периодического закона, который открыл Дмитрий Иванович Менделеев в 1869 году. Изначальный вариант этой таблицы 1869 - 1871 гг. и устанавливал зависимость свойств элементов от их атомной массы. На данный момент элементы сводятся в двумерную таблицу, в которой каждый столбец - это группа, определяющая основные физико-химические свойства, а строки - это периоды, схожие друг с другом. Наиболее распространены 2 формы таблицы: короткая и длинная.
ТАБЛИЦА МЕНДЕЛЕЕВА

Периодическая таблица Менделеева в классическом варианте (или короткая форма), основана на параллелизме степеней окисления химических элементов главных и побочных подгрупп. В каждой ячейке таблицы указан символ элемента, порядковый номер, относительная атомная масса, и название элемента.
Порядковый номер элемента - это число равное числу протонов в ядре атома и числу электронов, которые вращаются вокруг него.
Чтобы посмотреть все свойства конкретного химического элемента нужно перейти по ссылке нажав на символ элемента в таблице.
Периодическая система химических элементов Д.И. Менделеева
Расшифровка периодической системы химических элементов Д.И. Менделеева:
Номер группы (для большинства элементов) – общее число валентных электронов (электронов внешнего энергетического уровня, а также предпоследнего d-подуровня, если он застроен не полностью).
Число элементов в периоде – максимальная емкость соответствующего энергетического уровня:
2 элемента (1s 2 )
18 элементов (5s 2 4d 10 5p 6 )
8 элементов (2s 2 2p 6 )
32 элемента (6s 2 4f 14 5d 10 6p 6 )
8 элементов (3s 2 3p 6 )
18 элементов (4s 2 3d 10 4p 6 )
Построение периодов – в начале: два s-элемента, в конце: шесть р- элементов. В четвертом и пятом периодах между ними помещается по десять d-элементов, а в шестом и седьмом к ним добавляются четырнадцать f-элементов (формы электронных орбиталей).
В периоде – свойства химических элементов различаются между собой, т.к. электронные конфигурации валентных электронов их атомов различны.
В подгруппе – свойства элементов сходны между собой, т.к. электронные конфигурации валентных электронов их атомов сходны.
Причина периодичности свойств химических элементов заключается в периодической повторяемости сходных электронных конфигураций внешних энергетических уровней.
Формы электронных орбиталей (электронные семейства)
Классификация химических элементов по электронным конфигурациям их атомов (электронные орбитали)
внешний (n) s-подуровень
внешний (n) р-подуровень
предвнешний (n–1 ) d-подуровень
(n-2)f 1–14 (n-1)d 1–10 ns 1–2
третий снаружи (n–2) f-подуровень
Графическое изображение орбиталей
Свойства элементов таблицы Менделеева
Металлы – элементы главных подгрупп с числом валентных электронов от 1 до 3 (подгруппы IA, IIA, IIIА, кроме элемента бора), а также германий, олово, свинец, сурьма, висмут и полоний.
Неметаллы – бор и элементы главных подгрупп с числом валентных электронов от 4 до 7 (подгруппы IVA, VA, VIA, VIIA) кроме германия, олова, свинца, сурьмы, висмута и полония.
Переходные элементы – элементы побочных подгрупп (IB-VIIB); в виде простых веществ ведут себя как металлы.
Благородные газы – элементы подгруппы VIIIA, полностью застроенные энергетические подуровни s 2 p 6 , для гелия s 2 .
Галогены – элементы подгруппы VII(a) таблицы Менделеева, реагируют со всеми простыми веществами, кроме некот. неметаллов, являются энергичными окислителями, к ним относят F, Cl, Br, I, At, Ts.
Лантанойды – 15 элементов III группы 6-го периода, металлы с атомными номерами 57–71. Все они имеют стабильные изотопы, кроме прометия.
Актинойды – 15 радиоактивных элементов III группы 7-го периода с атомными номерами 89–103.
В периодах с увеличением порядкового номера элемента прослеживается следующая закономерность:
Все элементы таблицы Менделеева, исключая гелий, неон и аргон, образуют кислородные соединения, которые изображены общими формулами под каждой группой в порядке возрастания степени окисления элементов: R2O, RO, R2O3, RO2, R2O5, RO3, R2O7, RO4, где R - обозначает элемент группы.
Элементы главных подгрупп, начиная с IV группы, образуют газообразные водородные соединения: RH4, RH3, RH2, RH. Соединения RH4 имеют нейтральный характер; RH3 – слабоосновной; RH2 – слабокислый; RH – сильнокислый характер.
История открытия периодического закона Менделеевым Д.И.
Самый важный вклад в систематизацию химических элементов внёс русский выдающийся химик Дмитрий Иванович Менделеев, автор труда "Основы химии", который в марте 1869 года представил Русскому химическому обществу (РХО) периодический закон химических элементов, изложенный в нескольких основных положениях.
В 1871 году Менделеев в итоговой статье «Периодическая законность химических элементов» дал формулировку Периодического закона: "Свойства элементов, а потому и свойства образуемых ими простых и сложных тел стоят в периодической зависимости от атомного веса". Тогда же Менделеев придал своей периодической таблице классический вид (короткая таблица, смотрите ниже).

В современном изложении периодический закон химических элементов звучит так: "Свойства простых веществ, а также свойства и формы соединений элементов находятся в периодической зависимости от заряда ядра атомов элементов (порядкового номера)."
Периодическая таблица элементов Менделеева длинная форма
Длинная форма таблицы Менделеева (или длиннопериодная форма) состоит из 18 групп с лева на право от щелочных металов до благородных газов. считается официальной версией с 1989 года.

Таблица Менделеева для печати в хорошем качестве скачать
Вы можете скачать таблицу Менделеева на выбор короткую или длинную форму в цветном и черно-белом цвете, для этого откройте по ссылке ниже изображение и сохраните его себе на компьютер.
____________
Источник информации:
1. Большой химический справочник / А.И.Волков, — М.: 2005.
2. Большая энциклопедия химических элементов. Периодическая таблица Менделеева / И.А.Леенсон. — Москва : 2014.
Таблица Менделеева
Периодическая система химических элементов (табли́ца Менделе́ева) — классификация химических элементов, устанавливающая зависимость различных свойств элементов от заряда атомного ядра. Система является графическим выражением периодического закона, установленного русским химиком Д. И. Менделеевым в 1869 году. Её первоначальный вариант был разработан Д. И. Менделеевым в 1869—1871 годах и устанавливал зависимость свойств элементов от их атомного веса (по-современному, от атомной массы). В современном варианте системы предполагается сведение элементов в двумерную таблицу, в которой каждый столбец (группа) определяет основные физико-химические свойства, а строки представляют собой периоды, в определённой мере подобные друг другу.
Классический вид таблицы Менделеева
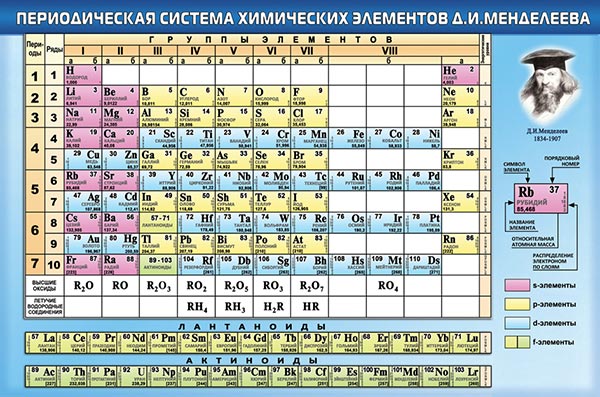
История открытия Периодического закона.
К середине XIX века были открыты 63 химических элемента, и попытки найти закономерности в этом наборе предпринимались неоднократно. В 1829 году Дёберейнер опубликовал найденный им «закон триад»: атомный вес многих элементов близок к среднему арифметическому двух других элементов, близких к исходному по химическим свойствам (стронций, кальций и барий; хлор, бром и йод и др.). Первую попытку расположить элементы в порядке возрастания атомных весов предпринял Александр Эмиль Шанкуртуа (1862), который разместил элементы вдоль винтовой линии и отметил частое циклическое повторение химических свойств по вертикали. Обе указанные модели не привлекли внимания научной общественности. В 1866 году свой вариант периодической системы предложил химик и музыкант Джон Александр Ньюлендс, модель которого («закон октав») внешне немного напоминала менделеевскую, но была скомпрометирована настойчивыми попытками автора найти в таблице мистическую музыкальную гармонию. В этом же десятилетии появились ещё несколько попыток систематизации химических элементов; ближе всего к окончательному варианту подошёл Юлиус Лотар Мейер (1864). Д. И. Менделеев опубликовал свою первую схему периодической таблицы в 1869 году в статье «Соотношение свойств с атомным весом элементов» (в журнале Русского химического общества); ещё ранее (февраль 1869 г.) научное извещение об открытии было им разослано ведущим химикам мира. По легенде, мысль о системе химических элементов пришла к Менделееву во сне, однако известно, что однажды на вопрос, как он открыл периодическую систему, учёный ответил: «Я над ней, может быть, двадцать лет думал, а вы думаете: сидел и вдруг… готово». Написав на карточках основные свойства каждого элемента (их в то время было известно 63, из которых один — дидим Di — оказался в дальнейшем смесью двух вновь открытых элементов празеодима и неодима), Менделеев начинает многократно переставлять эти карточки, составлять из них ряды сходных по свойствам элементов, сопоставлять ряды один с другим. Итогом работы стал отправленный в 1869 году в научные учреждения России и других стран первый вариант системы («Опыт системы элементов, основанной на их атомном весе и химическом сходстве»), в котором элементы были расставлены по девятнадцати горизонтальным рядам (рядам сходных элементов, ставших прообразами групп современной системы) и по шести вертикальным столбцам (прообразам будущих периодов). В 1870 году Менделеев в «Основах химии» публикует второй вариант системы («Естественную систему элементов»), имеющий более привычный нам вид: горизонтальные столбцы элементов-аналогов превратились в восемь вертикально расположенных групп; шесть вертикальных столбцов первого варианта превратились в периоды, начинавшиеся щелочным металлом и заканчивающиеся галогеном. Каждый период был разбит на два ряда; элементы разных вошедших в группу рядов образовали подгруппы. Сущность открытия Менделеева заключалась в том, что с ростом атомной массы химических элементов их свойства меняются не монотонно, а периодически. После определённого количества разных по свойствам элементов, расположенных по возрастанию атомного веса, свойства начинают повторяться. Например, натрий похож на калий, фтор похож на хлор, а золото похоже на серебро и медь. Разумеется, свойства не повторяются в точности, к ним добавляются и изменения. Отличием работы Менделеева от работ его предшественников было то, что основ для классификации элементов у Менделеева была не одна, а две — атомная масса и химическое сходство. Для того, чтобы периодичность полностью соблюдалась, Менделеевым были предприняты очень смелые шаги: он исправил атомные массы некоторых элементов (например, бериллия, индия, урана, тория, церия, титана, иттрия), несколько элементов разместил в своей системе вопреки принятым в то время представлениям об их сходстве с другими (например, таллий, считавшийся щелочным металлом, он поместил в третью группу согласно его фактической максимальной валентности), оставил в таблице пустые клетки, где должны были разместиться пока не открытые элементы. В 1871 году на основе этих работ Менделеев сформулировал Периодический закон, форма которого со временем была несколько усовершенствована. Научная достоверность Периодического закона получила подтверждение очень скоро: в 1875—1886 годах были открыты галлий (экаалюминий), скандий (экабор) и германий (экасилиций), для которых Менделеев, пользуясь периодической системой, предсказал не только возможность их существования, но и, с поразительной точностью, целый ряд физических и химических свойств.
Читайте также: