Золото это металл или неметалл
Обновлено: 30.06.2024
Золото (лат. Aurum), Au, химический элемент 1 группы периодической системы Менделеева; атомный номер 79, атомная масса 196,9665; тяжёлый металл жёлтого цвета, относящийся к благородным. Состоит из одного устойчивого изотопа 197Au.
Обзоры приведены в соответствии с энциклопедическими статьями С. А. Погодина и А. И. Стадниченко.
Разделы страницы о золоте как веществе и материале:
Физические и физико-химические свойства золота
ЗОЛОТО (Aurum) Au, хим. элемент I гр. периодич. системы, ат. н. 79, ат. м. 196,9665; относится к благородным металлам. В природе один стабильный изотоп 197 Аu. Конфигурация внеш. электронной оболочки 5d106s1; степени окисления +1, +3, редко +5; энергии ионизации Аu0 : Аи+ : Аu2+ : Аu3+ соответственно равны 9,2258, 20,5 и 30,5 эВ; электроотрицательность по Полингу 2,4 сродство к электрону 2,8 эВ; атомный радиус 0,144 нм, ионные радиусы (в скобках указаны координац. числа) Аu+ 0,151 нм (6), Аu3+ 0,082 нм (4), 0,099 нм (6).
3олото - желтый металл; кристаллич. решетка гранецентрир. кубическая, а = 0,40786 нм, z = 4, пространств. группа Fm3m.
Золото — мягкий, очень пластичный, тягучий металл (может быть проковано в листки толщиной до 8·10-5 мм, протянуто в проволоку, 2 км которой весят 1 г): твердость по Моосу ~ 2,5, по Бринеллю 220-250 МПа; модуль упругости 81 ГПа; sраст 10-25 МПа. Золото хорошо проводит тепло и электричество.
Золото весьма стойко против химических воздействий. Оно устойчиво на воздухе и в воде. С О2, Н2, N2, P, Sb и С непосредственно не взаимодействует. Фосфид Аu2Р3 (DH0обр -102 кДж/моль) и антимонид AuSb2 (DH0обр - 13 кДж/моль) получают косвенным путем.
3олото не растворяется в р-рах щелочей и к-тах, раств. в горячей H2SeO4, смесях к-т - Н2SО4 с HNO3, H2SO4 с НМnО4, а также в царской водке (НСl + НNO3): Аu + HNO3 + 4НСl : H[AuCl4] + NO + 2Н2О; после осторожного выпаривания выделяются желтые кристаллы комплексной золотохлористоводородной к-ты НАuСl4.3Н2О. В водных р-рах цианидов (Na, Ca, К) при доступе О2 или др. окислителей золота раств. с образованием дицианоаурат-иона (цианирование): 2Au + 4CN- + Н2О + 0,5О2 : 2[Au(CN)2]- + 2OH-, что лежит в основе важнейшего пром. способа извлечения золота из руд. С галогенами в отсутствие влаги золото без нагревания не взаимод., при нагр. порошка золота в атмосфере галогенов образуются золота галогениды.
С многими металлами золото дает сплавы. На легком образовании амальгамы золота основан один из методов извлечения золота из горных пород. Соед. золота неустойчивы, в водных р-рах гидролизуются, легко восстанавливаются до металла.
Химические свойства золота и его соединений
Конфигурация внешних электронов атома золота 5d10 6s1. В соединениях золото имеет валентности 1 и 3 (известны комплексные соединения, в которых золото 2-валентно).
Для золота характерна лёгкая восстановимость его из соединений до металла и способность к комплексообразованию. Существование закиси золота, т. е. оксида золота (I) Au2O - сомнительно.
С неметаллами (кроме галогенов) золото не взаимодействует. С галогенами золото образует галогениды, например 2Au + 3Cl2 =2AuC13. В смеси соляной и азотной кислот золото растворяется, образуя золотохлористоводородную кислоту H [AuCl4].
В растворах цианида натрия NaCN (или калия KCN) при одновременном доступе кислорода золото превращается в цианоаурат (I) натрия 2Na [Au (CN)2]. Эта реакция, открытая в 1843 П. Р. Багратионом, получила практическое применение только в конце 19 в. (см. Цианирование).
Хлорид золота (I) AuCl получается при нагревании хлорида золота (III): AuC13 = AuCl + C12.
Хлорид золота (III) AuC13 получается действием хлора на порошок или тонкие листочки золота при 200 °С. Красные иглы AuCl3 дают с водой коричнево-красный раствор комплексной кислоты: AuC13 +Н2О=Н2[AuOC13].
При осаждении раствора AuC13 едкой щёлочью выпадает амфотерная жёлто-коричневая гидроокись золота(III) Au(OH)3 c преобладанием кислотных свойств; поэтому её называют золотой кислотой, а её соли — ауратами (III). При нагревании гидроокись золота (III) превращается в окись золота Au2O3, которая выше 220° разлагается по реакции: 2Au2O3 = 4Au + 3O2.
При восстановлении солей золота хлоридом олова (II) 2AuC13 + 3SnCl2 = 3SnCl4 + 2Au образуется весьма стойкий пурпуровый коллоидный раствор золота (кассиев пурпур); это используется в анализе для обнаружения золота. Количественное определение золота основано на его осаждении из водных растворов восстановителями (FeSO4, H2SO3, H2C2O4 и др.) или на применении пробирного анализа.
Гидроксид Au(OH)3 - темно-коричневые кристаллы; при нагревании дегидратируется с образованием сначала АuО(ОН), а затем сесквиоксида Аu2О3, к-рый выше 160°С разлагается на золото и О2; растворимость в воде 2,4.10-12 моль/л при 20°С, в р-рах НNО3 - до 0,38 моль/л при 25 °С, в растворах NaOH - до 8.10-4 моль/л при 25°С. В последнем случае в растворе золото находится в виде гидроксоаурат-ионов [Аu(ОН)4]- (рН 7-13). Образуется Аu(ОН)3 при добавлении концентрированного раствора щелочи или Mg(OH)2 к растворам Н[АuСl4].
Ауpaты неустойчивы, легко разлагаются при нагревании. Аураты щелочных металлов хорошо растворяются в воде, растворимость растет с увеличением ионного радиуса катиона; аураты Mg, Ca, Sr, Ba, Тl(I) ограниченно растворимы. Аураты с некоторыми органическими веществами образуют взрывчатые смеси. Предполагают, что при действии на гидроксид золота растворов щелочи образуются аурат-анионы [Н2АuО3]-, [HAuO3]2-, [AuO3]3-. См. также табл. 2.
Другие кислородные соединения золота неустойчивы, легко образуют взрывчатые смеси. Соединение Аu2О3 с аммиаком Au2O3.4NH3 называется "гремучим золотом"; взрывается при 145°С, иногда и при более низких температурах; без взрыва растворяется в растворах цианидов щелочных металлов.
Гемисульфид золота Au2S - черно-коричневые кристаллы; DG0обр 29 кДж/моль; плохо раств. в воде (произведение р-римости 4.10-69 при 25 °С), раств. в р-рах цианидов и полисульфидов щелочных металлов. Получают взаимод. конц. р-ра K[Au(CN)2] с H2S с послед. нагреванием до кипения с избытком соляной к-ты. Сесквисульфид Au2S3 - черные кристаллы; разлагается при нагр. до 200 °С; не раств. в соляной и серной к-тах, раств. в HNO3 с выделением элементарного золота, р-рах KCN, бромной воде. Получают взаимод. H2S с АuСl3 или комплексными хлоридами золота в безводном эфире на холоду. Известны комплексные соед., содержащие анионы [AuS3]2-, [AuS2]-, [AuS]-, [Au(SO3)2]3-, [Au(S2O3)2]3- .
Моноселенид AuSe существует в двух кристаллич. модификациях моноклинной сингонии. При обработке солянокислых р-ров золота на холоду селеноводородом осаждается сесквиселенид Au2Se3.H2Se, устойчивый (после сушки) в интервале 40-390°С; при 535-650°C разлагается с выделением элементарного золота.
Селенат (IV) Au2(SeO3)3.3H2SeO3 лимонно-желтые кристаллы; не раств. в воде, раств. в соляной и селенистой (при нагр.) к-тах.
Селенат (VI) Au2(SeO4)3 желтые кристаллы; DH0обр — 954 кДж/моль; не раств. в воде, разлагается соляной к-той, раств. в H2SO4, HNO3 и горячей конц. H2Se04.
Теллурид (гемителлурид) АuТе2 - кристаллы от латунно-желтого до серебристо-белого цвета с металлич. блеском; плотн. 9,3 г/см, DH0обр — 11 кДж/моль; хрупок, твердость по Моосу 2,5-3.
Тиоцианат AuSCN - бесцв. кристаллы; не раств. в воде и орг. р-рителях; при 140°С разлагается до металлич. золота и (SCN)n; под действием воды образует в р-рах прочные комплексные анионы [Au(SCN)2]- и [Au(SCN)4]- .
Коллоидное золото
При восстановлении золота в разб. р-рах его солей, а также при электрич. распылении золота в воде образуются коллоидные р-ры золота, окраска к-рых зависит от степени дисперсности частиц, а интенсивность окраски от их концентрации. Частицы золота в коллоидном р-ре отрицательно заряжены. Гидрофобный золь золота в солянокислом водном р-ре можно представить схемой:
[Аu]m - ядро мицеллы (число атомов т в зависимости от условий может меняться от неск. сотен до миллионов единиц); АuСl4- - ионы, определяющие отрицательный заряд коллоидной частицы золота и величину потенциала адсорбционного слоя толщиной d0; Н+ - противоионы, определяющие потенциал диффузионного слоя (электрокинетич. потенциал), из к-рых х ионов находится в размытой части двойного слоя толщиной d; n - кол-во ионов АuСl4-, адсорбированных на поверхности ядра мицеллы, при этом п
Сетевые обзоры и статьи о золоте
Библиография по золоту
См. также литературу при статье Золота сплавы.
- Общая металлургия, М., 1967.
- Некрасов Б. В., Основы общей химии, т. 3, М., 1970.
- Реми Г., Курс неорганической химии, пер. с нем., т. 2, М., 1966.
- Краткая химическая энциклопедия, т. 2, М., 1963.
- Левинсон Н. Р., Изделия из цветного и чёрного металла, в кн.: Русское декоративное искусство, т. 1—3, М., 1962—65.
- Вернадский В. И., Биогеохимические очерки. 1922—1932, М. — Л., 1940.
- Благородные металлы. Справочник, под ред. Е. М. Савицкого, М., 1984;
- Борисов С. М., Золото в экономике современного капитализма, М., 1968.
- Бусев А. И., Иванов В. М., Аналитическая химия золота, М., 1973;
- Магакьян И. Г., Рудные месторождения, 2 изд., Ер., 1961;
- Малышев В. М., Румянцев Д. В., Золото, М., 1979;
- Марфунин А. С., История золота, М., 1987.
- Михалевский Ф. И., Золото в период мировых войн, [М.], 1945;
- его же, Золото в системе капитализма после второй мировой войны, М., 1952;
- Паддефет Р., Химия золота, пер. с англ., М., 1982;
- Плаксин И. Н., Золото, в кн.: Краткая химическая энциклопедия, т. 2, М., 1966;
- Реми Г., Курс неорганической химии, пер. с нем., т. 2, М., 1966, с. 439—451;
- Русское золотое и серебряное дело 15—20 веков, М., 1967 (библ. с. 289—93);
- B. C. Стрижко, М. А. Меретуков.
- Ullmanns Enzykiopadie dertechnischen Chemie, 3 Aufl., Bd 8, Munch. — B., 1957, S. 253—307;
- Rosenberg М., Geschichte der Goldschmiedekunst auf technischer Grundlage, Fr./M., 1918.
На правах рекламы (см. условия): ◀ ◀ ◀ Место для размещения коммерческих ссылок (см. , пожалуйста, условия) ▶ ▶ ▶ --> Хотите продать золотое кольцо? Скупка Златия поможет напольные покрытия Продаём с оплатой картой в режиме онлайн
Ключевые слова для поиска сведений о свойствах, добыче и выплавке золота: На русском языке: физические и химические свойства золота, атомные размеры и электронные оболочки Au; На английском языке: gold, Au.
Золото
Au, химический элемент 1 группы периодической системы Менделеева; атомный номер 79, атомная масса 196,9665; тяжёлый металл жёлтого цвета. Состоит из одного устойчивого изотопа 197 Au.
Историческая справка. З. было первым металлом, известным человеку. Изделия из З. найдены в культурных слоях эпохи неолита (5—4-е тыс. до н. э.). В древних государствах — Египте, Месопотамии, Индии, Китае добыча З., изготовление украшений и др. предметов из него существовали за 3—2 тыс. до н. э. З. часто упоминается в Библии, «Илиаде», «Одиссее» и др. памятниках древней литературы. Алхимики называли З. «царём металлов» и обозначали его символом Солнца ⊙; открытие способов превращения неблагородных металлов в З. было главной целью алхимии (См. Алхимия).
Распространённость в природе. Среднее содержание З. в литосфере составляет 4,3∙10 -7 % по массе. В магме и магматических породах З. рассеяно, но из горячих вод в земной коре образуются гидротермальные месторождения З., имеющие важное промышленное значение (кварцевые золотоносные жилы и др.). В рудах З. в основном находится в свободном (самородном) состоянии (см. Золото самородное) и лишь очень редко образует минералы с селеном, теллуром, сурьмой, висмутом. Пирит и др. сульфиды часто содержат примесь З., которое извлекают при переработке медных, полиметаллических и др. руд.
В биосфере З. мигрирует в комплексе с органическими соединениями и механическим путём в речных взвесях. 1 л морской и речной воды содержит около 4∙10 -9 г З. На участках золоторудных месторождений подземные воды содержат З. приблизительно 10 -6 г/л. Оно мигрирует в почвах и оттуда попадает в растения; некоторые из них концентрируют З., например хвощи, кукуруза. Разрушение эндогенных месторождений З. приводит к образованию россыпей З., имеющих промышленное значение. З. добывается в 41 стране; его основные запасы сосредоточены в СССР, ЮАР и Канаде.
Физические и химические свойства. З. — мягкий, очень пластичный, тягучий металл (может быть проковано в листки толщиной до 8∙10 -5 мм, протянуто в проволоку, 2 км которой весят 1 г), хорошо проводит тепло и электричество, весьма стойко против химических воздействий. Кристаллическая решётка З. гранецентрированная кубическая, а = 4,704 Å. Атомный радиус 1,44 Å, ионный радиус Au 1+ 1,37 Å. Плотность (при 20°С) 19,32 г/см 3 , tпл 1064,43°С, tkип 2947°С; термический коэффициент линейного расширения 14,2∙10 -6 (0—100°С); удельная теплопроводность 311,48 вт/(м∙К) [0,744 кал/см (сек∙°С]; удельная теплоёмкость 132,3 дж/(кг∙К) [0,0316кал/г∙°С] (при 0°—100°С); удельное электросопротивление 2,25∙10 -8 ом (м (2,25∙10 -6 ом (см) (при 20°С); температурный коэффициент электросопротивления 0,00396 (0—100°С). Модуль упругости 79∙103Мн/м 2 (79∙10 2 кгс/мм 2 ), для отожжённого З. предел прочности при растяжении 100—140 Мн/м 2 (10—14 кгс/мм 2 ), относительное удлинение 30—50%, сужение площади поперечного сечения 90%. После пластической деформации на холоду предел прочности повышается до 270—340 Мн/м 2 (27—34 кгс/мм 2 ). Твёрдость по Бринеллю 180 Мн/м 2 (18 кгс/мм 2 ) (для З. отожжённого около 400 °С).
Конфигурация внешних электронов атома З. 5d 10 6s 1 . В соединениях З. имеет валентности 1 и 3 (известны комплексные соединения, в которых З. 2-валентно). С неметаллами (кроме галогенов) З. не взаимодействует. С галогенами З. образует галогениды, например 2Au + 3Cl2 =2AuC13. В смеси соляной и азотной кислот З. растворяется, образуя золотохлористоводородную кислоту H [AuCl4]. В растворах цианида натрия NaCN (или калия KCN) при одновременном доступе кислорода З. превращается в цианоаурат (I) натрия 2Na [Au (CN)2]. Эта реакция, открытая в 1843 П. Р. Багратионом, получила практическое применение только в конце 19 в. (см. Цианирование). Для З. характерна лёгкая восстановимость его из соединений до металла и способность к комплексообразованию. Существование закиси З., т. е. оксида З. (I) Au2O, сомнительно. Хлорид З. (I) AuCl получается при нагревании хлорида З. (III): AuC13 = AuCl + C12.
Хлорид З. (III) AuC13 получается действием хлора на порошок или тонкие листочки З. при 200 °С. Красные иглы AuC13 дают с водой коричнево-красный раствор комплексной кислоты: AuC13 +Н2О=Н2[AuOC13].
При осаждении раствора AuC13 едкой щёлочью выпадает амфотерная жёлто-коричневая гидроокись З.(III) Au (OH)3 c преобладанием кислотных свойств; поэтому её называют золотой кислотой, а её соли — ауратами (III). При нагревании гидроокись З. (III) превращается в окись З. Au2O3, которая выше 220° разлагается по реакции:
образуется весьма стойкий пурпуровый коллоидный раствор З. (кассиев пурпур); это используется в анализе для обнаружения З. Количественное определение З. основано на его осаждении из водных растворов восстановителями (FeSO4, H2SO3, H2C2O4 и др.) или на применении пробирного анализа (См. Пробирный анализ).
Получение З. и его аффинаж. Из россыпных месторождений З. можно извлечь отмучиванием, основанным на большой разности плотностей З. и пустой породы. Этот способ, применявшийся уже в глубокой древности, сопряжён с большими потерями. Он уступил место амальгамации (См. Амальгамация) (известной уже в 1 в. до н. э. и применявшейся в Америке начиная с 16 в.) и цианированию, получившему широкое распространение в Америке, Африке и Австралии в 1890-х гг. В конце 19 — начале 20 вв. основным источником З. стали коренные месторождения. Золотоносную породу сначала подвергают дроблению и обогащению. Из полученного концентрата извлекают З. раствором цианида калия или натрия. Из раствора комплексного цианида осаждают З. цинком; при этом выпадают и примеси. Для очистки (аффинажа) З. электролизом (способ Э. Вольвилла, 1896) аноды, отлитые из нечистого З., подвешивают в ванне, содержащей солянокислый раствор AuC13, катодом служит лист чистого З. При прохождении тока примеси выпадают в осадок (анодный ил, шлам), а на катоде отлагается З. чистотой не менее 99,99%.
Применение. З. в условиях товарного производства выполняет функцию денег (См. Деньги) (см. раздел Экономическое значение). В технике З. применяют в виде сплавов с др. металлами, что повышает прочность и твёрдость З. и позволяет экономить его (см. Золотые сплавы). Содержание З. в сплавах, применяемых для изготовления ювелирных изделий, монет, медалей, полуфабрикатов зубопротезного производства и т.д., выражают пробой (см. Проба благородных металлов, Ювелирные сплавы); обычно добавкой служит медь (т. н. лигатура). В сплаве с платиной З. используется в производстве химически стойкой аппаратуры, в сплаве с платиной и серебром — в электротехнике. Соединения З. используют в фотографии (тонирование).
З. в искусстве. З. применяется с древнейших времён в ювелирном искусстве (См. Ювелирное искусство) (украшения, культовая и дворцовая утварь и т.д.), а также для золочения (См. Золочение). Благодаря своей мягкости, ковкости, способности тянуться З. поддаётся особо тонкой обработке чеканкой, литьём, гравировкой. З. используют для создания разнообразных декоративных эффектов (от глади жёлтой полированной поверхности с плавными переливами световых бликов до сложных фактурных сопоставлений с богатой светотеневой игрой), а также для выполнения тончайшей филиграни (См. Филигрань). З., часто окрашенное примесями др. металлов в различные цвета, применяется в сочетании с драгоценными и поделочными камнями (См. Драгоценные и поделочные камни), жемчугом, Эмалью, Чернью.
В медицине препараты З. используют в виде взвеси в масле (отечественный препарат кризанил, зарубежный — миокризин) или водорастворимых препаратов (зарубежные — санкризин и солганал) для инъекций при лечении хронических ревматических артритов, эритематозной красной волчанки, часто в сочетании с гормональными и др. препаратами. Препараты З. нередко вызывают побочные явления (повышение температуры тела, раздражение кишечника, почек и др.). Противопоказания к применению препаратов З.: тяжёлые формы туберкулёза, сахарный диабет, заболевания сердечно-сосудистой системы, печени, почек, крови.
Радиоактивное З. (чаще 198 Au) вводят в ткани в виде штифтов, гранул и т.п. — для гамма-терапии (См. Гамма-терапия) и в виде коллоидных растворов — для бета-терапии (См. Бета-терапия). Его применяют при лечении опухолей, обычно в сочетании с хирургическим и медикаментозным лечением, а также с диагностическими целями — в виде коллоидных растворов при исследовании ретикуло-эндотелиальной системы, печени, селезёнки и др. органов.
Лит.: Плаксин И. Н., Золото, в кн.: Краткая химическая энциклопедия, т. 2, М., 1966; Реми Г., Курс неорганической химии, пер. с нем., т. 2, М., 1966, с. 439—451; Ullmanns Enzykiopädie dertechnischen Chemie, 3 Aufl., Bd 8, Münch. — B., 1957, S. 253—307; Магакьян И. Г., Рудные месторождения, 2 изд., Ер., 1961; Русское золотое и серебряное дело 15—20 веков, М., 1967 (библ. с. 289—93); Rosenberg М., Geschichte der Goldschmiedekunst auf technischer Grundlage, Fr./M., 1918.
Экономическое значение. З. в условиях товарного производства выполняет функцию всеобщего эквивалента. «Первая функция золота состоит в том, чтобы доставить товарному миру материал для выражения стоимости, т. е. для того, чтобы выразить стоимости товаров как одноименные величины, качественно одинаковые и количественно сравнимые» (Маркс К., в кн.: Маркс К. и Энгельс Ф., Соч., 2 изд., т. 23, с. 104). Выражая стоимость всех др. товаров, З. в качестве всеобщего эквивалента приобретает особую потребительную стоимость, становится деньгами. «Золото и серебро по природе своей не деньги, но деньги по своей природе — золото и серебро» (Маркс К., там же, т. 13, с. 137). Товарный мир выделил З. в качестве денег потому, что оно обладает наилучшими для денежного товара физическими и химическими свойствами: однородностью, делимостью, сохраняемостью, портативностью (большой стоимостью при небольших объёме и весе), легко поддаётся обработке. Значительное количество З. применяется для изготовления монет или в форме слитков хранится в качестве золотого запаса центральных банков (государства). З. широко используется для промышленного потребления (в радиоэлектронике, приборостроении и др. прогрессивных отраслях), а также как материал для изготовления ювелирных изделий.
Первоначально З. употреблялось исключительно для выделки украшений, затем оно стало служить средством сбережения и накопления богатств, а также обмена (сначала в форме слитков). В качестве денег З. использовалось ещё за 1500 лет до н. э. в Китае, Индии, Египте и государствах Месопотамии, а в Древней Греции — в 8—7 вв. до н. э. В Лидии, богатой месторождениями З., в 7 в. до н. э. началась чеканка первых в истории монет. Имя лидийского царя Креза (правил около 560—546 до н. э.) стало синонимом несметного богатства. На территории СССР (в Армении) монеты из З. Чеканились в 1 в. до н. э. Но в древности и в средние века З. не являлось основным валютным металлом. Наряду с ним функции денег выполняли медь и серебро.
Погоня за З., страсть к обогащению были причинами многочисленных колониальных и торговых войн, в эпоху Великих географических открытий толкали на поиски новых земель. Поток драгоценных металлов в Европу после открытия Америки явился одним из источников первоначального накопления капитала (См. Первоначальное накопление капитала). До середины 16 в. из Нового Света в Европу ввозилось преимущественно З. (97—100% ввозимого металла), а со 2-й трети 16 в., после открытия богатейших месторождений серебра в Мексике и Перу — преимущественно серебро (85—99%). В России в начале 19 в. стали разрабатываться новые месторождения З. на Урале и в Сибири, и в течение трёх десятилетий страна занимала первое место в мире по его добыче. В середине 19 в. были открыты богатые месторождения З. в США (Калифорния) и Австралии, в 1880-х гг. — в Трансваале (Южная Африка). Развитие капитализма, расширение межконтинентальной торговли усилили спрос на денежные металлы, и, хотя добыча З. возросла, во всех странах наряду с З. в качестве денег ещё продолжало широко использоваться серебро. В конце 19 в. произошло резкое снижение стоимости серебра вследствие совершенствования способов его добычи из полиметаллических руд. Рост мировой добычи З. и особенно прилив его в Европу и США из Австралии и Африки ускорили вытеснение обесценившегося серебра и создали условия для перехода большинства стран к монометаллизму (золотому) в его классической форме золотомонетного стандарта (см. Золотой стандарт). Первой к золотому монометаллизму перешла в конце 18 в. Великобритания. К начальник 20 в. золотая валюта утвердилась в большинстве стран мира.
Отражая отношения людей в условиях стихийного товарного производства, власть З. выступает на поверхности явлений как отношение вещей, кажется натуральным внутренним свойством З. и порождает золотой и денежный фетишизм (см. Деньги, Товарный фетишизм). Страсть к накоплению золотых богатств растет безгранично, толкает на чудовищные преступления. Особенно возрастает власть З. при капитализме, когда товаром становится рабочая сила. Образование при капитализме мирового рынка расширило сферу обращения З. и сделало его мировыми деньгами.
В период общего кризиса капитализма подрывается золотой стандарт. Во внутреннем обращении капиталистических стран господствующими становятся бумажные деньги и неразменные на З. банкноты. Ограничиваются или вовсе запрещаются вывоз З. и его купля-продажа. В связи с этим З. перестаёт выполнять функции средства обращения и средства платежа, но, выступая идеально как мера стоимости, а также сохраняя значение средства образования сокровищ и мировых денег, остаётся базой денежных систем и главным средством окончательного урегулирования взаимных денежных требований и обязательств капиталистических стран. Размеры запасов З. — важный показатель устойчивости капиталистических валют и экономического потенциала отдельных стран (см. также Золотой запас, Золотовалютные резервы). Купля-продажа З. для промышленного потребления, а также и для частной тезаврации (накопления) осуществляется на специальных рынках золота (см. Рынки золота). Выпадение З. из свободного межгосударственного рыночного оборота вызвало сокращение его доли в валютной системе капиталистического мира и, прежде всего, в валютных резервах капиталистических стран (с 89% в 1913 до 71% в 1928, 69% в 1958 и 55% в 1969). Всё более значительная часть вновь добываемого З. поступает для тезаврации и промышленного использования (в современной химической промышленности, для ракетостроения, космической техники). Так, за 1960—70 частная тезаврация З. возросла в 3,3 раза, его промышленное и ювелирное использование почти в 2,3 раза, золотые запасы капиталистических стран сохранились практически на одном уровне (41 млрд. долл.). (О добыче З. в капиталистических странах см. в ст. Золотодобывающая промышленность.)
В условиях социалистической экономики З. также является всеобщим эквивалентом, выступая мерой стоимости и масштабом цен. С 1 января 1961 золотое содержание советского рубля установлено в 0,987412 г чистого З. Это же количество З. Положено в основу переводного рубля — международной социалистической валюты стран — членов СЭВ. На мировом социалистическом рынке З. выполняет функцию мировых денег.
Лит.: Михалевский Ф. И., Золото в период мировых войн, [М.], 1945; его же, Золото в системе капитализма после второй мировой войны, М., 1952; Борисов С. М., Золото в экономике современного капитализма, М., 1968.

Золото — минерал, являющийся природным твёрдым раствором серебра (следы, до 43%) в золоте; обычны примеси (следы, до 0,9%) меди, железа, свинца, реже – висмута, ртути, платины, марганца и др. Известны разновидности с повышенным содержанием меди – до 20% (медистое золото, купроаурит), висмута – до 4% (висмутистое золото, висмутаурит), платиноидов (платинистое и иридистое золото; порпецит – Au, Pd, родит – Au, Rh), природные амальгамы (Au, Hg).
СТРУКТУРА
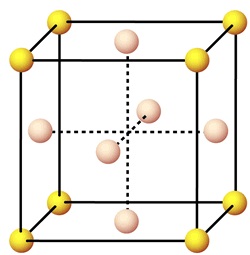
Кристаллическая структура золота
Кристаллизуется в кубической сингонии, в виде октаэдров, ромбододекаэдров, кубов и более сложных по форме кристаллов; нередко они искажены, сильно вытянуты, образуя “проволочки”, “волоски”, или уплощены параллельно грани октаэдра. Для самородного золота особенно низкопробного, характерно многообразие форм роста, оно обычно в виде скелетных кристаллов, дендритов, нитевидных и скрученно-нитевидных кристаллов. Широко распространены прожилковидные и неправильные комковидные, “крючковатые” выделения; на их поверхности нередко сохраняются отпечатки кристаллов других минералов, агрегаты которых включали скопления самородного золота. Травление выявляет кристаллически-зернистое строение золотых частиц.
СВОЙСТВА

Золотые слитки и самородки
Золото — очень тяжёлый металл: плотность чистого золота равна 19,32 г/см³ (шар из чистого золота диаметром 46,237 мм имеет массу 1 кг). Диамагнетик, то есть, магнитное поле в золоте ослабевает. Среди металлов по плотности занимает седьмое место после осмия, иридия, рения, платины, нептуния и плутония. Сопоставимую с золотом плотность имеет вольфрам (19,25). Высокая плотность золота облегчает его добычу, отчего даже простые технологические процессы — например, промывка на шлюзах, — могут обеспечить высокую степень извлечения золота из промываемой породы.
Золото — очень мягкий металл: твёрдость по шкале Мооса ~2,5, по Бринеллю 220—250 МПа (сравнима с твёрдостью ногтя).
Золото также высокопластично: оно может быть проковано в листки толщиной до ~0,1 мкм (100 нм) (сусальное золото); при такой толщине золото полупрозрачно и в отражённом свете имеет жёлтый цвет, в проходящем — окрашено в дополнительный к жёлтому синевато-зеленоватый. Золото может быть вытянуто в проволоку с линейной плотностью до 2 мг/м.
Температура плавления золота 1064,18 °C (1337,33 К), кипит при 2856 °C (3129 К). Плотность жидкого золота меньше, чем твёрдого, и составляет 17 г/см 3 при температуре плавления. Жидкое золото довольно летучее, и активно испаряется задолго до температуры кипения.
ЗАПАСЫ И ДОБЫЧА

Содержание золота в земной коре очень низкое — 4,3·10 -10 % по массе (0,5-5 мг/т), но месторождения и участки, резко обогащённые металлом, весьма многочисленны. Золото содержится и в воде. Один литр и морской, и речной воды содержит менее 5·10 −9 граммов Au, что примерно соответствует 5 килограммам золота в 1 кубическом километре воды.
Золоторудные месторождения возникают преимущественно в районах развития гранитоидов, небольшое их количество ассоциирует с основными и ультраосновными породами.
Для получения золота используются его основные физические и химические свойства: присутствие в природе в самородном состоянии, способность реагировать лишь с немногими веществами (ртуть, цианиды). С развитием современных технологий более популярными становятся химические способы.
В 1947 году американские физики Ингрем, Гесс и Гайдн проводили эксперимент по измерению эффективного сечения поглощения нейтронов ядрами ртути. В качестве побочного эффекта эксперимента было получено около 35 мкг золота. Таким образом, была осуществлена многовековая мечта алхимиков — трансмутация ртути в золото. Однако экономического значения такое производство золота не имеет, так как обходится во много раз дороже добычи золота из самых бедных руд.
ПРОИСХОЖДЕНИЕ

Изделия из золота
Самородное золото – главная форма нахождения золота в природе. Оно концентрируется в гидротермальных месторождениях образуя золотые руды, неравномерно распределяясь в трещиноватом жильном кварце и в сульфидах – пирите, арсенопирите, пирротине и др. В существенно сульфидных рудах самородное золото тонкодисперсное. При окислении руд на земной поверхности мелкое самородное золото частично растворяется и переотлагается; в ряде случаев оно обогащает верхние части рудных тел. Процессы их разрушения приводят к освобождению частиц самородного золота и их накоплению в россыпях; перемещаясь водными потоками вместе с другим кластическим материалом, частицы окатываются, округляются, деформируются, частично перекристаллизовываются; в результате электрохимической коррозии на них образуется тонкая оболочка высокопробного золота, что приводит к общему повышению пробы самородного золота в россыпях.
ПРИМЕНЕНИЕ

По своей химической стойкости и механической прочности золото уступает большинству платиноидов, но незаменимо как материал для электрических контактов. Поэтому в микроэлектронике золотые проводники и гальванические покрытия золотом контактных поверхностей, разъёмов, печатных плат используются очень широко.
Золото используется в качестве мишени в ядерных исследованиях, в качестве покрытия зеркал, работающих в дальнем инфракрасном диапазоне, в качестве специальной оболочки в нейтронной бомбе. Тонкий слой золота (20 нм) на внутренней поверхности оконных и витражных стекол существенно уменьшает нежелательные тепловые потери зимой, а летом предохраняет внутренние помещения зданий и транспортных средств от нагревания инфракрасными лучами.
Золотые припои очень хорошо смачивают различные металлические поверхности и применяются при пайке металлов. Тонкие прокладки, изготовленные из мягких сплавов золота, используются в технике сверхвысокого вакуума.
Традиционным и самым крупным потребителем золота является ювелирная промышленность. Ювелирные изделия изготавливают не из чистого золота, а из его сплавов с другими металлами, значительно превосходящими золото по механической прочности и стойкости. В настоящее время для этого служат сплавы Au-Ag-Cu, которые могут содержать добавки цинка, никеля, кобальта, палладия. Стойкость к коррозии таких сплавов определяются, в основном, содержанием в них золота, а цветовые оттенки и механические свойства — соотношением серебра и меди.
Значительные количества золота потребляет стоматология: коронки и зубные протезы изготовляют из сплавов золота с серебром, медью, никелем, платиной, цинком. Такие сплавы сочетают коррозионную стойкость с высокими механическими свойствами.
Соединения золота входят в состав некоторых медицинских препаратов, используемых для лечения ряда заболеваний (туберкулёза, ревматоидных артритов и т. д.). Радиоактивный изотоп 198 Au (период полураспада 2,967 сут.) используется при лечении злокачественных опухолей в радиотерапии.
ЗОЛОТО
Au (aurum)
химический элемент IB подгруппы (Cu, Ag, Au) периодической системы элементов, благородный металл. Золото широко используется в монетном деле, чеканке, ювелирных изделиях, произведениях искусства и в условиях товарного производства выполняет функцию всеобщего стоимостного эквивалента. В природе, как правило, встречается в свободном состоянии (самородное золото). Известно человечеству с древности и применяется по крайней мере уже 6000 лет. Золото легко обрабатывается и с давних пор ценится за красоту и коррозионную стойкость. В минералах встречается только в соединениях с теллуром или селеном, которые, однако, очень редки (например, теллуриды, такие, как кренерит AuTe2 и сильванит (AuAg)Te2). Золото часто сопутствует минералам серебра, меди и изредка других металлов, золотые руды могут содержать драгоценные металлы платиновой группы. Природное золото встречается в золотоносных песках, в виде тонких прожилок в кварце, но обнаруживали его и в виде больших самородков, до 82 кг. Морская вода также содержит следы золота, но несмотря на все попытки извлечение его из морской воды коммерчески невыгодно. По оценкам, общая масса золота на Земле составляет примерно 110 000 т, что соответствует кубу с ребром ок. 20 м. Существуют два типа месторождений золота - в россыпях и в рудах. В золотоносных песках в руслах ручьев и рек легкие породы со временем вымываются, и на дне остаются зерна золота, которые легко промыть и отфильтровать. (Известны связанные с обнаружением россыпей золота периоды массового увлечения золотоискательством - т.н. золотая лихорадка, например, на Аляске в 1896.) В рудных жилах или жилах золотоносного кварца золото внедряется в другой минерал, часто залегающий глубоко под землей. Золотоносные руды добывают мощными экскаваторами, бурением, взрывными работами, а золото выделяют и рафинируют механическими или химическими методами.
Применение. С древности золото шло на изготовление украшений и монет. Драгоценности, кубки и другие сосуды, предметы церковной утвари делают из золота уже тысячи лет. Так как золото - мягкий металл, для увеличения твердости его обычно используют в виде сплавов с другими металлами. Состав сплава определяют пробой (количество долей золота из 1000) или в каратах (доля от 24), например, 18 карат золота составляют 18/24 массы сплава. Покрытия из золота (золочение) обычно производят при совместном осаждении с серебром или медью из цианидных растворов. Золотую фольгу (сусальное золото) изготовляют из листового золота в виде тончайших (доли мкм) полосок, которые высоко ценятся за красоту и устойчивость к атмосферному воздействию; их используют для архитектурных украшений и тиснения на книгах. Золото и его соединения применяют в живописи, керамике, фотографии, стоматологии (зубные протезы) и как лекарственные средства. Например, некоторые соединения золота эффективны в лечении ревматических артритов, а искусственный радиоактивный изотоп 198Au - при радиотерапии опухолей. Благодаря очень хорошей электрической проводимости и высокой коррозионной стойкости золото применяют для изготовления транзисторов, выпрямителей и печатных плат (см. также ТРАНЗИСТОР; ПОЛУПРОВОДНИКОВЫЕ ЭЛЕКТРОННЫЕ ПРИБОРЫ). Из-за отражающей способности в ИК-диапазоне золото нашло применение в аэронавтике и космической технике, а также при изготовлении отражательных стекол. Многие столетия золото широко использовалось для чеканки монет и до сих пор является основой денежных систем. С 1870 до Первой мировой войны золото было главным стандартом в торговых операциях. После войны роль золота в международной денежной системе сильно уменьшилась. Тем не менее золотой запас сохраняет значение как резервный фонд мировых денег и как средство обеспечения устойчивости валюты, особенно в период инфляции. СВОЙСТВА ЗОЛОТА
Атомный номер 79 Атомная масса 196,9666 Стабильный изотоп (единственный природный) 197 Число известных изотопов (радиоактивных, искусственных) 21 Содержание в земной коре, % (масс.) 4Ч10-7 Содержание в морской воде, мг/л
Энциклопедия Кольера. — Открытое общество . 2000 .
Полезное
Смотреть что такое "ЗОЛОТО" в других словарях:
ЗОЛОТО — ЗОЛОТО, злато ср. самый дорогой крушец (металл), находимый в самородном виде, ·т.е. не в руде. Червонное золото, чистое, одной пробы с червонцами. Красное золото, с медным сплавом; белое, с серебряным сплавом, также | платина. Швейное золото,… … Толковый словарь Даля
Золото — – химический элемент, обозначается символом Au от латинского слова aurum. Простое вещество благородный металл желтого цвета, являющийся биржевым товаром. Золото известно человечеству с бронзового века. Его добычей занимались в Месопотамии и… … Банковская энциклопедия
Золото — Бизнес * Банкротство * Бедность * Благополучие * Богатство * Воровство * Выгода * Деньги * Долги * Скупость * Золото * Игра * Идея * Конкуренция * Планирование * Прибыль * … Сводная энциклопедия афоризмов
золото — всемогущее (Барыкова); всесильное (Садовников); могучее (Иванов Классик) «О золото крылатое, о золото парящее! О золото несытое, жестокое и мстящее! О золото лучистое, сквозь темный вихрь горящее! О золото живое. Лукавое, глухое!» (Брюсов,… … Словарь эпитетов
Золото — металл красивого желтого цвета, тонколистовое (сусальное) золото имеет зеленоватый оттенок. Золото с трудом образует химические соединения, оно химически устойчиво на воздухе, в воде и в кислотах, за исключением царской водки (в последней золото… … Официальная терминология
ЗОЛОТО — (лат. Aurum ) Аu, химический элемент I группы периодической системы, атомный номер 79, атомная масса 196,9665. Благородный металл желтого цвета, ковкий; плотность 19,32 г/см³, tпл 1064,4оC. Химически весьма инертен, на воздухе не изменяется… … Большой Энциклопедический словарь
ЗОЛОТО — (Aurum), хим. обозначение Аи, ат. вес 197,2; в периодической системе занимает по порядку 79 е место, 9 е в 1 й группе; очень мягкий, в высшей степени тягучий и ковкий металл желтовато красного цвета, очень тонкие листочки (листовое золото)… … Большая медицинская энциклопедия
Золото — (Aurum), Au, химический элемент I группы периодической системы, атомный номер 79, атомная масса 196,9665; относится к благородным металлам; мягкий тяжелый металл желтого цвета; плотность 19,32 г/см3, tпл 1064,4°C; химически инертно. В природе… … Иллюстрированный энциклопедический словарь
ЗОЛОТО — хим. элемент, символ Au (лат. Aurum), ат. н. 79, ат. м. 196,96, плотность 19320 кг/м3, tпл = 1064°С. Хотя золото редкий элемент, но оно стало первым известным человеку металлом, так как встречается в природе в самородном состоянии. Золото… … Большая политехническая энциклопедия
ЗОЛОТО — (символ Аu), встречающийся в природе ПЕРЕХОДНЫЙ ЭЛЕМЕНТ. Встречается как побочный продукт электролитической облагороженной меди. Используется в ювелирном деле, в изготовлении разъемов для электронного оборудования и как эквивалент в международных … Научно-технический энциклопедический словарь
ЗОЛОТО — ЗОЛОТО, золота, мн. нет, ср. 1. Один из благородных металлов, желтого цвета, употр. для драгоценных изделий и как мерило ценности. Браслет из чистого золота. Золото высокой пробы. Червонное золото. 2. собир. Изделия из золота. Сундуки полны… … Толковый словарь Ушакова
ЗОЛОТО — дар или проклятие человечеству
Не существует металла, кроме золота, который в течение веков занимал умы человечества. Его добывали тяжким трудом, за ним посылали экспедиции в дальние страны. И все ради того, чтобы украсить себя сиянием желтого, солнечного металла. Из него делали украшения, короны и даже ткали драгоценные материи.
Плиний Старший писал «я видел Агриппину, супругу принцепса Клавдия… одетую в военный плащ, сотканный из золота без всякой примеси другой материи».
Какое оно
Золото входит в обособленную группу драгоценных металлов.

Как знать, презирающая чернь и холопов, надменное злато «не желает» вступать в контакт (химические реакции) с другими элементами. Драгоценным оно было всегда — красота, блеск, долговечность металла полагались аристократам и прочим любимцам судьбы.
Химические и физические свойства:
- Чистое золото имеет очень низкую твердость — 2,5-3. Кто читал книги об истории, помнит, что золотые монеты нередко «пробовали на зуб». На настоящих монетах оставался след от зубов, на фальшивой (с большой долей примесей, обычно меди) — нет.
- Золото плавится при температура 1064°С; нагреете до 2947 °С — начнет кипеть и улетучиваться.
- Удельный вес металла 19,3 г/см3. Килограмм золота легко поместится в кармане или дамской сумочке — его легко «упаковать» в кубик со стороной 3,7 см.
- Ковкость металла поражает. Всего один грамм можно раскатать в лист площадью в половину квадратного метра. Это «сусальное золото».
- Для производства украшений у злата есть еще одно привлекательное свойство. Металл очень пластичный и тягучий, а значит – легко сгибается и растягивается.
- Кристаллическая структура решетки металла кубическая, гранецентрированная.
- Химически металл очень инертен. В нормальных условиях он не желает реагировать с другими элементами. Исключение — ртуть.
- Растворить солнечный металл можно в «царской водке» (смеси азотной с соляной кислотами в пропорции 1:3). Медленно, но реагирует с цианидами, йодистым калием, жидким бромом.
| Название, символ, номер | Зо́лото / Aurum (Au), 79 |
|---|---|
| Атомная масса (молярная масса) | 196,966569(4)[1] а. е. м. (г/моль) |
| Электронная конфигурация | [Xe] 4f14 5d10 6s1 |
| Радиус атома | 144 пм |
| Химические свойства | |
| Ковалентный радиус | 134 пм |
| Радиус иона | (−3e) 185 (+1e) 137 пм |
| Электроотрицательность | 2,64 (шкала Полинга) |
| Электродный потенциал | Au←Au3+ 1,50 В, Au←Au+ 1,70В |
| Степени окисления | −1,1,3,5 |
| Энергия ионизации (первый электрон) | 889,3 (9,22) кДж/моль (эВ) |
| Термодинамические свойства простого вещества | |
| Плотность (при н. у.) | 19,3-19,32[2][3] г/см³ |
| Температура плавления | 1337,33 К (1064,18 °C, 1947,52 °F)[2] |
| Температура кипения | 3129 К (2856 °C, 5173 °F)[2] |
| Уд. теплота плавления | 12,68 кДж/моль |
| Уд. теплота испарения | ~340 кДж/моль |
| Молярная теплоёмкость | 25,39[4] Дж/(K·моль) |
| Молярный объём | 10,2 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | кубическая гранецентрированная типа Cu, пр. группа Fm3m |
| Параметры решётки | 4,0781 Å |
| Отношение c/a | 1 |
| Температура Дебая | 170,00 K |
| Прочие характеристики | |
| Теплопроводность | (300 K) 318 Вт/(м·К) |
| Номер CAS | 7440-57-5 |
Месторождения и их классификация
Происхождение нашего драгоценного металла в месторождениях зависит от вида породы:
- Золото-кварцевые формации. Приурочены к зонам разломов. Распределение металла неравномерно; образуются обогащенные участки, называемые «бонанцами» или «рудными столбами».
- Месторождения золото-полисульфидно-кварцевой формации. Приурочены к гранитоидным и субвулканическим комплексам. Среднее содержание металла 10-15 г/т.
- Золото-лиственнитовые месторождения. К ним относится Хаак-Саирское (Тува), Мечниковское, Кировское (Урал) месторождения.
- Золото-сульфидные месторождения. Связаны с вулканогенно-осадочными толщами.
- Золото-порфировые месторождения. К этому типу относятся Березняковское (Урал), Юбилейное (Казахстан), Кызык-Чадр (Тува) месторождения.
- Месторождения зон окисления. Приурочены к верхним горизонтам сульфидных залежей на многих колчеданных месторождениях.
- Россыпные месторождения часто сопровождают коренные золоторудные поля. Длина россыпей от 200-300 метров, реже 3-5 км. Ширина россыпей 20-30 метров, реже — 100-300 метров. По условиям залегания существуют россыпи, связанные с руслами, поймами рек, террасами, долинами, межгорными впадинами.
Крупнейшее в мире месторождение золота расположено в ЮАР. По некоторым данным, здесь получают до половины мировой добычи.
Много ли злата на Земле
Многие аналитики считают, что запасы добытого «презренного металла» подсчитать сложно.
Эксперты дают цифры, разнящиеся на порядки (от 155 000 тонн до 2,5 миллионов тонн).
Существуют страны, где процветает нелегальная «заготовка» золота, а иные государства предпочитают держать в тайне объемы добычи. Принцип «вы мои деньги не считайте» работает как у отдельного гражданина, так и на государственном уровне.
Добыча металла с древних времен до наших дней
Золото — удивительный металл. Все полезные ископаемые добываются, чтобы использовать и расходовать, его же в основном копят. Государства и отдельные граждане.
От Египта до Америки
Считается, что первыми добычу желтого металла начали египтяне. Хроники зафиксировали добычу металла в Аравийско-Нубийской провинции. Там были богатейшие месторождения. Еще во времена Тутмоса III в год там добывали около 50 тонн золота. А всего за время эксплуатации месторождение дало более 3500 тонн металла.
Однако месторождение истощилось. Многие историки связывают упадок Египта именно с падением количества драгоценного металла в государстве.
В Европе нашли новые месторождения (Испания, Австро-Венгрия). А с испанскими завоеваниями в Америке солнечный металл хлынул в Старый Свет потоком.
Из них в промышленности использовали 12%, из 50% люди сделали украшения.
В любом случае, добыча драгметалла стимулировала развитие металлургии, а заодно и международную торговлю.

Современная добыча золота
Времена золотой лихорадки, которые сотрясали страны, давно прошли. Жестокая романтика, когда тысячи людей разорялись, а многие и гибли, ушли в прошлое. Хотя единицы из них неприлично богатели.
Сейчас золотодобыча учитывает прибыли и накладные расходы, ни шагу не ступит без предварительной разведки месторождений, оценки экономических рисков, строительства рудников с применением надлежащего оборудования.
В современное время добычу золотосодержащей руды ведут в основном на большой глубине или из истощенных россыпных месторождений. Золото в природе — ресурс не возобновляемый, а добывают его с незапамятных времен. Еще в старину «сняты сливки» с богатейших месторождений, а нам, потомкам, остается тяжелая работа выбирать золото из уже «очищенных» мест. Или, как вариант, желтый металл добывают на большой глубине.
Из руды — в благородный металл
Современные золотодобывающие предприятия оснащены хорошим оборудованием, там трудятся специалисты своего дела.
Подробно о переработке руды в солнечный металл можно прочитать в статье «Драгоценные металлы».
Золото и его сплавы
Драгоценный металл золото ювелиры используют в виде сплавов. Издревле известен электр (или электрон) – сплав золота и серебра. Об этом писал Гомер в «Одиссее»: «дворец Менелая сверкал золотом, электром, серебром и слоновой костью».
В позднесредневековой Японии для ювелирных изделий применялись сплавы: сякудо (красная медь), у-кин (жадное золото) — медно-золотой сплав (3-25% драгметалла); тюсё — медь с добавкой золота (<3%), ао-кин (тусклое золото) — аналог электра.
Сейчас палитра цветов сплавов расширилась, ювелиры используют золото: белое, лимонное, красное, синее, черное, розовое, зеленое. К злату добавляют кадмий, палладий, никель, серебро, медь, цинк — эти добавки придают необходимый оттенок сплаву.
Познавательно: «аметистовое» золото (пурпурное, фиолетовое), сплав, изобретенный в Сингапуре, востребован у ювелиров. Сейчас оно на пике моды.
Свойства драгоценного металла (устойчивость к коррозии, пластичность, ковкость) нашли ему место в жизни человека:

Интересно: журнал British Medical Journal опубликовал результаты исследования останков Дианы де Пуатье, фаворитки короля Франции Генриха II. В ее 60 лет она выглядела 30-летней. Причина (по выводу исследователей) в количестве золота, содержавшемся в костях и волосах останков фаворитки. Оно превышало норму в десятки раз. Диана принимала эликсиры с драгоценным металлом, которые ей привозили из Египта.
Драгметаллы — в монеты
Власть золота над человеком в полной мере проявилась, когда из предмета роскоши «презренный металл» стал мерой стоимости товара — деньгами. Первыми догадались делать монеты из золота лидийцы.
Последний лидийский царь Крез (помните, конечно – «богат как Крез») придумал биметаллическую (золото-серебро) систему. Идея была такой удачной, что жила и процветала многие века.
Дарий, персидский царь, начал вместо клейма чеканить на монетах собственное изображение.
Монетарным стандартом между золотом и серебром часто был 1:10. Но соотношения постоянно менялись. В Древнем Египте серебро было дороже золота.

Сколько золота в колечке
Государства жестко контролируют меры чистоты, то есть содержание драгоценных металлов, в сплавах.
Для этого разработана система проб. Это определение количество чистого металла в сплаве. Это количество (проба) называется клеймом.
Существует 4 системы проб. Самые популярные — каратная и метрическая.
Метрическая система принята в странах, подписавших Конвенцию о клеймении драгметаллов. Это Россия, Франция, Германия, Израиль, Кипр и еще несколько стран.
Британскую каратную систему предпочитают в Канаде, Швейцарии, США. Ирландцы мудро ставят на изделии обе пробы — каратную и метрическую. А Великобритания ставит метрическую пробу, но в описании товара указывает и каратную.

Познавательно: хотите пересчитать караты в метрическую пробу — умножьте число карат на 125 и разделите на 3. То есть, 18 каратное изделие будет соответствовать пробе 750 (18х125:3).
Пересчитаем метрическую пробу в караты — метрическую пробу умножаем на 24 и делим на 1000. То есть, изделие с пробой 750 будет соответствовать 18 каратам.
Подделки, фальшивки…
Вынуждены вас огорчить: больше 70% ввозимого в Россию золота — фальсификация. Много золотых украшений ввозят, не затрудняя проверками таможню и пробирный контроль, так что будьте осторожны при покупке ювелирных изделий.
Порой отличить подделку просто невозможно, несмотря на проверку на детекторе. Особенно, если украшение импортное.
Покупать ювелирные украшения лучше в солидных салонах и пусть это будет производство известных российских или зарубежных фирм. Стоимость изделия будет выше, чем на распродажах и в сомнительных местах, но вероятность нарваться на подделку меньше.
При покупке обращайте внимание на наличие клейма (его подделка — уголовщина, с таким большинство мошенников стараются не связываться).
Внимательно осмотрите «изнанку» изделия — чем она аккуратнее, чем тщательнее закреплены камни — тем выше гарантия подлинности.
Подушка безопасности
В качестве объекта инвестиций современные украшения из золота не рассматриваются, разве что дорогой и редкий антиквариат. Хотите инвестировать — покупайте драгметаллы в слитках, монетах, или открывайте обезличенные металлические счета.
Можно заниматься биржевой торговлей, но это доступно профессионалам (если желаете получать прибыль).
В любом случае «не кладите все яйца в одну корзину». То есть, если отложили крупную сумму на инвестиции, минимизируйте риски — пробуйте разные варианты.
По данным Геологической службы США (USGS) частные накопления золота составляют не менее 100 000 тонн.
Рекомендуем видео: Почему золото так ценится?

Мне 42 года и я специалист в области минералогии. Здесь на сайте я делюсь информацией про камни и их свойства — задавайте вопросы и пишите комментарии!
Читайте также:
