Какое строение имеют металлы
Обновлено: 15.05.2024
Определение металлов можно дать с позиций химии, физики и техники.
В химии металлы — это химические элементы, находящиеся в левой части периодической системы элементов Д. И. Менделеева, которые обладают особым механизмом взаимодействия валентных электронов (ионов) с ядром как в самих металлах, так и при вступлении в химические реакции с другими элементами, в том числе с металлами.
Физика характеризует металлы как твердые тела, обладающие цветом, блеском, способностью к плавкости (расплавлению) и затвердеванию (кристаллизации), тепло- и электропроводностью, магнитными и другими свойствами.
В технике металлы — это конструкционные материалы, обладающие высокой обрабатываемостью (ковкостью, штампуемостью, обрабатываемостью резанием, паяемостью, свариваемостью и др.), прочностью, твердостью, ударной вязкостью и рядом других ценных свойств, благодаря которым они находят широкое применение.
Русский ученый М. В. Ломоносов (1711 — 1765), исследуя металлы и неметаллы в своем труде «Первые основания металлургии или рудных дел», дал металлам определение: «Металлом называется светлое тело, которое ковать можно. Таких тел находим только шесть: золото, серебро, медь, олово, железо и свинец». Это определение М. В. Ломоносов дал в 1773 г., когда известны были только шесть металлов.
Из металлов, добываемых из недр земли, получают большую группу конструкционных материалов, применяемых в различных отраслях промышленности. В природе одни металлы встречаются в чистом, самородном виде, другие — в виде оксидов (соединений металла с кислородом), нитридов и сульфидов, из которых состоят различные руды этих металлов.
Самыми распространенными металлами, применяемыми в качестве конструкционных материалов, являются железо, алюминий, медь и сплавы на основе этих металлов.
К металлам относятся более 80 элементов периодической системы Менделеева. Все эти металлы подразделяются на две большие группы: черные металлы и цветные металлы.
Характерными признаками черных металлов являются темно-серый цвет, блеск, высокие плотность и температура плавления, твердость, прочность, вязкость и полиморфизм (аллотропия). По физикохимическим свойствам черные металлы подразделяют на пять групп:
- железистые (железо, кобальт, никель, марганец);
- тугоплавкие (вольфрам, рений, тантал, молибден, ниобий, ванадий, хром, титан и др.);
- урановые — актиниды (уран, торий, плутоний и др.);
- редкоземельные — лантаниды (лантан, церий, иттрий, скандий и др.);
- щелочно-земельные (литий, натрий, калий, кальций и др.).
Из этих пяти групп черных металлов особенно широкое применение в промышленном производстве находят железистые и тугоплавкие металлы.
Железистые металлы, кроме марганца, называют еще ферромагнетиками. Ферромагнетики способны намагничиваться и притягивать металлы своей группы.
К тугоплавким относятся металлы, которые имеют температуру плавления выше температуры плавления железа (1 539 °С): титан — 1 667 °С, ванадий — 1 902 °С, хром — 1 903 °С, молибден — 2 615 °С, ниобий — 2 460 °С, тантал — 2 980 °С, вольфрам — 3 410 °С. Тугоплавкие металлы в основном применяются как легирующие элементы в производстве жаропрочных, жаростойких, теплостойких и специальных сплавов, в том числе твердых сплавов и высоколегированных сталей.
2. Строение металлов
Атомно-кристаллическая структура металлов. Как известно, все вещества состоят из атомов, в том числе и металлы. Каждый металл (химический элемент) может находиться в газообразном, жидком или твердом агрегатных состояниях. Каждое агрегатное состояние будет иметь свои особенности, отличные друг от друга. В газообразном металле расстояние между атомами велико, силы взаимодействия малы и атомы хаотично перемещаются в пространстве; газ стремится к расширению в сторону большего объема. При понижении температуры и давления вещество переходит в жидкое состояние. Свойства жидкого вещества резко отличаются от свойств газообразного. В жидком металле атомы сохраняют лишь так называемый ближний порядок атомов, т. е. в объеме расположено небольшое количество атомов, а не атомы всего объема. При понижении температуры жидкий металл переходит в твердое состояние, которое имеет строгую закономерность расположения атомов.
Если условно провести вертикальные и горизонтальные линии связи через центры атомов, можно увидеть, что у металлов в твердом состоянии атомы расположены в строго определенном порядке и представляют собой множество раз повторяющиеся элементарные геометрические фигуры — параллелепипеды (рис. 1). Наименьшую геометрическую фигуру называют элементарной ячейкой. Элементарные ячейки, расположенные на горизонтальных и вертикальных кристаллографических плоскостях (рис. 2), образуют пространственную кристаллическую решетку.
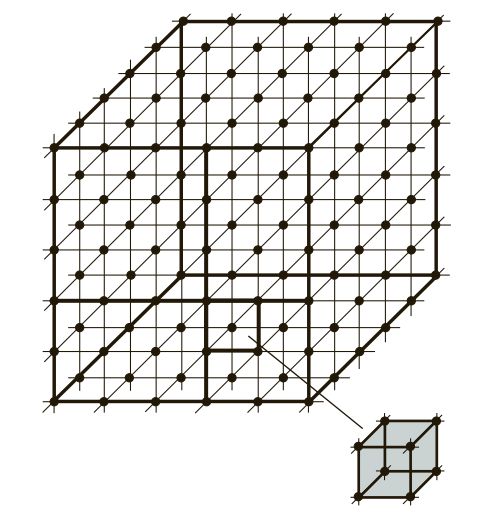
Рис. 1. Схема расположения элементарных геометрических ячеек в атомных решетках металлов и сплавов
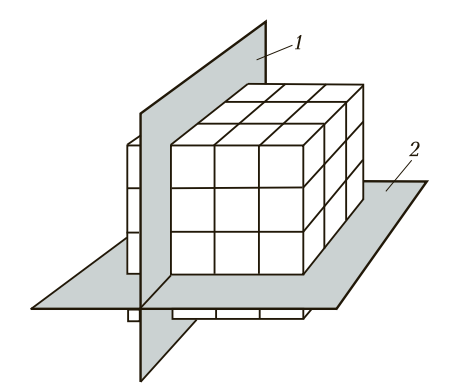
Рис. 2. Расположение кристаллографических плоскостей: 1 и 2 — соответственно горизонтальная и вертикальная кристаллографические плоскости
Элементарные кристаллические решетки характеризуют следующие основные параметры: расстояние между атомами по осям координат (по линиям связи), углы между линиями связи, координационное число — число атомов, находящихся на наиболее близком и равном расстоянии от любого атома в решетке. Форму элементарной ячейки рассматривают по кристаллографическим плоскостям в трех измерениях.
Таким образом, любой металл можно представить не как однородную цельную массу, а как массу, сложенную из множества элементарных ячеек. Блок элементарных атомных кристаллических ячеек образует атомно-кристаллическую ячейку (решетку). Если выделить эту элементарную ячейку, то в зависимости от металла получим следующие типы кристаллических ячеек (рис. 3): куб (К), объемно-центрированный куб (ОЦК), гранецентрированный куб (ГЦК), гексагональная плотноупакованная ячейка (ГПУ), гексагональная простая ячейка (Г) и др.
Простая кубическая ячейка (рис. 3, а) характерна для неметаллов, которые обладают наибольшими плотностью и удельным весом, и имеет восемь атомов, которые расположены в каждой вершине куба.
Объемно-центрированная кубическая ячейка (рис. 3, б ) состоит из восьми атомов, которые расположены по одному атому в каждой вершине куба, и одного, находящегося в центре куба на равных расстояниях от его граней. Эту форму атомной кристаллической ячейки имеют железо модификации Fe-α, ванадий, вольфрам, молибден, тантал и хром, т. е. в основном черные металлы.
Гранецентрированная кубическая ячейка (рис. 3, в) имеет 14 атомов — по одному атому в каждой вершине куба (восемь атомов) и по одному атому в центре каждой грани (шесть атомов). Гранецентрированную кубическую ячейку имеют алюминий, железо модификации Fe-γ, золото, кобальт, медь, никель, платина и серебро, в основном это цветные металлы и часть черных металлов.
Гексагональная плотноупакованная ячейка (рис. 3, г) состоит из 17 атомов. Форма геометрического тела, которую образуют эти атомы, является шестигранной призмой. При этом по шесть атомов расположены в каждой вершине верхнего и нижнего оснований, по одному атому в центре этих оснований и три атома в центре одной их трех граней (через грань). Гексагональную плотноупакованную ячейку имеют бериллий, кадмий, магний, ванадий, тантал.
Простая гексагональная ячейка (рис. 3, д) состоит из 12 атомов, которые расположены в вершинах верхнего и нижнего оснований шестигранной призмы. Такую кристаллическую ячейку имеют ртуть и цинк.
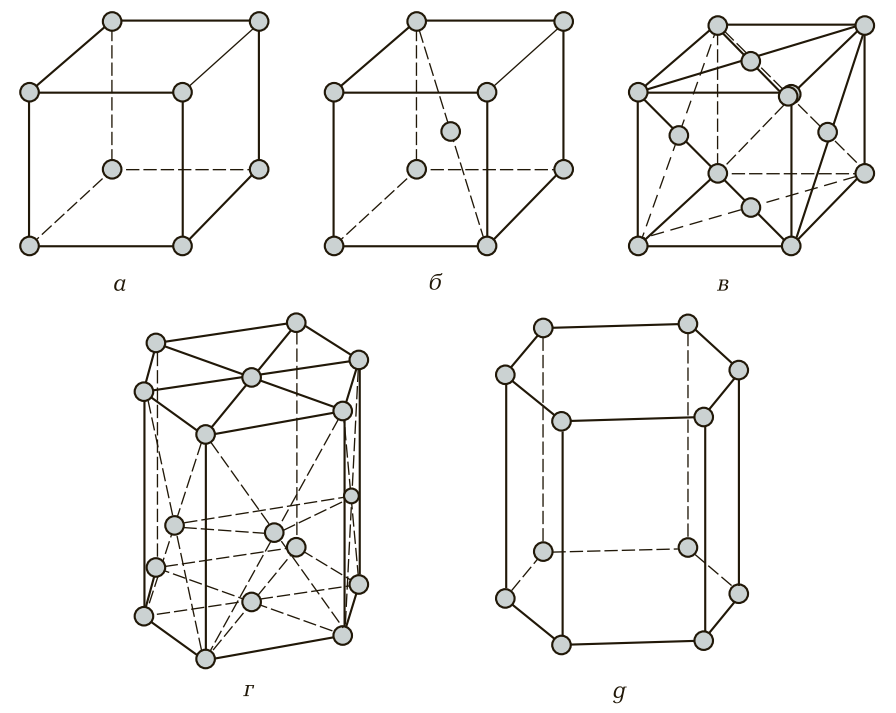
Рис. 3. Геометрические формы элементарных кристаллических ячеек: а — куб; б — объемно-центрированный куб; в — гранецентрированный куб; г — гексагональная плотноупакованная ячейка; д — гексагональная простая ячейка
Связь между атомами в кристаллической решетке и между решетками осуществляется за счет так называемой металлической связи. От прочности этой связи зависят прочность и твердость металлов. Чем выше эта связь, тем бо´льшую прочность и твердость имеют металлы. Механизм связи между атомами в решетке и между решетками имеет сложную физико-химическую природу.
В практике идеальное расположение кристаллических решеток обычно не наблюдается. Кристаллы, образуемые кристаллическими решетками, имеют искаженную геометрическую форму и различную величину.
Анизотропия металлов. Анизотропия (от гр. anisos — неравный и tropos — направление) — неодинаковость физических свойств среды (тела) в различных направлениях. Анизотропия предполагает зависимость свойств металлов от направления по плоскостям атомно-кристаллических решеток. Чем больше в плоскости атомов, тем выше свойства металлов. В горизонтальных плоскостях в любой форме атомно-кристаллических решеток больше, чем в вертикальных плоскостях. Следовательно, прочность металлов, испытанная в горизонтальном направлении, выше, чем в вертикальном. Анизотропия проявляется в процессе обработки конструкционных материалов давлением (проката, волочения, штамповки и других технологических способов получения заготовок и изделий).
На рис. 2 кристаллографические плоскости совпадают с линиями связи, проходящими через атомы металла. Форма элементарной кристаллической ячейки, расстояние между атомами и прочность металлической связи определяют физические, механические и технологические свойства металлов. Если исследуемый металл рассматривать по трем кристаллографическими плоскостям, по линиям связи между атомами, то можно заметить, что свойства по этим трем измерениям будут различны. Число атомов в этих плоскостях неодинаково. Металлическая связь между горизонтально и вертикально расположенными атомами также неодинакова. Это, в свою очередь, приводит к различной прочности металлов в продольном и поперечном направлениях. Например, предел прочности меди в продольном направлении будет в 2 раза больше, чем в поперечном.
Все металлы анизотропны, так как они состоят из кристаллов. Кристаллическое строение металлов обусловливает пластическую деформацию, т. е. изменение внешней формы и размеров под действием нагрузок без разрушения. Способность металлов и сплавов пластически деформироваться положена в основу их обработки давлением (прокатка, волочение, ковка, штамповка и прессование). При обработке давлением, например прокатке (рис. 4, а), происходит перемещение одного слоя атомных решеток по другому по кристаллографическим плоскостям (рис. 4, б).
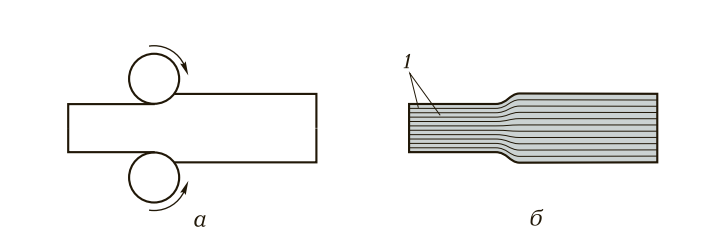
Рис. 4. Схема деформации металлов и сплавов (прокатка): а — деформация; б — скольжение металлов по кристаллографическим плоскостям в процессе деформации; 1 — кристаллографические плоскости
В процессе деформации металла при прокатке происходит не только изменение поперечных и продольных размеров заготовок, но и изменение микроструктуры металла.
Зерна под действием давления прокатных валков искажаются, приобретая продолговатую или пластинчатую форму, а затем преобразуются в волокна. Изменение микроструктуры металла в процессе деформации условно показано на рис. 5.
Процесс кристаллизации. Рассмотрим, как происходит образование кристаллов у чистых металлов. Установлено, что процесс кристаллизации металлов из жидкого состояния в твердое идет в две стадии:
- образование центров кристаллизации;
- рост кристаллов вокруг этих центров (рис. 6).
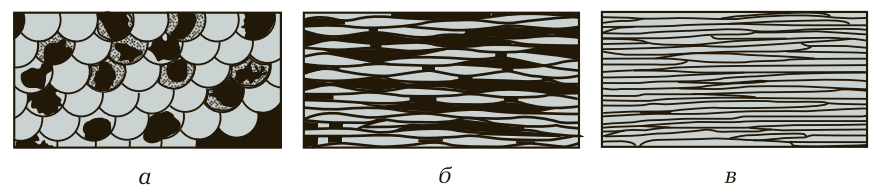
Рис. 5. Изменение микроструктуры металла в процессе деформации: а — микроструктура металла до деформации; б — микроструктура металла после первой операции деформации; в — микроструктура металла после окончательной деформации
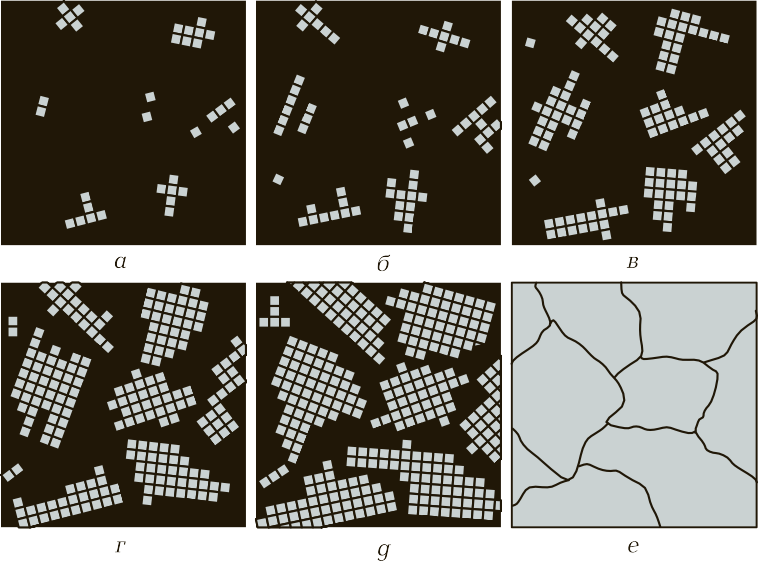
Рис. 6. Процесс кристаллизации металлов и сплавов: а — е — последовательные этапы процесса
Далее вновь появляются новые центры, и происходит рост твердой фазы вокруг первичных и вторичных центров. Процесс происходит до того момента, пока образованные таким образом кристаллы не будут соприкасаться друг с другом и не будет наличия жидкой фазы металла (см. рис. 6, г — е). Когда образование кристалла идет в жидкой фазе (в расплавленном металле), он будет иметь правильную форму, т. е. состоять из определенных геометрических фигур правильной формы. Когда кристаллы начинают соприкасаться друг с другом, а процесс затвердевания еще не закончен, тогда происходят искажения формы зерен. В практике замечено, что когда идет быстрое охлаждение, образуются мелкие зерна — мелкозернистая структура. При медленном охлаждении появление новых центров кристаллизации замедляется, но происходит рост зерна вокруг первичных центров кристаллизации. В этом случае металл будет иметь крупнозернистую структуру.
Процесс образования кристаллов в жидком состоянии и перехода металла в твердое состояние называется первичной кристаллизацией. Величина и форма зерна влияет на механические свойства металлов. Чем зерна мельче и чем правильнее их форма, тем большую твердость и прочность будет иметь металл. Чем зерна больше и чем искаженнее их форма, тем ниже твердость и прочность металла.
Аллотропия металлов. Такие металлы, как железо, кобальт, никель и др., обладают способностью изменять кристаллическую решетку при нагревании в твердом состоянии. Процесс изменения кристаллических решеток в твердом состоянии называется вторичной кристаллизацией, или аллотропией, а состояние вещества (металла) при наличии нескольких кристаллических решеток при изменении параметров (давления, температуры) — аллотропическими модификациями, или полиморфизмом. Такие металлы, как железо, молибден, вольфрам, литий в твердом состоянии при нормальной температуре имеют объемно-центрированную кубическую ячейку; алюминий, медь, серебро в твердом состоянии при нормальной температуре имеют форму гранецентрированной кубической ячейки.
На рис. 7 представлены кривые нагрева и охлаждения металла (на примере марганца). Аллотропные состояния (модификации), имеющие те или иные кубические ячейки, обозначаются греческими буквами. Первоначальное аллотропное состояние при нормальной температуре обозначается буквой α, при дальнейших повышении температуры и перекристаллизации металла — буквами β, γ, δ и т. д. При охлаждении металлов и сплавов процесс аллотропного превращения происходит в обратном порядке, как правило при тех же температурах.
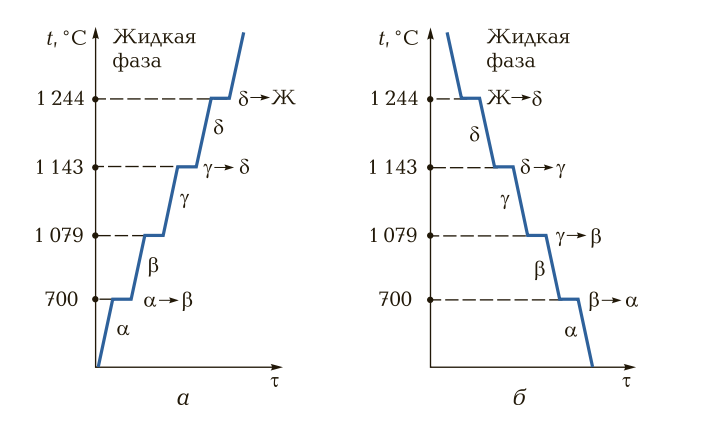
Рис. 7. Кривые нагрева (а) и охлаждения (б) марганца: t — температура; τ — время
Кристаллическое строение металлов

Металлы – особая группа элементов в периодической таблице Менделеева. В отличие от неметаллов элементы этой группы являются исключительно восстановителями с положительной степенью окисления, а также обладают пластичностью, твёрдостью, упругостью, что обусловлено кристаллическим строением металлов.
Общее строение
Металлы – твёрдые вещества, имеющие кристаллическое строение. Исключение составляет ртуть – жидкий металл. Кристаллические решётки представляют собой упорядоченные определённым образом атомы металла. Каждый атом состоит из положительно заряженного ядра и нескольких отрицательно заряженных электронов. В атомах металлов недостаточно электронов, поэтому они являются ионами.
Единица кристаллической решётки – элементарная кристаллическая ячейка, в условных узлах и на гранях которой находятся положительно заряженные ионы. Их удерживают вместе металлические связи, возникающие за счёт беспорядочного движения отделившихся от атомов электронов (благодаря чему атомы превратились в ионы).
Отрицательно заряженные электроны держат на равном расстоянии положительно заряженные электроны, предавая кристаллической решётке правильную геометрическую форму.
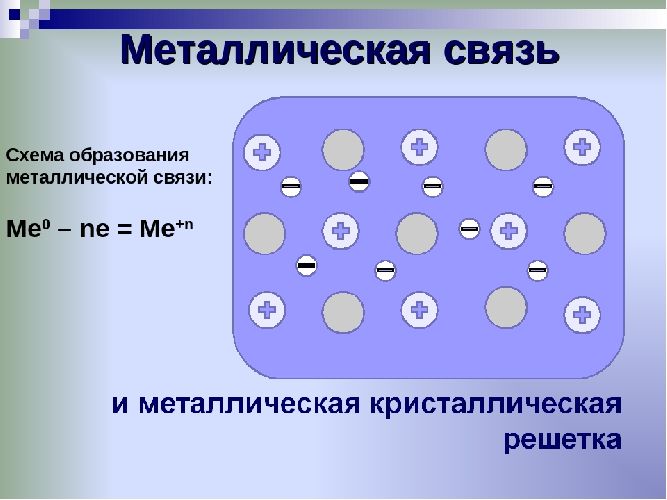
Рис. 1. Схема металлической связи.
Свободное движение электронов обусловливает электро- и теплопроводность металлов.
Виды решёток
Элементарные кристаллические ячейки могут иметь различную конфигурацию. В связи с этим выделяют три типа кристаллических решёток:
- объемно-центрированная (ОЦК) кубическая – состоит из 9 ионов;
- гранецентрированная (ГЦК) кубическая – включает 14 ионов;
- гексагональная плотноупакованная (ГПУ) – состоит из 17 ионов.
ОЦК представляет собой куб, в узлах которого находится по атому. В центре куба, на пересечении диагоналей располагается девятый ион. Этот тип характерен для железа, молибдена, хрома, вольфрама, ванадия.
Элементарной кристаллической ячейкой типа ГЦК является куб с ионами в узлах и в середине каждой грани – на пересечении диагоналей. Такое строение имеют медь, серебро, алюминий, свинец, никель.
Третий тип имеет вид гексагональной призмы, в узлах которой находится по шесть ионов с каждой стороны. Посередине между шестью узлами располагается по одному иону. В середине призмы между шестиугольными гранями находится равносторонний треугольник, который составляют три иона.
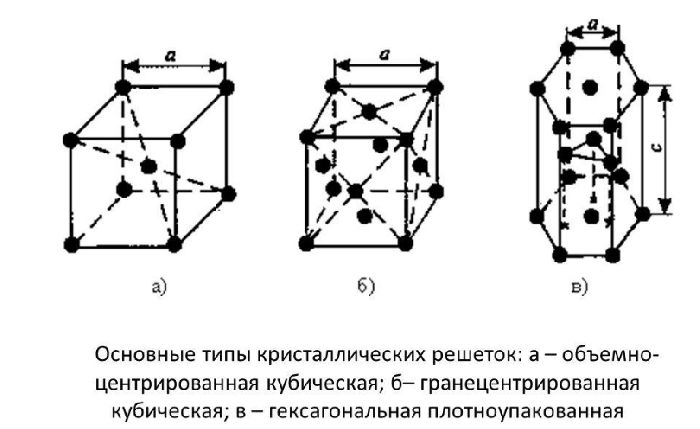
Рис. 2. Типы решёток.
Металл может содержать большое количество дефектов атомного строения. Дефекты влияют на свойства металла.
Характеристика решётки
Кристаллические решётки характеризуются компактностью или степенью наполненности. Компактность определяют показатели:
- параметр решётки – расстояние между атомами;
- число атомов;
- координационное число – количество соседних ячеек;
- плотность упаковки – отношение объёма, занимаемого атомами, к полному объёму решётки.
При подсчёте количества атомов следует помнить, что атомы в узлах и на гранях входят в состав соседних ячеек.
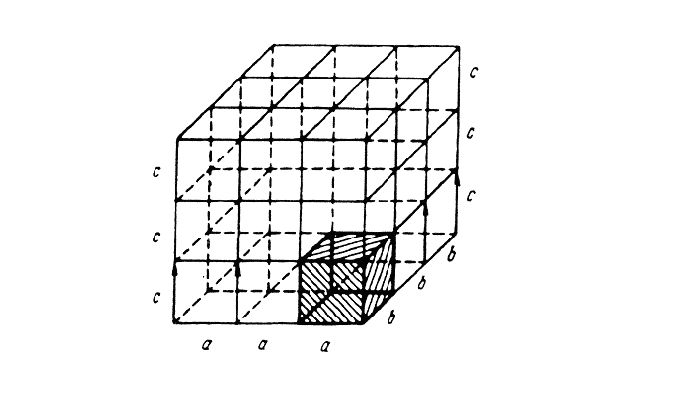
Рис. 3. Кристаллические ячейки составляют решётку.
Что мы узнали?
Узнали кратко об атомно-кристаллическом строении металлов. Металлы – твёрдые кристаллические вещества. Единицей решётки является элементарная кристаллическая ячейка. Благодаря металлическим связям ионы в узлах ячеек удерживаются на одинаковом расстоянии. Различают три типа кристаллических решёток – ОЦК, ГЦК и ГПУ, отличающихся количеством атомов и геометрической формой.
Металлы

К металлам относится большая часть элементов периодической системы – 82 химических элементов. Какими свойствами они обладают, и чем отличаются от неметаллов?
Общая характеристика
Металлами называют группу элементов, в виде простых веществ, которые обладают металлическими свойствами (пластичность, ковкость, блеск, электронная проводимость и т. д.)
Основное отличие элементов-металлов – они обладают только восстановительными свойствами, а в реакциях могут только окисляться. В соединениях они могут иметь только положительные степени окисления как в элементарных положительно заряженных ионах, так и в сложных ионах, где они образуют положительные центры.
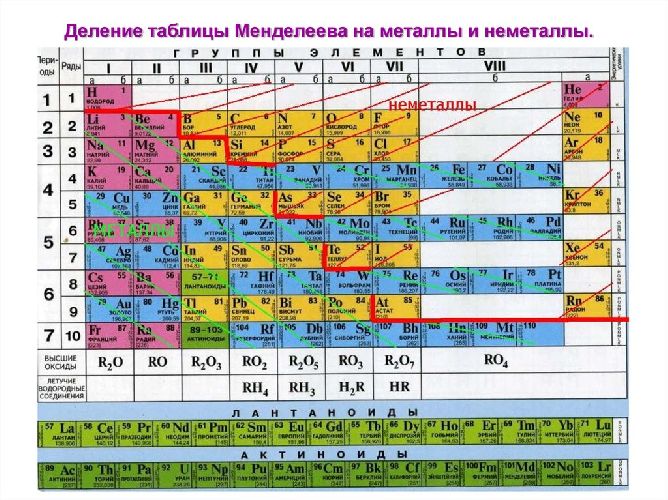
Рис. 1. Список металлов.
Как правило, на внешнем уровне элементов металлов находится небольшое число электронов (1-3), значения электроотрицательности невысокие. К металлам относятся все s-элементы (кроме водорода и гелия), d- и f-элементы, а также p-элементы под чертой бор-астат. Для типичных металлов характерен большой размер атомов, что способствует легкости отдачи валентных электронов. Образующиеся положительные ионы устойчивы, так как имеют завершенную внешнюю электронную оболочку.
Физические и химические свойства
Все металлы, кроме ртути, при нормальных условиях в виде простых веществ находятся в твердом агрегатном состоянии и образуют металлическую кристаллическую решетку.

Рис. 2. Металлы в таблице Д.И. Менделеева.
Таблица «Металлы»
В следующей таблицы представлены группы основных металлов:
| Группа металлов | Металл |
| Щелочные | литий, натрий, калий и т.д. |
| Щелочноземельные | кальций, стронций, барий и т.д. |
| Переходные | уран, титан, железо, платина и т.д. |
| постпереходные | алюминий, свинец, олово и т.д. |
| Тугоплавкие | молибден, вольфрам |
| Цветные | медь, титан, магний и т.д. |
| Благородные | золото, серебро и т.д. |
Металлы пластичны и ковки, особенно если на внешнем электронном уровне атомов по одному электрону: слои атомов перемещаются относительно друг друга без разрушения кристаллической решетки (щелочные металлы, медь, серебро, золото). В атомах непластичных хрупких металлов хрома и марганца – большое число валентных электронов.
Плотность, твердость, температура плавления металлов изменяются в широком диапазоне и зависят от атомной массы, строения атома и геометрии кристаллической решетки. Самый легкий металл – литий (плотность 0,53 г/см 3 ), самый тяжелый – осмий (плотность 22,5 г/см 3 ). Металлы с плотностью больше 5 г/см 3 относят к тяжелым, меньше 5 г/см 3 – к легким металлам.
Самая низкая температура плавления у ртути (-39 градусов по Цельсию), самый тугоплавкий металл – вольфрам (температура плавления 3410 градусов по Цельсию.) Энергия атомизации вольфрама составляет 836 кДж/моль, а температура кипения его 5930 градусов.
Металлы вступают в реакцию как с простыми, так и со сложными веществами. Как типичные восстановители металлы реагируют почти со всеми неметаллами-окислителями (кислород, сера, азот и т. д.):
Также металлы реагируют с такими сложными веществами, как оксиды и гидроксиды, разбавленные растворы кислот, с растворенными в воде щелочами.
В пределах одного и того же периода металлические свойства ослабевают, а неметаллические усиливаются; в пределах одной и той же группы (в главной подгруппе) металлические свойства усиливаются, а неметаллические ослабевают

Рис. 3. Металлы главных подгрупп.
Нахождение металлов и способы их получения
Самый распространенный на земле элемент-металл – алюминий. За ним следуют железо, кальций, натрий.
Некоторые металлы встречаются в природе в самородном состоянии (золото, ртуть, платина), но в основном они находятся в природе в виде оксидов и солей.
Получение металлов происходит с помощью металлургии (получение из руд), пирометаллургии (получение с помощью реакции восстановления при высокой температуре), гидрометаллургии (извлечение из руд в виде растворимых соединений), электрометаллургии (получение металлов электролизом расплавов и растворов их соединений).
Металлы – вещества, которые обладают высокой электро- и теплопроводностью, ковкостью, пластичностью и металлическим блеском. В данной статье по химии 9 класса рассматриваются их физические и химические свойства, формулы класса металлов, а также способы получения.
Строение металлов
Все металлы состоят из огромного количества кристаллических зерен, которые соединяются между собой. Такое зернистое кристаллическое строение вещества можно увидеть, применяя специальные микроскопы, получившие название металлографических. Они отличаются от обычных тем, что здесь применяется боковое освещение металла, потому что металлы непрозрачны и их невозможно освещать снизу. В таких микроскопах источник света располагается так, чтобы часть лучей отражалась от поверхности металлов и попадала в объектив.

Рис. 1. Металломикроскоп.
Справа сверху — лучи света, отраженные от поверхности шлифа, идут в объектив микроскопа. Справа внизу — поверхность чистого железа, видимая с помощью металломикроскопа.
На рисунке 1 представлен один из таких микроскопов. Прежде чем рассматривать в нем образец, поверхность металла тщательно очищают наждачной бумагой, шлифуют и полируют до зеркального блеска. Такой образец называют шлифом. Затем поверхность шлифа подвергают так называемому травлению, для чего он смачивается в течение 2—3 мин раствором, чаще всего содержащим азотную кислоту и этиловый спирт. Применяют и другие растворы для травления шлифов. Делают это вот для чего: различные зерна сплава неодинаково растворяются кислотой, вследствие чего на поверхности металла выступают отдельные грани кристаллов, и когда протравленную часть шлифа освещают, то часть зерен отражает падающий на них свет прямо на объектив. Эти места под микроскопом кажутся светлыми. Другие зерна отражают свет в сторону, поэтому кажутся темными. Другой оттенок и даже окраску приобретают под микроскопом места сцепления отдельных кристаллических зерен, так называемые межкристаллитные участки (рис. 2).
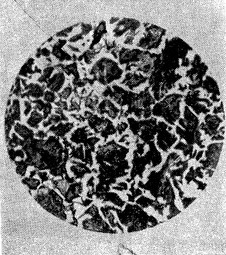
Рис. 2. Шлифованная пластинка под микроскопом (травление стали 2-процентным спиртовым раствором азотной кислоты).
Применение металломикроскопа дало возможность установить, какое строение имеют металлы, как расположены в сплаве отдельные зерна, какие неметаллические включения содержат сплавы, отражение трещин на поверхности сплавов и т. д. На рисунке 3 приведена микрофотография чугуна, где ясно видны отдельные включения графита.

/>
Рис. 3. Графит в чугуне (темные включения):
а-крупнопластинчатый графит в обычном сером чугуне; б-мелкопластинчатый графит в модифицированном сером чугуне (модификация 0.15%); в-шаровидные графитовые включения в чугуне, модифицированном магнием (×100).
Металломикроскоп в настоящее время является одним из приборов любой лаборатории, где изучают свойства различных металлов и сплавов.
Кристаллическая решетка металлов
С кристаллами вы уже знакомы. Так, например, изучая поваренную соль, вы знаете, что она состоит из 8 отдельных кристаллов кубической формы. Само слово «кристалл» происходит от греческого слова «кристаллос», означающее «лед». В будущем так стали называть все твердые тела, которые имеют определенную геометрическую форму. В природе подавляющее большинство твердых тел находится в кристаллическом состоянии. Железо как одно из твердых тел при застывании также образует кристаллы. Кристалл железа имеет кубическую решетку. Однако, рассматривая под микроскопом поверхность металла, мы не увидим этой правильной кубической формы кристаллов. Неправильная форма кристаллов возникает потому, что в расплаве при его затвердевании возникает много мельчайших зародышей, которые образуют более крупные кристаллы. Эти крупные кристаллы, сталкиваясь, начинают теснить, сдавливать друг друга. Следовательно, в затвердевающем слитке металла одновременно находится огромное количество кристаллов. Нарушению их формы способствует не только то, что они теснят друг друга, но также неодинаковая температура в различных местах остывания. Отдельные кристаллические зерна в застывшем металле имеют различную форму и величину. Они отделены друг от друга прослойкой, которая состоит из различных неметаллических включений. Эти неметаллические включения всегда присутствуют в том или другом количестве в металле.
На рисунке 4 представлена схема образования зернистой структуры металла при его застывании.

Рис. 4. Схема роста кристаллов в застывающем расплаве:
а-образуются зародыши; б-растут кристаллы; в-кристаллы начинают теснить друг друга; г-отдельные зерна сращиваются.
Вещества, входящие в состав стали, имеют различную температуру плавления, а, следовательно, и затвердевания. Например, чистое железо становится твердым уже при температуре 1539° С, а в соединении с серой или другими элементами температура затвердевания более низкая. Поэтому слой металла, затвердевающий в первую очередь, состоит из наиболее тугоплавких элементов, например, железа и углерода. Такие примеси, как сера и фосфор, дают более легкоплавкие сплавы и затвердевают в последнюю очередь. Сера и фосфор — вредные примеси потому что их присутствие значительно уменьшает прочность сплава, делает его хрупким и малопригодным для изделий.
При затвердевании сплава более легкоплавкие соединения железа с серой и фосфором концентрируются в верхней части слитка и застывают в последнюю очередь, поэтому сплав железа с фосфором и серой собирается в верхней части слитка.
В кристаллах атомы каждого металла распределяются в строго определенном порядке. Они образуют так называемую пространственную решетку, которую нельзя увидеть ни в один из существующих микроскопов. Однако с помощью рентгеновских установок и других современных приборов можно изучить расположение атомов в кристаллической решетке.
Типы кристаллических решеток металлов
Среди металлов чаще всего встречаются три типа решеток, к первым из них относятся кубические объемноцентрированные. Они характерны тем, что атомы в них находятся в вершинах и центре куба например у лития, хрома, ванадия и других металлов (рис. 5,а).
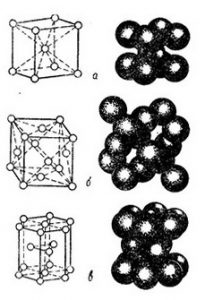
Рис.5. Типы кристаллических решеток металла:
в-гексагональная (плотная упаковка).
Ко второму типу относят решетку кубическую гранецентрированную (рис. 5,6), атомы в (которой расположены в вершинах куба и его гранях (например, у алюминия, меди, свинца, никеля, золота, серебра и платины).
Третий тип — это гексагональные, или шестиугольные, плотно упакованные решетки (рис.5,в). Они встречаются у магния, цинка, кадмия и бериллия.
Как видно из схемы, приведенной на рисунке 6, наиболее плотные упаковки атомов имеют гранецентрированные и гексагональные решетки.
Рис.6. Схема строения металла.
В узлах решетки положительно заряженные ионы. В промежутка находятся свободные электроны.
Интересно отметить, что некоторые металлы, в частности железо, цинк и никель, могут существовать в нескольких кристаллических формах, переходя из одной в другую. Этот переход совершается при различных температурах. Такие видоизменения, когда одно и то вещество может находиться в различных кристаллических формах, называются аллотропическими, а сами вещества аллотропными. Название «аллотропия» происходит от греческих слов «аллос»—другой, «тропос»—свойство.
Углерод может встречаться в природе в виде графита и алмаза, причем, как вы помните, графит является мягким веществом, оставляющим след на бумаге, в то время как алмаз один из наиболее твердых природных веществ. Температуры плавления алмаза и графита различны.
Известно аллотропическое видоизменение серы (ромбическая и призматическая). Ромбическая сера образуется при температуре ниже 96° С, выше этой температуры она переходит в призматическую. В зависимости от изменения кристаллического строения изменяются и свойства вещества.
Такие же аллотропические изменения наблюдают и у железа. Оно имеет решетку центрированного куба то температуры 910° С, а в интервале температур 910—1390° С совершается переход в гранецентрированную.
Аллотропические превращения металла легко наблюдать на примере олова. Обычное серебристо-белое олово имеет сложную кристаллическую решетку, которая устойчива при температуре выше 18° С, при более низкой температуре атомы олова в кристаллах начинают перестраиваться. Упаковка их (атомов) становится менее прочной, блестящее олово теряет блеск, ковкость и превращается в хрупкое серое олово, имеющее другую кристаллическую решетку.
Это явление было давно замечено и получило название «оловянной чумы», так как оловянные изделия — тарелки из олова, кубки, органы в церкви — иногда вдруг начинали разрушаться. «Оловянная чума» была большим бедствием. Как бороться с ней, не знали, потому что не знали причины ее происхождения. Сейчас нам ясно, что если нагревать изделие из олова, «заболевшее оловянной чумой», то кристаллы серого олова будут перестраиваться в кристаллы белого олова, и оно вновь приобретает ковкость и белый цвет.
Строение металлов
На схемах кристаллов (рис. 5) условно в кристаллической решетке проведены линии, соединяющие один атом металла с другим. В действительности никаких линий, соединяющих атомы, в узлах решетки нет. Они уложены плотно, соприкасаясь друг с другом. В узлах решетки находятся положительно заряженные ионы, окруженные электронами. Валентные электроны атомов металлов так же, как и сами атомы, находятся в беспрерывном колебании. Но внешне электроны (валентные) могут легче покинуть свой атом и перейти к соседнему. Следовательно, в кристаллической решетке имеются так называемые свободные электроны, или свободный электронный «газ», присущий всему комплексу атомов. Таким образом, возникает взаимодействие электронов внешних оболочек атомов металла. Благодаря этому внешнему взаимодействию электронов создается связь между атомами металла, возникают силы сцепления, прочно удерживающие атомы металла в кристаллической решетке (рис. 6). Ионы атомов металлов в кристаллической решетке, окруженные подвижными (незакрепленными) электронами, получили название ион-атомов, в отличие от обычных ионов.
То, что мы говорили о кристаллической решетке металлов, относится к чистым металлам, но мы знаем, что в практике применяют преимущественно сплавы.
Читайте также:
