Определение газов в металле
Обновлено: 19.09.2024
Ниже представлена схема классификации газовых включений и существования газов в стали. Графа схемы «газы в стали» включают в себя: 1 — твердые растворы кислорода, азота и водорода в железе; 2 — химические соединения кислорода и азота, т. е. окислы и нитриды железа и других элементов, присутствующих в стали, и 3 — механические газообразные включения в микропорах и газовых пузырях как в форме элементарных газов водорода и азота, так и в виде соединений газов. Таким образом, газы могут находиться как в металлической субстанции в виде твердых растворов, так и в неметаллических включениях.
Для определения кислорода в цеховых лабораториях применяется метод Герти, сущность которого состоит в определении количества окиси алюминия в металле, раскисленном избытком алюминия (до,1%), предварительно введенного в пробу жидкого металла.
Азот в заводских лабораториях чаще всего определяется по методу Ледебура-Чижевского, который основан на том, что при растворении стали в кислотах связанный азот переходит в аммонийную соль. При нагревании со щелочью аммонийная соль разлагается, и отгоняющийся аммиак поглощается в приемнике определенным объемом титрованной серной кислоты. Количество поглощенного аммиака далее может быть определено или путем обратного титрования, или колометрически с реактивом Несслера. В литературе имеются указания также о кондуктометрическом методе. Азот, связанный в виде нитридов, нерастворимых в кислотах, не может быть определен этим методом, если нитридный остаток не подвергать дополнительной обработке. Этим методом не определяется также свободный азот, заключенный в микропорах металла.
Отбор проб стали на водород по ходу плавки существенно отличается от обычного отбора проб, предназначенных для анализа на другие элементы. Благодаря особой способности водорода к диффузии даже при комнатной температуре возможны потери водорода как в процессе отбора пробы, так и в период хранения ее перед анализом. Общее количество водорода в образце с течением времени уменьшается. Вместе с этим происходит перераспределение водорода между фазами. Количество водорода в твердом растворе железа уменьшается за счет его удаления в окружающее пространство и в полости внутри металла, количество же водорода в микропорах и газовых пузырях благодаря этому постепенно увеличивается.
Весьма существенным является отбор проб таким способом, чтобы зафиксировать в металле весь содержащийся водород в данный момент, а в дальнейшем сохранить пробу без потерь водорода или учесть выделившееся количество его в процессе хранения. Резкое охлаждение металла фиксирует большую часть водорода, так что закаленная проба довольно близка по содержанию водорода к исходному жидкому металлу. Для получения пробы с чистой поверхностью и такого размера, чтобы можно было воспользоваться ею для определения водорода без дополнительной механической обработки, рекомендуется отбирать пробу в кварцевую пипетку ф 6 мм и немедленно закаливать ее в холодной воде. Закаленную пробу следует хранить в сосуде с твердой углекислотой и ацетоном или в жидком азоте. В практике заводских лабораторий отобранную на водород пробу хранят под слоем жидкости в специальных приборах. Выделяющийся в микробюретку водород следует учитывать. В качестве инертной жидкости применяется глицерин.

Водород в настоящее время часто определяется методом нагрева образца в вакууме. Иногда образец нагревают в вакуумированном замкнутом объеме и о количестве выделившегося водорода судят по изменению давления, измеряемого обычным U-образным ртутным манометром. Однако этот метод не может считаться безупречным. С одной стороны, отсчет по ртутному манометру слишком груб, с другой стороны, возникает целый ряд побочных обстоятельств, искажающих результаты анализа. Сюда относятся, в первую очередь, мешающее влияние металлических возгонов, а также возможность неполноты выделения водорода из-за установившегося состояния равновесия между водородом в газообразной и твердой фазах.
В ЦНИИТМАШе разработан прибор для определения водорода в стали методом нагрева образца в высоком вакууме с последующим удалением выделившегося водорода из нагреваемого пространства с помощью ртутного диффузионного насоса и измерением количества газа в калиброванном: объеме по изменению давления, измеряемого наклонным дифференциальным манометром, заполненным дибутилфталатом, упругость пара которого имеет величину того же порядка, что и упругость пара ртути. На рис. 1 представлена схема установки системы ЦНИИТМАШ для определения водорода методом нагрева в высоком вакууме. В отличие от приборов подобного типа установка ЦНИИТМАШ практически не содержит ртути и может работать не требуя чистки. Температура нагрева образца зависит от структурного состояния стали. На основании данных об изменении коэффициента диффузии водорода через а- и у- железо в зависимости от температуры, рекомендуется простые стали анализировать при 650°, а аустенитные при 850°С и выше.


где v — объем выделившегося водорода; T — температура, при которой происходило измерение; l — изменение уровня дибутилфталата на шкале манометра; К — постоянная прибора, которая, в свою очередь, определяется по уравнению:

где v1 — объем градуировочного крана, см3-, P1 и T1— атмосферное давление и температура, при которых градуировали прибор; р0 = 760 мм рт. ст.; l1— смещение уровня жидкости в манометре при одном повороте градуировочного крана.
В табл. 1 приведены данные по определению водорода (сж3/100 г) в различных материалах описанным методом.
Метод вакуумного нагрева имеет ряд недостатков: 1) сорта сталей, которые могут исследоваться этим методом, ограничены, так как определению мешает углерод, марганец и ряд других элементов; 2) выделяющиеся при экстракции газы не представляют чистого водорода, и в зависимости от состава металла могут содержать его от 80 до 95%.
Универсальным методом, позволяющим определить все три газа из одной пробы одновременно, является метод горячей экстракции, или, как его теперь называют, метод плавки в высоком вакууме.

Сущность метода состоит в том, что проба исследуемого металла плавится в графитовом тигле в вакууме порядка 10в-3—10в-4 мм рт. ст. при температуре 1600—1700°. Содержащиеся в металле окислы при этом восстанавливаются углеродом тигля, и кислород переходит в газообразную фазу в виде окиси углерода. Присутствующие в стали нитриды разлагаются, выделяя элементарный азот, одновременно при этом из металла переходит в газообразную фазу также и водород, содержащийся в пробе. Полученная смесь газов CO, N2, Н2 откачивается системой насосов и анализируется. В качестве плавочного устройства, как уже указывалось выше, может служить индукционная печь высокой частоты или графитовая печь сопротивления.
Газы из печи во всех современных установках откачиваются ртутным диффузионным насосом.
Анализ газовой смеси может производиться различными способами: масс-спектральным, спектральным, химическим по изменению давления в калиброванном объеме. Эти методы не требуют перевода газовой смеси от состояния вакуума к атмосферному давлению.
Газовая смесь может быть также собрана при атмосферном давлении с помощью коллекторных насосов (например, капельного), различных модификаций насоса Теплера или диафрагменного насоса Файхтингера и проанализирована при атмосферном давлении. В этом случае используется обычный газоанализатор или микрогазоанализатор. В последнее время для этой же цели нашел применение метод газовой хроматографии, с использованием в качестве газа носителя аргона или двуокиси углерода.
Для заводских лабораторий наиболее разработанными методами анализа газовых смесей являются метод изменения объема при постоянном атмосферном давлении или же изменения давления в калиброванном объеме. В качестве плавочного устройства более простыми и доступными для заводских лабораторий являются вакуумные печи с графитовым сопротивлением.

На рис. 2 представлена схема установки системы ЦНИИТМАШ для определения газов в стали. Установка состоит из вакуумной печи с графитовым сопротивлением в виде спирали, к верхнему концу которой подводится ток по графитовой трубке-экрану. Графитовый тигель с внутренним диаметром 14 мм вмещает около 120 г жидкого металла. Схема печи представ лена на рис. 3. Печь работает от трансформатора 7,5 квт при максимальном напряжении вторичной обмотки 20 в через регулятор РНО-250-10.
Для создания высокого вакуума в установке служит диффузионный ртутный насос ДРН-50 в паре с форвакуумным насосом ВН-461. Экстрагированные газы собираются ртутнокапельным насосом и анализируются при атмосферном давлении в газоанализаторе. Измерение вакуума в печи и на форвакуумной стороне диффузионного насоса осуществляется вакууметрами ВТ-2.
Особенностью конструкции установки системы ЦНИИТМАШ является то, что вакуумная печь установлена непосредственно на диффузионном насосе. Это позволяет до минимума сократить длину канализации между печью и насосом, значительно снизить ее сопротивление и тем ускорить от-качку газов из печного пространства. Кроме того, перезарядка печи не требует отсоединения последней от вакуумной части установки, т. е. при каждой перезарядке исключается нарушение этого крайне важного и конструктивно трудного по своему осуществлению узла.
При таком расположении печи газы откачиваются снизу через специальные каналы в контактных кольцах. Последние снабжены резьбой для ввинчивания в них графитовых нагревательных элементов и помещаются внутри печи в специальных гнездах, охлаждаемых снаружи водой.
Экстрагированная газовая смесь анализируется следующим образом. После измерения объема смеси в бюретке, смесь переводится в поглотитель, состоящий из насыщенного раствора хлористого аммония в 25%-ном аммиаке и небольшого количества полухлористой меди. Здесь происходит поглощение окиси углерода в присутствии медной стружки. Пары аммиака поглощаются затем 10%-ным раствором серной кислоты, а к оставшейся смеси водорода и азота добавляется кислород, полученный электролизом раствора едкого калия.. После сжигания смеси избыточный кислород поглощается тем же медноаммиачным поглотителем. При наличии в газовой смеси метана количество последнего может быть учтено после сжигания по количеству поглощенной углекислоты в сосуде с 30%-ным раствором щелочи. Этот метод газового анализа удобен тем, что не требует предварительной очистки электролитического кислорода, идущего на сжигание газовой смеси.

Вся установка смонтирована на специальном металлическом столе, на передней панели которого сосредоточено управление установкой, а контрольно-измерительные приборы расположены на щитке над газоанализатором. Внутри стола помещены диффузионный и фор вакуумный насосы.
Последний подвешен на амортизирующих пружинах. Установка имеет габариты 1600х950х1950 мм и вес около 500 кг. Потребляемая мощность в процессе дегазации печи — около 8 квт. Время дегазации в зависимости от качества графита от 1,5 до 2,5 час, и получаемая при этом величина поправки лежит в пределах 0,1—0,05 см3 за 30 мин. Чувствительность метода при навеске 10 г составляет по кислороду и азоту 1*10в-3 и по водороду 1*10в-4%. В табл. 2 приведены данные по определению газов в стали 40ХН на этой установке.

Определение газов на установке системыЦНИИТМАШ возможно для большинства технически важных железных сплавов с указанной выше точностью. Однако в настоящее время большое применение находят жаропрочные сплавы на никелевой основе, которые содержат небольшие количества газов, а также стали, выплавленные в инертных атмосферах или в вакууме. Для таких случаев в ЦНИИТМАШ сконструирована более чувствительная установка, схема которой приведена на рис. 4. Установка состоит из блока питания, экстракционной и аналитической частей. Блок питания включает понижающий трансформатор мощностью 7 кет и вариатор напряжения РНО-250-10. В экстракционную часть входит вакуум-печь с графитовым сопротивлением, установленная на ртутном диффузионном насосе ДРН-10. Печь по конструкции подобна применяемой в предыдущей установке, только меньших размеров. Аналитическая часть состоит из малогабаритного металлического диффузионного насоса конструкции ЦНИИТMAШ, наклонного дифференциального манометра, заполненного дибутилфталатом, и сосудов с окисью меди, ангидроном и аскаритом. Для анализа газовой смеси вначале с помощью дибутилфталатного манометра измеряется общее количество газа с точностью 1*10в-3 мл. Затем газ приводится в соприкосновение с окисью меди, нагретой до 300°. При этом сгорают водород и окись углерода. Пары воды поглощаются ангидроном и по уменьшению давления определяется количество водорода в газовой смеси. Затем остаток газа (после сжигания и адсорбции водяных паров) приводят в контакт с аскаритом. Уменьшение давления дает количество двуокиси углерода, образовавшегося из окиси углерода при сгорании последней. Азот определяется как остаток. Количество каждого из указанных газов вычисляется по формуле (1), а прибор градуируется по данным расчета по формуле (2).

Чувствительность по кислороду и азоту составляет 1*10в-4 и по водороду 1*10в5 при навеске 1г. В табл. 3 приведены данные по определению газов в сталях на этой установке.
Установка имеет габариты 1800х490х1800 мм и весит около 300 кг. Потребляемая мощность составляет около 5 квт.
Определение газов в металле
ГОСУДАРСТВЕННЫЙ СТАНДАРТ СОЮЗА ССР
Методы определения газов
Steels and alloys. Methods for determination of gases
Срок действия с 01.07.91
до 01.07.96*
________________________________
* Ограничение срока действия снято по протоколу N 5-94
Межгосударственного Совета по стандартизации,
метрологии и сертификации (ИУС N 11/12, 1994 год). -
Примечание изготовителя базы данных.
1. РАЗРАБОТАН И ВНЕСЕН Министерством металлургии СССР
В.П.Замараев, В.В.Покидышев, А.А.Иванов, В.М.Скосырев, В.Т.Абабков, А.А.Сахарнов, Л.Н.Дмитрова
2. УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Постановлением Государственного комитета СССР по управлению качеством продукции и стандартам от 27.04.90 N 1048
4. ССЫЛОЧНЫЕ НОРМАТИВНО-ТЕХНИЧЕСКИЕ ДОКУМЕНТЫ
Обозначение НТД, на который дана ссылка
* Письмом Росстандарта от 08.05.2019 г. N 8311-ИК/03 разъясняется, что "В пункте 1.1 ГОСТ 17745-90 допущена опечатка". Следует читать: Общие требования к методам анализа - по ГОСТ 28473-90, здесь и далее по тексту. - Примечание изготовителя базы данных.
Настоящий стандарт устанавливает метод восстановительного плавления в вакууме или в потоке инертного газа-носителя для определения кислорода (при массовой доле от 0,0005 до 0,2%), азота (при массовой доле от 0,0005 до 0,8%) и водорода (при массовой доле от 0,00005 до 0,01%) и метод нагрева или плавления в вакууме или в потоке инертного газа-носителя для определения водорода (при массовой доле от 0,00005 до 0,01%) в сталях и сплавах на основе железа, никеля, кобальта, железо-никеля.
Метод восстановительного плавления для определения массовых долей кислорода, азота и водорода основан на плавлении образца в графитовом тигле в вакууме или в потоке инертного газа-носителя, экстрагировании содержащихся в нем газов и последующем анализе кислорода, водорода и азота в экстрагированной газовой смеси физическими или физико-химическими методами.
Метод нагрева или плавления для определения массовой доли водорода основан на нагреве или плавлении образца в контейнере из керамического материала в вакууме или в потоке инертного газа-носителя, экстрагировании водорода из образца и определении его количества физическими или физико-химическими методами.
Метод восстановительного плавления применяется при разногласии в оценке качества сталей и сплавов.
Допускается по согласованию сторон применять методы для чугунов, ферросплавов и сплавов на основе марганца.
1. ОБЩИЕ ТРЕБОВАНИЯ
1.1. Общие требования к методам анализа - по ГОСТ 28437.
1.2. Отбор проб для изготовления образцов для анализа - по ГОСТ 7565.
Допускается отбор проб с помощью кварцевой трубки, размеры которой обеспечивают получение плотной пробы без пор и усадочных дефектов, а также специальных пробоотборников. Охлаждение проб осуществляют на воздухе или в воде.
2. АППАРАТУРА, МАТЕРИАЛЫ И РЕАКТИВЫ
2.1. Для определения кислорода применяется экспресс-анализатор типа АК 7516 с техническими характеристиками:
время анализа - 82 с;
максимальная мощность - 11 кВА;
расход аргона 0,5 дм/мин;
чувствительный элемент - ячейка кулонометрического титрования.
2.2. Для определения азота применяется экспресс-анализатор типа AM 7514 с техническими характеристиками:
время анализа - не более 120 с;
расход гелия - 1,02 дм/мин;
чувствительный элемент-детектор по теплопроводности.
2.3. Для определения водорода применяется прибор типа RH-2 фирмы "Леко" с техническими характеристиками:
расход газа - 0,26-0,30 дм/мин;
время анализа - не более 420 с;
максимальная мощность - 4,5 кВА;
чувствительный элемент - детектор по теплопроводности.
2.4. Блок-схемы проборов для измерения массовой доли газов в общем виде приведены на чертеже.
Блок-схемы приборов для измерения массовой доли газов:
а - методом плавления (нагрева) в потоке инертного газа-носителя (1 - источник инертного газа-носителя;
2 - редуктор; 3 - экстракционная печь; 4 - реакционный блок; 5 - аналитический блок;
6 - блок управления; 7 - блок электропитания печи)
б - методом плавления (нагрева) в вакууме (1 - форвакуумный насос; 2 - экстракционная печь;
3 - газосборочный насос; 4 - реакционный блок; 5 - аналитический блок; 6 - блок управления;
7 - блок электропитания печи)
Допускается применение других средств измерений с метрологическими характеристиками не хуже, чем у вышеуказанных приборов.
Перечень приборов приведен в приложении.
2.5. Весы для взвешивания образцов - любые, обеспечивающие требуемую точность взвешивания, в том числе и автоматические, которыми оборудованы приборы для газового анализа. Образцы для анализа взвешивают с пределом допускаемой погрешности, не превышающий 0,001 г при массе образцов до 0,1 г и 0,002 г - при массе образцов свыше 0,1 г.
Гелий газообразный чистотой не менее 99,99%.
Аргон газообразный по ГОСТ 10157.
Азот газообразный по ГОСТ 9293.
Водород газообразный по ГОСТ 3022.
Окись углерода газообразная чистотой не менее 99,5%.
Углерод четыреххлористый по ГОСТ 20288.
Спирт этиловый ректификованный технический по ГОСТ 18300.
Бензин авиационный по ГОСТ 1012.
Меди (II) окись по ГОСТ 16539.
Никель H1, H2 по ГОСТ 849*.
* На территории Российской Федерации действует ГОСТ 849-97. - Примечание изготовителя базы данных.
Олово 01, 02 по ГОСТ 860.
Бязь хлопчатобумажная по ГОСТ 11680.
Допускается использование других материалов, в том числе поставляемых фирмами-производителями приборов по качеству не ниже указанных в стандарте.
3. ПОДГОТОВКА К АНАЛИЗУ
3.1. Подготовка образцов
3.1.1. Для анализа применяют компактные образцы с чистой без цветов побежалости поверхностью, без пор, раковин и заусенцев, обработанные на металлорежущих станках, напильником (надфилем) или абразивом, не содержащим соединений анализируемого (анализируемых) газов.
При определении массовой доли азота допускается использование образцов в виде крупной стружки.
При изготовлении образцов не допускается нагрев металла свыше 70 °С.
Масса образцов должна составлять 0,05-2,0 г для определения массовой доли кислорода и азота и 0,05-12,0 г - для определения массовой доли водорода.
3.1.2. Для проведения анализа изготовляют не менее трех компактных образцов.
3.1.3. Перед проведением анализа образцы обезжиривают промывкой в спирте (эфире, авиационном бензине или четыреххлористом углероде). При определении массовой доли кислорода и азота допускается очистка образцов перед анализом физическими или физико-химическими методами, в том числе электрохимическим полированием и травлением в кислотах с применением ультразвука.
Если используются образцы в виде стружки, то допускается проведение анализа без их промывки.
Влияние газов на свойства металла
Определение газов в металле проводится путем установления составляющих, которые при первоначальном взаимодействии с металлом находятся в газообразном состоянии или выделяются из металла в этом состоянии. Наиболее часто встречаются в металле – водород, кислород, азот. Сложные газы H20, CO, CO2, SO2 образуются в процессе выделения газов из металла.
Газы находятся в металле в форме:
- газовых включений (пор, пузырей),
-химических соединений (оксидов, нитридов, гидридов),
-растворов внедрения (статически равномерно распределяются в его кристаллической решетке)
-адсорбированных на поверхности металла тонких слоев.
Влияние газов на свойства металла зависит от формы присутствия газа.
При высокой температуре газы в жидком металле находятся в растворенном состоянии. При снижении температуры уменьшается растворимость газов что приводит к выделению их из раствора. При кристаллизации слитка выделяющиеся газы могут образовывать газовые пузыри и поры, что нарушает сплошность металла, уменш. плотность, и приводит к снижению качества металла.
Газы, растворенные в твердом металле снижают механические свойства, коррозионную стойкость, ухудшают магнитные характеристики.
ВОДОРОД. Вызывает появление флокенов - внутренних трещин.
Влияет на механические свойства металла вызывая водородное охрупчивание стали, при котором наблюдается снижение пластических свойств металла. Водородная хрупкость стали связана с повышением давления водорода в микропорах металла. Давление водорода превышающее предел упругости металла, приводит к деформации кристаллической решетки и облегчает разрушение металла при испытании. Водород снижает усталостные свойства стали, облегчая образование трещин, ведущих к разрушению образца при испытаниях на длительную прочность т.е. под влиянием длительной статической нагрузки, способствует коррозионному растрескиванию стали, возникновению в стали дефектов – пузыри, центральная пористость, пятнистая ликвация.
АЗОТ – вредное влияние азота проявляется в снижении пластических свойств малоуглеродистых сталей. С понижением температуры из феррита (тв.р-р углерода в α Fe) выделяется мелкозернистая фаза нитридов Fe4N. Этот процесс при низких температурах происходит медленно и называется старением стали. Выделение азота в отдельную фазу сопровождается возникновением напряженности структуры металла, повышением его твердости и хрупкости, снижением пластичности.
В средне и малоуглеродистых сталях наличие азота вызывает хрупкий (интеркристаллитный) излом, который связан с ослаблением границ зерен аустенита (тв.р-р углерода в g Fe) вследствие выделения включений нитридов.
Кислород.- общее содержание кислорода в стали, состав, структура форма и расположение кислородных включений их количество влияют на механические и другие свойства металлов и сплавов.
Изменяя кристаллическую решетку и микроструктуру металла, примеси газов даже в небольших концентрациях существенно влияют на физико-химические характеристики и эксплуатационные свойства металлов и сплавов. В основном это влияние отрицательное.
В изделиях важно распределение газов по микро- и макроструктуре, и перераспределение их условиях эксплуатации под влиянием окружающей атмосферы и механической нагрузки.
Определение газов необходимо – при выплавке и других переделах для того чтобы свести к минимуму их содержание, для анализа готовой продукции, для изучения и прогнозирования поведения изделий в процессе эксплуатации. содержание газов на металлопродукцию нормировано ГОСТом.
Методы определения газов должны решать задачи:
Экспресс-анализ металла по ходу плавки, массовый анализ готовой продукции, распределение в металле, определение газов на поверхности металла.
Разработан ряд способов пробоотбора металла, но наиболее перспективные методы непосредственного анализа жидкого металла.
РАСТВОРИМОСТЬ ГАЗОВ В МЕТАЛЛИЧЕСКИХ РАСПЛАВАХ
К газам в стали относят, как правило, азот и водород. Особенностью растворения азота и водорода в металлических расплавах является то, что они диссоциируют на атомы. В этом случае реакция растворения газа (Г) записывается в виде
Величина растворимости газов в чистых металлах невелика (например, при 1873 К растворимость азота в железе составляет 0,044%). Растворы можно считать разбавленными и подчиняющимися закону Сивертса (частный случай закона Генри):
где – константа Сивертса, являющаяся функцией температуры.
Если рассмотреть растворение газов в сплавах, то вместо концентрации следует подставлять значение активности, тем самым учитывать влияние добавляемого элемента на растворимость газа. Связь между растворимостью газа в чистом металле и легированном растворе можно определить, исходя из следующих соображений.
Допустим, что при постоянных температуре и давлении в равновесии с газовой фазой (Г) находятся два расплава: чистый металл (`) и металл с добавками легирующих элементов (``). Естественно, что активность азота в обоих растворах должна быть одинаковой:
Из соотношений (36), (37) следует
Выражение (38) позволяет рассчитать концентрацию азота в расплаве известного состава. Значение коэффициента активности целесообразно определять по значениям параметров взаимодействия (табл. 10). Константу равновесия реакции (34) определяют по данным об изменении энергии Гиббса (табл. 11).
При изменении давления и температуры жидкого металла возможно как выделение газа, так и поглощение его расплавом. Для расчета объема газа, выделившегося из расплава при понижении давления и постоянной температуре можно использовать уравнение Менделеева – Клапейрона:
где – объем газа, – масса газа, – молекулярная масса газа, г/моль; R=8,314 Дж/(моль·К) – газовая постоянная.
Значение параметров взаимодействия в расплавах на основе и [1]
| Растворитель | |||||
| N | 0,047 | –0,0123 | –0,0467 | –0,0197 | 0,123 |
| H | 0,026 | 0,0020 | 0,0033 | –0,0012 | 0,065 |
| N | –0,043 | –0,1000 | –0,051 | 0,090 | |
| H | 0,033 | 0,0020 |
Изменение энергии Гиббса при растворении газов [4]
| Растворитель | Газ | Дж/моль |
| A | B | |
| N | 10 500 | 20,37 |
| H | 36 500 | 30,46 |
| N | 69 270 | 18,68 |
| H | 20 100 | 35,10 |
1. Определить растворимость азота и водорода в расплаве , а также в легированных расплавах на их основе, при температурах Т1 и Т2 .
2. Рассчитать объем газа, выделившегося из расплава при уменьшении давления с 1 атмдо величины . Данные в табл. 12.
Вырожденный электронный газ в металлах
Распределение электронов по различным квантовым состояниям в той или иной системе подчиняется принципу Паули, согласно которому в одном состоянии (с одинаковым набором четырех квантовых чисел) не может быть более одного электрона.
Отсюда следует, что все свободные электроны в металле не могут располагаться на одном самом низшем энергетическом уровне даже при 0 К. Согласно принципу Паули, электроны вынуждены последовательно заполнять энергетические уровни в направлении возрастания энергии.
Для фермионов среднее число частиц в квантовом состоянии и вероятность заселённости квантового состояния совпадают, так как квантовое состояние либо может быть не занято, либо в нем будет находиться одна частица. Это означает, что для фермионов
где – функция распределения электронов по состояниям (2.2).
Если – химический потенциал электронного газа при
Т = 0 К, то согласно (2.2) и (2.7), среднее число электронов в квантовом состоянии с энергией Е равно
Из (2.8) следует, что при Т = 0 К функция распределения при и , если .
График этой функции приведен на рис. 2.1 а, из которого следует, что при Т = 0 К все нижние квантовые состояния, вплоть до состояния с энергией, , заняты электронами, а все состояния с энергией, большей , свободны.
| а) | б) |
| Рис. 2.1 |
Следовательно, есть максимальная кинетическая энергия, которую могут иметь электроны проводимости в металле, при 0 К. Величину принято называть энергией или уровнем Ферми и обозначать .
Энергия Ферми рассматривается как параметр распределения ферми-частиц, а само распределение Ферми-Дирака обычно записывают в виде
Для металлов при не слишком высоких температурах выполняется неравенство .
Это означает, что электронный газ в металлах практически всегда находится в состоянии сильного вырождения. Температура Т0 вырождения находится из условия . Она определяет границу, выше которой квантовые эффекты перестают быть существенными. Соответствующие расчёты показывают, что для электронов в металле , т.е. для всех температур, при которых металл может существовать в твердом состоянии, электронный газ в металле вырожден.
При температурах, отличных от 0 К, функция распределения Ферми-Дирака, плавно изменяется от 1 до 0 в узкой области энергий порядка кТ в окрестности (рис. 2.1, б).
Из (2.8) видно, что при функция распределения при любой температуре (рис. 2.1, б).
Поэтому со статистической точки зрения уровень Ферми при любой температуре представляет собой энергетический уровень, вероятность заполнения которого равна .
Если принять условие тождественности энергетических состояний двух электронов с одинаковым набором трех квантовых чисел n, ℓ, mℓ, но с противоположными направлениями спинов, то можно считать, что на одном энергетическом уровне может находиться два электрона.
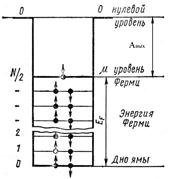
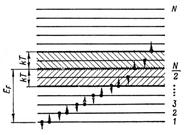
На рис. 2.2 наглядно представлено распределение электронов по состояниям при Т = 0 К (рис. 2.2 а) и Т > 0 К (рис. 2.2 б).
 |  |
| а) | б) |
| Рис. 2.2 |
Работа выхода электронов из металла определяется расстоянием от уровня Ферми до нулевого энергетического уровня (рис. 2.2 а). При Т > 0 К энергетические переходы осуществляют электроны вблизи уровня Ферми в полосе шириной 2кТ (рис. 2.2 б).
В металлах, где концентрация свободных электронов очень высока (≈ 10 28 м -3 ), электронный газ всегда находится в вырожденном состоянии и описывается распределением Ферми-Дирака.
С невырожденным электронным газом приходится иметь дело в собственных (беспримесных) и в слаболегированных полупроводниках. Концентрация свободных электронов в таких полупроводниках значительно ниже, чем в металлах, и колеблется в зависимости от содержания активных примесей от 10 16 – 10 19 до 10 23 – 10 24 м -3 . При таких концентрациях электронный газ становится невырожденным и может описываться распределением Максвелла-Больцмана.
Читайте также:
