Процессы электролиза используют при получении металлов
Обновлено: 08.07.2024
В § 45 вы познакомились с электрохимическим методом промышленного получения металлов, который основан на электролизе, — электрометаллургией.
У этого метода есть две разновидности. Первая — это проведение электролиза расплава соединений металлов. Особенности этого способа вы рассмотрели на примере электролиза расплава хлорида магния.
Вторая разновидность электрохимического метода, называемая гидроэлектрометаллургией, основана на электролизе водных растворов солей металлов. Преимущество этого метода, по сравнению с электролизом расплавов, заключается в том, что он не требует энергетических затрат на расплавление вещества. Ограничение электролитического метода извлечения металлов из водных растворов состоит в том, что он пригоден лишь для металлов, стоящих в ряду активности металлов правее алюминия.
Особенность проведения электролиза водных растворов солей заключается в том, что наряду с процессами восстановления ионов металла на катоде и окисления анионов соли на аноде протекает конкурирующий процесс электролиза молекул воды. В результате на катоде может выделяться водород, а на аноде — кислород.
Процессы на катоде:
2Н + + 2е – = Н2↑ при рН < 7;
Процессы на аноде:
2Н2О – 4е – = О2↑ + 4Н + при рН ≤ 7;
4ОН – – 4е – = О2↑ + 2Н2О при рН > 7.
Процессы на катоде
Способность металлов восстанавливаться на катоде при электролизе водного раствора солей определяется положением металла в ряду активности.
Катионы металлов в левой части ряда активности, заканчивая алюминием (Li + , Na + , K + , . Аl 3+ ), при электролизе не восстанавливаются. Вместо них восстанавливается водород из молекул воды:
Катионы металлов, расположенных в ряду активности правее водорода (Cu 2+ , Ag + , Hg 2+ , Pt 2+ , Au 3+ ), при электролизе восстанавливаются на катоде до металла:
Cu 2+ + 2е – = Cu 0 ;
Au 3+ + 3е – = Au 0 .
Этот процесс доминирует, но если электролит имеет сильно кислую среду, то одновременно с ионами металла могут восстанавливаться ионы водорода:
Катионы металлов, расположенных в ряду активности между алюминием и водородом (Mn 2+ , Zn 2+ , Сr 3+ , Fe 2+ , . Pb), при электролизе восстанавливаются на катоде одновременно с водородом из воды:
Ni 2+ + 2e – = Ni 0 ;
При электролизе водных растворов солей металлов следует учитывать возможность протекания процессов гидролиза, который ускоряется в результате образования гидроксид-ионов в электролите вблизи катода. В результате на поверхности катода могут образовываться нерастворимые основные соли и основания:
Электропроводность электрода уменьшается, и процесс электролиза замедляется или прекращается. Один из способов борьбы с таким явлением — подкисление электролитов.
Процессы на аноде
На аноде протекают процессы окисления компонентов электролита. В процессе окисления может участвовать и материал самого анода. Различают процессы электролиза в растворах с активным и инертным анодами.
Инертные аноды не окисляются под действием электрического тока и не реагируют с веществами раствора. При электролизе они служат лишь передатчиками электронов. Инертными являются электроды из графита, платины, платинированного титана.
К активным относятся аноды, изготовленные из Сu, Ag, Fe, Ni, Sn, Zn. Металл активных анодов в процессе электролиза разрушается и переходит в раствор в виде ионов. Активные аноды обычно применяют в промышленности при получении покрытий путём электрохимического восстановления металлов из растворов, поскольку растворение металлического анода в процессе электролиза восполняет убыль ионов восстанавливаемого металла из электролита. При этом они обеспечивают постоянство состава раствора, скорости процесса электролиза, состава и свойств получаемых металлических покрытий.
Рассмотрим подробнее процессы, протекающие при электролизе растворов на инертных анодах. Можно выделить следующие закономерности (табл. 31.1):
• в растворах бескислородных кислот и их солей (кроме HF и фторидов) на аноде окисляются анионы, например:
• в растворах кислородсодержащих кислот и их солей в случае максимальной степени окисления атомов неметалла в анионе ( , ) окисляются атомы кислорода в молекулах воды с выделением газообразного кислорода:
• в растворах кислородсодержащих кислот и их солей, в анионах которых содержатся атомы неметалла в промежуточной степени окисления ( , ), окисляются именно эти атомы в составе анионов, например:
Таблица 31.1. Способность к окислению на аноде анионов при электролизе водных растворов солей
В водном растворе не окисляются; окислению подвергаются молекулы воды с выделением кислорода:
В водном растворе легко окисляются, например:
В специально созданных условиях в водных растворах может идти процесс окисления и кислородсодержащих анионов с максимальной степенью окисления неметалла. Например, электролизом концентрированного раствора гидросульфата калия получают сильный окислитель — пероксодисульфат калия:
Примеры использования электролиза водных растворов солей металлов в промышленности и в лаборатории
При разработке условий электролиза следует учитывать, что продукты электролиза могут вступать в химические реакции с электродами и водными растворами или между собой.
Промышленный электролиз водного раствора NaCl. Процесс используют для получения водорода, хлора и каустической соды (NaOH). При этом на катоде выделяется водород:
а в растворе накапливается каустическая сода:
Если не разделить продукты электролиза, то между образовавшимися газами произойдёт химическая реакция.
В растворе также возможно взаимодействие хлора со щёлочью:
Cl2 + 2NaOH = NaClO + NaCl + H2O.
Для того чтобы между продуктами электролиза не происходило взаимодействие, катодное и анодное пространство разделяют мембраной (рис. 108.2).
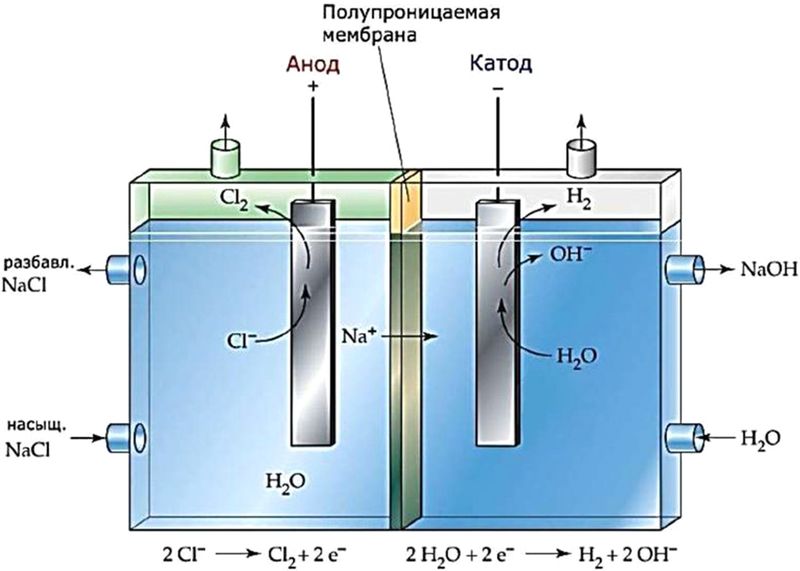
Рис. 108.2. Схема электролизёра с ионообменной мембраной для электролиза раствора хлорида натрия. Мембрана пропускает ионы Na + , но не пропускает ионы Cl – и OH –
С 2015 года в ОАО «Беларуськалий» функционирует цех мембранного электролиза. Продукцией цеха являются: водный раствор гидроксида калия (с массовой долей KOH 46−54 % ); твёрдый гидроксид калия (с массовой долей KOH 9 0−95 % ); соляная кислота (с массовой долей HCl 28−35 % ); гипохлорит натрия NaClO.
Электролиз растворов солей в лаборатории.
Для наглядности при рассмотрении особенностей электролиза водных растворов солей обратимся к химическому эксперименту.
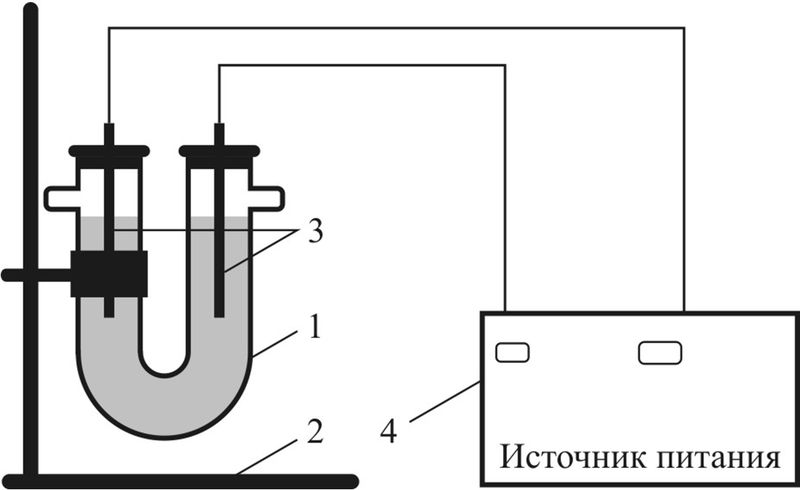
Рис. 108.3. Схема прибора для электролиза:
1 — U-образная трубка (электролизёр);
2 — штатив;
3 — электроды (графитовые стержни);
4 — источник питания постоянного тока
Опыт 1. Проведём электролиз водного раствора CuSO4. Для этого соберём прибор по схеме, представленной на рис. 108.3. В U-образную трубку нальём раствор сульфата меди(II) и опустим два графитовых стержня, закреплённых в резиновых пробках. Стержни с помощью проводов присоединим к источнику тока, на котором поддерживается напряжение постоянного тока до 12 В.
Рис. 108.4. Осаждённая медь на графитовом электроде после проведения электролиза раствора сульфата меди(II)
При пропускании электрического тока через раствор CuSO4 на стержне, присоединённом к положительному полюсу источника тока (анод), можно наблюдать выделение пузырьков газа (это кислород), а на стержне, присоединённом к отрицательному полюсу (катод), — появление красного налёта (это восстановленная медь) (рис. 108.4).
Объяснить наблюдаемое явление можно следующими процессами.
В растворе сульфата меди происходит диссоциация:
При подключении электродов к источнику тока в растворе электролита происходит направленное движение ионов к электродам, имеющим противоположные заряды.
На катоде происходит восстановление меди, которая образует красный налёт на электроде:
Сu 2+ + 2e – = Сu 0
На аноде (положительно заряженном электроде) происходит окисление молекул воды с выделением кислорода:
Суммарное уравнение процессов на электродах в молекулярной форме:
Опыт 2. Проведите электролиз водного раствора йодида калия.
Для проведения электролиза раствора KI воспользуемся установкой из примера 1 (рис. 108.3).
В U-образную трубку нальём раствор KI и пропустим через него электрический ток. Через 3–5 минут, отключив ток и достав электроды, в катодное пространство добавим 2−3 капли фенолфталеина, а в анодное пространство прильём крахмальный клейстер.

Рис. 108.5. Электролизёр после проведения электролиза раствора йодида калия и добавления раствора фенолфталеина (катодное пространство) и крахмального клейстера (анодное пространство)
Раствор в катодном пространстве окрашивается в малиновый цвет, что свидетельствует о щелочной среде. В анодном пространстве наблюдается выделение жёлто-бурого вещества, при добавлении к которому 2–3 капель крахмального клейстера происходит посинение раствора, что указывает на присутствие в растворе йода (рис. 108.5).
Таким образом, продуктами электролиза водного раствора йодида калия являются I2 и щёлочь.
Наблюдаемые явления свидетельствуют о протекании на электродах следующих реакций:
2Н2О + 2e – = Н2↑ + 2ОН – на катоде;
2I – – 2e – = I2 на аноде.
Суммарное уравнение процесса электролиза в молекулярной форме:
Электролиз с активными анодами в промышленности. Помимо электрохимического осаждения металлических покрытий и получения порошков металлов, этот метод применяют для извлечения металлов из растворов, а также для очистки (рафинирования) металлов от содержащихся в них примесей. Так получают чистое золото, медь и многие другие металлы.
Например, при очистке (рафинировании) меди исходный металл, содержащий нежелательные примеси, служит анодом. Анод погружают в раствор сульфата меди(II). При пропускании тока медь на аноде окисляется, её ионы переходят в раствор, перемещаются к катоду и на нём восстанавливаются. Примеси в этом процессе не участвуют из-за их малой концентрации, и поэтому на катоде образуется слой чистой меди.
Процессы электролиза с активными анодами используют для получения покрытий из оксидов металлов. Так, при проведении электролиза с анодом из алюминия его поверхность окисляется, покрываясь слоем оксида. Такой процесс специального наращивания оксида на поверхности металла называют электрохимическим оксидированием (или анодированием). Анодирование применяют для защиты металла от коррозии, придания его поверхности декоративного внешнего вида, повышенной твёрдости.
Методом электролиза растворов солей на поверхность различных изделий наносят покрытия из металлов и их сплавов, композитов с неметаллами, что придаёт изделиям нужные свойства (повышенная коррозионная стойкость, декоративная отделка, электропроводность и др.). К распространённым промышленным процессам относятся цинкование, никелирование, меднение, хромирование, оловянирование, золочение и серебрение.
В НИИ физико-химических проблем Белорусского государственного университета разработаны и внедрены в промышленность процессы электрохимического осаждения покрытий из сплавов металлов и композиционных покрытий металл — оксид металла, например: Ni—B , Ni—P , Ni—Sn , Au—Co , Сu—CuO—Cu2O , Ni — алмаз (алмаз в виде тонко измельчённого порошка). Такие покрытия более твёрдые, износо- и коррозионностойкие, чем покрытия из индивидуальных металлов, обладают декоративным внешним видом (рис. 108.6).
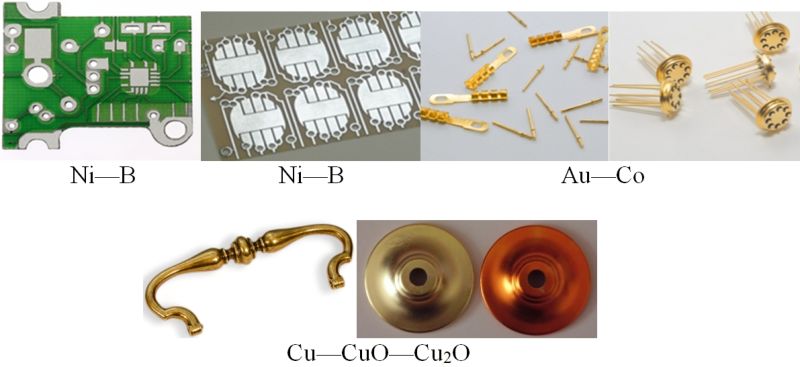
Рис. 108.6. Покрытия на часовых платах, платах кредитных карточек, корпусах транзисторов, фурнитурных изделиях
Электролиз водных растворов используется также в синтезе различных неорганических веществ, в обработке поверхностей металлов (азотирование, борирование, электрополировка, очистка), в очистке сточных вод (процессы электрокоагуляции, электроэкстракции, электрофлотации). Электролизом получают кислород и водород.
При электролизе водных растворов солей на катоде восстанавливаются катионы металлов, расположенных в ряду активности после водорода.
На катоде не восстанавливаются катионы металлов IA- и IIA-групп , расположенных в начале ряда активности, а также алюминий, вместо них восстанавливается водород из молекул воды.
На катоде одновременно с водородом из воды восстанавливаются катионы металлов, расположенных в ряду активности между алюминием и водородом.
На аноде в растворах солей бескислородных кислот окисляются анионы (кроме фторид-ионов).
На аноде в растворах солей кислородсодержащих кислот с максимальной степенью окисления неметалла ( , ) окисляются молекулы воды с выделением кислорода.
Вопросы, задания, задачи
1. Какие из веществ — каменная соль, сахар, медный купорос, глицерин, серная кислота — могут подвергнуться электролизу в водном растворе?
2. Объясните, почему алюминий нельзя получить электролизом водного раствора его хлорида.
3. Приведите уравнения реакций на электродах при электролизе водного раствора сульфата никеля(II).
4. Сравните продукты электролиза расплава и водного раствора хлоридов натрия, никеля(II) и меди(II). Приведите соответствующие уравнения химических реакций.
5. При электролизе водного раствора хлорида натрия без разделения электродных пространств можно получить гипохлорит натрия. Приведите возможные уравнения электродных процессов и химических реакций в растворе.
6. Продукцией цеха мембранного электролиза ОАО «Беларуськалий» являются водный раствор гидроксида калия и соляная кислота. Приведите уравнения реакций, которые лежат в основе получения этих веществ.
7. Как изменится концентрация катионов и анионов в водных растворах CuCl2, Na2SO4, KI, NaOH, HCl при электролизе? Приведите соответствующие уравнения реакций.
8. В качестве лабораторного способа дезинфекции воды используется электролиз водного раствора хлорида натрия в портативных электролизёрах. Объясните процессы, на которых основан этот способ дезинфекции воды.
9. Сырьём для получения цинка является руда, содержащая цинковую обманку (ZnS). Продукт её обжига растворяют в серной кислоте и после нескольких стадий очистки от примесей (Cu 2+ , Fe 2+ , Fe 3+ и др.) подвергают электролизу. Приведите уравнения химических реакций, иллюстрирующих все основные стадии получения цинка.
10. Оксид марганца(IV) получают электролизом раствора сульфата марганца(II) в присутствии серной кислоты. Предположите, какие процессы протекают на электродах и приведите уравнения соответствующих реакций.
Самоконтроль
1. При электролизе водных растворов солей восстанавливаются ионы:
- а) Li + ;
- б) Mg 2+ ;
- в) Ni 2+ ;
- г) Au 3+ .
2. При электролизе водных растворов солей не восстанавливаются ионы:
- а) K + ;
- б) Са 2+ ;
- в) Cu 2+ ;
- г) Ag + .
3. Продуктами электролиза водного раствора калийной соли являются:
4. На катоде могут протекать процессы:
- а) 2Н2О + 2e – = Н2↑ + 2ОН – ;
- б) 2Н2О – 4e – = О2↑ + 4Н + ;
- в) 2Н + + 2e – = Н2↑;
- г) Ni 2+ + 2e – = Ni 0 .
5. При электролизе водного раствора хлорида натрия выделился водород объёмом 2,24 дм 3 (н. у.). Число электронов, отданных при этом ионами хлора, равно:
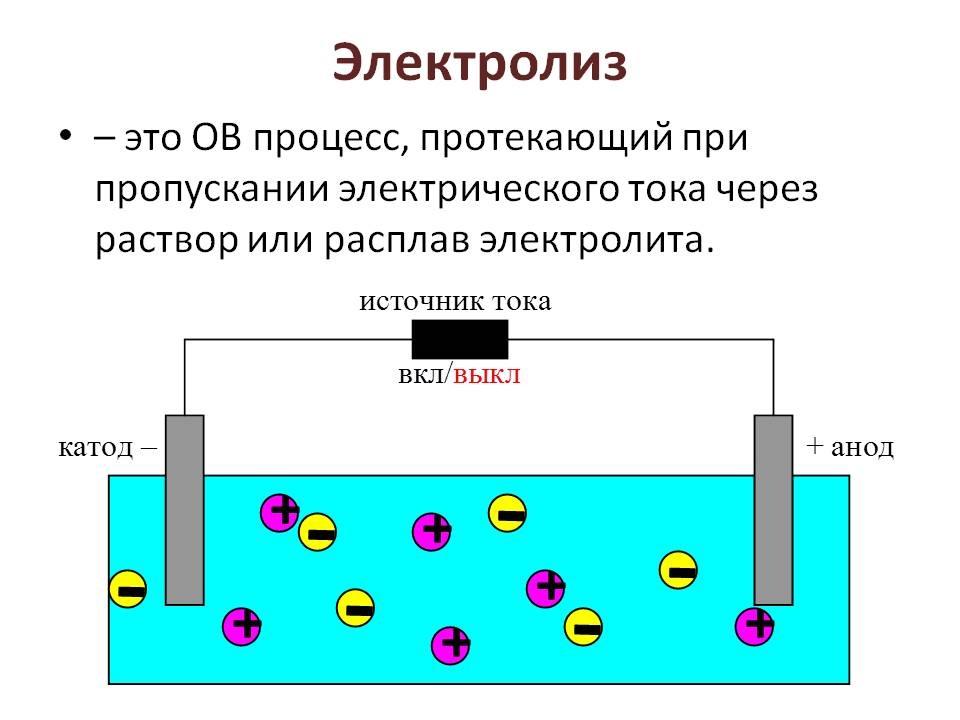
Электролиз
Электролиз в промышленных масштабах используется для извлечения из металлосодержащих руд металлов и их очищения от примесей. При помощи этого физико-химического процесса на производстве получают медь и алюминий. Заряд химических источников тока (аккумуляторов) также происходит, благодаря протеканию этой реакции.
Определение электролиза
Химическая реакция, в результате которой на электродах происходит оседание компонентов из электролитических растворов веществ, и протекающая под действием электрического тока – вот что такое электролиз. Он включает в себя комплекс процессов окисления и восстановления, происходящих на электродах. Обязательным условием является движение постоянного тока от электрода к электроду.
В чём заключается процесс
Технологический порядок электролиза, или ещё его называют гальванолизом, происходит по законам химии и физики. При этом берутся электропроводящие растворы (жидкости), в которых при помощи двух электродов организовано электрическое поле.
Внимание! Электроды имеют названия. Катод (К) – электрод, имеющий отрицательный потенциал, анод (А) – электрод с положительным потенциалом.
Ионы движутся упорядоченно через раствор, который носит название электролита. При этом ионы, относящиеся к металлам, водороду (катионы) направляются к катоду, к аноду стремятся ионы, принадлежащие к кислотным остаткам или гидроксильной группы (анионы). Катионы имеют положительный знак заряда, анионы – отрицательный. Пропускание электрического тока при электролизе может осуществляться, как через растворы, так и через расплавы электролитов.
Информация. При приготовлении электролита происходит диссоциация раствора на ионы. Это обусловлено взаимодействием растворителя на растворяемое вещество. Такая реакция называется первичной. Дальнейшее воздействие электрического тока на электролит вызывает вторичную реакцию гальванолиза.
Подобное разделение на первичность и вторичность позволило Майклу Фарадею обосновать законы, применяемые к гальванолизу.
Электролиз растворов
Использование воды для приготовления раствора электролита осложняет процесс. В растворах солей и щелочей вода ведёт себя при электролизе неоднозначно. Это проявляется в том, что H2O ведёт себя как окислитель, так и как восстановитель. На катоде она получает электроны и восстанавливает атомы водорода до газообразной формы водорода. На аноде вода отдаёт отрицательно заряженные частицы, тогда атомы кислорода окисляются до газообразной формы кислорода. Кислота, используемая в качестве раствора для электролита, лишена этой проблемы.
Катодные процессы
Катод, помещённый в растворы солей, притягивает к себе катионы металлов. Эти катионы выступают как окислители.
Важно! У отдельных металлов способности ионов окислять различны. Чтобы оценить способности окисления – восстановления, необходимо опираться на электрохимический ряд напряжений.

У каждого металла (далее обозначен как М) свой электрохимический потенциал (ЭХП). Чем он меньше, тем восстановительные свойства выше, а окислительная способность у соответствующих ионов этого металла ниже.
ЭХП величина относительная, потому у отдельных ионов разная величина ЭХП. У водорода он равен нулю.
Во время процесса электролиза, протекающего в растворах солей, выявлены следующие замечания:
- когда в солях присутствуют активные М, то не они восстанавливаются на катоде, а водород;
- если М в электролите имеет среднюю активность, то на катоде разряжаются (восстанавливаются) оба: и водород, и М;
- при неактивном М на катоде восстанавливается только он, потому что его ион – более сильный окислитель, чем водородный ион.
Примерами таких процессов на катоде могут служить следующие реакции:
- при активном М: 2H2O +2ē → H2 + 2OH—;
- при М средней активности: Men+ + nē → Me0 и 2H+2O +2ē → H20 + 2OH—, где Ме – это растворённый металл;
- в случае неактивного М в солях: Men+ + nē → Me0.
Замечено, что, когда с катодом взаимодействуют водородные катионы H+, происходит их разряжение до молекул водорода — 2H+ + 2ē → H20
Анодные процессы
Плюс, поданный на анод, притягивает к себе анионы вместе с молекулами воды. В данном случае анод является окислителем, а восстановители – молекулы H2O или анионы кислотных остатков.
В процессе гальванолиза на аноде происходят следующие реакции:
- кислотные остатки, не содержащие кислорода, окисляются до нулевой степени окисления: неМеn- – nē = неМе0, где – неМе – это неметалл;
- при содержании в остатке кислорода окисляется вода и выделяет молекулы кислорода (молекулярный кислород О2): 2H2O-2 – 4ē → O20 + 4H+;
- в случае контакта с анодом гидроксид-иона последний также окисляется: 4O-2H– – 4ē → O20 + 2H2O, с выделением молекулярного кислорода.
Исключение. Фтор обладает электроотрицательностью более высокой, чем кислород. Поэтому электролиз растворов фторидов протекает с окислением молекул воды вместо фторид-ионов.
Суммарные процессы электролиза
Что получается в суммарной реакции гальванолиза, можно рассмотреть на примере хлорида натрия. При пропускании электрического тока на электродах происходит следующее:
- катод – на нём восстанавливается H – водород: 2H+2O +2ē → H20 + 2OH–;
- анод – на электроде происходит окисление хлорид-ионов: 2Cl– – 2ē → Cl20.
В этой реакции электролиза не принимают участия ионы натрия. Тем не менее, они входят в суммарное уравнение раствора хлорида натрия при электролизе. Оно имеет вид:
2H+2O + 2NaCl– → H20 + 2NaOH + Cl20.
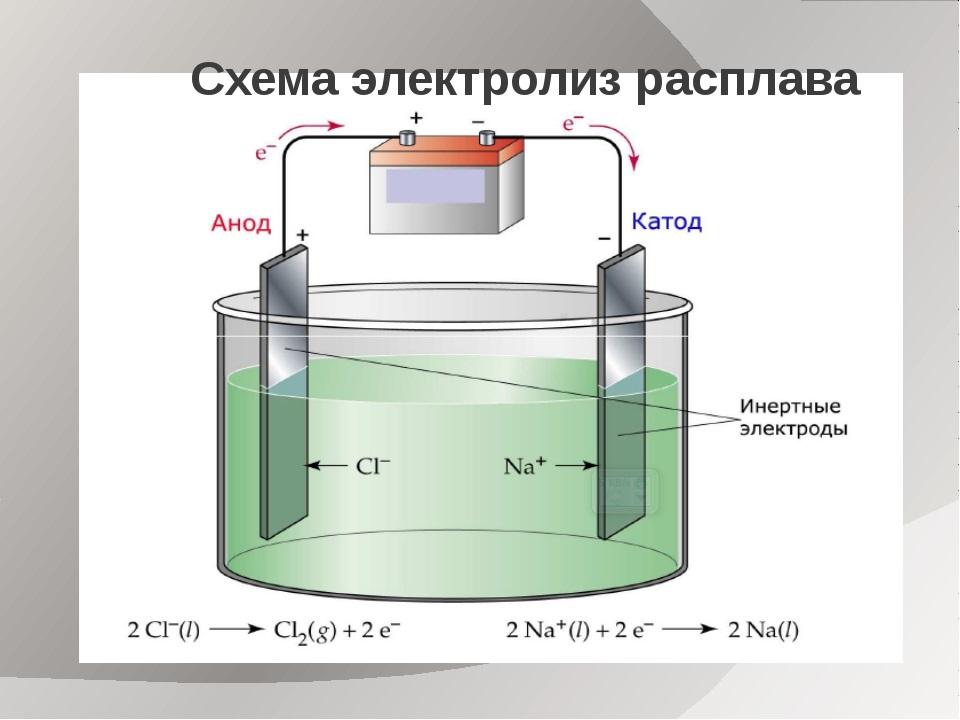
Электролиз расплавов
Если сравнить гальванолиз расплавов и растворов, то в расплавах все М: активные, малоактивные и неактивные, реагируют на процесс электризации одинаково.
Внимание! Вода при электролизе расплавов в электролите отсутствует. Поэтому осложнений, связанных с её вмешательством, не возникает. Описание такой реакции можно рассмотреть на примере расплава NaCl (хлористого натрия).
В этом случае на катоде происходит восстановление катионов Na:
Анод вызывает окисление анионов Cl:
Общее уравнение гальванолиза расплава NaCl будет иметь вид:
2Na+Cl– → 2Na0 + Cl20.
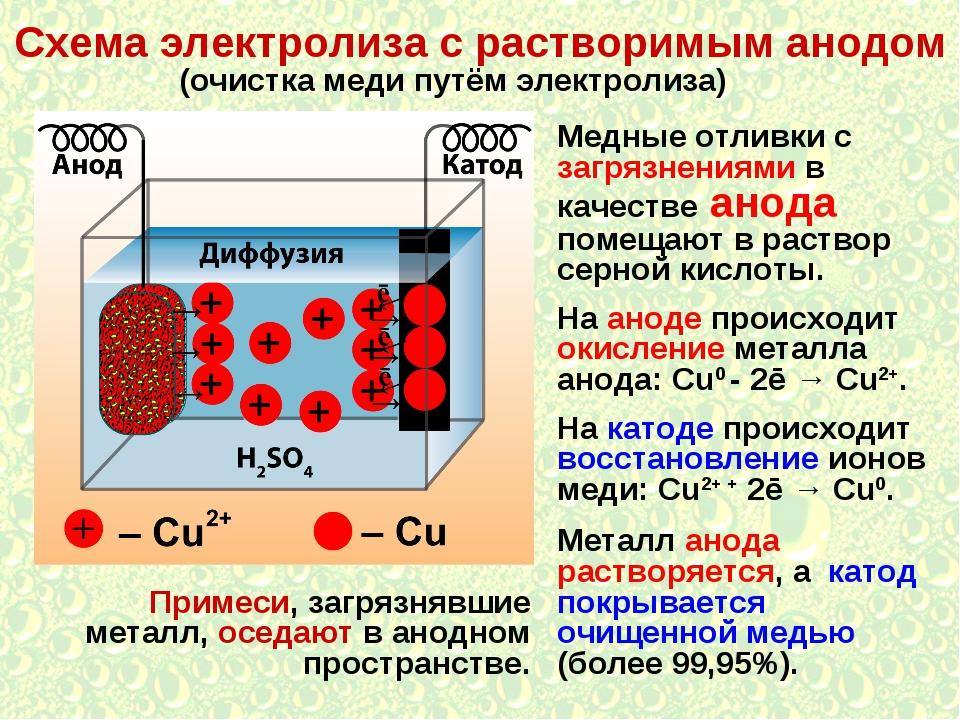
Электролиз с растворимыми электродами
В этом случае электролиз металлов осуществляется при помощи электродов, выполненных из того же М, который присутствует в электролите. Также электроды могут быть изготовлены из М активностью выше.
Важно! При протекании этого процесса на аноде восстанавливаются не анионы или молекулы H2O, а окисляется сам анод. Его частицы растворяются (окисляются) и восстанавливаются уже на катоде.
В случае с медным анодом при электролизе меди, где электролитом является сульфат меди, происходит следующее:
- ионы меди, входящие в раствор, восстанавливаются на катоде: Cu2+ + 2ē → Cu0;
- медный анод подвергается окислению своих частиц меди: Cu0 – 2ē → Cu2+.
Таким образом, если медную заготовку, имеющую примеси, использовать в качестве анода при гальванолизе в сульфате меди, то на катоде будет оседать медь в чистом виде. Анодный электрод при этом будет растворяться.
Вот перечень некоторых металлов, которые могут быть растворимыми электродами:
- медь (Cu);
- серебро (Ag);
- цинк (Zn);
- кобальт (Co);
- олово (Sn);
- никель (Ni);
- кадмий (Cd).
На растворимом аноде в начальной стадии электролиза процессы проходят при минимальном стандартном потенциале на электроде. Если электролиз не остановить, то значение потенциала отклоняется в отрицательную сторону. Это вызвано поляризацией из-за пребывания на катоде электронов.
К сведению. Потенциалы электродов могут отклоняться от их изначального значения в ходе электролиза. Это явление называют поляризацией. Она бывает электрохимической и концентрационной.
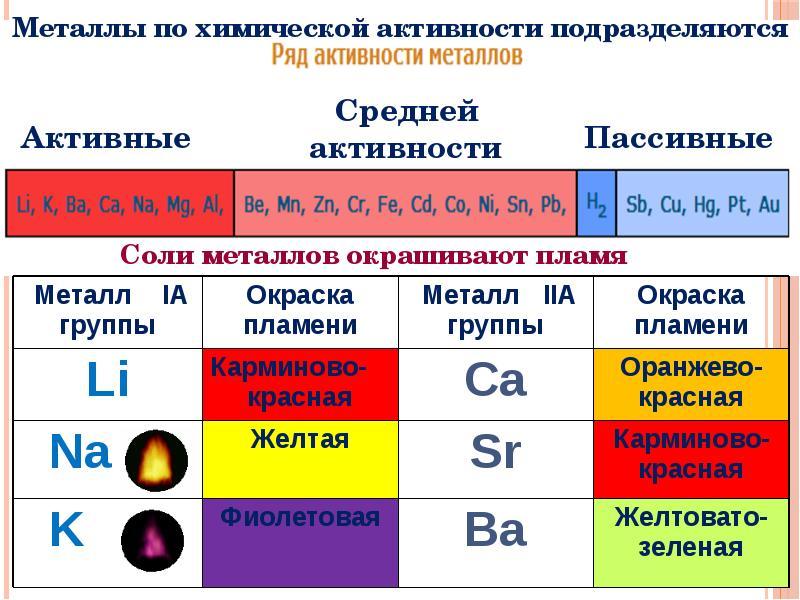
Активные металлы
Это тот тип металлов, который легко вступает в реакции. В периодической таблице это элементы 1-й и 2-й группы. Так как металлические свойства у элементов становятся слабее в ряду слева направо, то к ним относятся:
- щелочные металлы: литий, калий, натрий, цезий, франций, рубидий;
- щелочноземельные элементы: бериллий, магний, кальций, стронций, барий, радий;
- алюминий.
Данные металлы имеют один или два валентных электрона и легко их отдают, являясь восстановителями. К отличительным особенностям активных металлов относятся:
- мягкость;
- лёгкость;
- низкая температура плавления.
При взаимодействии с кислородом (на воздухе) щелочных металлов возможно самовозгорание. Самовозгорание щелочноземельных металлов происходит при повышении температуры. При взаимодействии их с водой образуются щёлочь и водород, вступая в реакцию с кислотами, они образуют соли.
Менее активные металлы и неактивные металлы
Среднюю активность проявляют металлы, стоящие в ряду после алюминия Al и до водорода H2.
К неактивным относятся элементы, стоящие правее водорода: медь (Cu), ртуть (Hg), серебро (Ag), платина (Pt), золото (Au).
Практическое применение в производстве
Такой электрохимический процесс, как электролиз, примеры которого можно увидеть повсеместно, является неотъемлемой частью промышленности:
- получение химически чистого сырья: фтор, хлор, щёлочи, чистые водород и кислород и т.д.;
- применение электролиза в гидрометаллургии: переработка сырья с содержанием металлов;
- элекрорафинирование (применение растворимых анодов) для окончательной очистки металлов;
- электроэкстракция (использование нерастворимых анодов) для выделения нужных металлов из растворов;
- гальванические процессы: гальванопластика и гальваностегия.
Информация. Процессы электролиза не протекают бесконтрольно. В цепь электролизёра включают медный кулонометр. Единица измерений прибора – 1 Кл (кулон). В этом случае контролируется количество результата (продукта) анодных, катодных реакций при 100%-ном выходе по току, необходимому для прохождения реакций.
Гальваностегия – способ электрохимического покрытия металлических поверхностей другими металлами:
- сталь подвергают никелированию, хромированию, оцинкованию;
- медь покрывают серебром, никелем и иными металлами.
Поверхность основания обрабатывают так, чтобы покрытие держалось крепко и защищало конструкцию от влияния внешних факторов. В то же время изделиям придавался эстетический вид.
Гальванопластика позволяет получать точные копии заготовки, выполненные из благородных металлов. Широко используется при изготовлении матриц, копий со скульптур, ювелирных изделий, деталей сложной геометрии. При этом способе важно, чтобы заготовка отделилась от покрытия.

Электролиз открывает широкие возможности для работы с металлами и электролитами. При помощи этого процесса можно самостоятельно выполнять работы не только в области гальванотехники, но и получать чистые металлы в небольших количествах. При этом не стоит путать самопроизвольные химические реакции в гальванических элементах и реакции, протекающие в электролизёрах.
Видео
Электролиз
Химические реакции, сопровождающиеся переносом электронов (окислительно-восстановительные реакции) делятся на два типа: реакции, протекающие самопроизвольно и реакции, протекающие при прохождении тока через раствор или расплав электролита.
Раствор или расплав электролита помещают в специальную емкость — электролитическую ванну .
Электрический ток — это упорядоченное движение заряженных частиц — ионов, электронов и др. под действием внешнего электрического поля. Электрическое поле в растворе или расплаве электролита создают электроды .
Электроды — это, как правило, стержни из материала, проводящего электрический ток. Их помещают в раствор или расплав электролита, и подключают к электрической цепи с источником питания.
При этом отрицательно заряженный электрод катод — притягивает положительно заряженные ионы — катионы . Положительно заряженный электрод ( анод ) притягивает отрицательно заряженные частицы ( анионы ). Катод выступает в качестве восстановителя, а анод — в качестве окислителя.

Различают электролиз с активными и инертными электродами. Активные (растворимые) электроды подвергаются химическим превращениям в процессе электролиза. Обычно их изготавливают из меди, никеля и других металлов. Инертные (нерастворимые) электроды химическим превращениям не подвергаются. Их изготавливают из неактивных металлов, например, платины , или графита .
Электролиз растворов
Различают электролиз раствора или расплава химического вещества. В растворе присутствует дополнительное химическое вещество — вода, которая может принимать участие в окислительно-восстановительных реакциях.
Катодные процессы
В растворе солей катод притягивает катионы металлов. Катионы металлов могут выступать в качестве окислителей. Окислительные способности ионов металлов различаются. Для оценки окислительно-восстановительных способностей металлов применяют электро-химический ряд напряжений :

Каждый металл характеризуется значением электрохимического потен-циала. Чем меньше потенциал , тем больше восстановительные свойства металла и тем меньше окислительные свойства соответствующего иона этого металла. Разным ионам соответствуют разные значения этого потенциала. Электрохимический потенциал — относительная величина. Электрохимический потенциал водорода принят равным нулю.
Также около катода находятся молекулы воды Н2О. В составе воды есть окислитель — ион H + .
При электролизе растворов солей на катоде наблюдаются следующие закономерности:
1. Если металл в соли — активный ( до Al 3+ включительно в ряду напряжений ), то вместо металла на катоде восстанавливается (разряжается) водород , т.к. потенциал водорода намного больше. Протекает процесс восстановления молекулярного водорода из воды, при этом образуются ионы OH — , среда возле катода — щелочная:
2H2O +2ē → H2 + 2OH —
Например , при электролизе раствора хлорида натрия на катоде будет вос-станавливаться только водород из воды.
2. Если металл в соли – средней активности (между Al 3+ и Н + ) , то на катоде восстанавливается (разряжается) и металл , и водород , так как потенциал таких металлов сравним с потенциалом водорода:
Me n+ + nē → Me 0
2 H + 2O +2ē → H2 0 + 2OH —
Например , при электролизе раствора сульфата железа (II) на катоде будет восстанавливаться (разряжаться) и железо, и водород:
Fe 2+ + 2ē → Fe 0
3. Если металл в соли — неактивный (после водорода в ряду стандартных электрохимических металлов) , то ион такого металла является более сильным окислителем, чем ион водорода, и на катоде восстанавливается только металл:
Например, при электролизе раствора сульфата меди (II) на катоде будет восстанавливаться медь:
Cu 2+ + 2ē → Cu 0
4. Если на катод попадают катионы водорода H + , то они и восстанавливаются до молекулярного водорода:
2H + + 2ē → H2 0
Анодные процессы
Положительно заряженный анод притягивает анионы и молекулы воды. Анод – окислитель. В качестве восстановителей выступаю либо анионы кислотных остаток, либо молекулы воды (за счет кислорода в степени окисления -2: H 2 O -2 ).
При электролизе растворов солей на аноде наблюдаются следующие закономерности:
1. Если на анод попадает бескислородный кислотный остаток , то он окисляется до свободного состояния (до степени окисления 0):
неМе n- – nē = неМе 0
Например : при электролизе раствора хлорида натрия на аноде окисляют-ся хлорид-ионы:
2Cl — – 2ē = Cl2 0
Действительно, если вспомнить Периодический закон: при увеличении электроотрицательности неметалла его восстановительные свойства уменьшаются. А кислород – второй по величине электроотрицательности элемент. Таким образом, проще окислить практически любой неметалл, а не кислород. Правда, есть одно исключение . Наверное, вы уже догадались. Конечно же, это фтор. Ведь электроотрицательность фтора больше, чем у кислорода. Таким образом, при электролизе растворов фторидов окисляться будут именно молекулы воды, а не фторид-ионы :
2H2 O -2 – 4ē → O2 0 + 4H +
2. Если на анод попадает кислородсодержащий кислотный остаток, либо фторид-ион , то окислению подвергается вода с выделением молекулярно-го кислорода:
3. Если на анод попадает гидроксид-ион, то он окисляется и происходит выделение молекулярного кислорода:
4 O -2 H – – 4ē → O2 0 + 2H2O
4. При электролизе растворов солей карбоновых кислот окислению под-вергается атом углерода карбоксильной группы, выделяется углекислый газ и соответствующий алкан.
Например , при электролизе растворов ацетатов выделяется углекислый газ и этан:
2 CH3 C +3 OO – –2ē → 2 C +4 O2+ CH3-CH3
Рассмотрим электролиз растворов различных солей.
Например , электролиз раствора сульфата меди. На катоде восстанавливаются ионы меди:
Катод (–): Cu 2+ + 2ē → Cu 0
На аноде окисляются молекулы воды:
Анод (+): 2H2 O -2 – 4ē → O2 + 4H +
Сульфат-ионы в процессе не участвуют. Мы их запишем в итоговом уравнении с ионами водорода в виде серной кислоты:
2 Cu 2+ SO4 + 2H2 O -2 → 2 Cu 0 + 2H2SO4 + O2 0
Электролиз раствора хлорида натрия выглядит так:
На катоде восстанавливается водород:
Катод (–): 2 H + 2O +2ē → H2 0 + 2OH –
На аноде окисляются хлорид-ионы:
Анод (+): 2 Cl – – 2ē → Cl2 0
Ионы натрия в процессе электролиза не участвуют. Мы записываем их с гидроксид-анионами в суммарном уравнении электролиза раствора хлорида натрия :
2 H + 2O +2Na Cl – → H2 0 + 2NaOH + Cl2 0
Следующий пример : электролиз водного раствора карбоната калия.
На катоде восстанавливается водород из воды:
На аноде окисляются молекулы воды до молекулярного кислорода:
Анод (+): 2H2 O -2 – 4ē → O2 0 + 4H +
Таким образом, при электролизе раствора карбоната калия ионы калия и карбонат-ионы в процессе не участвуют. Происходит электролиз воды:
2 H2 + O -2 → 2 H2 0 + O2 0
Еще один пример : электролиз водного раствора хлорида меди (II).
На катоде восстанавливается медь:
На аноде окисляются хлорид-ионы до молекулярного хлора:
Таким образом, при электролизе раствора карбоната калия происходит электролиз воды:
Cu 2+ Cl2 – → Cu 0 + Cl2 0
Еще несколько примеров: электролиз раствора гидроксида натрия.
На аноде окисляются гидроксид-ионы до молекулярного кислорода:
Анод (+): 4 O -2 H – – 4ē → O2 0 + 2H2O
Таким образом, при электролизе раствора гидроксида натрия происходит разложение воды, катионы натрия в процессе не участвуют:
При электролизе расплава на аноде окисляются анионы кислотных остатков, а на катоде восстанавливаются катионы металлов. Молекул воды в системе нет.
Например: электролиз расплава хлорида натрия. На катоде восстанавливаются катионы натрия:
Катод (–): Na + + ē → Na 0
На аноде окисляются анионы хлора:
Суммарное уравнение электролиза расплава хлорида натрия:
2 Na + Cl – → 2 Na 0 + Cl2 0

Еще один пример: электролиз расплава гидроксида натрия. На катоде восстанавливаются катионы натрия:
На аноде окисляются гидроксид-ионы:
Анод (+): 4 OH – – 4ē → O2 0 + 2H2O
Суммарное уравнение электролиза расплава гидроксида натрия:
4 Na + OH – → 4 Na 0 + O2 0 + 2H2O
Многие металлы получают в промышленности электролизом расплавов.
Например , алюминий получают электролизом раствора оксида алюминия в расплаве криолита. Криолит – Na3[AlF6] плавится при более низкой температуре (1100 о С), чем оксид алюминия (2050 о С). А оксид алюминия отлично растворяется в расплавленном криолите.
В растворе криолите оксид алюминия диссоциирует на ионы:
На катоде восстанавливаются катионы алюминия:
Катод (–): Al 3+ + 3ē → Al 0
На аноде окисляются алюминат-ионы:
Анод (+): 4Al O 3 3 – – 12ē → 2Al2O3 + 3 O2 0
Общее уравнение электролиза раствора оксида алюминия в расплаве криолита:
2 Al 2 О 3 = 4 Al 0 + 3 О 2 0

В промышленности при электролизе оксида алюминия в качестве электродов используют графитовые стержни. При этом электроды частично окисляются (сгорают) в выделяющемся кислороде:
C 0 + О2 0 = C +4 O2 -2
Если материал электродов выполнен из того же металла, который присутствует в растворе в виде соли, или из более активного металла, то на аноде разряжаются не молекулы воды или анионы, а окисляются частицы самого металла в составе электрода.
Например , рассмотрим электролиз раствора сульфата меди (II) с медными электродами.
На катоде разряжаются ионы меди из раствора:
На аноде окисляются частицы меди из электрода :
Анод (+): Cu 0 – 2ē → Cu 2+
Практическое применение электролиза
При прохождении через раствор или расплав электролита электрического тока, на электродах происходит выделение растворенных веществ или иных веществ, являющихся продуктами вторичных реакций на электродах. Этот физико-химический процесс и называется электролизом.

Суть электролиза
В создаваемом электродами электрическом поле, ионы в проводящей жидкости приходят в упорядоченное движение. Отрицательный электрод — это катод, положительный — анод.
К аноду устремляются отрицательные ионы, называемые анионами (ионы гидроксильной группы и кислотные остатки), а к катоду — положительные ионы, называемые катионами (ионы водорода, металлов, аммония и т. д.)
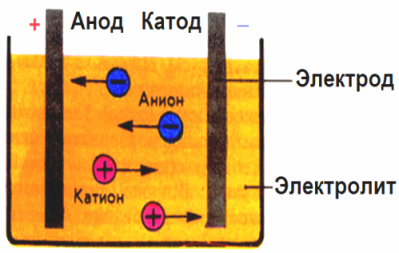
На электродах протекает окислительно-восстановительный процесс: на катоде происходит электрохимическое восстановление частиц (атомов, молекул, катионов), а на аноде — электрохимическое окисление частиц (атомов, молекул, анионов). Реакции диссоциации в электролите — это первичные реакции, а реакции, которые протекают непосредственно на электродах, называются вторичными.
Законы электролиза Фарадея
Разделение реакций электролиза на первичные и вторичные помогло Майклу Фарадею установить законы электролиза:
Первый закон электролиза Фарадея: масса вещества, осаждённого на электроде при электролизе, прямо пропорциональна количеству электричества, переданного на этот электрод. Под количеством электричества имеется в виду электрический заряд, измеряемый, как правило, в кулонах.
Второй закон электролиза Фарадея: для данного количества электричества (электрического заряда) масса химического элемента, осаждённого на электроде, прямо пропорциональна эквивалентной массе элемента. Эквивалентной массой вещества является его молярная масса, делённая на целое число, зависящее от химической реакции, в которой участвует вещество.
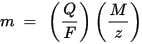
m — масса осаждённого на электроде вещества, Q — полный электрический заряд, прошедший через вещество F = 96 485,33(83) Кл·моль−1 — постоянная Фарадея, M — молярная масса вещества (Например, молярная масса воды H2O = 18 г/моль), z — валентное число ионов вещества (число электронов на один ион).
Заметим, что M/z — это эквивалентная масса осаждённого вещества. Для первого закона Фарадея M, F и z являются константами, так что чем больше величина Q, тем больше будет величина m. Для второго закона Фарадея Q, F и z являются константами, так что чем больше величина M/z (эквивалентная масса), тем больше будет величина m.
Электролиз широко применяется сегодня в промышленности и в технике. Например, именно электролиз служит одним из эффективнейших способов промышленного получения водорода, пероксида водорода, диоксида марганца, алюминия, натрия, магния, кальция и прочих веществ. Применяется электролиз для очистки сточных вод, в гальваностегии, в гальванопластике, наконец — в химических источниках тока. Но обо всем по порядку.
Получение чистых металлов из руд путем электролиза
Благодаря электролизу многие металлы извлекается из руд и подвергается дальнейшей переработке. Так, когда руду или обогащенную руду — концентрат — подвергают обработке реагентами, металл переходит в раствор, затем путем электроэкстракции металл выделяют из раствора. Чистый металл выделяется при этом на катоде. Таким путем получают цинк, медь, кадмий.
Электрорафинированию металлы подвергают для устранения примесей и чтобы перевести содержащиеся примеси в удобную для дальнейшей переработки форму. Металл, подлежащий очистке, отливают в виде пластин, и применяют эти пластины в качестве анодов при электролизе.
Когда ток проходит, металл анода растворяется, переходит в виде катионов в раствор, затем катионы разряжаются на катоде, и образуют осадок чистого металла. Примеси анода не растворяются - выпадают анодным шламом, или переходят в электролит, откуда непрерывно или периодически удаляются.
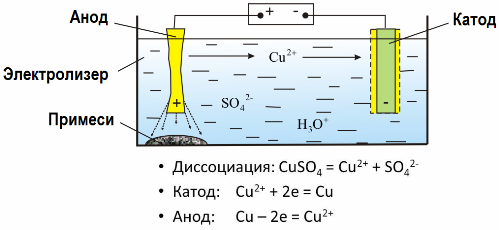
Рассмотрим в качестве примера электрорафинирование меди. Главный компонент раствора - сульфат меди — наиболее распространенная и дешевая соль этого металла. Раствор обладает низкой электрической проводимостью. Для ее увеличения в электролит добавляют серную кислоту.
Кроме того, в раствор вводят небольшие количества добавок, способствующих получению компактного осадка металла. Вообще, электролитическому рафинированию подвергают медь, никель, свинец, олово, серебро, золото.
Очистка сточных вод путем электролиза
Электролиз находит применение в очистке сточных вод (процессы электрокоагуляции, электроэкстракции и электрофлотации). Электрохимический метод очистки — один из наиболее часто применяемых. Для электролиза используют нерастворимые аноды (магнетит, оксид свинца, графит, марганец, которые наносят на титановую основу), или растворимые (алюминий, железо).
Такой метод применяют для выделения из воды токсичных органических и неорганических веществ. К примеру, медные трубы очищают от окалины раствором серной кислоты, и промышленные сточные воды приходится затем очищать путем электролиза с нерастворимым анодом. На катоде выделяется медь, которая снова может использоваться на том же предприятии.
Щелочные сточные воды очищают электролизом от цианистых соединений. С целью ускорения окисления цианидов, повышения электропроводности и экономии электроэнергии, к водам применяют добавку в виде хлорида натрия.
Электролиз проводят с графитовым анодом и стальным катодом. Цианиды разрушаются в ходе электрохимического окисления и хлором, который выделяется на аноде. Результативность такой очистки близка к 100%.
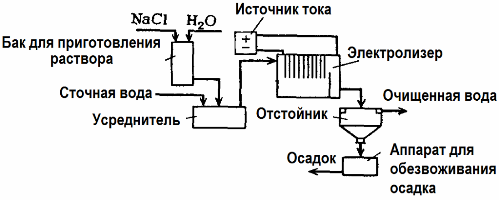
Кроме непосредственно электохимической очистки можно включить в процесс электролиза коагуляцию. Исключив добавки солей, электролиз проводят с растворимыми алюминиевыми или железными анодами. Тогда не только разрушаются загрязнители на аноде, но и растворяется сам анод. Образуются активные дисперсные соединения, которые коагулируют (сгущают) коллоидно-дисперсные загрязнения.
Этот метод эффективен при очистке сточных вод от жиров, нефтепродуктов, красителей, масел, радиоактивных веществ и т. д. Он называется электрокоагуляцией.
Гальваностегия
Гальваностегия — это электролитическое нанесение определенных металлов с целью защиты изделий от коррозии и для придания им соответствующего эстетического оформления (покрытие производят хромом, никелем, серебром, золотом, платиной и т. п.). Вещь тщательно очищают, обезжиривают, и используют как катод в электролитической ванне, в которую налит раствор соли того металла, которым необходимо покрыть изделие.
В качестве анода применяют пластину из этого же металла. Как правило применяют пару анодных пластин, а подлежащий гальваностегии предмет располагают между ними.
Гальванопластика
Гальванопластика - осаждение металла на поверхности разных тел для воспроизведения их формы: формы для отливки деталей, скульптур, печатных клише и т.д.

Гальваническое осаждение металла на поверхности предмета возможно лишь тогда, когда поверхность эта или весь предмет являются проводниками электрического тока, поэтому для изготовления моделей или форм желательно использовать металлы. Наиболее подходят для этой цели легкоплавкие металлы: свинец, олово, припои, сплав Вуда.
Эти металлы мягки, легко обрабатываются слесарным инструментом, хорошо гравируются и отливаются. После наращивания гальванического слоя и отделки металл формы выплавляют из готового изделия.
Однако наибольшие возможности для изготовления моделей все же представляют диэлектрические материалы. Чтобы металлизировать такие модели, нужно придать их поверхности электропроводность. Успех или неудача в конечном итоге зависят в основном от качества токопроводящего слоя. Слой этот может быть нанесен одним из трех способов.
Самый распространенный способ — графитирование, он пригоден для моделей из пластилина и других материалов, допускающих растирание графита по поверхности.
Следующий прием — бронзирование, способ хорош для моделей относительно сложной формы, для разных материалов, однако за счет толщины бронзового слоя несколько искажается передача мелких деталей.
И, наконец, серебрение, пригодное во всех случаях, но особенно незаменимое для хрупких моделей с очень сложной формой — растений, насекомых и т. п.
Химические источники тока
Также электролиз является основным процессом, благодаря которому функционируют самые современные химические источники тока, например батарейки и аккумуляторы. Здесь присутствуют два электрода, контактирующие с электролитом.
Между электродами устанавливается разность потенциалов — электродвижущая сила, соответствующая свободной энергии окислительно-восстановительной реакции. Подробнее смотрите здесь: Химические источники электрического тока
Лимонная батарейка (для увеличения нажмите нажмите на картинку)

Подробнее о том, как работает такая батарейка смотрите здесь: Как сделать батарейку из лимона в домашних условиях
Действие химических источников тока основано на протекании при замкнутой внешней цепи пространственно-разделённых процессов: на отрицательном аноде восстановитель окисляется, образующиеся свободные электроны переходят по внешней цепи к положительному катоду, создавая разрядный ток, где они участвуют в реакции восстановления окислителя. Таким образом, поток отрицательно заряженных электронов по внешней цепи идет от анода к катоду, то есть от отрицательного электрода к положительному.

Электролизом называется окислительно-восстанови-тельный процесс, протекающий на электродах при прохождении постоянного электрического тока через раствор или расплав электролита. Химические реакции протекают на электродах за счет электрической энергии. При электролизе катод является восстановителем, так как он отдает электроны, а анод — окислителем, так как он принимает электроны от анионов.
Например, если в раствор хлорида меди опустить электроды и пропустить постоянный электрический ток, то ионы меди будут двигаться к катоду, а ионы хлора — к аноду. На катоде происходит процесс восстановления: Cu2f + 2ё « Си, а на аноде — окисления: 2СГ - 2ё- С12. В итоге на катоде будет выделяться медь, а на аноде — хлор. Восстановительное и окислительное действие электрического тока во много раз сильнее химических восстановителей и окислителей.
Ни один химический окислитель не может отнять у иона фтора его электрон. Окислить ион фтора удалось лишь при электролизе расплава смеси безводного жидкого фтороводорода с фторидом калия. На угольном аноде выделяется фтор: 2F" - 2ё = F2, а на никелевом катоде — водород: 2Н+ + 2ё = Н2. Различают электролиз расплавов и растворов электролитов. Процессы в расплавленных электролитах — наи- более простой случай электролиза.
Так, в расплаве хлорида натрия содержатся ионы Na+ и С Г. При пропускании через него электрического тока ионы Na+ у катода присоединяют электроны и восстанавливаются до атомов натрия, ионы хлора СГу анода отдают электроны и окисляются до атомов хлора, которые затем образуют молекулы. Пример 1 Схема электролиза расплава NaCl расплав 2 процесс восстановления 1 процесс окисления электролиз 2NaCl -Г 2Na + CLf. Пример 2 Схема электролиза расплава СаВг2 1 процесс восстановления 1 процесс окисления электролиз СаВг2 Са + Вг2. Пример 3
Схема электролиза расплава КОН КОН К+ + ОН". расплав 4 процесс восстановления 1 процесс окисления электролиз — ионное уравнение электролиз — молекулярное урав- нение Если электролизу подвергается расплав, который содержит несколько различных катионов, то в этом случае последовательность восстановления определяется электродным потенциалом металла в данных условиях. В первую очередь восстанавливаются катионы металлов, обладающие большим значением электродного потенциала.
Более сложные процессы протекают при электролизе водных растворов электролитов, поскольку в этих процессах принимает участие вода. Рассмотрим электролиз концентрированного раствора хлорида натрия. В этом случае в растворе, кроме гидратированных ионов натрия и хлора, присутствуют молекулы воды и продукты ее диссоциации, которые участвуют в электродных реакциях. При прохождении тока через раствор к катоду будут двигаться катионы натрия и водород, а к аноду — хлорид и гидроксид-ионы. По этой причине реакции, протекающие на электродах, будут существенно отличаться от реакций, идущих в расплаве соли.
Возможно вам будут полезны данные страницы:
На катоде, вместо ионов натрия, будут восстанавливаться молекулы воды и ионы водорода, поскольку они обладают большей окислительной способностью с ионами натрия. На аноде происходит окисление хлорид-ионов (обладающих большей восстановительной способностью по сравнению с гидроксид-ионами). Пример 4 Схема электролиза раствора NaCl , расплав 1 процесс восстановления 1 процесс окисления электролиз электролиз 2NaCl + 2Н20 — Н2| + С12| + 2NaOH — молекулярное уравнение.
Последовательность, в которой происходит разряд ионов на катоде из растворов солей, определяется рядом стандартных электродных потенциалов, в котором металлы располагаются в ряд по нарастанию алгебраической величины их нормальных электродных потенциалов. Поясним, как образуется ряд стандартных электродных потенциалов. Погружение металла в раствор одноименной соли приводит к процессам перехода ионов металла с поверхности металла в раствор — растворение металла, или из раствора в металл — осаждение металла.
Вследствие этих процессов поверхность металла (электрода) приобретает положительный или отрицательный заряд, причем его величина и знак будут определяться природой металла, концентрацией соли в растворе и температурой. Гидратированные катионы и анионы, находящиеся в растворе, притягиваются заряженными поверхностями металлов, в результате чего на поверхности раздела металл-раствор образуется два слоя с противоположными зарядами — так называемый двойной электрический слой.
Разность потенциалов этого слоя носит название электродного потенциала. Непосредственно измерить величину потенциала отдельного электрода не представляется возможным. Поэтому электродные потенциалы измеряют путем сопоставления с потенциалом принятого для сравнения электрода. В качестве последнего обычно применяют стандартный водородный электрод, величину потенциала которого условно принимают за ноль. Этот электрод состоит из платиновой пластинки, покрытой платиновой чернью (электролитически осажденной платиной), которая погружена в 1 М раствор серной кислоты и омывается струей газообразного водорода под давлением 1 атм.
Если теперь пластинку любого металла, погруженную в раствор его соли, содержащий 1 моль ионов металла в 1000 г воды, соединить с водородным электродом с помощью так называемого «электролитического ключа», то получится гальванический элемент, электродвижущую силу которого (ЭДС) легко измерить. Эта ЭДС, измеренная при 25 °С, называется стандартным электродным Ряд стандартных электродных потенциалов металлов потенциалом данного металла.
Располагая металлы в порядке возрастания алгебраической величины их стандартных электродных потенциалов, получают ряд стандартных электродных потенциалов металлов.- Чем левее металл в ряду стандартных потенциалов, тем труднее его ион разряжается при электролизе. При этом возможны три случая: (TJ Катионы металлов, имеющих стандартный потенциал больший, чем у водорода (от Си2+ до Аи3+), прн электролизе практически полностью восстанавливаются на катоде.
(Т) Катионы металлов, имеющих малую величину стандартного электродного потенциала (от Li+ до А13+ включительно), не восстанавливаются на катоде, а вместо них восстанавливаются молекулы воды. [з] Катионы металлов, имеющих стандартный электродный потенциал меньший, чем у водорода, но больший, чем у алюминия (от А13+ до Н2), при электролизе на катоде восстанавливаются одновременно с молекулами воды. Если же водный раствор содержит катионы различных металлов, то при электролизе выделение их на катоде протекает в порядке уменьшения алгебраической величины стандартного электродного потенциала соответствующего металла.
Так, из смеси катионов Ag+, Cu2+, Zn2+ сначала будут восстанавливаться катионы серебра, затем катионы меди и последними — катионы цинка. Характер реакций, протекающих на аноде, зависит как от присутствия молекул воды, так и от вещества, из которого сделан анод. Аноды бывают нерастворимые и растворимые. Первые изготавливаются из угля, графита, платины (в процессе электролиза они не переходят в раствор в виде ионов); вторые — из меди, серебра, цинка, кадмия, никеля и др. металлов (в процессе электролиза переходят в раствор в виде ионов, т. е. разрушаются).
На нерастворимом аноде в процессе электролиза происходит окисление анионов или молекул воды. При этом анионы бескислородных кислот и их солей (СГ, Br", I", S2") окисляются у анода. При электролизе водных растворов щелочей кислоро-досодержащих кислот и их солей (S042~, N03", С032~, Р043~), а также фторидов на аноде происходит электрохимическое окисление воды с выделением кислорода. Рассмотрим возможные случаи электролиза раствора солей на угольных электродах (электроды не участвуют в окислительно-восстановительных реакциях). Электролиз раствора соли, образованной активным металлом, стоящим в ряду напряжений до алюминия и кислотным остатком кислородосодержащей кислоты сводится к электролизу воды.
Пример 5 Схема электролиза водного раствора MgS04 MgS04 т± Mg2+ + SO2", раствор электролиз Учитывая, что 4Н+ + 40Н" — 4Н20, электролиз 2Н20 - 2H2t+02|. Электролиз раствора соли, образованной малоактивным металлом, стоящим в ряду напряжений после водорода, и кислотным остатком кислородосодержащей кислоты. В данном случае при электролизе получается металл, кислород, а в катодно-анодном пространстве образуется соответствующая кислота. Пример 6 Схема электролиза водного раствора CuS04 CuS04 Cu2+ + SO2", процесс восстановления 1 процесс окисления K(-): Cu2+ + 2ё Си0 электролиз электролиз 2CuS04 + 2Н20 — 2Cu + 021 + 2H2S04.
Электролиз раствора соли, образованной активным металлом (до А1) и кислотным остатком галогено-водородной кислоты. При электролизе получается водород, галоген, в катодно-анодном пространстве — щелочь. Пример 7 Схема электролиза водного раствора СаС12 СаС12 Са2+ + 2СГ, раствор НОН Н+ + ОН~. 1 процесс восстановления 1 процесс окисления электролиз , электролиз Электролиз раствора соли, образованный малоактивным металлом и кислотным остатком галоге-новодородной кислоты.
При электролизе получается металл и галоген. Пример 8 Схема электролиза водного раствора , раствор 1 процесс восстановления А(+): 2С1 - 2ё С12 1 процесс окисления лектролиз электролиз Если соль образована металлом, стоящим в ряду напряжения от алюминия до водорода и в процессе восстановления принимает участие вода, то процесс электролиза идет в зависимости от концентрации раствора соли. Чем менее концентрированный раствор, тем менее интенсивно восстанавливается металл. P^J Пример 9 Схема электролиза водного раствора Ni(N03)2 раствор 1 процесс окисления электролиз '2 2 1 1 ' электролиз P^l Пример 10 I
Схема элек электролиза водного раствора NaOH NaOH Na+ 4- ОН", раствор НОН Н+ 4- ОН". > 1 процесс восстановления / электролиз электролиз 2Н20 -V 2H?t + 0„t • 2 процесс восстановления 1 процесс окисления Пример 11 Схема электролиза водного раствора HgSC^ H2S04 2Н* + so;-, раствор НОН Н+ + ОН". nsr 2 процесс восстановления 1 процесс окисления электролиз электролиз 2На0 - 2H2t+02t-Растворимый анод при электролизе сам подвергается окислению (растворению), т. е. посылает электроны во внешнюю цепь.
Так, при электролизе раствора сульфата никеля с никелевым анодом процесс сводится к выделению никеля на катоде и постепенному растворению анода. Количество сульфата никеля в растворе остается неизменным. Пример 12 Схема электролиза водного раствора NiS04 с растворимым анодом раствор Количественно процесс электролиза описывается законами Фарадея: |Т) Количество вещества, восстановленного на катоде или окисленного на аноде, пропорционально количеству прошедшего через раствор или расплав электричества: m-kM^Q, где т — масса окисленного или восстановленного вещества; его молярная масса эквивалента;.
Q — количество электричества, прошедшего через электролит; к — коэффициент пропорциональности. [2] Количество окисляющихся или восстанавливающихся на электродах веществ при пропускании одного и того же количества электричества пропорциональны их молярным массам эквивалентов. Оба закона Фарадея можно выразить общей формулой: где F — число Фарадея. Учитывая, что количество электричества Q равно произведению силы тока J в амперах на время т в секундах, формулу можно написать так:
Величина Е называется электрохимическим эквивалентом вещества и характеризует собой массу вещества, которое восстанавливается на катоде или окисляется на аноде при прохождении через электролит одного кулона электричества. Молярная масса эквивалента связана с электрохимическим эквивалентом отношением: - EF.
Пример 13 Вычислите объем кислорода, выделившегося на угольном аноде при пропускании через разбавленный раствор серной кислоты тока силой 5 А в течение часа.
Дано: Найти: У(02) Решение: 1) Уравнение электролиза: электролиз 2) Находим количество электричества: ? = /• г; Q = 5 • 3600 = 18 ООО Кл. 3) Определим массу кислорода, выделившегося на аноде: 4) Найдем, какой объем при н. у. займет 1,492 г кислорода. Для этого сначала найдем количество вещества: 1,492 Y(Oz) - 32 - 0,047 моль. Откуда V(02) = 0,047 • 22,4 = 1,044 л. Ответ: V(02) = 1,044 л. Пример 14 Рассчитайте время, необходимое для полного выделения хлора, содержащегося в 2 л 0,5 Н раствора хлорида калия при электролизе этого раствора током силой 5 А. Дано: V(C\2) - 2 л СН(КС1) = 0,5 1=5 А
Найти: Решение: Определяем, что в 2 л 0,5 Н раствора хлорида калия содержится: 2 • 0,5 e 1 моль • экв. соли, для разложения которой требуется 96 500 Кл. Исходя из этого: Q 96 500 т = —, т = ——— = 321,8 мин = 5,3 ч. • I 5 • 1 Ответ: т= 5,3 час. Пример 15 Между какими из следующих попарно взятых веществ, формулы которых даны ниже (электролит берется в виде водного раствора), будет протекать реакция замещения: а) А1 + Cu(N03)2; б) Zn + MgS04.
Напишите уравнения реакции в ионной форме. Решение: В рассматриваемых реакциях замещения свободный металл будет вытеснять металл из соли в раствор в том случае, если он обладает большей восстановительной способностью по сравнению с металлом, образующим соль. Сравнивая пары металлов— А1 и Си; Zn и Mg, мы видим из их положения в электрохимическом ряду напряжений, что реакция замещения возможна только в первом случае и она отразится следующим уравнением: 2А1° + 3Cu2f - 3Cu° + 2AI8*. Применение электролиза расплавов и растворов огромно.
Такие ценные металлы, как алюминий, натрий, цинк, олово, свинец, кадмий, серебро, золото, получают исключительно путем электролиза. В производстве никеля, магния, меди, белой жести электрохимическая продукция составляет 80-90 %. Хлор и его кислородные соединения в промышленности получают также электрохимически. Все шире развиваются электрохимические методы получения органических соединений. Электролиз начинают применять для обессоливания воды, для укрепления грунтов за счет удаления воды (электроосмос).
Его развитие тесно связано с проблемой получения чистых и особо чистых материалов. Ни одна отрасль машиностроения не может обойтись без электрохимических методов обработки поверхности металлических изделий. Электрохимическим методом наносят металлические покрытия, которые предохраняют металл от ржавчины. Электролиз используют для получения точных копий с различных предметов — гальванопластика. Предмет, с которого хотят получить копию, покрывают воском и получают матрицу.
| Поверхность восковой матрицы покрывают |
тонким слоем графита, делая ее проводящей электрический ток. Графитовый катод опускают в ванну с раствором сульфата меди, анодом служит медь. При электролизе медный анод растворяется, а на катоде осаждается медь. С помощью гальванопластики изготавливаются клише для печати матрицы грампластинок, металлизируют различные предметы. Электролиз используют для очистки металлов от примесей. Рафинирование (очистка) меди основано на анодном растворении металла.
В больших ваннах подвешивают ряд пластин из черновой меди, а между ними — тонкие пластинки чистой меди, заливают электролит и пропускают ток. Анод — черновая медь — растворяется, а на пластинках из чистой меди, которые служат катодом, нарастает слой очищенной меди. Электролитическая медь содержит 99,97 % чистой меди. Вопросы и задачи для самостоятельного решения 1. Укажите отличие проводников первого рода от проводников второго рода.
2. Укажите, от каких факторов зависит последователь- ность расположения металлов по величинам их электродных потенциалов. 3. Объясните, почему электродные потенциалы металлов имеют положительный или отрицательный знак. 4 Объясните, почему последовательность изменения активности металлов в ряду стандартных электродных потенциалов не совпадает с последовательностью изменения активности металлов в группах и периодах периодической системы.
5. Цинковые пластинки опущены в растворы нитратов калия, кальция, никеля и свинца. В каких случаях будут протекать химические реакции? Напишите соответствующие уравнения процессов в молекулярной и ионно-молекулярной формах. 6. Какая масса технического цинка, содержащего 2 % примесей, требуется для вытеснения из раствора нитрата меди (II) 6,35 г меди? Ответ: 6,67 г. 7. Какие процессы, протекающие на электродах, объединяются общим названием * электролиз*?
8. Чем вызвана необходимость пространственного разделения процессов, протекающих на электродах? 9. Объясните, чем определяется последовательность восстановления катионов на катоде при электролизе растворов электролитов? 10. Какие факторы предопределяют выбор материала для электродов при проведении процесса электролиза? 11. Какими показателями оценивается эффективность процессов электролиза?
12. При получении каких веществ в народном хозяйстве используется электролиз? 13. Составьте схемы электролиза водного раствора нитрата цинка, если: а) анод угольный; б) анод цинковый. 14. Какие химические процессы происходят у катода и у анода при электролизе раствора иодида натрия. 15. Чем отличается электролиз расплава едкого натра "От электролиза его раствора? Какие вещества и в каком количестве выделяются при электролизе раствора едкого натра, если через раствор пропускают ток силой 10 А в течение 10 ч 44 мин? Ответ: 44,8 л Н2 и 22,4 л 02 (н. у.).
16. Какое количество продуктов будет получено при электролизе расплава едкого натра током силой 0,6 А в течение Зч? Ответ: 1,54 г Na; 0,38 л 02 (н. у.). 17. Будет ли меняться в ходе электролиза водного раствора гидроксида калия: масса гидроксида калия в растворе; концентрация раствора? Почему? 18. Какое количество электричества необходимо пропустить через раствор поваренной соли для получения 1 г едкого натра? Ответ: 2412,5 Кл. 19. С каким полюсом батареи — положительным или отрицательным — должна быть соединена металлическая деталь при ее хромировании?
20. Определите объем водорода, выделившегося на катоде (н. у.) при электролизе водного раствора серной кислоты, если известно, что при этом вступило в реакцию 1,505' 1024 электронов. Ответ: 28 л. 21. При прохождении через раствор соли трехвалентного металла тока силой ЗА в течение 15 мин на катоде выделилось 1,071 г металла. Определите атомную массу металла. Ответ: 114,9. 22.
При электролизе раствора нитрата хрома (III) током силой 1 А масса хромового катода возросла на 10 г. Какое количество электричества было пропущено через раствор и в течение какого времени? Ответ: 55700 Кл; 15 ч 28 мин. 23. Через раствор нитрата никеля (II) в течение 2 ч 27 мин пропускали ток силой 3,5 А. Определите, на сколько граммов за это время уменьшилась масса никелевого анода. Ответ: 9,4 г. 24. При электролизе током силой 2 А в течение 40 мин на катоде выделилось 4,542 г некоторого металла. Определите молярную массу эквивалента этого металла. Ответ: 91,3 г.
Присылайте задания в любое время дня и ночи в ➔
Официальный сайт Брильёновой Натальи Валерьевны преподавателя кафедры информатики и электроники Екатеринбургского государственного института.
Сайт предназначен для облегчения образовательного путешествия студентам очникам и заочникам по вопросам обучения . Наталья Брильёнова не предлагает и не оказывает товары и услуги.
Читайте также:
