Самый активный металл имеет схему строения атома
Обновлено: 05.05.2024
За лето ребенок растерял знания и нахватал плохих оценок? Не беда! Опытные педагоги помогут вспомнить забытое и лучше понять школьную программу. Переходите на сайт и записывайтесь на бесплатный вводный урок с репетитором.
Вводный урок бесплатно, онлайн, 30 минут
Предварительный просмотр:
Контрольная работа в рамках итоговой аттестации по химии в 8 классе
Каждое правильно выполненное задание части 1 (с выбором ответа) оценивается в 1 балл. Правильным считается, если обведен только один номер верного ответа.
Задание части 2 (с кратким ответом) считается выполненным верно, если указанные в ответе цифры (и их порядок) соответствуют правильно выбранным вариантам ответа. Полный правильный ответ оценивается 2 баллами, за неполный правильный ответ – 1 балл, за неверный ответ (или его отсутствие) – 0 баллов.
Задание части 3 (с развёрнутым ответом) считается выполненным верно, если правильно записаны три уравнения реакций (3 балла). Правильно записаны 2 уравнения реакций – 2 балла. Правильно записано одно уравнение реакции – 1 балл.
Максимальное количество баллов представлено в таблице 1.
Максимальное количество баллов
Итоговая контрольная работа
Оценивание работы представлено в таблице 2. Таблица 2
А1. К неметаллам относится:
1) 2,8,2; 2) 2,8,3; 3) 2,8,8,2; 4) 2,8,7
А2. К химическим явлениям относится:
1) плавление парафина; 2) дробление горной породы;
3) скисание молока; 4) замерзание воды
А3. С соляной кислотой реагируют каждое из пары веществ:
1) медь, гидроксид меди (2); 2) натрий, гидроксида натрия;
3) серная кислота, оксид серы (4); 4) вода, гидроксид калия
А4. Сумма коэффициентов в уравнении реакции между серной кислотой и оксидом калия равна: 1) 4; 2) 5; 3) 6; 4) 8
А5. Верны ли следующие суждения:
А. Лакмус в растворе кислоты краснеет
Б. Кислород собирают вытеснением воздуха, держа пробирку вверх дном
1) верно только А; 2) верно только Б; 3) верны оба суждения; 4) оба суждения неверны.
А6. Масса соли, находящейся в растворе массой 300 г.с массовой долей растворённого вещества 50%, равна: 1) 6 г.; 2) 160 г.; 3) 150 г.; 4) 600 г.
А7. Масса гидроксида натрия, вступившего в реакцию с 2 моль серной кислоты равна:
1) 1,6 г.; 2) 80 г.; 3) 120 г.; 4) 160 г.
В1. Выберите реакции замещения из данных уравнений реакций:
1) К 2 S + H 2 SO 4 = H 2 S + К 2 SO 4 ; 2) Zn + FeCI 2 = ZnCI 2 + Fe;
3) 2NH 3 = 3H 2 + N 2 ; 4) H 2 + Ca = CaH 2
5) H 2 S O 4 + Ca = Ca S O 4 + H 2 ;
В2. Установите соответствие между уравнениями реакций и ошибками в их написании.
А) CaO + 2 НSO 4 = СaSO 4 + H 2 O
1) в 1 формуле и расстановке коэффициентов
Б) HCI + NaOH = NaCI + H 2 O
2) в 2 формулах и расстановке коэффициентов
В) HPO 4 + AlOH = AlPO 4 + H 2 O
3) в расстановке коэффициентов
С1. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
P —> P 2 O 5 —> H 3 PO 4 —> Na 3 PO 4
А1. Самый активный металл имеет схему строения атома:
1) 2,1; 2) 2,2; 3) 2,8,1; 4) 2,8,2
А2. Чистое вещество – это: 1) глина; 2)соль; 3) варенье; 4) молоко
А3. С гидроксидом натрия реагируют каждое из пары веществ:
3) вода, гидроксид калия; 4) серная кислота, оксид серы (4)
А4. Сумма коэффициентов в уравнении реакции между азотной кислотой и гидроксидом меди(II) равна: 1) 4; 2) 5; 3) 6; 4) 8
А5. Верны ли следующие суждения о правилах безопасной работы в химической лаборатории?
А. При нагревании вещества не касаться дном пробирки фитиля спиртовки.
Б. Не направлять пробирку с нагреваемой жидкостью в сторону соседа
А6. Массовая доля кислорода в нитрате алюминия равна: 1) 80%; 2) 67%; 3) 58%.; 4) 1%;
А7. Масса воды, полученной при взаимодействии 11,2 л. кислорода с водородом равна:
1) 18 г.; 2) 36 г.; 3) 201 г.; 4) 403 г.
В1. . Выберите реакции обмена из данных уравнений реакций:
5) H 2 S O 4 + CaО = Ca S O 4 + H 2 O;
Контрольная работа в рамках итоговой аттестации по химии в 9 классе по Рудзитису
материал по химии (9 класс) по теме
В материалах представлено 2 варианта работы по методическому комплексу Рудзитиса. работа содержит 3 части. Даны нормы оценивания работы.Работа проводится в декабре после изучения материала по азоту и соединениям азота.
| Вложение | Размер |
|---|---|
| krv_ramkah_it_att_dekabr9_klassrudzit.docx | 26.53 КБ |
Подтяните оценки и знания с репетитором Учи.ру
Контрольная работа в рамках итоговой аттестации по химии в 9 классе
А2. Сумма коэффициентов в уравнении реакции между серной кислотой и оксидом калия равна:
1) 4; 2) 5; 3) 6; 4) 8
А3. Электрический ток проводит:
1) водный раствор спирта; 2) раствор гидроксида натрия;
3) расплав сахара; 4) водный раствор глюкозы.
А4. Практически необратимо протекает реакция ионного обмена между растворами:
1) гидроксидом натрия и сульфатом меди(II); 2) хлоридом кальция и нитратом бария;
3) гидроксидом калия и нитратом натрия; 4) серной кислотой и хлоридом натрия.
А5. В реакцию с аммиаком вступает:
1) хлорид натрия; 2) водород; 3) соляная кислота; 4) гидроксид натрия.
А6. Верны ли следующие суждения о правилах безопасной работы в химической лаборатории?
А. Нельзя брать твёрдые реактивы руками.
Б. Необходимо внимательно наблюдать за испарением жидкости из раствора соли, наклонившись над нагреваемой фарфоровой чашкой
А7. Масса серной кислоты, полученной при взаимодействии оксида серы(VI) количеством вещества 2 моль с водой равна:
1) 192 г.; 2) 196 г.; 3) 2 г.; 4) 144 г.
В1. Выберите уравнения реакций, в которых элемент водород является восстановителем.
1) S + H 2 = H 2 S; 2) 2NH 3 = 3H 2 + N 2 ;
3) H 2 S O 4 + Ca = Ca S O 4 + H 2 ; 4) 2H 2 + О 2 = 2H 2 O;
5) H 2 + Ca = CaH 2
В2. Установите соответствие между молекулярным и сокращённым ионным уравнениями реакций.
А) Na 2 CO 3 + 2H NО 3 = 2Na NО 3 + CO 2 ↑ + H 2 O
1) Na 2 CO 3 + 2H + = 2Na + + CO 2 ↑+ H 2 O
2) H + + OH - = H 2 O
В) H 3 PO 4 + 3Ag NО 3 = Ag 3 PO 4 ↓ + 3H NО 3
3) 3Ag + + PО 4 3- = Ag 3 PO 4 ↓
4) CO 3 2- + 2H + = CO 2 ↑+ H 2 O
5) H 3 PO 4 = 3H + + PО 4 3-
А1. Самый активный неметалл имеет схему строения атома:
1) 2,4; 2) 2,7; 3) 2,8,5; 4) 2,8,7
А2. Сумма коэффициентов в уравнении реакции между азотной кислотой и гидроксидом меди(II) равна:
1) раствор хлорида натрия; 2) раствор гидроксида цинка;
1) гидроксидом натрия и хлоридом калия; 2) серной кислотой и нитратом натрия;
3) гидроксидом калия и сульфатом натрия; 4) серной кислотой и нитратом бария.
А5. В реакцию с азотной кислотой вступает:
1) хлорид натрия; 2) водород; 3) медь; 4) золото.
А7. Масса аммиака, полученного при взаимодействии 11,2 л азота с водородом равна:
1) 8,5 г.; 2) 17 г.; 3) 22,4 г.; 4) 68 г.
В1. Выберите уравнения реакций, в которых элемент водород является окислителем.
1) N 2 + O 2 = 2NO; 4) 2NO + O 2 = 2NO 2 ;
2) N 2 + 3H 2 = 2NH 3 ; 5) N 2 + 3Mg = Mg 3 N 2 ;
3) N 2 + 5Cl 2 = 2N Cl 5 .
Контрольная работа в рамках итоговой аттестации по химии в 8 классе по Рудзитису
материал по химии (8 класс) по теме
В материале представлены 2 варианта работы с ответами и нормами оценивания. Работа проводится в марте после изучения классов веществ. Работа состоит из трёх частей.
| Вложение | Размер |
|---|---|
| kr_v_ramk_it_att_8_kl_mart_rudzitis.docx | 25.78 КБ |
Активные металлы

Металлы, легко вступающие в реакции, называются активными металлами. К ним относятся щелочные, щелочноземельные металлы и алюминий.
Положение в таблице Менделеева
Металлические свойства элементов ослабевают слева направо в периодической таблице Менделеева. Поэтому наиболее активными считаются элементы I и II групп.
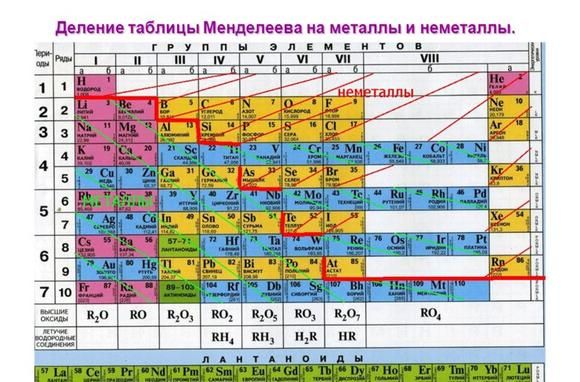
Рис. 1. Активные металлы в таблице Менделеева.
Все металлы являются восстановителями и легко расстаются с электронами на внешнем энергетическом уровне. У активных металлов всего один-два валентных электрона. При этом металлические свойства усиливаются сверху вниз с возрастанием количества энергетических уровней, т.к. чем дальше электрон находится от ядра атома, тем легче ему отделиться.
Наиболее активными считаются щелочные металлы:
- литий;
- натрий;
- калий;
- рубидий;
- цезий;
- франций.
К щелочноземельным металлам относятся:
- бериллий;
- магний;
- кальций;
- стронций;
- барий;
- радий.
Узнать степень активности металла можно по электрохимическому ряду напряжений металлов. Чем левее от водорода расположен элемент, тем более он активен. Металлы, стоящие справа от водорода, малоактивны и могут взаимодействовать только с концентрированными кислотами.

Рис. 2. Электрохимический ряд напряжений металлов.
К списку активных металлов в химии также относят алюминий, расположенный в III группе и стоящий левее водорода. Однако алюминий находится на границе активных и среднеактивных металлов и не реагирует с некоторыми веществами при обычных условиях.
Свойства
Активные металлы отличаются мягкостью (можно разрезать ножом), лёгкостью, невысокой температурой плавления.
Основные химические свойства металлов представлены в таблице.
Реакция
Уравнение
Исключение
Щелочные металлы самовозгораются на воздухе, взаимодействуя с кислородом
Литий реагирует с кислородом только при высокой температуре
Щелочноземельные металлы и алюминий на воздухе образуют оксидные плёнки, а при нагревании самовозгораются
Реагируют с простыми веществами, образуя соли
Алюминий не вступает в реакцию с водородом
Бурно реагируют с водой, образуя щёлочи и водород
Реакция с литием протекает медленно. Алюминий реагирует с водой только после удаления оксидной плёнки
Реагируют с кислотами, образуя соли
Взаимодействуют с растворами солей, сначала реагируя с водой, а затем с солью
Активные металлы легко вступают в реакции, поэтому в природе находятся только в составе смесей – минералов, горных пород.

Рис. 3. Минералы и чистые металлы.
Что мы узнали?
К активным металлам относятся элементы I и II групп – щелочные и щелочноземельные металлы, а также алюминий. Их активность обусловлена строением атома – немногочисленные электроны легко отделяются от внешнего энергетического уровня. Это мягкие лёгкие металлы, быстро вступающие в реакцию с простыми и сложными веществами, образуя оксиды, гидроксиды, соли. Алюминий находится ближе к водороду и для его реакции с веществами требуются дополнительные условия – высокие температуры, разрушение оксидной плёнки.
Читайте также:
