Презентация по химии металлы 8 класс
Обновлено: 17.05.2024
За лето ребенок растерял знания и нахватал плохих оценок? Не беда! Опытные педагоги помогут вспомнить забытое и лучше понять школьную программу. Переходите на сайт и записывайтесь на бесплатный вводный урок с репетитором.
Вводный урок бесплатно, онлайн, 30 минут
Предварительный просмотр:
Подписи к слайдам:
МЕТАЛЛЫ Титков Иван 9 класс г. Екатеринбург
Металлы – ковкие, пластичные, тягучие вещества, которые имеют металлический блеск, тепло- и электропроводны.
Свойства металлов: Плотная кристаллическая структура Характерный металлический блеск Высокая теплопроводность и электрическая проводимость Уменьшение электрической проводимости с ростом температуры Низкие значения потенциала ионизации Ковкость и тягучесть Способность к образованию сплавов « Металлы - тела твердые, ковкие, блестящие…» М. В. Ломоносов
МЕТАЛЛЫ Цветные металлы и их сплавы Черные металлы – железо и его сплавы, в которых оно составляет основную часть Благородные металлы
Благородные металлы Их называют так потому, что они практически не окисляются на воздухе даже при повышенной температуре и не разрушаются при действии на них растворов кислот и щелочей (кроме «царской водки – смеси азотной и соляной кислот») Золото Серебро Платина, рутений и некоторые другие
Черные металлы Это железо и все его сплавы, в которых оно составляет основную часть. Этими сплавами являются чугуны и стали.
Цветные металлы и их сплавы Они получили такое название потому, что имеют различную окраску. Например, медь светло-красная, никель, олово, серебро - белые, свинец - голубовато-белый, золото -желтое. Из сплавов в практике нашли большое применение: бронза - сплав меди с оловом и другими металлами, латунь - сплав меди с цинком, баббит - сплав олова с сурьмой и медью и др.
Пластичность – это важнейшее свойство металлов изменять свою форму при ударе, прокатываться в тонкие листы и вытягиваться в проволоку.
Металлы различаются по твёрдости Мягкие: щелочные; свинец, олово и т.д. Твёрдые: - хром, титан, молибден. Sn Pb Ti Cr
Металлы различаются по температуре плавления Легкоплавкие: щелочные; свинец, олово и т.д. Тугоплавкие: вольфрам; платина и т.д. Sn Pb W
Металлы различаются по плотности Наименьшая плотность: щелочные Высокая плотность: осмий, ртуть Li Hg Os
Методы получения металлов пирометаллургические гидрометаллургические электрометаллургические Восстановление металлов из соединений при высокой температуре Восстановление металлов из водных растворов их соединений Восстановление металлов из расплавов соединений под действием электрического тока
Использование металлов в военном деле: Сухопутные войска ВВС ВМФ Непосредственно в оружии
Сухопутные войска Наибольшее применение нашли железо и его сплавы, а также цветные металлы.
Военно-воздушные силы и космос Наибольшее применение нашли легкие металлы – алюминий, титан и их сплавы.
Военно-морской флот Наибольшее применение нашли железо и его сплавы, а также цветные металлы.
Спасибо за внимание.
По теме: методические разработки, презентации и конспекты
Презентация по теме "Металлы. Строение свойства, применение" 9,11 класс
Металлы, положение в периодической системе, строение, свойства и применение.

презентация по теме: "Металлы и Неметаллы"
Большинство встречающихся в природе простых веществ - металлы. Некоторые из них мы часто встречаем в повседневной жизни, так что знаем, как они выглядят и для чего их можно использовать.Неметаллы - эт.

Презентация по теме "Металлы"
Презентация может использоваться в урочной и внеурочной деятельности.
Презентации по теме "Металлы"
Данные презентации можно использовать для изучения темы "Металлы" и на элективных курсах или в профильных классах.

Учебная презентация по теме "Металлы"
В разработке представлена презентация для 9 класса по химии.
Презентация по теме "Металлы в природе"
Презентация содержит подборку фотографий по теме "Металлы в природе" 8 класс.
Разработка урока с презентацией по теме " Металлы в жизни человека"
Урок обобщения знаний. Помогает проанализировать значение, применение металлов в разных аспектах деятельности человека, акцентировать внимание на металлургическом комплексе нашего города.Урок решает .
Открытый урок по химии "Простые вещества - металлы" конспект + презентация
презентация к уроку по химии (8 класс) на тему
Материал содержит конспект и презентацию открытого урока по химии в 8 классе по программе Габриелян О.С.
| Вложение | Размер |
|---|---|
| konspekt_otkrytogo_uroka_po_himii.doc | 92.5 КБ |
| prostye_veshchestva_-_metally.ppt | 744 КБ |
Подтяните оценки и знания с репетитором Учи.ру
Предварительный просмотр:
МКОУ «Нестеровская ООШ»
Открытый урок по химии в 8 классе по теме:
«Простые вещества – металлы»
Разработала учитель биологии, химии и географии
Белова Римма Евгеньевна
- повторение особенностей строения атомов элементов-металлов и образования металлической связи
- усвоение знаний о физических свойствах металлов и их применении в хозяйстве.
- образовательные: систематизировать сведения о строении атомов элементов-металлов, изменении металлических свойств в периодах и главных подгруппах таблицы Д. И. Менделеева, структуре кристаллической решетки; изучить физические свойства простых веществ – металлов и их значение;
- воспитательные: создать условия для повышения познавательной активности учащихся, развивать коммуникативные навыки, воспитывать позитивное отношение к химии, критическое отношение к оценке знаний;
- развивающие: создать условия для развития универсальных учебных действий: а) познавательных : постановка и решение проблемы, действия со знаково-символическими средствами, умение работать с информацией, анализ, установление причинно-следственных связей, доказательство суждений;
б) личностных : соотношение цели действия и его результата, ориентация в межличностных отношениях; в) коммуникативных: умение грамотно выражать свои мысли, постановка вопросов, сотрудничество в паре, ведение диалога; г) регулятивных: целеполагание, планирование, определение последовательности действий, контроль, коррекция, оценка, саморегуляция.
Тип урока – урок «открытия» новых знаний.
Оборудование: коллекция металлов, изделия из металлов, лоток для лабораторных опытов, карточки с заданиями, инструктивная карта лабораторной работы, учебник «О. С. Габриелян, Химия, 8 класс», презентация «Простые вещества – металлы», интерактивная доска, цифровые ресурсы ФЦИОР.
- Организационный момент.
- Ознакомление с темой и целью урока.
- Планирование урока.
- Актуализация знаний.
- Изучение физических свойств металлов и установление взаимосвязи между ними и применением металлов.
- Закрепление.
I. Учитель: Здравствуйте! Сегодня мы начинаем путешествие по увлекательному миру веществ. Но для начала нам необходимо определить первый пункт назначения и маршрут. ( На электронной доске – слайд №2 )
А для этого попробуйте отгадать загадку Слайд 3
Пахать и строить – все он может
Если огонь ему поможет
Отгадка лежит у меня на столе. (Демонстрация изделий из металлов: гвоздя, ложки, кольца, проволоки).
Учитель. Совершенно верно, сегодня мы будем говорить о металлах. Слайд 4
Напомните, пожалуйста, к какой группе веществ относятся металлы?
Учащиеся: Металлы относятся к простым веществам.
Учитель: Какие вещества называют простыми?
У чащиеся: Простыми называют вещества, состоящие из атомов одного химического элемента.
Учитель: Давайте сформулирует тему нашего урока: «Простые вещества – металлы» Слайд 4
Итак, мы определили станцию, но как же до нее добраться? Нам необходимо составить план изучения данной темы.
У вас на партах лежат карточки с заданиями ( Приложение 1 ). Ознакомьтесь с ними, пожалуйста, но не заполняйте.
Учащиеся предлагают этапы освоения нового материала. Слайд 5
- 1. Повторить особенности строения металлов и металлической связи.
- 2. Познакомиться с общими физическими свойствами металлов.
Учитель: Итак, повторим особенности строения атомов металлов и связи, которая для них характерна, а на основании знаний о связи познакомимся с физическими свойствами металлов. Слайд 6
- В главных подгруппах правее и выше линии «B – At» – неметаллы; левее и ниже – металлы. Элементы, оказавшиеся вблизи этой линии, проявляют переходные свойства.
- В побочных подгруппах находятся только металлы.
Учитель вызывает трех учеников к доске с заданием записать электронные и графические формулы для атомов натрия, магния и алюминия.
Задание для всего класса – проверить правильность выполнения задания.
На основе схем, записанных на доске, ученики формулируют вывод
Слайд 6 продолжение
- Для металлов характерно небольшое число электронов на внешнем энергетическом уровне (1-3).
- При образовании химических связей атомы металлов отдают внешние электроны, а атомы неметаллов их захватывают.
Учитель: Вспомните, ребята, как изменяются свойства атомов химических элементов в периоде? в группе?
Ответы учащихся. Слайд 7
Учитель : Какая связь образуется между атомами элементов-металлов? В чем ее особенность? Слайд 8
Учащиеся: Между атомами элементов-металлов образуется металлическая связь. Её особенность заключается в том, что она образована атом-ионами посредством обобществленных электронов.
- Учитель : Эта важнейшая особенность образования металлической связи является основной причиной особенных физических свойств металлов. Слайд 9
Видеосюжет Интернет-ресурса ФЦИОР «Физические свойства металлов».
Учитель : Какие физические свойства обуславливает наличие свободных электронов.
Учитель: А теперь давайте познакомимся с физическими свойствами металлов на практике. Для этого проведём лабораторную работу. Работаем по инструктивной карте. ( Приложение 2 ).Время – 5 минут.
Запись свойств в тетрадь: Слайд 10
- Металлический блеск.
- Непрозрачность.
- Цвет у большинства металлов светло-серый, исключения: медь – красновато-оранжевого, золото – желтого, цезий – светло-желтого цвета.
- Твердость (исключение: ртуть – жидкий металл).
- Пластичность.
- Теплопроводность.
- Электропроводность.
- Плотность и температура плавления различны.
Учащиеся проводят анализ рис.45 в учебнике (с.83).
Учитель: На основании всего вышесказанного можно сделать вывод: Металлы – это ковкие, пластичные вещества, которые имеют металлический блеск, тепло- и электропроводны.
А как вы думаете, зачем нам нужны знания о металлах?
Учащиеся предлагают варианты ответа.
Учитель: Вышеперечисленные физические свойства явились причиной широкой области применения металлов. Слайд 11
VI. Учитель : Вернёмся к тестам – карточкам. Выполните задания согласно инструкции. (Работа с тестами) Передайте для проверки соседу по парте. Оцените работы, подпишите и сдайте мне.
Я предлагаю вам послушать химическую сказку.
В одном Менделеевском царстве, периодическом государстве в семиэтажном дворце поселились коренные жители. Называли их в зависимости от местожительства в занимаемых комнатах.
Впрочем, догадайтесь сами. Одни жители в этом дворце были бедны, но беспечны. Хотя в карманах у большинства из них было мало монет, никто не горевал по этому поводу. Если же заводилась хоть одна лишняя монета, то характер их портился, они становились агрессивными и даже опасными, поэтому скорее хотели от неё избавиться, чтобы стать опять добрыми и веселыми.
Другие жители - «знать» этой страны отличалась от простых граждан своей скупостью. Свои монеты они неохотно одалживали и при малейшей возможности стремились забрать еще. Не смотря на разное материальное благополучие – бедные жители и знать были уверенны в себе и жили под девизом «мой дом - моя крепость».
Кем были жители этого Менделеевского царства?
Ответы учащихся: Металлы и неметаллы .
VII. Учитель : Наш урок подходит к концу.
На заключительном этапе предлагаю дать оценку уроку. Продолжите, пожалуйста, фразу: Слайд 12
Сегодня на уроке я узнал……
Было интересно, потому что…..
На уроке мне не понравилось…
VIII. Запись домашнего задания.
Учитель: Всем спасибо за работу. Д. И. Менделеев сказал: «Жить- это значит узнавать!» ( слайд № 15 ). Стремитесь к новым знаниям, открытиям и победам. Всего хорошего, до свидания!
1. У металлов на внешнем энергетическом уровне …………..электрона.
2. У всех металлов имеется ………………………….блеск.
3. Все металлы по агрегатному состоянию…………………………………. за исключением……………..
4. Все металлы……………………………цвета, за исключением металлов …………….
5. Все металлы проводят……………………………….
6. Общность физических свойств металлов объясняется наличием у них………………связи.
7. Определите тип химической связи:
Инструктивная карта по выполнению лабораторной работы
"Физические свойства металлов"
Лабораторная работа «Физические свойства металлов»
Цель: Познакомиться с физическими свойствами металлов.
Оборудование: Лоток с набором образцов металлов, алюминиевая проволока, медная проволока.
- Рассмотрите образцы металлов и определите есть ли у них блеск. Зафиксируйте результат.
- Определите являются ли образцы металлов прозрачными. Результат занесите в таблицу.
- Внимательно рассмотрите все образцы и установите: твердыми или жидкими являются металлы. Зафиксируйте результат.
- Рассмотрите образцы металлов и определите цвет каждого из них. Зафиксируйте результат.
- Несколько раз перегните образцы алюминия и меди и установите, пластичны ли они? Зафиксируйте результат.
- Определите из жизненного опыта тепло и электропроводность алюминия и меди Результат занесите в таблицу.
Презентация к уроку по химии в 8 классе Подготовила учитель химии МКОУ «Нестеровская ООШ» Белова Римма Евгеньевна Простые вещества - металлы
Загадка: Пахать и строить, всё он может, если огонь ему поможет.
Тема урока: Простые вещества – металлы
План изучения темы. 1. Повторить особенности строения металлов и металлической связи. 2. Познакомиться с общими физическими свойствами металлов. Выяснить значение металлов.
В главных подгруппах правее и выше линии « B – At » – неметаллы; левее и ниже – металлы. Элементы, оказавшиеся вблизи этой линии проявляют переходные свойства. В побочных подгруппах находятся только металлы. Для металлов характерно небольшое число электронов на внешнем энергетическом уровне (1-3) и электроотрицательность ниже 2. При образовании химических связей атомы металлов отдают внешние электроны, а атомы неметаллов их захватывают.
Группы элементов Увеличение Числа электронов на последнем уровне Радиуса атома Неметаллических свойств Способности принимать электроны (окислительные свойства) У в е л и ч е н и е Числа уровней Радиуса атома Металлических свойств Способности отдавать е
Физические свойства металлов.
Металлический блеск Непрозрачность Цвет у большинства металлов светло-серый, исключения: медь – красновато-оранжевого, золото – желтого, цезий – светло-желтого цвета Твердость (исключение: ртуть – жидкий металл) Пластичность Теплопроводность Электропроводность Плотность и температура плавления различны
ВЫВОД: Металлы – это ковкие, пластичные вещества, которые имеют металлический блеск, тепло- и электропроводны.
Применение металлов Изготовление проводников Получение сплавов Ядерная энергетика Производство ювелирных украшений Машино-строение Изготовление посуды, инструментов Изготовление строймате-риалов Электро-ника
Продолжите фразу : Сегодня на уроке я узнал…… Было интересно, потому что….. На уроке мне не понравилось…
Домашнее задание: § 14 Сборник задач: №№357, 358, 362-364. Составить кроссворд на тему «Простые вещества – металлы»
Презентация "Простые вещества металлы"
презентация к уроку по химии (8 класс) на тему
Данная презентация может быть полезна при изучении темы "Простые вещества металлы" в 8 , а также при повторении в 9 классе.
| Вложение | Размер |
|---|---|
| prostye_veshchestva_me.pptx | 1 МБ |
Простые вещества Металлы Работу выполнила Круглова И.А. учитель химии МОУ « Глажевская СОШ » Киришского р-на Ленинградской обл.
Цели урока: Повторить особенности строения атомов металлов и металлическую химическую связь Познакомить с общими физическими свойствами металлов Дать понятие об аллотропии
содержание Положение металлов в Периодической системе Д.И.Менделеева особенности строения атомов металлов металлическая химическая связь общие физические свойства металлов понятие аллотропии на примере олова проверим знания
Положение в Периодической системе Д.И.Менделеева Из 110 элементов – 88 металлы Li B Ниже диагонали B –At и элементы побочных подгрупп Fr At
Особенности строения атомов металлов 1-3 е на внешнем уровне большой R a Ме 0 – n е Ме + n
Химическая связь Металлическая в металлах и сплавах Ионная между ионами металла и неметалла
Общие физические свойства металлов Твердость Электропроводность Теплопроводность Металлический блеск Ковкость и пластичность Звон Цвет
Общие физические свойства металлов 1. Твердость ( кроме Hg ) Ртуть- жидкий металл Самый твердый - хром Cr ( царапает стекло) Мягкие – щелочные металлы Li , Na , K , Rb , Cs
2.Электропроводность и теплопроводность Ag Cu Au Al Mg Zn Fe Pb Hg Электропроводность уменьшается Хорошие проводники Ag Cu Au Al Плохие - Pb Hg
3.Металлический блеск Самый блестящий- Hg Венецианские зеркала Менее блестящий- А g Современные зеркала
4.Ковкость и пластичность Наиболее пластичные металлы- Au Ag Cu Sn Pb Zn Подсвечники из золота Очень хрупкие- Cr Mn Хром
5.Звон Самые звонкие- Ag Cu Au Царь-колокол
6.Цвет Черные – Fe и сплавы Чугунная решетка Цветные среди них драгоценные Au Ag Pt Золотые яйца работы К.Фаберже
Аллотропия олова Белое олово b- Sn (металл) Серое олово a- Sn (неметалл)
Отгадайте фамилию русского ученого, который сказал: «Металлом называется светлое тело, которое ковать можно». Ломоносов
Проверим знания: Вариант 1 1. Какие свойства подчеркивал М. В. Ломоносов, характеризуя металлы как "светлые тела, которые ковать можно"? Выберите правильный ответ: а) теплопроводность, б) обычно серый цвет с металлическим блеском, в) электрическую проводимость, г) пластичность. 2. Выберите самый пластичный драгоценный металл: а) золото, б) серебро, в) платина. 3. Причина электрической проводимости металлов заключается в характерном для них строении: а) наличие в узлах кристаллической решетки ионов, б) наличие в узлах кристаллической решетки атомов, в) присутствие подвижных обобществленных электронов. Вариант 2 1. Как на практике используют пластичность металлов? Выберите правильный ответ: а) делают зеркала, б) используют в качестве проводника электрического тока, в) выковывают изделия разной формы, . г) прокатывают в листы, д ) производят легкие сплавы для конструирования самолетов, ракет, е) вытягивают в проволоку. 2. Выберите самые электропроводные металлы: а) золото, б) серебро, в) натрий, г) железо, д ) медь е) марганец ж) алюминий з ) магний Буквы ответа расположите в порядке убывания электропроводности металлов. 3. Причина пластичности металлов заключается в их строении: а) присутствие подвижных обобществленных электронов, б) наличие в узлах кристаллической решетки ионов, в) наличие в узлах кристаллической решетки атомов.
Презентация по химии на тему "Простые вещества - металлы" (8 класс)

«Оловянная чума»
Роберт Скотт
(англ.),
полярный исследователь
Весной 1912 года погибла экспедиция Р.Скотта к Южному полюсу. Причина гибели – «оловянная чума». Экспедиция осталась без горючего из-за того, что топливо просочилось из запаянных оловом баков, поражённых «оловянной чумой»
При t=-33°С белое олово максимально быстро переходит в серое

«Оловянная чума»
Наполеон Бонапарт
Возможно «Оловянная чума» как на одна из причин поражения армии Наполеона в России в 1812 г. — рассыпались оловянные пуговицы на мундирах.
При t=-33°С белое олово максимально быстро переходит в серое

«Оловянная чума»
Музей
А.В. Суворова
г. С-Петербург
«Оловянная чума» погубила ценнейшие коллекции оловянных солдатиков. В петербургском музее А.Суворова, в подвале, где они хранились, лопнули зимой батареи отопления.
При t=-33°С белое олово максимально быстро переходит в серое

Агрегатное состояние – твердые в-ва
искл.:
От сереблисто-белого до темно-серого, искл. Au (желтый) и Cu (красно-коричневый).
Цвет
Электро- и теплопроводность
Причина – относительно
свободные е
_
Hg – жидкий металл

Как правило пластичные (Au, Ag, Cu, Al и др.), искл. Sn (серое),
Твердые (Cr, Fe) и мягкие (Au, Na, K).
Изменяется в широком интервале
Самая высокая:
Tпл.(W)= +3380°С
Самая низкая?
Tпл.(Hg)= − 38,8°С
Пластичность/хрупкость
Твердость/мягкость
Температура плавления

Искл.:
золото и медь
От серебристо-белого до серого
бериллий
германий
литий
Металлический блеск



Температура плавления
Легкоплавкие tТугоплавкие t >1000ºC

Плотность металлов
Легкие (pТяжелые(p>0,5г/мл)

Домашнее задание
Спасибо за внимание!
Белый учебник 8Г, 8К
§ 14, с.85 №1,4
Синий учебник 8А,8Б
§ 13, с. №

Фотографии металлов и неметаллов, изображения кристаллических решеток взяты из ресурсов ИНТЕРНЕТ:
Краткое описание документа:
Данную презентацию учащиеся могут использовать для самостоятельного изучения нового материала, если пропустили урок по какой-либо причине (болезнь, соревнования и т.п.). Возможно использование презентации для повторения материала, например при подготовке к контрольной работе.
Элементы данной презентации можно использовать при введении в тему "Металлы в 9 классе.
Презентация содержит информацию об отличительных физических свойствах металлов, о их возможном применении, а также об аллотропных модификациях на прмере олова.
Рабочие листы и материалы для учителей и воспитателей
Более 3 000 дидактических материалов для школьного и домашнего обучения
Презентация по химии для 8 класса по теме "Простые вещества - металлы"

Презентация по химии для 8 класса по теме "Простые вещества - металлы" соответствует программе О.С. Габриеляна.
Просмотр содержимого документа
«Презентация по химии для 8 класса по теме "Простые вещества - металлы"»

Простые вещества-

Цели урока:
- Повторить особенности строения атомов металлов и металлическую химическую связь
- Познакомиться с общими физическими свойствами металлов
Положение в Периодической системе Д.И.Менделеева
Ниже диагонали
B –At и элементы побочных подгрупп

Особенности строения атомов металлов
Химическая связь
в металлах и

Общие физические свойства металлов

Как раньше люди использовали свои знания о металлах?

Отгадайте фамилию русского ученого, который сказал: «Металлом называется светлое тело, которое ковать можно».
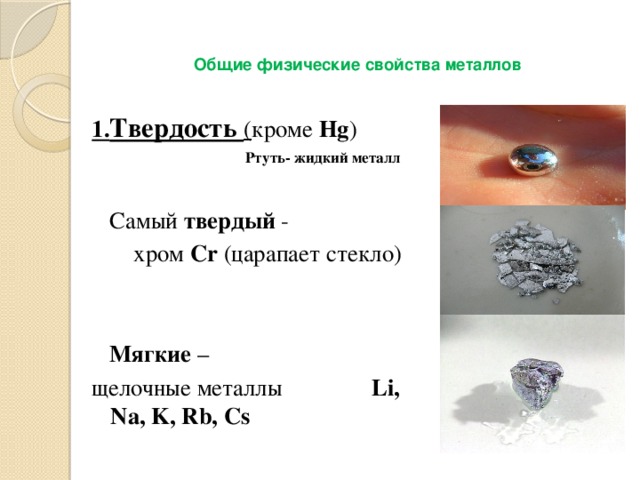
1. Твердость ( кроме Hg )
Ртуть- жидкий металл
Самый твердый -
хром Cr (царапает стекло)
щелочные металлы Li, Na, K, Rb, Cs

2.Электропроводность и теплопроводность Ag Cu Au Al Mg Zn Fe Pb Hg Электропроводность уменьшается
Ag Cu Au Al
3.Металлический блеск
4.Ковкость и пластичность
- Очень хрупкие-
- Наиболее пластичные металлы- Au Ag Cu Sn Pb Zn
Подсвечники из золота

Пластичность - важнейшее свойство металлов изменять свою форму при ударе, прокатываться в тонкие листы и вытягиваться в проволоку.

Царь-колокол

Fe и сплавы
Чугунная решетка
Золотые яйца работы К.Фаберже
Вариант 2
1. Как на практике используют пластичность металлов?
Выберите правильный ответ:
а) делают зеркала,
б) используют в качестве проводника электрического тока,
в) выковывают изделия разной формы, .
г) прокатывают в листы,
д) производят легкие сплавы для конструирования самолетов, ракет,
е) вытягивают в проволоку.
2. Выберите самые электропроводные металлы:
а) золото, б) серебро, в) натрий, г) железо,
д) медь е) марганец ж) алюминий з) магний
Буквы ответа расположите в порядке убывания электропроводности металлов.
3. Причина пластичности металлов заключается в их строении:
а) присутствие подвижных обобществленных электронов,
б) наличие в узлах кристаллической решетки ионов,
в) наличие в узлах кристаллической решетки атомов.
Вариант 1
1. Какие свойства подчеркивал М. В. Ломоносов, характеризуя металлы как "светлые тела, которые ковать можно"? Выберите правильный ответ:
а) теплопроводность,
б) обычно серый цвет с металлическим блеском,
в) электрическую проводимость,
г) пластичность.
2. Выберите самый пластичный драгоценный металл:
а) золото, б) серебро, в) платина.
3. Причина электрической проводимости металлов заключается в характерном для них строении:
а) наличие в узлах кристаллической решетки ионов,
б) наличие в узлах кристаллической решетки атомов,
в) присутствие подвижных обобществленных электронов.
Читайте также:
