Свойства металлов структура металлов
Обновлено: 19.05.2024
Определение металлов можно дать с позиций химии, физики и техники.
В химии металлы — это химические элементы, находящиеся в левой части периодической системы элементов Д. И. Менделеева, которые обладают особым механизмом взаимодействия валентных электронов (ионов) с ядром как в самих металлах, так и при вступлении в химические реакции с другими элементами, в том числе с металлами.
Физика характеризует металлы как твердые тела, обладающие цветом, блеском, способностью к плавкости (расплавлению) и затвердеванию (кристаллизации), тепло- и электропроводностью, магнитными и другими свойствами.
В технике металлы — это конструкционные материалы, обладающие высокой обрабатываемостью (ковкостью, штампуемостью, обрабатываемостью резанием, паяемостью, свариваемостью и др.), прочностью, твердостью, ударной вязкостью и рядом других ценных свойств, благодаря которым они находят широкое применение.
Русский ученый М. В. Ломоносов (1711 — 1765), исследуя металлы и неметаллы в своем труде «Первые основания металлургии или рудных дел», дал металлам определение: «Металлом называется светлое тело, которое ковать можно. Таких тел находим только шесть: золото, серебро, медь, олово, железо и свинец». Это определение М. В. Ломоносов дал в 1773 г., когда известны были только шесть металлов.
Из металлов, добываемых из недр земли, получают большую группу конструкционных материалов, применяемых в различных отраслях промышленности. В природе одни металлы встречаются в чистом, самородном виде, другие — в виде оксидов (соединений металла с кислородом), нитридов и сульфидов, из которых состоят различные руды этих металлов.
Самыми распространенными металлами, применяемыми в качестве конструкционных материалов, являются железо, алюминий, медь и сплавы на основе этих металлов.
К металлам относятся более 80 элементов периодической системы Менделеева. Все эти металлы подразделяются на две большие группы: черные металлы и цветные металлы.
Характерными признаками черных металлов являются темно-серый цвет, блеск, высокие плотность и температура плавления, твердость, прочность, вязкость и полиморфизм (аллотропия). По физикохимическим свойствам черные металлы подразделяют на пять групп:
- железистые (железо, кобальт, никель, марганец);
- тугоплавкие (вольфрам, рений, тантал, молибден, ниобий, ванадий, хром, титан и др.);
- урановые — актиниды (уран, торий, плутоний и др.);
- редкоземельные — лантаниды (лантан, церий, иттрий, скандий и др.);
- щелочно-земельные (литий, натрий, калий, кальций и др.).
Из этих пяти групп черных металлов особенно широкое применение в промышленном производстве находят железистые и тугоплавкие металлы.
Железистые металлы, кроме марганца, называют еще ферромагнетиками. Ферромагнетики способны намагничиваться и притягивать металлы своей группы.
К тугоплавким относятся металлы, которые имеют температуру плавления выше температуры плавления железа (1 539 °С): титан — 1 667 °С, ванадий — 1 902 °С, хром — 1 903 °С, молибден — 2 615 °С, ниобий — 2 460 °С, тантал — 2 980 °С, вольфрам — 3 410 °С. Тугоплавкие металлы в основном применяются как легирующие элементы в производстве жаропрочных, жаростойких, теплостойких и специальных сплавов, в том числе твердых сплавов и высоколегированных сталей.
2. Строение металлов
Атомно-кристаллическая структура металлов. Как известно, все вещества состоят из атомов, в том числе и металлы. Каждый металл (химический элемент) может находиться в газообразном, жидком или твердом агрегатных состояниях. Каждое агрегатное состояние будет иметь свои особенности, отличные друг от друга. В газообразном металле расстояние между атомами велико, силы взаимодействия малы и атомы хаотично перемещаются в пространстве; газ стремится к расширению в сторону большего объема. При понижении температуры и давления вещество переходит в жидкое состояние. Свойства жидкого вещества резко отличаются от свойств газообразного. В жидком металле атомы сохраняют лишь так называемый ближний порядок атомов, т. е. в объеме расположено небольшое количество атомов, а не атомы всего объема. При понижении температуры жидкий металл переходит в твердое состояние, которое имеет строгую закономерность расположения атомов.
Если условно провести вертикальные и горизонтальные линии связи через центры атомов, можно увидеть, что у металлов в твердом состоянии атомы расположены в строго определенном порядке и представляют собой множество раз повторяющиеся элементарные геометрические фигуры — параллелепипеды (рис. 1). Наименьшую геометрическую фигуру называют элементарной ячейкой. Элементарные ячейки, расположенные на горизонтальных и вертикальных кристаллографических плоскостях (рис. 2), образуют пространственную кристаллическую решетку.
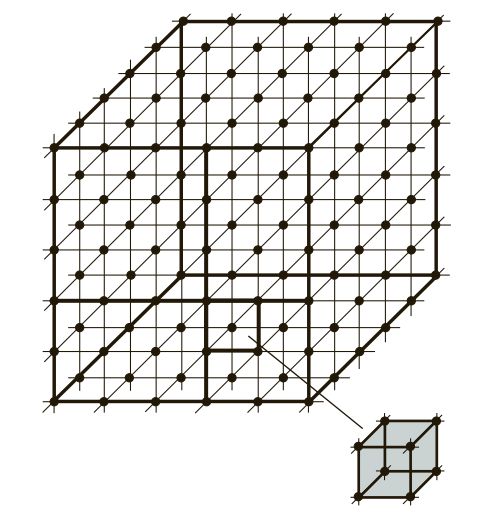
Рис. 1. Схема расположения элементарных геометрических ячеек в атомных решетках металлов и сплавов
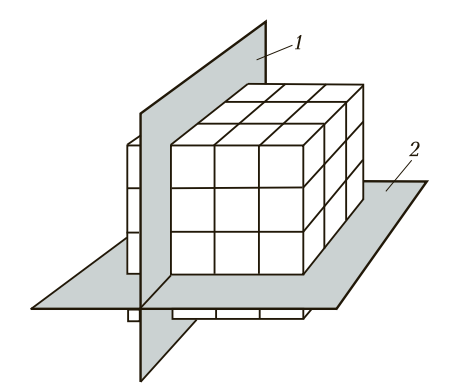
Рис. 2. Расположение кристаллографических плоскостей: 1 и 2 — соответственно горизонтальная и вертикальная кристаллографические плоскости
Элементарные кристаллические решетки характеризуют следующие основные параметры: расстояние между атомами по осям координат (по линиям связи), углы между линиями связи, координационное число — число атомов, находящихся на наиболее близком и равном расстоянии от любого атома в решетке. Форму элементарной ячейки рассматривают по кристаллографическим плоскостям в трех измерениях.
Таким образом, любой металл можно представить не как однородную цельную массу, а как массу, сложенную из множества элементарных ячеек. Блок элементарных атомных кристаллических ячеек образует атомно-кристаллическую ячейку (решетку). Если выделить эту элементарную ячейку, то в зависимости от металла получим следующие типы кристаллических ячеек (рис. 3): куб (К), объемно-центрированный куб (ОЦК), гранецентрированный куб (ГЦК), гексагональная плотноупакованная ячейка (ГПУ), гексагональная простая ячейка (Г) и др.
Простая кубическая ячейка (рис. 3, а) характерна для неметаллов, которые обладают наибольшими плотностью и удельным весом, и имеет восемь атомов, которые расположены в каждой вершине куба.
Объемно-центрированная кубическая ячейка (рис. 3, б ) состоит из восьми атомов, которые расположены по одному атому в каждой вершине куба, и одного, находящегося в центре куба на равных расстояниях от его граней. Эту форму атомной кристаллической ячейки имеют железо модификации Fe-α, ванадий, вольфрам, молибден, тантал и хром, т. е. в основном черные металлы.
Гранецентрированная кубическая ячейка (рис. 3, в) имеет 14 атомов — по одному атому в каждой вершине куба (восемь атомов) и по одному атому в центре каждой грани (шесть атомов). Гранецентрированную кубическую ячейку имеют алюминий, железо модификации Fe-γ, золото, кобальт, медь, никель, платина и серебро, в основном это цветные металлы и часть черных металлов.
Гексагональная плотноупакованная ячейка (рис. 3, г) состоит из 17 атомов. Форма геометрического тела, которую образуют эти атомы, является шестигранной призмой. При этом по шесть атомов расположены в каждой вершине верхнего и нижнего оснований, по одному атому в центре этих оснований и три атома в центре одной их трех граней (через грань). Гексагональную плотноупакованную ячейку имеют бериллий, кадмий, магний, ванадий, тантал.
Простая гексагональная ячейка (рис. 3, д) состоит из 12 атомов, которые расположены в вершинах верхнего и нижнего оснований шестигранной призмы. Такую кристаллическую ячейку имеют ртуть и цинк.
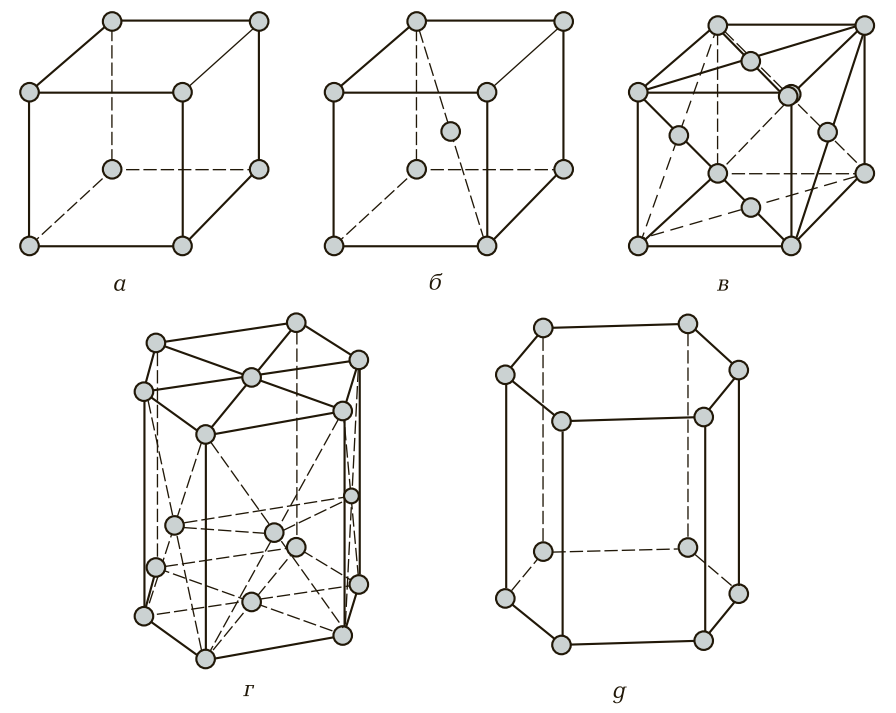
Рис. 3. Геометрические формы элементарных кристаллических ячеек: а — куб; б — объемно-центрированный куб; в — гранецентрированный куб; г — гексагональная плотноупакованная ячейка; д — гексагональная простая ячейка
Связь между атомами в кристаллической решетке и между решетками осуществляется за счет так называемой металлической связи. От прочности этой связи зависят прочность и твердость металлов. Чем выше эта связь, тем бо´льшую прочность и твердость имеют металлы. Механизм связи между атомами в решетке и между решетками имеет сложную физико-химическую природу.
В практике идеальное расположение кристаллических решеток обычно не наблюдается. Кристаллы, образуемые кристаллическими решетками, имеют искаженную геометрическую форму и различную величину.
Анизотропия металлов. Анизотропия (от гр. anisos — неравный и tropos — направление) — неодинаковость физических свойств среды (тела) в различных направлениях. Анизотропия предполагает зависимость свойств металлов от направления по плоскостям атомно-кристаллических решеток. Чем больше в плоскости атомов, тем выше свойства металлов. В горизонтальных плоскостях в любой форме атомно-кристаллических решеток больше, чем в вертикальных плоскостях. Следовательно, прочность металлов, испытанная в горизонтальном направлении, выше, чем в вертикальном. Анизотропия проявляется в процессе обработки конструкционных материалов давлением (проката, волочения, штамповки и других технологических способов получения заготовок и изделий).
На рис. 2 кристаллографические плоскости совпадают с линиями связи, проходящими через атомы металла. Форма элементарной кристаллической ячейки, расстояние между атомами и прочность металлической связи определяют физические, механические и технологические свойства металлов. Если исследуемый металл рассматривать по трем кристаллографическими плоскостям, по линиям связи между атомами, то можно заметить, что свойства по этим трем измерениям будут различны. Число атомов в этих плоскостях неодинаково. Металлическая связь между горизонтально и вертикально расположенными атомами также неодинакова. Это, в свою очередь, приводит к различной прочности металлов в продольном и поперечном направлениях. Например, предел прочности меди в продольном направлении будет в 2 раза больше, чем в поперечном.
Все металлы анизотропны, так как они состоят из кристаллов. Кристаллическое строение металлов обусловливает пластическую деформацию, т. е. изменение внешней формы и размеров под действием нагрузок без разрушения. Способность металлов и сплавов пластически деформироваться положена в основу их обработки давлением (прокатка, волочение, ковка, штамповка и прессование). При обработке давлением, например прокатке (рис. 4, а), происходит перемещение одного слоя атомных решеток по другому по кристаллографическим плоскостям (рис. 4, б).
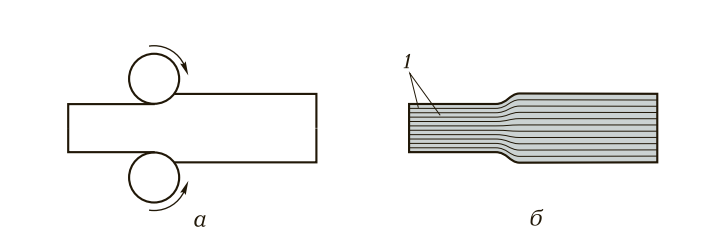
Рис. 4. Схема деформации металлов и сплавов (прокатка): а — деформация; б — скольжение металлов по кристаллографическим плоскостям в процессе деформации; 1 — кристаллографические плоскости
В процессе деформации металла при прокатке происходит не только изменение поперечных и продольных размеров заготовок, но и изменение микроструктуры металла.
Зерна под действием давления прокатных валков искажаются, приобретая продолговатую или пластинчатую форму, а затем преобразуются в волокна. Изменение микроструктуры металла в процессе деформации условно показано на рис. 5.
Процесс кристаллизации. Рассмотрим, как происходит образование кристаллов у чистых металлов. Установлено, что процесс кристаллизации металлов из жидкого состояния в твердое идет в две стадии:
- образование центров кристаллизации;
- рост кристаллов вокруг этих центров (рис. 6).
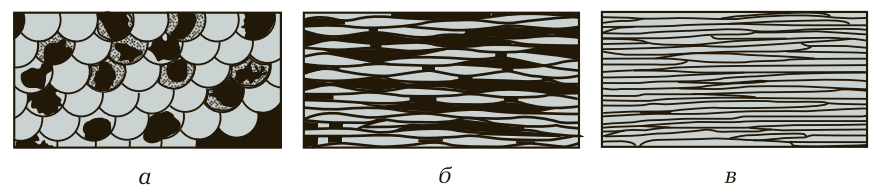
Рис. 5. Изменение микроструктуры металла в процессе деформации: а — микроструктура металла до деформации; б — микроструктура металла после первой операции деформации; в — микроструктура металла после окончательной деформации
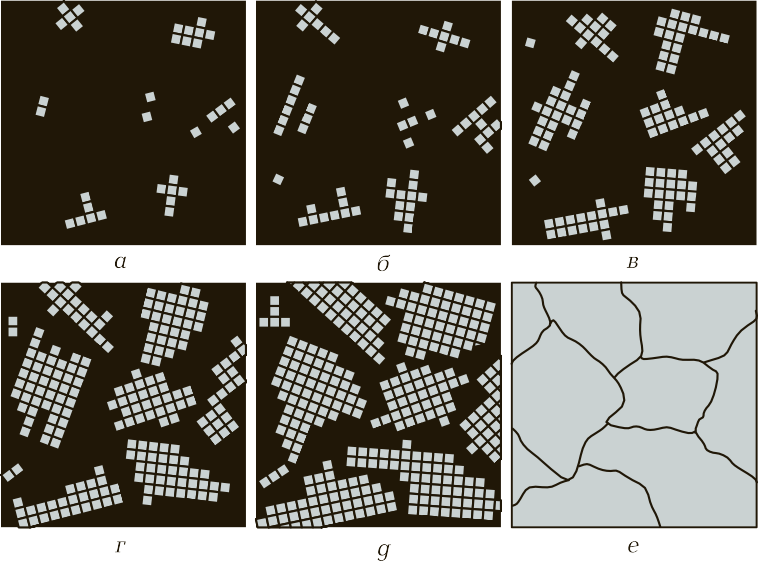
Рис. 6. Процесс кристаллизации металлов и сплавов: а — е — последовательные этапы процесса
Далее вновь появляются новые центры, и происходит рост твердой фазы вокруг первичных и вторичных центров. Процесс происходит до того момента, пока образованные таким образом кристаллы не будут соприкасаться друг с другом и не будет наличия жидкой фазы металла (см. рис. 6, г — е). Когда образование кристалла идет в жидкой фазе (в расплавленном металле), он будет иметь правильную форму, т. е. состоять из определенных геометрических фигур правильной формы. Когда кристаллы начинают соприкасаться друг с другом, а процесс затвердевания еще не закончен, тогда происходят искажения формы зерен. В практике замечено, что когда идет быстрое охлаждение, образуются мелкие зерна — мелкозернистая структура. При медленном охлаждении появление новых центров кристаллизации замедляется, но происходит рост зерна вокруг первичных центров кристаллизации. В этом случае металл будет иметь крупнозернистую структуру.
Процесс образования кристаллов в жидком состоянии и перехода металла в твердое состояние называется первичной кристаллизацией. Величина и форма зерна влияет на механические свойства металлов. Чем зерна мельче и чем правильнее их форма, тем большую твердость и прочность будет иметь металл. Чем зерна больше и чем искаженнее их форма, тем ниже твердость и прочность металла.
Аллотропия металлов. Такие металлы, как железо, кобальт, никель и др., обладают способностью изменять кристаллическую решетку при нагревании в твердом состоянии. Процесс изменения кристаллических решеток в твердом состоянии называется вторичной кристаллизацией, или аллотропией, а состояние вещества (металла) при наличии нескольких кристаллических решеток при изменении параметров (давления, температуры) — аллотропическими модификациями, или полиморфизмом. Такие металлы, как железо, молибден, вольфрам, литий в твердом состоянии при нормальной температуре имеют объемно-центрированную кубическую ячейку; алюминий, медь, серебро в твердом состоянии при нормальной температуре имеют форму гранецентрированной кубической ячейки.
На рис. 7 представлены кривые нагрева и охлаждения металла (на примере марганца). Аллотропные состояния (модификации), имеющие те или иные кубические ячейки, обозначаются греческими буквами. Первоначальное аллотропное состояние при нормальной температуре обозначается буквой α, при дальнейших повышении температуры и перекристаллизации металла — буквами β, γ, δ и т. д. При охлаждении металлов и сплавов процесс аллотропного превращения происходит в обратном порядке, как правило при тех же температурах.
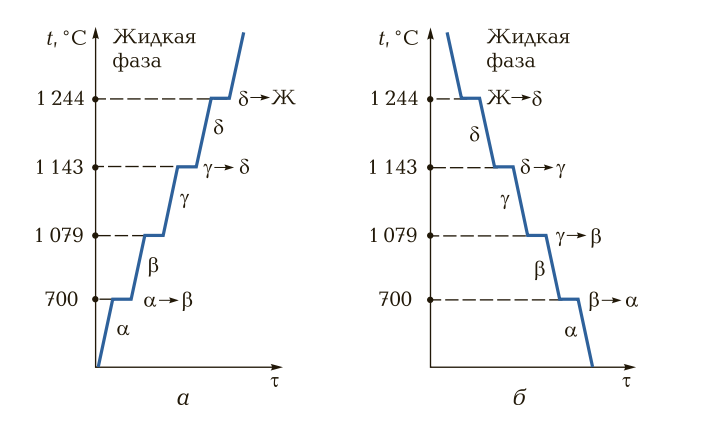
Рис. 7. Кривые нагрева (а) и охлаждения (б) марганца: t — температура; τ — время
Что такое металлы и их строение
Лекция по теме "СТРОЕНИЕ,СВОЙСТВА МЕТАЛЛОВ И МЕТОДЫ ИХ ИСПЫТАНИЯ"
Металлы – один из классов конструкционных материалов, характеризующийся определенным набором свойств:
К физическим свойствам металлов относят плотность, температуру плавления, цвет, блеск, непрозрачность, теплопроводность, электропроводность, тепловое расширение. По плотности металлы разделяют на легкие (до 3000 кг/м 3 ) и тяжелые (от 6000 кг/м 3 и выше); по температуре плавления — на легкоплавкие (до 973 К) и тугоплавкие (свыше 1173 К). Каждый металл или сплав обладает определенным, присущим ему цветом.
Прочность — способность металла в определенных условиях и пределах не разрушаясь воспринимать те или иные воздействия, нагрузки. Это свойство учитывается при изготовлении и проектировании изделий, выборе того или иного металла, сплава. Наибольшее напряжение, которое может выдержать металл, не разрушаясь, называют пределом прочности, или временным сопротивлением разрыву. Образцы для измерения прочности подвергают испытанию на специальной разрывной машине, которая постепенно, с возрастающей силой растягивает образец до полного разрыва.
Упругость — свойство металла восстанавливать свою форму после прекращения действия внешних сил, вызвавших деформацию. Наибольшее напряжение, после которого металл возвращается к своей первоначальной форме, называют пределом упругости. Если при дальнейшем повышении нагрузки напряжение превышает предел упругости и удлинение сохраняется после разгрузки образца, такое состояние называют остаточным удлинением. Далее наступает предел текучести, т.е. образец продолжает удлиняться без увеличения нагрузки.
Пластичность — свойство металла под действием внешних сил изменять, не разрушаясь, свою форму и размеры и сохранять остаточные (пластические) деформации после устранения этих сил . Данное свойство также определяется и измеряется на разрывной машине. Высокой пластичностью обладают золото, серебро, платина и их сплавы. Менее пластичны медь, алюминий, свинец. Это свойство металлов имеет большое значение в давильном и штамповочном производстве, волочении, прокатке.
Твердость — свойство металлов сопротивляться проникновению в них другого тела под действием внешней нагрузки, что необходимо учитывать при выборе инструментов для обработки металлов резанием. Например, важно знать твердость обрабатываемого металла, чтобы подобрать соответствующую фрезу или сверло. Испытания металлов на твердость проводят на специальных приборах — твердометрах.
Выносливость — свойство металлов сопротивляться действию повторных нагрузок . Температурные условия значительно влияют на механические свойства металлов: при нагревании их прочность понижается, а пластичность увеличивается; при охлаждений некоторые металлы становятся хрупкими, например, сталь некоторых марок, цинк и его сплавы. Нехладноломкими являются алюминий и медь.
Хрупкость — некоторые металлы обладают хрупкостью и при нормальных условиях, примером является серый чугун. В производстве изделий учитывается способность металлов поддаваться обработке, т.е. такие их технологические свойства, как ковкость, жидкотекучесть, литейная усадка, свариваемость, спекаемость, обрабатываемость резанием и некоторые другие.
Ковкость — способность металлов подвергаться ковке и другим видам обработки давлением (прокатке, прессованию, волочению, штамповке). Металлы могут коваться в холодном состоянии (золото, серебро, медь), а также в горячем (сталь).
Износостойкость – способность материала сопротивляться поверхностному разрушению под действием внешнего трения.
Коррозионная стойкость – способность материала сопротивляться действию агрессивных кислотных, щелочных сред.
Жаростойкость – это способность материала сопротивляться окислению в газовой среде при высокой температуре.
Жаропрочность – это способность материала сохранять свои свойства при высоких температурах.
Хладостойкость – способность материала сохранять пластические свойства при отрицательных температурах.
Антифрикционность – способность материала прирабатываться к другому материалу.
Жидкотекучесть — свойство расплавленного металла заполнять литейную форму. Высокой жидкотекучестью обладают цинк и его сплавы, чугун, бронза, олово, силумин (сплав алюминия с кремнием), латунь, некоторые магниевые сплавы. Низкой жидкотекучестью обладают сталь, красная медь, чистое серебро.
Литейная усадка —уменьшение объема металла при переходе из жидкого состояния в твердое. Это необходимо учитывать при изготовлении формы для отливки. Отливка получается всегда меньше модели, по которой сделана форма. Металлы с большой усадкой для литья почти не используют.
Свариваемость — способность металла прочно соединяться путем местного нагрева и расплавления свариваемых кромок изделия. Сплавы свариваются труднее, чистые металлы — легче. Легко свариваются изделия из малоуглеродистой стали. Плохо поддаются сварке чугун и высокоуглеродистые легированные стали.
Из химических свойств металлов и их сплавов наиболее важными в производстве художественных изделий являются растворение (взаимодействие с кислотами и щелочами) и окисление (антикоррозийная стойкость, т.е.стойкость к воздействию окружающей среды — газов, воды и т.д.).
Растворение (разъедание) — способность металлов растворяться в сильных кислотах и едких щелочах. Это свойство широко используется в различных областях производства художественных изделий. Растворение бывает частичное и полное. Частичное применяется для создания чистой поверхности изделия.
Окисление — способность металлов соединяться с кислородом и образовывать окислы металлов.
Данные свойства обусловлены особенностями строения металлов.
Все металлы, затвердевающие в нормальных условиях, представляют собой кристаллические вещества, то есть укладка атомов в них характеризуется определённым порядком – периодичностью, как по различным направлениям, так и по различным плоскостям. Этот порядок определяется понятием кристаллическая решётка.
Другими словами, кристаллическая решетка это воображаемая пространственная решетка, в узлах которой располагаются частицы, образующие твердое тело.
Элементарная ячейка – элемент объёма из минимального числа атомов, многократным переносом которого в пространстве можно построить весь кристалл.
Элементарная ячейка характеризует особенности строения кристалла. Основными параметрами кристалла являются:
· размеры ребер элементарной ячейки. a, b, c – периоды решетки – расстояния между центрами ближайших атомов. В одном направлении выдерживаются строго определенными.
· углы между осями ().
· координационное число (К) указывает на число атомов, расположенных на ближайшем одинаковом расстоянии от любого атома в решетке.
· базис решетки количество атомов, приходящихся на одну элементарную ячейку решетки.
Рис. Схема кристаллической решетки
Классификация возможных видов кристаллических решеток была проведена французским ученым О. Браве, соответственно они получили название «решетки Браве». Всего для кристаллических тел существует четырнадцать видов решеток, разбитых на четыре типа;
· примитивный – узлы решетки совпадают с вершинами элементарных ячеек;
· базоцентрированный – атомы занимают вершины ячеек и два места в противоположных гранях;
· объемно-центрированный – атомы занимают вершины ячеек и ее центр;
· гранецентрированный – атомы занимают вершины ячейки и центры всех шести граней
В металлических материалах, как правило, формируются три типа кристаллических решеток: объемноцентрированная кубическая (ОЦК), гранецентрированная кубическая (ГЦК) и гексагональная плотноупакованная (ГП). Элементарные ячейки ОЦК, ГЦК и ГП решеток показаны на рис. 9.

Рис. Типы кристаллических решеток металлов.
а) Г.Ц.К, б) О.Ц.К., в) Г.П.У.
Основными типами кристаллических реш¨ток являются:
- Объемно - центрированная кубическая (ОЦК), атомы располагаются в вершинах куба и в его центре
- Гранецентрированная кубическая (ГЦК), атомы располагаются в вершинах куба и по центру каждой из 6 граней
- Гексагональная, в основании которой лежит шестиугольник:
- простая – атомы располагаются в вершинах ячейки и по центру 2 оснований (углерод в виде графита);
- плотноупакованная (ГПУ) – имеется 3 дополнительных атома в средней плоскости (цинк).
ОЦК решетку имеют такие металлы, как вольфрам, молибден, ниобий, низкотемпературные модификации железа, титана, щелочные металлы и ряд других металлов. Серебро, медь, алюминий, никель, высокотемпературная модификация железа и ряд других металлов имеют ГЦК решетку. ГП решетка у магния, цинка, кадмия, высокотемпературной модификации титана.
2. Физическая природа деформации металлов
Деформацией называется изменение формы и размеров тела под действием напряжений.
Напряжение – сила, действующая на единицу площади сечения детали.
Напряжения и вызываемые ими деформации могут возникать при действии на тело внешних сил растяжения, сжатия и т.д.,
Деформация металла под действием напряжений может быть упругой и пластической.
Упругой называется деформация, полностью исчезающая после снятия вызывающих ее напряжений.
При упругом деформировании изменяются расстояния между атомами металла в кристаллической решетке. Снятие нагрузки устраняет причину, вызвавшую изменение межатомного расстояния, атомы становятся на прежние места, и деформация исчезает.
Упругая деформация на диаграмме деформации характеризуется линией ОА (рис.).
Рис. Диаграмма зависимости деформации металла от действующих напряжений
Зависимость между упругой деформацией и напряжением выражается законом Гука
где: Е - модуль упругости.
Пластической или остаточной называется деформация после прекращения действия вызвавших ее напряжений.
В результате развития пластической деформации может произойти вязкое разрушение путем сдвига.
Механические свойства определяют поведение материала при деформации и разрушении от действия внешних нагрузок.
В зависимости от условий нагружения механические свойства могут определяться при:
статическом нагружении – нагрузка на образец возрастает медленно и плавно.
динамическом нагружении – нагрузка возрастает с большой скоростью, имеет ударный характер.
Прочность – способность материала сопротивляться деформациям и разрушению.
Испытания проводятся на специальных машинах, которые записывают диаграмму растяжения, выражающую зависимость удлинения образца (мм) от действующей нагрузки Р, т.е. .
Но для получения данных по механическим свойствам перестраивают: зависимость относительного удлинения от напряжения
Твердость – это сопротивление материала проникновению в его поверхность стандартного тела (индентора), не деформирующегося при испытании.
3. Методы определения твердости
О твердости судят либо по глубине проникновения индентора (метод Роквелла), либо по величине отпечатка от вдавливания (методы Бринелля, Виккерса, микротвердости).
Наибольшее распространение получили методы Бринелля, Роквелла, Виккерса. Схемы испытаний представлены на рис. 7.1.
Рис. Схемы определения твердости: а – по Бринеллю; б – по Роквеллу; в – по Виккерсу
3.1. Твердость по Бринеллю ( ГОСТ 9012)
Испытание проводят на твердомере Бринелля (рис.7.1 а)
В качестве индентора используется стальной закаленный шарик диаметром D 2,5; 5; 10 мм, в зависимости от толщины изделия.
Нагрузка Р, в зависимости от диаметра шарика и измеряемой твердости: для термически обработанной стали и чугуна – , литой бронзы и латуни – , алюминия и других очень мягких металлов – .
Продолжительность выдержки: для стали и чугуна – 10 с, для латуни и бронзы – 30 с.
Полученный отпечаток измеряется в двух направлениях при помощи лупы Бринелля.
Твердость определяется как отношение приложенной нагрузки Р к сферической поверхности отпечатка F:
Стандартными условиями являются D = 10 мм; Р = 3000 кгс; = 10 с. В этом случае твердость по Бринеллю обозначается НВ 250, в других случаях указываются условия: НВ D / P / , НВ 5/ 250 /30 – 80.
3.2. Метод Роквелла ГОСТ 9013
Основан на вдавливании в поверхность наконечника под определенной нагрузкой (рис. 7.1 б)
Индентор для мягких материалов (до НВ 230) – стальной шарик диаметром 1/16” (1,6 мм), для более твердых материалов – конус алмазный.
Нагружение осуществляется в два этапа. Сначала прикладывается предварительная нагрузка (10 ктс) для плотного соприкосновения наконечника с образцом. Затем прикладывается основная нагрузка Р1, втечение некоторого времени действует общая рабочая нагрузка Р. После снятия основной нагрузки определяют значение твердости по глубине остаточного вдавливания наконечника h под нагрузкой.
В зависимости от природы материала используют три шкалы твердости (табл. 7.1)
Шкалы для определения твердости по Роквеллу
3.3. Метод Виккерса
Твердость определяется по величине отпечатка (рис.7.1 в).
В качестве индентора используется алмазная четырехгранная пирамида.с углом при вершине 136 o .
Твердость рассчитывается как отношение приложенной нагрузки P к площади поверхности отпечатка F:
Нагрузка Р составляет 5…100 кгс. Диагональ отпечатка d измеряется при помощи микроскопа, установленного на приборе.
Преимущество данного способа в том, что можно измерять твердость любых материалов, тонкие изделия, поверхностные слои. Высокая точность и чувствительность метода.
Способ микротвердости – для определения твердости отдельных структурных составляющих и фаз сплава, очень тонких поверхностных слоев (сотые доли миллиметра).
Аналогичен способу Виккерса. Индентор – пирамида меньших размеров, нагрузки при вдавливании Р составляют 5…500 гс
3.4. Метод царапания.
Алмазным конусом, пирамидой или шариком наносится царапина, которая является мерой. При нанесении царапин на другие материалы и сравнении их с мерой судят о твердости материала.
Можно нанести царапину шириной 10 мм под действием определенной нагрузки. Наблюдают за величиной нагрузки, которая дает эту ширину.
3.5. Динамический метод (по Шору)
Шарик бросают на поверхность с заданной высоты, он отскакивает на определенную величину. Чем больше величина отскока, тем тверже материал.
Конспект лекции по теме "Металлы - особенности строения атомов, способы получения и свойства" дисциплины ОУД.10 Химия, специальности Фармация, СПО
Более 80% известных элементов образуют простые вещества — металлы. К ним относятся s -элементы I и II групп (исключение — водород), все d - и f - элементы, а также р-элементы III группы (кроме бора), IV группы (олово, свинец), V группы cурьма, висмут) и VI группы (полоний).
Особенности строения атомов металлов:
♦ небольшое число электронов на внешнем энергетическом уровне (как правило, один-три электрона). Исключение — атомы р-элементов IV-VI групп;
♦ малые заряды ядер и большие радиусы атомов по сравнению с атомами неметаллов данного периода;
♦ сравнительно слабая связь валентных электронов с ядром;
♦ низкие значения электроотрицательности.
В связи с этим атомы металлов легко отдают валентные электроны и превращаются в положительно заряженные ионы, т. е. м еталлы - восстановители.
Однако способность отдавать электроны проявляется у металлов неодинаково. В периодах с увеличением зарядов ядер атомов уменьшаются их радиусы, увеличивается число электронов на внешнем уровне и усиливается связь валентных электронов с ядром. Поэтому в периодах слева направо восстановительная способностъ атомов металлов уменьшается.
В главных подгруппах с возрастанием атомных номеров элементов увеличиваются радиусы их атомов и уменьшается притяжение (валентных электронов к ядру. Поэтому в главных подгруппах сверху вниз восстановительная активность атомов металлов возрастает. Следовательно, наиболее активными восстановителями являются щелочные и щелочно-земельные металлы.
Только некоторые металлы (золото, платина) находятся в природе в виде простых веществ (в самородном состоянии). Металлы, расположенные в электрохимическом ряду напряжений между оловом и золотом, встречаются как в виде простых веществ, так и в составе соединений. Большинство же металлов находятся в природе в виде соединений — оксидов, сульфидов, карбонатов и т. д. Распространенность металлов в природе уменьшается в ряду:
Содержание в земной коре (массовая доля, %) уменьшается
Получение металлов из их соединений — задача металлургии. Металлургия — наука о промышленном получении металлов из природного сырья. Различают черную (производство железа и его сплавов) и цветную (производство всех остальных металлов сплавов) металлургию. Любой металлургический процесс является процессом восстановления ионов металла различными восстановителями:
Me n + + пе - = Me
В зависимости от условий проведения процесса восстановления различают несколько способов получения металлов.
2. Способы получения металлов
Пирометаллургия — восстановление безводных соединений при высокой температуре
С или СО (карботермия)
Сульфиды предварительно обжигают:
2 = 2 ZnO + 2 S 02
ZnO + С = Zn + 2СО
Fe, Cu, Pb, Sn, Cd, Zn
Mn, Cr, W, Mo, Ti, V
H 2 (водородотермия)
Оксиды активных металлов (МgО, СаО, А1203 и др.) водородом не восстанавливаются
Cu, Ni, W, Fe, Mo, Cd, Pb
Электрометаллургия – восстановление электрическим током
2 1
электролиз 2 Na + Cl 2
Щелочные металлы, Be , Mg , Ca (из расплавленных хлоридов), Al – из расплавленного оксида
К Ni 2+ + 2е - = Ni 2
А 2Н2О - 4е - = O 2 + 4Н + 1
4 + 2Н2О электролиз 2 Ni + О2 + Н2 SO 4
Гидрометаллургия – восстановление из растворов солей
Металл, входящий в состав руды, переводят в раствор, затем восстанавливают более активным металлом:
Задания для самостоятельной работы
1. Атому магния в степени окисления +2 соответствует электронная конфигурация:
а ) 1s 2 2s 2 2 р 6 3s 2 3 р 6 ; в ) 1s 2 2s 2 2 р 4 ;
б) 1 s 2 2 s 2 2р 6 ; г ) 1 s 2 2 s 2 2р 6 3 s 2 ;
2. При частичном восстановлении водородом 30 г оксида кобальта. В получили смесь оксида и металла массой 26,8 г. Определите количество вещества водорода, вступившего в реакцию, и массовую долю кобальта в полученной смеси.
3. При электролизе раствора сульфата меди ( II ) в растворе образовалась кислота (около анода), на нейтрализацию которой затрачен раствор объемом 16 см (р = 1,05 г/см 3 ) с массовой долей гидроксида калия 6%. Вычислите массу меди, которая выделилась на катоде.
4. Для восстановления марганца из оксида марганца(1\/) путем алюмотермии было смешано 10,8 г алюминия и 26,2 г оксида. Определите, какое из исходных веществ осталось и какова его масса.
3. Физические свойства металлов
Все металлы обладают металлической кристаллической решеткой, особенности которой определяют их общие физические и механические свойства.
Общие свойства металлов:
1). Все металлы являются твердыми веществами, за исключением ртути.
2). Металлический блеск и непрозрачность металлов — результат отражения световых лучей.
3). Электро- и теплопроводность обусловлены наличием в металлических решетках свободных электронов.
С повышением температуры электропроводность металлов уменьшается, а с понижением температуры — увеличивается. Около абсолютного нуля для многих металлов характерно явление сверхпроводимости.
4). Металлы обладают ковкостью и пластичностью. По определению М. В. Ломоносова, «металлом называется светлое тело, которое ковать можно». Металлы легко прокатываются в листы, вытягиваются в проволоку, поддаются ковке, штамповке, прессованию.
Специфические физические свойства металлов:
1). по значению плотности металлы делят на легкие (плотность меньше 5 г/см 3 ): Na , Са , Mg , Al , Ti — и тяжелые (плотность больше 5 г/см 3 ): Zn , Cr , Sn , Mn , Ni , С u , Ag , Pb , Hg , Аи, W , Os - самый тяжелый ;
2). по значению температуры плавления — на легкоплавкие ( t пл < 1000 °С): Hg , Na , Sn , Pb , Zn , Mg , Al , Ca , Ag — и тугоплавкие ( t пл > 1000 ° C ): Au , Cu , Mn , Ni , Fe , Ti , Cr , Os , W - самый тугоплавкий;
3). из металлов самые мягкие — щелочные (их можно резать ножом), самый твердый — хром (царапает стекло).
4). по отношению к магнитным полям металлы подразделяют на три группы:
а) ферромагнитные — способны намагничиваться под действием даже слабых магнитных полей ( Fe , Со, Ni );
б) парамагнитные — проявляют слабую способность к намагничиванию даже в сильных магнитных полях ( Al , Cr , Ti );
в) диамагнитные — не притягиваются к магниту ( Sn , С u , Bi ).
4. Химические свойства металлов
Если атомы большинства неметаллов могут как отдавать, так и присоединять электроны, проявляя окислительно-восстановительную двойственность, то атомы металлов способны только отдавать валентные электроны, проявляя восстановительные свойства: Me - пе - = Me п+ (окисление)
Как восстановители металлы взаимодействуют с неметаллами, водой, растворами щелочей, кислот и солей.
1). Взаимодействие металлов с простыми веществами — неметаллами
Металлы при определенных условиях взаимодействуют с неметаллами, например с кислородом образуют оксиды:
Из щелочных металлов только литий сгорает на воздухе с образованием оксида:
Основной продукт окисления натрия — пероксид:
При горении других щелочных металлов образуются супероксиды, например:
Оксиды натрия и калия могут быть получены при нагревании смеси пероксида с избытком металла в отсутствие кислорода:
На реакции пероксида натрия с оксидом углерода (1 V ) основана регенерация воздуха в изолированных помещениях (например, на подводных лодках):
Основные сведения о металах
В настоящее время известно 107 химических элементов, которые делятся на две основные группы: металлы и неметаллы (металлоиды). Большинство элементов (83) — металлы, отличительными признаками которых являются непрозрачность, специфический блеск, высокая теплопроводность и электропроводность, ковкость и др. При обычной температуре все металлы, кроме ртути, находятся в твердом состоянии. Металлоиды не имеют таких свойств.
В настоящее время выплавляют около 75 металлов и огромное количество сплавов.
Внутреннее строение металлов и их сплавов
Все вещества состоят из атомов, а атом — из положительно заряженного ядра и вращающихся вокруг него отрицательно заряженных электронов (рис. 1). В ядре находятся положительно заряженные частицы — протоны. Количество протонов при обычном состоянии атома равно количеству электронов, т. е. атом электрически нейтрален. Число электронов, обозначенное порядковым номером в периодической системе элементов Д. И. Менделеева, для каждого элемента различно. Атом при определенных условиях может терять и приобретать электроны. Если электронов станет больше, чем протонов, то он будет заряжен отрицательно, а если меньше, то положительно. Такой электрически заряженный атом называется попом.
Электроны вращаются вокруг ядра по орбитам, число которых определяется номером периода элемента в периодической, системе.
У металлов на внешней орбите находятся один, два или три электрона, слабо связанных с ядром, поэтому под воздействием положительно заряженных атомов они могут отрываться от своего атома, превращая его в положительно заряженный ион. Электроны, свободно переходящие от одного атома к другому, называются свободными.
Атомы металлоидов при определенных условиях стремятся заполнить внешнюю оболочку, т. е. присоединить электроны и превратиться в отрицательно заряженные ноны.
ОСНОВНЫЕ СВЕДЕНИЯ О МЕТАЛЛАХ И СПЛАВАХ
Используемые в технике металлические материалы разделяют на простые и сложные металлы (сплавы).
Простые металлы состоят из одного основного элемента и незначительного количества примесей других элементов. Например, технически чистая медь содержит от 0,1 до 1 % примесей свинца, висмута, сурьмы и других элементов.
Сплавы — это сложные металлы, представляющие сочетание какого-либо простого металла (основы сплава) с другими металлами или неметаллами. Например, латунь — сплав меди с цинком. Здесь основу сплава составляет медь.
Химический элемент, входящий в состав металла или сплава, называется компонентом. По числу компонентов сплавы делятся на двухкомпонентные (двойные), трех-компонентные (тройные) и т. д.
Большинство сплавов получают сплавлением компонентов в жидком состоянии.
Сплавы превосходят простые металлы по прочности, твердости, обрабатываемости и т. д. Вот почему они применяются в технике значительно шире простых металлов. Например, железо — мягкий металл, почти не применяющийся в чистом виде. Зато самое широкое применение в технике имеют сплавы железа с углеродом — стали и чугуны.
Все применяемые в технике металлы и сплавы делят ся на черные и цветные.
К черным металлам относятся железо и его сплавь (сталь и чугун). Все остальные металлы и сплавы состав представляют группу цветных металлов.
Наибольшее распространение в технике получили черные металлы. Это обусловлено большими запасами железных руд в земной коре, сравнительной простотой технологии выплавки черных металлов, их высокой прочностью.
Цветные металлы применяются в технике реже, чем черные. Это объясняется незначительным содержанием многих цветных металлов в земной коре, сложностью процесса их выплавки из руд, недостаточной прочностью. Цветные металлы дороже черных. Во всех случаях, когда это возможно, их заменяют черными металлами, пластмассами и другими материалами.
Из большого числа цветных металлов и сплавов в сельскохозяйственной технике наибольшее распространение получили сплавы алюминия, меди, а также подшипниковые сплавы.
Все металлы и сплавы в твердом состоянии имеют
кристаллическое строение, т. е. их атомы (ионы) расположены в строго определенном порядке. Этим кристаллические тела отличаются от аморфных тел, у которых атомы расположены хаотично. Аморфными телами являются стекло, клей, воск и др.

Если атомы металла мысленно соединить прямыми линиями, то получится правильная геометрическая система, называемая пространственной кристаллической решеткой. Из кристаллической решетки можно выделить элементарную кристаллическую ячейку, представляющую комплекс атомов, повторением которого в трех измерениях можно построить всю решетку. Наиболее распространены три типа элементарных кристаллических ячеек металлов (рис. 1): кубическая объемно-центрированная (такую решетку имеют хром, вольфрам, молибден и др.), кубическая гранецентрированная (алюминий, медь, свинец и др.) и гексагональная (цинк, магний и др.).
В узлах кристаллических решеток металлов расположены положительно заряженные ионы, удерживаемые на определенном расстоянии друг от друга свободными электронами. Такое внутреннее строение обусловливает характерные признаки металлов, такие, как высокая электро- и теплопроводность, пластичность (ковкость) и др.
Свойства металлов и сплавов зависят от природы их атомов, типа кристаллической решетки и от расстояния между атомами в решетке.
Все свойства металлов делятся на физические, химические, механические и технологические.
Физические свойства металлов и сплавов определяются цветом, плотностью, температурой плавления, тепловым расширением, тепло- и электропроводностью, а также магнитными свойствами (табл. 1). Плотность металла — величина, определяемая отношением массы металла к занимаемому им объему. Она измеряется в кг/м 3 . Для снижения массы изделия необходимо использовать материалы с небольшой плотностью (сплавы магния, алюминия и титана).
Температура плавления — температура, при которой металл переходит из твердого состояния в жидкое. Знание температуры плавления металлов и сплавов необходимо в металлургии, в литейном производстве, при горячей обработке металлов давлением, при сварке, пайке и других процессах, сопровождающихся нагреванием металлических материалов.
Тепловое расширение - изменение линейных размеров и объема металлического материала при нагревани. Неодинаковость величины теплового линейного расширения материалов характеризуется коэффициентом линейного расширения а, который показывает, на какую долю первоначальной длины при 0 °С удлинилось тело вследствие нагревания его на 1 °С. Тепловое расширение металлов необходимо учитывать при изготовлении и эксплуатации точных, сложностью приборов и инструментов, изготовлении литейных форм, Прокладке железнодорожных рельс и т. д.
Теплопроводность — способность металлов передавать' Теплоту от более нагретых частей тела к менее нагретым. Среди металлических материалов лучшей теплопроводностью обладают серебро, медь, алюминий.
Электропроводность — способность металлов провопить электрический ток. Она оценивается на практике Величиной удельного электросопротивления р. Чем меньше электросопротивление, тем более электропроводен металлический материал. Высокой электропроводностью Обладают те металлы, которые хорошо проводят электрический ток (серебро, медь, алюминий).
Способность металлов намагничиваться под действием магнитного поля/называют магнитной проницаемостью. Сильно выраженными магнитными свойствами обладают железо, никель, кобальт и их сплавы. Эти металлы называют ферромагнитными
Механическими свойствами металлов называется совокупность свойств, характеризующих способность металлических материалов сопротивляться воздействию внешних усилий (нагрузок).
К механическим свойствам металлов. относятся:
прочность — способность материала сопротивляться действий внешних сил без разрушения; упругость — способность материала восстанавливать свою первоначальную форму и размеры после прекращения действия внешних сил, вызвавших деформацию;
пластичность — способность материала изменять свою форму и размеры под действием внешних сил, не разрушаясь, и сохранять полученные деформации после прекращения действия внешних сил;
твердость — способность материала оказывать сопротивление проникновению в него другого, более твердого тела;
вязкость — способность, металлических материалов оказывать сопротивление быстро возрастающим (ударным) нагрузкам; хрупкость — свойство, обратное вязкости;
1 ползучесть — свойство металлических материалов медленно и непрерывно пластически деформироваться при длительной нагрузке и высоких температурах; усталость — процесс постепенного накопления повреждений материала под действием повторно-переменных напряжений, приводящих к уменьшению долговечности, образованию трещин и разрушению. Способность металлических материалов противостоять усталости называется выносливостью.
Механические свойства являются основной характеристикой металлов и сплавов, поэтому на заводах созданы специальные лаборатории, где производятся различные испытания с целью определения этих свойств.
Механические испытания можно разделить на:
статические, при которых нагрузка, действующая на металлический образец или деталь, остается постоянной или возрастает крайне медленно;
динамические (ударные), при которых нагрузка возрастает быстро и действует в течение незначительного времени;
испытание при повторных или знакопеременных нагрузках — нагрузках, изменяющихся многократно по величине или по величине и направлению.
Рассмотрим основные виды испытаний металлов с целью определения их механических свойств.
Технологические свойства характеризуют способность металлов поддаваться различным видам технологической обработки для получения определенной формы, размеров и свойств: Они имеют большое значение при выборе металлических материалов для изготовления деталей машин и конструкций. Из технологических свойств наибольшее значение имеют обрабатываемость резанием, свариваемость, ковкость, прокаливаемость, литейные свойства.
Обрабатываемостью резанием называется способность металлов подвергаться обработке режущими инструментами для придания деталям определенной формы, размеров (с необходимой точностью) и чистоты поверхности. Обрабатываемость резанием определяется по скорости резания, усилию резания и по шероховатости обрабатываемой поверхности. При разных методах обработки (точении, сверлении, фрезеровании и т. д.) обрабатываемость одного и того же металла может быть различной.
Свариваемостью называется свойство металла или сплава образовывать при установленной технологии сварки соединения, отвечающие требованиям, обусловленным конструкцией и эксплуатацией изделия. Свариваемость углеродистых сталей ухудшается с по-вышением содержания в них углерода. Ковкостью называется способность металла без разрушения поддаваться обработке давлением (ковке, штамповке, прокатке и т. д.). Ковкость металла зависит от его пластичности. Чем металл более пластичен, тем лучше он поддается обработке давлением.
Металлы обладают ковкостью как в холодном, так и в нагретом состоянии. В холодном состоянии хорошо куются латуни и сплавы алюминия, сталь — в нагретом • состоянии. Чугун из-за повышенной хрупкости обработке давлением не подвергается.
Прокаливаемость — способность стали воспринимать закалку на определенную глубину от поверхности. Прокаливаемость стали определяется по виду излома, по измерению твердости в различных точках сечения образца, а также методом торцовой закалки.
Литейные свойства металлов определяются жидкоте-кучестью, усадкой и склонностью к ликвации. Жидкоте кучесть — это способность расплавленного металла заполнять форму и давать плотные отливки с точной конфигурацией. Усадка — сокращение объема расплавленного металла при затвердении и последующем охлаждении. Ликвация — неоднородность химического состава твердого металла в разных частях отливки. .
При выборе литейных материалов учитывают, что чугун обладает высокими литейными свойствами: хорошей жидкотекучестью, небольшой усадкой и незначительной склонностью к ликвации. Литейные свойства стали хуже, чем чугуна.
Читайте также:
