Во всех соединениях металлов имеют степени окисления
Обновлено: 02.07.2024
Степень окисления является важной характеристикой состояния атома в молекуле.
В соединениях с ионной связью степени окисления элементов равны зарядам ионов. Например:
Na +1 Cl -1 Степень окисления натрия = +1
Степень окисления хлора = —1
Ca +2 F2 -1 Степень окисления кальция = +2
Степень окисления фтора = —1
Mg +2 O -2 Степень окисления магния = +2
Степень окисления кислорода = -2
В соединениях с ковалентной неполярной связью (в молекулах простых веществ) степени окисления элементов равны нулю.
Например: Н2 0 , Cl2 0 ; O2 0 , F2 0 , Si 0 , C 0 , S 0 …
В соединениях с ковалентной полярной связью степень окисления элемента — это условный заряд его атома в молекуле, если считать, что молекула состоит из ионов, т. е. рассматривать ковалентные полярные связи как ионные связи. При этом считают, что общие электронные пары полностью переходят к атомам элементов с большей ЭО.
Например, в молекуле хлороводорода HCl ковалентная полярная связь Н : Cl. Если общая электронная пара полностью перейдет к атому хлора (ЭОСl > ЭОН), то связь станет ионной. На атоме Н появится заряд +1, на атоме хлора будет заряд —1. Следовательно, степени окисления атомов в молекуле равны: Н +1 Cl -1 . (Степени окисления записывают над символами элементов.)
Любая молекула является электронейтральной, поэтому алгебраическая сумма степеней окисления всех атомов в молекуле всегда равна нулю.
Некоторые элементы во всех сложных веществах имеют постоянную степень окисления:
Элементы с постоянной степенью окисления Степень окисления
б) Элементы II группы (кроме Hg): Be, Mg, Ca, +2

Водород и кислород в большинстве сложных веществ имеют постоянные степени окисления, но есть исключения:
Все другие элементы в различных соединениях имеют разные степени окисления, т.е. являются элементами с переменной степенью окисления.

Например, определим степени окисления углерода в различных соединениях. Одновременно напишем графические формулы этих соединений, чтобы показать валентность углерода.

Вы видите, что степень окисления углерода изменяется от – 4 до +4, а валентность углерода во всех соединениях равна IV.

Степени окисления могут иметь и дробные значения. Например:
Необходимо знать, что:
1.Металлы во всех сложных соединениях имеют только положительные степени окисления.
2.Неметаллы могут иметь и положительные, и отрицательные степени окисления. В соединениях с металлами и водородом степени окисления неметаллов всегда отрицательные.
З. Высшая (максимальная) степень окисления элемента, как правило, равна номеру группы, в которой находится элемент в периодической системе.
4.Низшая (минимальная) степень окисления металлов равна нулю. Низшая степень окисления неметаллов обычно равна: — (8 — номер группы, в которой находится элемент).
5.Значения степеней окисления элемента между высшей и низшей степенями окисления называются промежуточными.

Например, элемент-неметалл азот (V группа) может иметь следующие степени окисления:
Правила определения степени окисления
При определении степени окисления элемента, следует руководствоваться следующими положениями:
1. Степень окисления атомов элементарных металлов равна нулю (Na, Сa, Al и т.д.).
2. Степень окисления атомов неметаллов в молекулах простых веществ равна нулю (N2, Cl2, O2, H2 и т.д.).
3. Во всех соединениях щелочные металлы имеют степень окисления (+1), щелочноземельные (+2).
4. Водород в соединениях с неметаллами имеет степень окисления (+1), а в солеобразных гидридах (NаН, СаН2 и т.д.) (–1).
5. Фтор — наиболее электроотрицательный элемент, в соединениях с другими элементами имеет степень окисления (–1).
6. Кислород в соединениях проявляет степень окисления (–2). Исключение составляют OF2, в котором степень окисления кислорода (+2), и пероксиды, например, H2O2 , Na2O2 , в которых степень окисления кислорода (–1).
7. Степень окисления может быть не только целым, но и дробным числом. Так, в KO2 и KO3 для кислорода она соответственно равна (–1/2) и (–1/3).
8. В нейтральных молекулах алгебраическая сумма всех степеней окисления равна нулю.
9. Алгебраическая сумма степеней окисления всех атомов, входящих в ион, равна заряду иона.
Пример 1.
Найти степень окисления хрома в молекуле K2Cr2О7.
Составим для этой молекулы уравнение:
(+1)×2 + x×2 + (–2)×7 = 0,
где (+1) — степень окисления калия; 2 — число атомов калия; x — степень окисления хрома; 2 — число атомов хрома; (–2) — степень окисления кислорода; 7 — число атомов кислорода.
Решая уравнение, получаем x = +6.
Пример 2.
Определить степень окисления хлора в ионе СlО4 – .
Составим для данного иона уравнение:
x×1+ (–2)×4 = –1,
где x — степень окисления хлора; (–2) — степень окисления кислорода; 4 — число атомов кислорода; (–1) — заряд всего иона.
1.4. Важнейшие восстановители иокислители
Величина степени окисления атома элемента в составе соединения дает информацию о том, в каком процессе этот атом может участвовать.
Атомы, имеющие в соединении низшую степень окисления, могут выступать только в роли восстановителя. Они способны только отдавать электроны и окисляться, проявляя восстановительные свойства, например:
N –3 , P –3 , Cl –1 , O –2 , S –2 , I –1 , F –1 и т.п.
Атомы в соединениях, имеющие высшую степень окисления, являются только окислителями. Они могут только принимать электроны и восстанавливаться, проявляя при этом окислительные свойства, например:
Атомы, проявляющие в соединениях промежуточную степень окисления, могут проявлять как окислительные, так и восстановительные свойства. Это зависит от того, реагируют ли они с более сильными окислителями или с более сильными восстановителями, например:
Mn +6 , Fe +2 , Sn +2 , S +4 , N +3 и т.п.
Например, четырехвалентная сера может быть как восстановителем:
S +4 – 2ē→ S +6 (окисление),
так и окислителем:
S +4 + 4ē→ S 0 (восстановление).
Такое свойство называется окислительно-восстановительной двойственностью.
Если говорить об окислительно-восстановительных свойствах эламентов в виде простых веществ, то они согласуются с величиной электроотрицательности данного элемента. Восстановителями обычно являются элементарные вещества, характеризующиеся наименьшими значениями энергии ионизации. К ним относятся металлы, водород. Окислителями обычно являются элементарные вещества, характеризующиеся наибольшим сродством к электрону: F2, O2. Атомы элементарных веществ, характеризующиеся средними значениями электроотрицательности, обладают и окислительными, и восстановительными свойствами, например:
1.5. Изменение окислительно-восстановительных свойств
простых веществ по периодам и группам
Соотношение окислительных и восстановительных свойств простого (элементарного) вещества определяется числом электронов на последнем энергетическом уровне атома. В Периодической системе элементов в пределах периода с повышением порядкового номера элемента, т.е. при движении слева направо, восстановительные свойства простых веществ понижаются, а окислительные возрастают и становятся максимальными у галогенов. Так, например, в третьем периоде Na — самый активный в периоде восстановитель, а хлор — самый активный в периоде окислитель. Это обусловлено увеличением количества электронов на последнем уровне, сопровождающимся уменьшением радиуса атома и приближением строения последнего уровня к устойчивому восьмиэлектронному состоянию. Металлы имеют небольшое число электронов на последнем уровне, поэтому они никогда не принимают "чужие" электроны и могут только отдавать свои. Напротив, неметаллы (кроме фтора) могут не только принимать, но и отдавать электроны, проявляя как восстановительные, так и окислительные свойства. Фтор проявляет только окислительные свойства, так как обладает наибольшей относительной электроотрицательностью из всех элементов. Таким образом, лучшие восстановители — щелочные металлы, а лучшие окислители — элементы главных подгрупп седьмой (галогены) и шестой групп.
В пределах группы изменение окислительно-восстановительных свойств обусловлено увеличением радиуса атома, что приводит к меньшему удерживанию электронов последнего энергетического уровня. У элементов как главных, так и побочных подгрупп с повышением порядкового номера (т.е. при движении сверху вниз) усиливаются восстановительные свойства и ослабевают окислительные. Поэтому из щелочных металлов наиболее активные восстановители — Сs и Fr, а наиболее активный окислитель из галогенов — фтор.
Элементы побочных подгрупп (они размещаются в четных рядах больших периодов) являются d-элементами и имеют на внешнем энергетическом уровне атомов 1-2 электрона. Поэтому эти элементы являются металлами и в состоянии простого вещества могут быть только восстановителями.
Степень окисления и общая характеристика элементов по группам Периодической системы
Литий, натрий, калий, рубидий, цезий и франций – типичные, самые активные металлы. Электронная формула внешнего слоя:
Единственный электрон внешнего уровня легко уходит при образовании химической связи.
Единственная возможная степень окисления в соединениях +1.
Низшая степень окисления 0 – в простых веществах – металлах.
I группа побочная подгруппа (подгруппа меди) – металлы медь, серебро, золото
Электронная формула внешнего слоя:
(n–1)d 10 ns 1
т.е. происходит перескок одного s-электрона на предвнешний d-подуровень. Заполненный d-подуровень обуславливает низкую реакционную способность этих металлов, подгруппу меди также называют благородными металлами. Наличие валентных d-электронов приводит к неоднозначной степени окисления в соединениях:
наиболее характерные степени окисления:
Cu +1, +2
Ag +1, +3
Au +1, +3
II группа главная подгруппа – щелочноземельные металлы
Бериллий, магний, кальций, стронций барий и радий – типичные металлы, вниз по группе металлические свойства усиливаются.
Единственная возможная степень окисления в соединениях +2.
II группа побочная подгруппа (подгруппа цинка) – металлы цинк, кадмий, ртуть.
(n–1)d 10 ns 2
Это типичные металлы средней активности.
Цинк и кадмий имеют постоянную степень окисления +2.
Ртуть имеет две устойчивые степени окисления +1 и +2.
III группа главная подгруппа – бор, алюминий, галлий, индий, таллий.
ns 2 np 1
Бор в большинстве соединений имеет степень окисления +3
Алюминий имеет постоянную степень окисления +3.
Галлий, индий, таллий могут проявлять степени окисления от +1 и +3.
Низшая степень окисления 0 – для всех элементов подгруппы.
III группа побочная подгруппа – все элементы могут проявлять степени окисления от +1 и +3.
IV группа главная подгруппа – углерод, кремний, германий, олово, свинец.
ns 2 np 2
Для завершения внешнего слоя требуется или присоединить 4 электрона (степень окисления –4), или отдать 4 электрона (степень окисления +4). Следует помнить, что элементы-металлы могут только отдавать электроны, поэтому никогда не проявляют отрицательную степень окисления.
Для элементов IV группы достаточно устойчивой является и степень окисления +2. Кроме того, элемент углерод в органических соединениях обнаруживает любую (иногда и дробную) степень окисления в пределах от –4 до +4. Это говорит об ограничении в применении понятия «степень окисления» в ковалентных органических соединениях.
C (неметалл) –4, 0, +2, +4 (возможна любая от –4 до +4)
Si (неметалл) –4, 0, +2, +4
Sn (металл) 0, +2, +4
Pb (металл) 0, +2, +4
IV группа побочная подгруппа – металлы титан, цирконий и гафний могут проявлять степени окисления от 0 и +4, последняя наиболее устойчива.
V группа главная подгруппа – азот, фосфор, мышьяк, сурьма, висмут.
ns 2 np 3
N (неметалл, газ) –3, 0, +1, +2, +3, +4, +5 (возможна любая от –3 до +5)
P (неметалл) –3, 0, +3, +5
As (неметалл) –3, 0, +3, +5
Sb (металл, амфотерный) 0, +3, +5
Bi (металл) 0, +3, +5
V группа побочная подгруппа – металлы ванадий, ниобий, тантал – могут проявлять степени окисления от 0 и +5, последняя наиболее устойчива.
VI группа главная подгруппа – кислород, сера, селен, теллур, полоний.
ns 2 np 4
а для элементов, кроме кислорода, присутствует предвнешний d-подуровень:
(n–1)d 0 ns 2 np 4
Вступая в реакции, атомы серы, селена, теллура и полония могут переходить в возбужденное состояние – спаренные s- и p-электроныпереходят на свободный d-подуровень:
(n–1)d 1 ns 2 np 3
(n–1)d 2 ns 1 np 3
При перекрывании орбиталей, содержащих эти неспаренные электроны, образуются ковалентные связи и можно говорить о проявлении степени окисления +4 и +6.
Кислород, как элемент второго периода, не имеет свободного d-подуровня, поэтому его максимальная степень окисления +2 (проявляется только в соединении с фтором OF2) т.е. не равна номеру группы.
Вниз по группе металлические свойства усиливаются, неметаллические – ослабевают. Кислород – газ, сера и селен – типичные неметаллы, теллур занимает промежуточное положение, чаще его относят к неметаллам, полоний металл.
Для неметаллов подгруппы характерна низшая степень окисления –2 (для завершения внешнего слоя требуется или присоединить 2 электрона).
O (неметалл, газ) –2, –1, 0, +2
S (неметалл) –2, 0, +4, +6
Sе (неметалл) –2, 0, +4, +6
Те (неметалл) 0, +2,+4, +6
VI группа побочная подгруппа – металлы хром, молибден, вольфрам.
Cr +2, +3, +4, +6
Mo, W +2, +3, +4, +5, +6
VII группа главная подгруппа – галогены, типичные неметаллы фтор, хлор, бром, йод и астат.
ns 2 np 5
для элементов, кроме фтора, присутствует предвнешний d-подуровень:
(n–1)d 0 ns 2 np 5
Фтор – элемент с наибольшей электроотрицательностью, в соединениях может проявлять только отрицательную степень окисления –1. Максимальная степень окисления у фтора 0, т.е., как и у кислорода, не равна номеру группы.
Остальные галогены имеют вакантный d-подуровень, на который при образовании химической связи могут переходить спаренные s- и p-электроны:
(n–1)d 1 ns 2 np 4
(n–1)d 2 ns 2 np 3
(n–1)d 3 ns 1 np 3
Низшая степень окисления у всех галогенов –1 (для завершения внешнего слоя требуется или присоединить 1 электрон).
Возможные степени окисления (выделены более характерные):
F –1, 0
VII группа побочная подгруппа – металлы марганец, технеций и рений.
VIII группа главная подгруппа – благородные газы гелий, неон, аргон, криптон, ксенон и радон.
Все они имеют заполненную внешнюю электронную оболочку:
ns 2 np 6
поэтому не образуют соединений, и, соответственно, имеют степень окисления 0. При нормальных условиях они представляют собой одноатомные газы.
VIII группа побочная подгруппа отличается от остальных – каждый период содержит не один, а три элемента этой подгруппы.
В VIII группе побочной подгруппе находятся типичные металлы. Обычно в ней выделяют триаду железа (железо, кобальт, никель) и платиновую группу (рутений, родий, палладий, осмий, иридий, платина).
Триада железа: наиболее характерные степени окисления:
Fe 0, +2, +3, +4, +6
Co 0, +2, +3, +4
Ni 0, +2, +3, +4
Металлы платиновой группы Ru, Rh, Pd, Os, Ir, Pt могут иметь различные степени окисления в соединениях, для Pt более характерными являются +2, +4, +6.
Лекция 15. Общие химические свойства металлов
С химической точки зрения металл – это элемент, который во всех соединениях проявляет положительную степень окисления.Из известных в настоящее время 109 элементов 86 являются металлами. Основной отличительной особенностью металлов является наличие в конденсированном состоянии свободных, не связных с определенным атомом электронов. Эти электроны способны перемещаться по всему объему тела. Наличие свободных электронов определяет всю совокупность свойств металлов. В твердом состоянии большинство металлов имеет кристаллическую высокосимметричную структуру одного из типов: кубическую объемноцентрированную, кубическую гранецентрированную или гексагональную плотноупакованную (рис. 1).
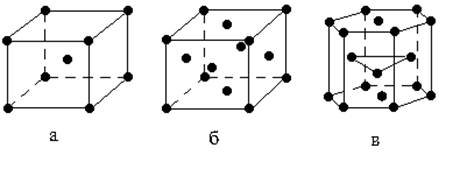
Рис. 1. Типичная структура кристалла металлов: а – кубическая объемноцентрированная; б–кубическая гранецентрированная; в – плотная гексагональная
Существует техническая классификация металлов. Обычно выделяют следующие группы: черные металлы (Fe); тяжелые цветные металлы(Cu, Pb, Zn, Ni, Sn, Co, Sb, Bi, Hg, Cd), легкие металлы с плотностью менее 5 г/см 3 (Al, Mg, Ca и т.д.), драгоценные металлы (Au, Ag и платиновые металлы) и редкие металлы (Be, Sc, In, Ge и некоторые другие).
В химии металлы классифицируются по их месту в периодической системе элементов. Различают металлы главных и побочных подгрупп. Металлы главных подгрупп называют непереходными. Эти металлы характеризуются тем, что в их атомах происходит последовательное заполнение s– и p– электронных оболочек.
Типичными металлами являются s–элементы (щелочные Li, Na, K, Rb, Cs, Fr и щелочноземельные Be, Mg, Ca, Sr, Ba, Ra металлы). Данные металлы расположены в Iа и IIа подгруппах (т. е., в главных подгруппах I и II групп). Этим металлам отвечает конфигурация валентных электронных оболочек ns 1 или ns 2 (n – главное квантовое число). Для данных металлов характерно:
а) металлы имеют на внешнем уровне 1 – 2 электрона, поэтому проявляют постоянные степени окисления +1, +2;
б) оксиды этих элементов носят основной характер (исключение –бериллий, т.к. малый радиус иона придает ему амфотерные свойства);
в) гидриды имеют солеобразный характер и образуют ионные кристаллы;
г) возбуждение электронных подуровней возможно только у металлов IIА группы с последующей sp–гибридизацией орбиталей.
К p–металлам относятся элементы IIIа (Al, Ga, In, Tl), IVа (Ge, Sn, Pb), Vа (Sb, Bi) и VIа (Ро) групп с главными квантовыми числами 3, 4, 5, 6. Данным металлам отвечает конфигурация валентных электронных оболочек ns 2 p z (z может принимать значение от 1 до 4 и равно номеру группы минус 2). Для данных металлов характерно:
а) образование химических связей осуществляется s – и p–электронами в процессе их возбуждения и гибридизации (sp–и spd), однако сверху вниз по группам способность к гибридизации падает;
б) оксиды p– металлов амфотерные или кислотные (основные оксиды только у In и Tl);
в) гидриды p–металлов имеют полимерный характер (AlH3)n или газообразный (SnH4 ,PbH4 и т. д.), что подтверждает сходство с неметаллами, открывающими эти группы.
В атомах металлов побочных подгрупп, называемых переходными металлами, происходит застраивание d– и f– оболочек, в соответствии с чем их делят на d–группу и две f–группы лантаноиды и актиноиды.
К переходным металлам относят 37 элементов d–группы и 28 металлов f–группы. К металлам d–группы относят элементы Ib (Cu, Ag, Au), IIb (Zn, Cd, Hg), IIIb (Sc, Y, La, Ac), IVb (Ti, Zr, Hf, Db), Vb (V, Nb, Ta, Jl), VIb (Cr, Mo, W, Rf), VIIb (Mn, Tc, Re, Bh) и VIII групп (Fe, Co, Ni, Ru, Rh, Pd, Os, Ir, Rt, Hn, Mt, Db, Jl, Rf, Bh, Hn, Mt). Этим элементам отвечает конфигурация 3d z 4s 2 . Исключения составляют некоторые атомы, в том числе атомы хрома с полузаполненной 3d 5 –оболочкой (3d 5 4s 1 ) и меди – с полностью заполненной 3d 10 –оболочкой (3d 10 4s 1 ). Эти элементы обладают некоторыми общими свойствами:
1. все они образуют сплавы между собой и другими металлами;
2. наличие частично заполненных электронных оболочек обусловливает способность d–металлов образовывать парамагнитные соединения;
3. в химических реакциях они проявляют переменную валентность (за немногими исключениями), а их ионы и соединения, как правило, окрашены;
4. в химических соединениях d–элементы электроположительны. "Благородные" металлы, обладая высоким положительным значением стандартного электродного потенциала (Е>0), взаимодействуют с кислотами необычным образом;
5. ионы d–металлов имеют вакантные атомные орбитали валентного уровня (ns, np, (n–1) d), поэтому они проявляют акцепторные свойства, выступая в качестве центрального иона в координационных (комплексных) соединениях.
Химические свойства элементов определяются их положением в Периодической системе элементов Менделеева. Так, металлические свойства сверху вниз в группе возрастают, что обусловлено уменьшением силы взаимодействия между валентными электронами и ядром вследствие увеличения радиуса атома и за счет возрастания экранирования электронами, расположенными на внутренних атомных орбиталях. Это приводит к облегчению ионизации атома. В периоде металлические свойства уменьшаются слева направо, т.к. это связано с увеличением заряда ядра и тем самым с увеличением прочности связи валентных электронов с ядром.
В химическом отношении атомы всех металлов характеризуются сравнительной легкостью отдачи валентных электронов (т.е. малой величиной энергии ионизации) и низким значением сродства к электрону (т.е. малой способностью удерживать избыточные электроны). Как следствие этого низкое значение электроотрицательности, т.е., способность образовывать только положительно заряженные ионы и проявлять в своих соединениях только положительную степень окисления. В связи с этим металлы в свободном состоянии являются восстановителями.
Восстановительная способность разных металлов неодинакова. Для реакций в водных растворах она определяется значением стандартного электродного потенциала металла (т.е. положением металла в ряду напряжений) и концентрацией (активностью) его ионов в растворе.
Взаимодействие металлов с элементарными окислителями (F2, Cl2, O2, N2, S и т.д.). Например, реакция с кислородом, как правило, протекает следующим образом
где n – валентность металла.
Взаимодействие металлов с водой. Металлы, обладающие стандартным потенциалом менее –2,71 В, вытесняют водород из воды на холоде с образованием гидроксидов металлов и водорода. Металлы со стандартным потенциалом от –2,7 до –1,23 В вытесняют водород из воды при нагревании
Остальные металлы с водой не реагируют.
Взаимодействие с щелочами. С щелочами могут реагировать металлы, дающие амфотерные оксиды, и металлы, обладающие высокими степенями окисления, в присутствии сильного окислителя. В первом случае металлы образуют анионы своих кислот. Так, реакция взаимодействия алюминия с щелочью запишется уравнением
в котором, лигандом является ион гидроксида. Во втором случае образуются соли, например K2CrO4 .
Взаимодействие металлов с кислотами. С кислотами металлы реагируют различно в зависимости от численного значения стандартного электродного потенциала (Е) (т.е. от положения металла в ряду напряжения) и окислительных свойств кислоты:
· в растворах галогеноводородов и разбавленной серной кислоты окислителем является только ион Н + , и поэтому с этими кислотами взаимодействуют металлы, стандартный потенциал которых меньше стандартного потенциала водорода:
Me + 2n H + = Me n+ + n H2;
· концентрированная серная кислота растворяет почти все металлы независимо от положения их в ряду стандартных электродных потенциалов (кроме Au и Pt). Водород при этом не выделяется, т.к. функцию окислителя в кислоте выполняет cульфат–ион (SO4 2– ). В зависимости от концентрации и условий проведения опыта cульфат–ион восстанавливается до различных продуктов. Так, цинк в зависимости от концентрации серной кислоты и температуры реагирует следующим образом:
– при очень высокой температуре 4Zn + 5H2SO4(конц.) = 4ZnSO4 + H2S +4H2O;
· в разбавленной и концентрированной азотной кислоте функцию окислителя выполняет нитрат–ион (NO3 – ), поэтому продукты восстановления зависят от степени разбавления азотной кислоты и активности металлов. В зависимости от концентрации кислоты, металла (величины его стандартного электродного потенциала) и условий проведения опыта нитрат–ион восстанавливается до различных продуктов. Так, кальций в зависимости от концентрации азотной кислоты реагирует следующим образом:
Концентрированная азотная кислота не реагирует (пассивирует) с железом, алюминием, хромом, платиной и некоторвми другими металлами.
Взаимодействие металлов друг с другом. При высоких температурах металлы способны реагировать друг с другом с образованием сплавов. Сплавы могут быть твердыми растворами и химическими (интерметаллическими) соединениями (Mg2Pb, SnSb, Na3Sb8, Na2K и др.).
Свойства металлического хрома (…3d 5 4s 1 ). Простое вещество хром представляет собой блестящий на изломе серебристый металл, который хорошо проводит электрический ток, имеет высокую температуру плавления (1890°С) и кипения (2430°С), большую твердость (в присутствии примесей, очень чистый хром мягок) и плотность (7,2 г/см 3 ).
При обычной температуре хром устойчив к действию элементарных окислителей и воде благодаря плотной окисной пленке. При высоких температурах хром взаимодействует с кислородом и другими окислителями.
Cr + Cl2(газ) ® CrCl3 (малиновый цвет)
С металлами при сплавлении хром образует интерметаллиды (FeCr2, CrMn3). При 600°С хром взаимодействует с парами воды:
В электрохимическом отношении металлический хром близок к железу:. Поэтому он может растворяться в неокисляющих (по аниону) минеральных кислотах, таких как галогеноводородные:
Сr + 2HCl ® CrCl2(голубой цвет) + H2.
На воздухе идет быстро следующая стадия:
Окисляющие (по аниону) минеральные кислоты растворяют хром до трехвалентного состояния:
В случае с HNO3(конц) происходит пассивация хрома – на поверхности образуется прочная пленка оксида – и металл не реагирует с кислотой. (Пассивный хром имеет высокий окислительно-восстановительный потенциал = + 1,3 В.)
Основная область применения хрома – металлургия: создание хромистых сталей. Так, в инструментальную сталь вводят 3 – 4% хрома, шарикоподшипниковая сталь содержит 0,5 – 1,5% хрома, в нержавеющей стали (один из вариантов): 18 – 25% хрома, 6 – 10% никеля, < 0,14% углерода, ~0,8% титана, остальное – железо.
Свойства металлического железа (…3d 6 4s 2 ). Железо – белый блестящий металл. Образует несколько кристаллических модификаций, устойчивых в определенном температурном интервале.
Химические свойства металлического железа определяются его положением в ряду напряжений металлов: .
При нагревании в атмосфере сухого воздуха железо окисляется:
В зависимости от условий и от активности неметаллов железо может образовывать металлоподобные (Fe3C, Fe3Si, Fe4N), солеподобные (FeCl2, FeS) соединения и твердые растворы (с C, Si, N, B, P, H).
В воде железо интенсивно корродирует:
При недостатке кислорода образуется смешанный оксид Fe3O4:
Разбавленная соляная, серная и азотная кислоты растворяют железо до двухвалентного иона:
Более концентрированная азотная и горячая концентрированная серная кислоты окисляют железо до трехвалентного состояния (выделяются NO и SO2 соответственно):
Очень концентрированная азотная кислота (плотность 1,4 г/см3) и серная (олеум) пассивируют железо, образуя на поверхности металла оксидные пленки.
Железо используют для получения железоуглеродистых сплавов. Велико биологическое значение железа, т.к. оно – составная часть гемоглобина крови. В организме человека содержится около 3 г железа.
Химические свойства металлического цинка (…3d 10 4s 2 ). Цинк – синевато-белый, пластичный и тягучий металл, но выше 200°С становится хрупким. Во влажном воздухе он покрывается защитной пленкой основной соли ZnCO3×3Zn(OH)2 или ZnO и дальнейшего окисления не происходит. При высоких температурах взаимодействует:
Исходя из величин стандартных электродных потенциалов, цинк вытесняет кадмий, который является его электронным аналогом, из солей: Cd 2+ + Zn ® Cd + Zn 2+ .
Благодаря амфотерности гидроокиси цинка металлический цинк способен растворяться в щелочах:
В разбавленных кислотах:
В концентрированных кислотах:
Значительная часть цинка расходуется для цинкования железных и стальных изделий. Широкое промышленное использование имеют сплавы цинка с медью (нейзильбер, латунь). Цинк широко используется при изготовлении гальванических элементов.
Химические свойства металлической меди (…3d 10 4s 1 ). Металлическая медь кристаллизуется в кубической гранецентрированной кристаллической решетке. Это ковкий мягкий, вязкий металл розового цвета с температурой плавления 1083°С. Медь находится на втором месте после серебра по электро- и теплопроводности, что обусловливает значение меди для развития науки и техники.
Медь реагирует с поверхности с кислородом воздуха при комнатной температуре, цвет поверхности становится темнее, а в присутствии CO2, SO2 и паров воды покрывается зеленоватой пленкой основных солей (CuOH)2CO3, (CuOH)2SO4.
Медь непосредственно соединяется с кислородом, галогенами, серой:
В присутствии кислорода металлическая медь взаимодействует с раствором аммиака при обычной температуре:
Находясь в ряду напряжений после водорода , медь не вытесняет его из разбавленных соляной и серной кислот. Однако в присутствии кислорода воздуха медь растворяется в этих кислотах:
Окисляющие кислоты растворяют медь с переходом ее в двухвалентное состояние:
Со щелочами медь не взаимодействует.
С солями более активных металлов медь взаимодействует, и эта окислительно-восстановительная реакция лежит в основе некоторых гальванических элементов:
Cu SO4 + Zn® Zn SO4 + Cu; E о = 1,1 B
Mg + CuCl2 ® MgCl2 + Cu; E о = 1,75 B.
Медь образует с другими металлами большое число интерметаллических соединений. Наибольшую известность и ценность имеют сплавы: латунь Cu–Zn (18 – 40% Zn), бронза Cu–Sn (колокольная – 20% Sn), инструментальная бронза Cu–Zn–Sn (11% Zn, 3 – 8% Sn), мельхиор Cu–Ni–Mn–Fe (68% Cu, 30% Ni, 1% Mn, 1% Fe).
Нахождение металлов в природе и способы получения.Вследствие высокой химической активности, металлы в природе находятся в виде различных соединений, и только малоактивные (благородные) металл – платина, золото и т.п. – встречаются в самородном (свободном) состоянии.
Наиболее распространенными природными соединениями металлов являются оксиды (гематит Fe2O3, магнетит Fe3O4, куприт Cu2O, корунд Al2O3, пиролюзит MnO2 и др.), сульфиды (галенит PbS, сфалерит ZnS, халькопирит CuFeS, киноварь HgS и т.д.), а также соли кислородосодержащих кислот (карбонаты, силикаты, фосфаты и сульфаты). Щелочные и щелочноземельные металлы встречаются преимущественно в виде галогенидов (фторидов или хлоридов).
Основная масса металлов получается путем переработки полезного ископаемого – руды. Поскольку металлы, входящие в состав руд находятся в окисленном состоянии, то их получение осуществляется путем реакции восстановления. Предварительно руду очищают от пустой породы
Образовавшийся концентрат оксида металла очищают от воды, а сульфиды, для удобства последующей переработки, переводят в оксиды путем обжига, например:
Для разделения элементов полиметаллических руд пользуются методом хлорирования. При обработке руд хлором в присутствии восстановителя образуются хлориды различных металлов, которые вследствие значительной и различной летучести могут быть легко отделены друг от друга.
Восстановление металлов в промышленности осуществляется посредством различных процессов. Процесс восстановления безводных соединений металлов при высоких температурах называют пирометаллургией. В качестве восстановителей используют металлы, более активные, чем получаемый, либо углерод. В первом случае говорят о металлотермии, во втором – карботермии, например:
Особое значение углерод приобрел как восстановитель железа. Углерод для восстановления металлов применяется обычно в виде кокса.
Процесс восстановления металлов из водных растворов их солей относится к области гидрометаллургии. Получение металлов осуществляется при обычных температурах, причем в качестве восстановителей могут быть использованы сравнительно активные металлы или электроны катода при электролизе. Электролизом водных растворов солей могут быть получены только сравнительно малоактивные металлы, расположенные в ряду напряжений (стандартных электродных потенциалов) непосредственно перед водородом или после него. Активные металлы – щелочные, щелочноземельные, алюминий и некоторые другие, получают электролизом расплава солей.
1. Общая характеристика элементов металлов
Из \(118\) известных на данный момент химических элементов \(96\) образуют простые вещества с металлическими свойствами, поэтому их называют металлическими элементами .
Металлические химические элементы в природе могут встречаться как в виде простых веществ, так и в виде соединений. То, в каком виде встречаются металлические элементы в природе, зависит от химической активности образуемых ими металлов.
Металлические элементы, образующие химически активные металлы ( Li–Mg ), в природе чаще всего встречаются в виде солей (хлоридов, фторидов, сульфатов, фосфатов и других).
Соли, образуемые этими металлами, являются главной составной частью распространённых в земной коре минералов и горных пород.


В растворённом виде соли натрия, кальция и магния содержатся в природных водах. Кроме того, соли активных металлов — важная составная часть живых организмов. Например, фосфат кальция Ca 3 ( P O 4 ) 2 является главной минеральной составной частью костной ткани.
Металлические химические элементы, образующие металлы средней активности ( Al–Pb ), в природе чаще всего встречаются в виде оксидов и сульфидов.


Металлические элементы, образующие химически неактивные металлы ( Cu–Au ), в природе чаще всего встречаются в виде простых веществ.
 |  |  |
| Рис. \(7\). Самородное золото Au | Рис. \(8\). Самородное серебро Ag | Рис. \(9\). Самородная платина Pt |
Исключение составляют медь и ртуть, которые в природе встречаются также в виде химических соединений.

В Периодической системе химических элементов металлы занимают левый нижний угол и находятся в главных (А) и побочных (Б) группах.
Рис. \(13\). Положение металлов в Периодической системе. Знаки металлических химических элементов расположены ниже ломаной линии B — Si — As — Te
В электронной оболочке атомов металлов на внешнем энергетическом уровне, как правило, содержится от \(1\) до \(3\) электронов. Исключение составляют только металлы \(IV\)А, \(V\)А и \(VI\)А группы, у которых на наружном энергетическом уровне находятся соответственно четыре, пять или шесть электронов.
В атомах металлов главных подгрупп валентные электроны располагаются на внешнем энергетическом уровне, а у металлов побочных подгрупп — ещё и на предвнешнем энергетическом уровне.
Радиусы атомов металлов больше, чем у атомов неметаллов того же периода. В силу отдалённости положительно заряженного ядра атомы металлов слабо удерживают свои валентные электроны.
Рис. \(14\). Характер изменения радиусов атомов химических элементов в периодах и в группах. Радиусы атомов металлов существенно больше, чем радиусы атомов неметаллов, находящихся в том же периоде
Главное отличительное свойство металлов — это их сравнительно невысокая электроотрицательность (ЭО) по сравнению с неметаллами.

Рис. \(15\). Величины относительных электроотрицательностей (ОЭО) некоторых химических элементов (по Л. Полингу). ОЭО металлических химических элементов уступает соответствующей величине неметаллических химических элементов
Атомы металлов, вступая в химические реакции, способны только отдавать электроны, то есть окисляться, следовательно, в ходе превращений могут проявлять себя в качестве восстановителей .
Читайте также:
